板蓝根药材及其制剂中告依春稳定性研究
张 昀,胡海廷,刘 欣
(河南大学 药学院,河南 开封 475004)
板蓝根为目前最常用的预防感冒药物之一,具有一定的抗病毒性。2010年版《中国药典》[1]表明其具有清热解毒、凉血利咽之功效。而板蓝根的主要抗病毒活性成分为告依春,因此,告依春含量的高低,决定了板蓝根抗病毒效果的好坏,2010版中国药典[1]将其作为板蓝根药材质量控制的指标。关于板蓝根药材及其制剂中告依春含量的测定方法文章比较多,但贮存条件对板蓝根药材及其制剂的影响未见报道。因此,我们以告依春含量为指标,考察不同温度对板蓝根药材及其制剂中告依春含量的影响,为板蓝根药材及其制剂的质量控制提供参考依据。
1 仪器与试药
TEMI880药物稳定试验箱(上海苏盈试验仪器有限公司);高效液相色谱仪Agilent1260;分析电子天平(BAS224S 赛多利斯科学仪器有限公司);超声仪(TP300天鹏电子技术(北京)有限公司)。
告依春对照品(中国药品生物检定所,批号111753-201103);板蓝根药材购于开封市乐仁堂总店(批号110923);板蓝根颗粒(白云山制药厂,批号F2F034);板蓝根含片(洛阳新春都生物制药有限公司生产,批号110901);板蓝根糖浆(李时珍医药集团有限公司,批号111001);甲醇、乙腈为色谱纯(天津四友精细化学品有限公司);水为超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
Aglient TC-C18(2)色谱柱(4.6 mm×250 mm,5 μm);流动相乙腈-0.2 g/L磷酸溶液(9∶91);检测波长245 nm;流速:1 mL/min;柱温30 ℃;进样量20 μL。高效液相色谱图,见图1。
2.2 对照品溶液的制备
按中国药典[1]板蓝根含量测定项下,对照品溶液的制备操作。
2.3 供试品溶液的制备
2.3.1 药材 按中国药典[1]板蓝根含量测定项下,供试品溶液的制备操作。
2.3.2 颗粒制剂 取样品各5袋,混匀,研细,称取0.500 3 g置10 mL容量瓶中,用超纯水溶解,超声提取10 min,冷却,摇匀,定容,用0.45 μm滤膜过滤,取续滤液,即得。
2.3.3 糖浆制剂 取样品5瓶,混匀,移取2.00 mL置10 mL容量瓶中,用超纯水溶解,定容,超声提取10 min,冷却,摇匀,用0.45 μm滤膜过滤,取续滤液,即得。
2.3.4 含片制剂 取样品10片,研细,混匀,称取0.399 9 g置10 mL容量瓶中,用超纯水溶解,超声提取10 min,冷却,定容,摇匀,用0.45 μm滤膜过滤,取续滤液,即得。

A.对照品 B.药材 C.板蓝根颗粒 D.复方板蓝根颗粒 E.板蓝根含片 F.板蓝根糖浆 1.告依春
2.4 线性关系考察
分别取浓度为0.4、1.2、2.4、3.2、4.8 mg/mL的告依春对照品溶液各20 μL,按2.1色谱条件进行测定,以峰面积(Y)对照品质量(X)进行线性回归,回归方程为Y=6157.4X+270.09 (r=1.000 0)。表明,告依春在8~96 μg与峰面积成良好的线性关系。
2.5 精密度实验
精密吸取2.4 mg/mL告依春对照品溶液20 μL,同一条件下重复进样6次,测定峰面积。结果,告依春RSD为1.5%,精密度良好。
2.6 稳定性实验
精密吸取2.4 mg/mL告依春对照品溶液20 μL,分别于0、4、8、12、16、20、24 h进样,测定峰面积。结果,告依春峰面积RSD为3.9%,在24 h内稳定。
2.7 加样回收率实验
按2.3项下取已知含量的药材及各个制剂,按2.3项下取样量分别减半,各精密称定6份,分别加入一定量的告依春对照品,按2.3项下,制备供试品溶液。结果,药材平均回收率为98.06%,RSD1.39%;单方颗粒平均回收率为97.28%,RSD1.03%;复方颗粒平均回收率为97.12%,RSD2.57%;含片平均回收率为98.24%,RSD3.06%;糖浆平均回收率为97.41%,RSD2.78%。
2.8 样品测量
分别将药材及各制剂置于5 ℃冰箱,30 ℃±5 ℃(相对湿度65%±5%)和40 ℃±2 ℃(相对湿度75%±5%)的稳定性试验箱中,于0,1,2,3,6个月取样。用外标法一点法计算各样品中告依春的含量,测定结果见表1。
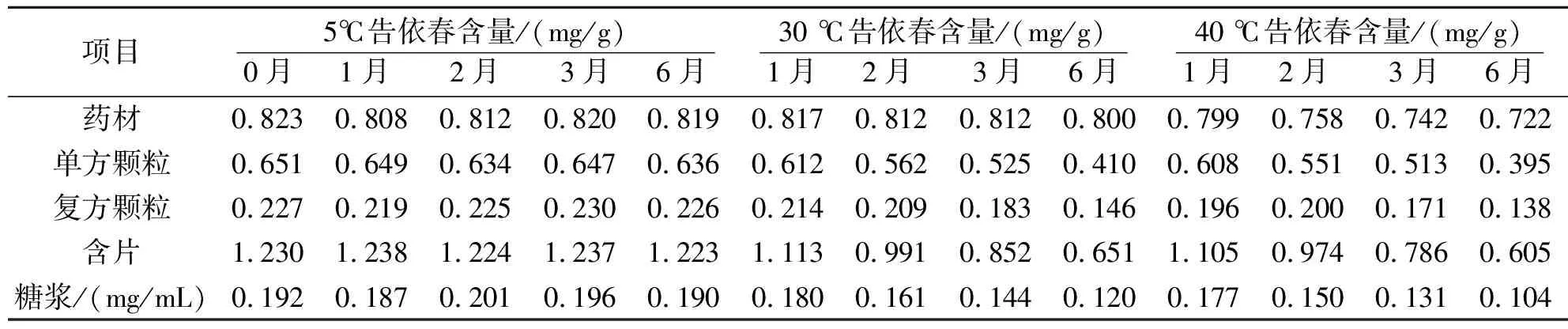
表1 不同温度样品中告依春含量(n=3)
3 讨论
由表1可知,不同温度对板蓝根药材及其制剂中告依春含量有影响。5℃时,告依春在药材及各种制剂中都很稳定,放置6 mon后未见明显变化。而在40 ℃(相对湿度75%±5%)时,放置6 mon后,药材中的含量相对0个月平均下降约15%,颗粒制剂均下降约40%,含片下降约50%,糖浆剂下降约45%;在30 ℃±5 ℃(相对湿度65%±5%)时,放置6 mon后,药材中的含量相对0个月平均下降约3%,变化不大,颗粒制剂均下降约35%,含片下降约48%,糖浆剂下降约38%。说明告依春在药材中相对比较稳定,一般的贮存条件对其影响不大。而含片制剂下降较多是因为含片出现了吸潮现象,其他剂型外观未见明显变化。因此,高温不利于板蓝根的保存,告依春会随温度升高而变得不稳定。因此,对不同厂家、不同产地板蓝根及其制剂中告依春含量的考察,应注意贮存温度对含量带来的影响[2-4],否则没有任何对比的意义。 我们对不同流动相和不同色谱柱的分离效果也进行了考察。筛选的流动相有甲醇-0.2 g/L磷酸溶液(7∶93)[1],甲醇-0.115 /L磷酸溶液(11∶89)[5],乙腈-水-磷酸-三乙胺(8.50∶90.72∶0.73∶0.05)[6-15],甲醇-水(15∶85)[15],乙腈-0.02%磷酸(9:91)等,复方板蓝根颗粒中干扰成分较多,不易分离,只有流动相为乙腈-0.2 g/L磷酸(9∶91),可以将全部剂型中的告依春很好的分离出来,故将其定为本实验所用流动相。对于色谱柱,考察了Aglient TC-C18(2) (4.6 mm×250 mm,5 μm)、Aglient HC-C18 (4.6 mm×250 mm,5 μm)、Agilent Eclipse Plus C18 (4.6 mm×150 mm,5 μm)、Thermo C18(4.6 mm×250 mm,5 μm)、Aglient HC-C18 (4.6 mm×150 mm,5 μm)等不同型号色谱柱的分离效果,发现在我们实验色谱条件下,色谱柱型号为(4.6 mm×250 mm,5 μm)的告依春均能达到完全分离,而Aglient HC-C18 (4.6 mm×150 mm,5 μm),分离度略差。因此应选用规格为(4.6 mm×250 mm,5 μm)的色谱柱。
药材的提取方法按中国药典[1]板蓝根项下操作。对于其他制剂,因为告依春易溶解于水,故采用水为提取溶剂。另外,由于三种制剂都溶于水,故采用水提超声10 min,使其快速溶解均匀。
参考文献:
[1] 国家药典委员会.《中国药典》2010年版[M].北京:中国医药科技出版社,2010:191.
[2] 方建国,万进,汤杰,等.板蓝根防治病毒感染性疾病的研究概况[J].中国中药杂志,2009,34(24):3 169-3 172.
[3] 黄家娣.板蓝根化学成分和药理作用综述[J].中国现代药物应用,2009,3(15):197-198.
[4] 吕红,吴雅红,陈立明.板蓝根颗粒UV指纹图谱的识别[J].中成药,2005,27(2):125-127.
[5] 初正云,王雪峰,程嘉艺,等.解毒胶囊抗流感病毒的实验研究[J].中成药,2007,29(9):1 281-1 284.
[6] 丁越,张彤,陶建生.板蓝根药材中有效成分的含量测定研究[J].中成药,2008,30(11):1 697-1 701.
[7] 胡晓燕,刘明华,孙琴,等.板蓝根抑菌活性部位的谱效关系研究[J].中草药,2013,44(12):1 615-1 619.
[8] 王璐,戴敬,牛小莲.HPLC 法测定清开灵软胶囊中(R,S)-告依春的含量[J].中国药房,2013,24(7):2 674-2 675.
[9] 康建,阚全程,张晓坚,等.板蓝根药材中水溶性成分高效液相特征图谱[J].中国医院药学杂志,2013,33(14):1 153-1 155.
[10] 王钢力,张铮,聂黎行,等.三种板蓝根制剂质量标准研究[J].中成药,2009,31(10):1 531-1 535.
[11] 崔田,张祖亮.高效液相色谱法测定板蓝根颗粒中表告依春含量[J].中国药业,2012,21(8):50.
[12] 安益强, 贾晓斌, 袁海建,等.HPLC测定板蓝根药材及其制剂中表告依春的含量[J].中国中药杂志,2008,33(18):2 074-2 076.
[13] 安益强, 贾晓斌, 陈彦,等.HPLC法测定不同产地板蓝根中表告依春[J].中草药,2008,39(11):1 739-1 741.
[14] 方宇,张昀,李钦.感冒解毒灵颗粒中(R,S)-告依春的稳定性研究[J].中成药,2013,35(7):130-132.
[15] 张叶,张蕾,王玉.RP-HPLC法测定板蓝根药材中腺苷和表告依春的含量[J].药物分析杂志,2008,28(11):1 848-1 850.

