壳聚糖胶囊大鼠30天喂养试验研究
吴 丹, 余永红
(1.江西省药品审评中心,江西南昌 330046;2.江西省食品药品检验所,江西南昌 330029)
壳聚糖胶囊大鼠30天喂养试验研究
吴 丹1, 余永红2
(1.江西省药品审评中心,江西南昌 330046;2.江西省食品药品检验所,江西南昌 330029)
[目的]观察壳聚糖胶囊30 d喂养大鼠产生的毒性。[方法]设低(0.83 g/kg·bw)、中(1.67 g/kg·bw)、高(3.33g/kg·bw)剂量组与对照组,连续喂养大鼠30 d观察动物生长发育状况、体重变化、平均进食量,计算食物利用率、脏器重量及脏器/体重比值,分析血常规指标和血生化指标,并进行大体解剖和组织病理分析。[结果]30 d喂养试验期间,动物生长发育良好,各指标与对照组比较无显著性差异(P>0.05)。大体解剖和组织病理分析未见与样品有关的异常改变。[结论]样品30 d喂养对大鼠未产生明显毒副作用。
壳聚糖;胶囊;大鼠; 毒性;喂养试验
甲壳素是地球上第二大可再生资源[1]。甲壳素脱除乙酰基后的产物是壳聚糖,其化学名称为(1,4)-2-氨基-2-脱氧-β-D-葡聚糖[2]。壳聚糖具有增进结肠功能、维持血清中脂质的正常含量、降低饭后葡萄糖导致的生理反应、抑制食欲、吸附胆汁酸、抗癌、降脂及降胆固醇、增强免疫力、保护胃肠、抗凝血等作用[3-4],近年来已被广泛用于保健食品开发。壳聚糖胶囊为口服固体制品,其功效成分D-氨基葡萄糖盐酸盐含量大于85.1 g/100g。笔者设低、中、高3个剂量组与对照组,连续喂养大鼠30 d壳聚糖胶囊,观察动物生长发育状况、体重变化、平均进食量,计算食物利用率、脏器重量及脏器/体重比值,分析血常规指标和血生化指标,并进行大体解剖和组织病理分析,观察壳聚糖胶囊30 d喂养大鼠产生的毒性。
1 材料与方法
1.1 材料与仪器
1.1.1 受试物。壳聚糖胶囊内容物由深圳某科技发展有限公司提供,人体口服推荐量为0.033 3 g/kg·bw(以成人体重60kg计)。
1.1.2 试验动物。清洁级SD大鼠由江西中医学院实验动物科技中心提供。实验动物生产许可证号为SCXK(赣)2005-0001。
1.1.3 主要仪器。全自动血液分析仪、全自动生化分析仪。
1.2 方法
1.2.1 试验方法。将雌雄各40只SD大鼠随机分成4组,低(0.83 g/kg·bw)、中(1.67 g/kg·bw)、高(3.33 g/kg·bw)剂量组(分别相当于人体推荐量的25、50、100倍)和对照组;按体重的10%换算成饲料量,低、中、高剂量样品分别以0.83%、1.67%、3.33%的比例与饲料混合,对照组喂食基础饲料;动物分笼饲养,自由摄食饮水,每天观察动物状况,每周加食2次,记录给食量和剩食量,并称重,计算摄食量和食物利用率。30 d后禁食16 h采血,禁食前、后(采血前)称重;以摘眼球方式采血,每只采血2份,1份做血常规检测,1份做生化检测,采血后经颈椎脱臼将动物处死并解剖,对肝、肾、脾、睾丸进行称重,计算脏/体比值,取肝、肾、脾、胃、十二指肠、睾丸、卵巢作病理切片检查。在对各剂量组动物作大体检查未发现明显病变和生化指标改变时,仅进行高剂量组及对照组动物主要脏器的组织病理学检查[5]。
1.2.2 统计方法。利用SPSS11.0软件对数据进行正态检验和方差齐性检验,如果数据为正态分布的方差齐性,则采用单因素方差分析进行组间比较;如果非正态分布或方差不齐,改用秩和检验进行分析[6]。
2 结果与分析
观察发现,各试验组动物生长发育良好,行为正常,未见中毒和死亡。对80只大鼠作大体解剖观察发现,各主要器官的尺寸、外观形态、色泽等未见异常。对高剂量组及对照组大鼠做镜检发现,肝脏、肾脏、胃肠、脾脏及睾丸(卵巢)未见明显的组织病理学变化。试验结果表明,各剂量组的平均进食量、大鼠体重、周食物利用率、总食物利用率与对照组比较无显著性差异(P>0.05)(表1~2);各剂量组雌雄大鼠的血常规指标和生化指标与对照组比较,无显著性差异(表3~4)。各剂量组大鼠禁食后体重、肝、肾、脾、睾丸重量和肝/体、脾/体、肾/体、雄鼠睾/体比值与对照组比较无显著性差异(表5~6)。
3 结论
30 d喂养试验期间,各试验组动物生长正常,各剂量组体重、增重、食物利用率与对照组比较无显著性差异(P>0.05),说明受试物对大鼠的正常生长发育和食物的吸收代
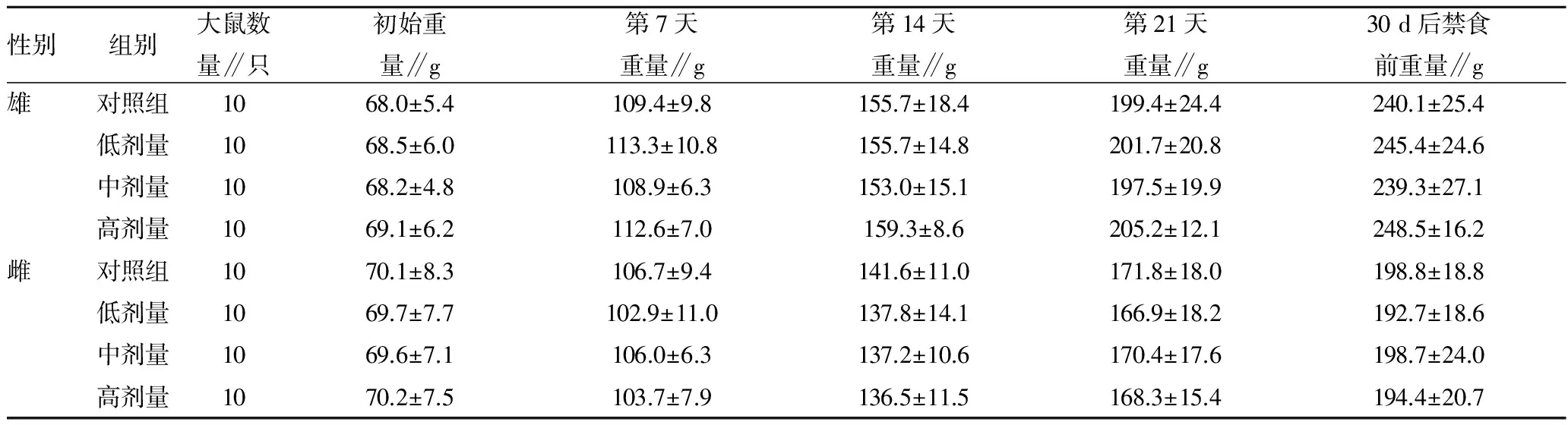
表1 壳聚糖胶囊对大鼠体重的影响
注:表中数据为平均值±标准误。
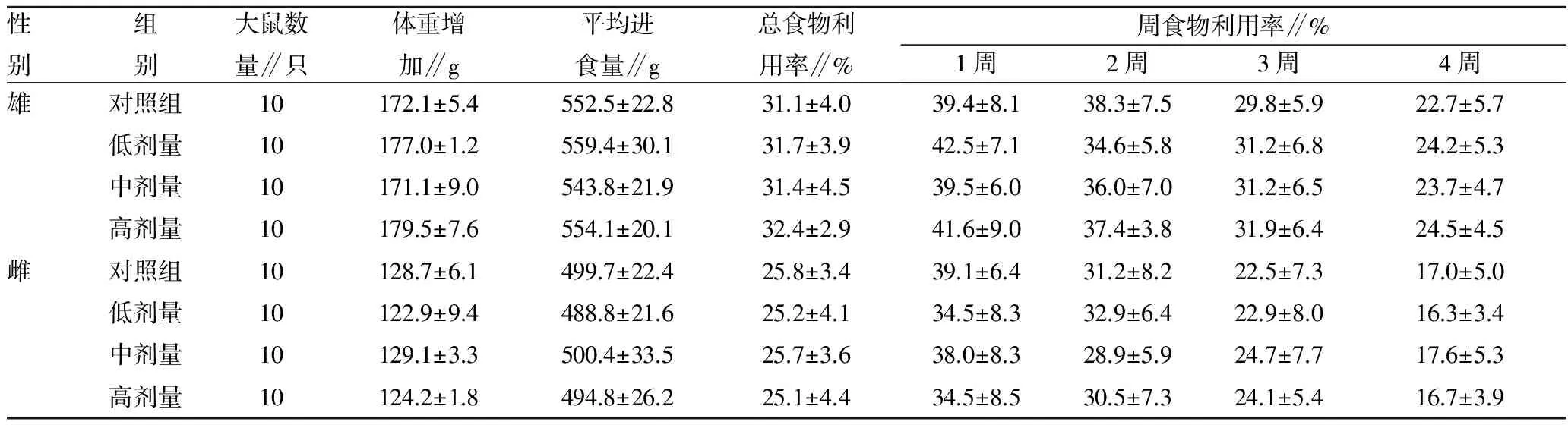
表2 壳聚糖胶囊对大鼠食物利用率的影响
注:表中数据为平均值±标准误。
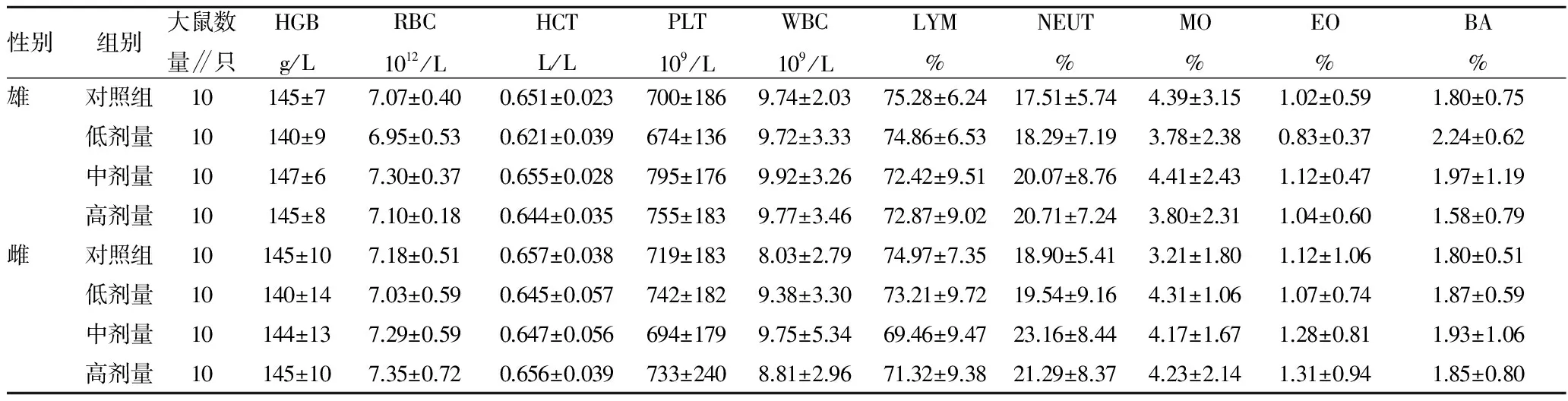
表3 壳聚糖胶囊对大鼠血常规指标的影响
注:表中数据为平均值±标准误。HGB为血红蛋白;RBC为红细胞总数;HCT为红细胞压积;PLT为血小板数;WBC为白细胞计数;LYM为淋巴细胞;NEUT为中性粒细胞;MO为单核细胞;EO为嗜酸性粒细胞;BA为嗜碱性粒细胞。
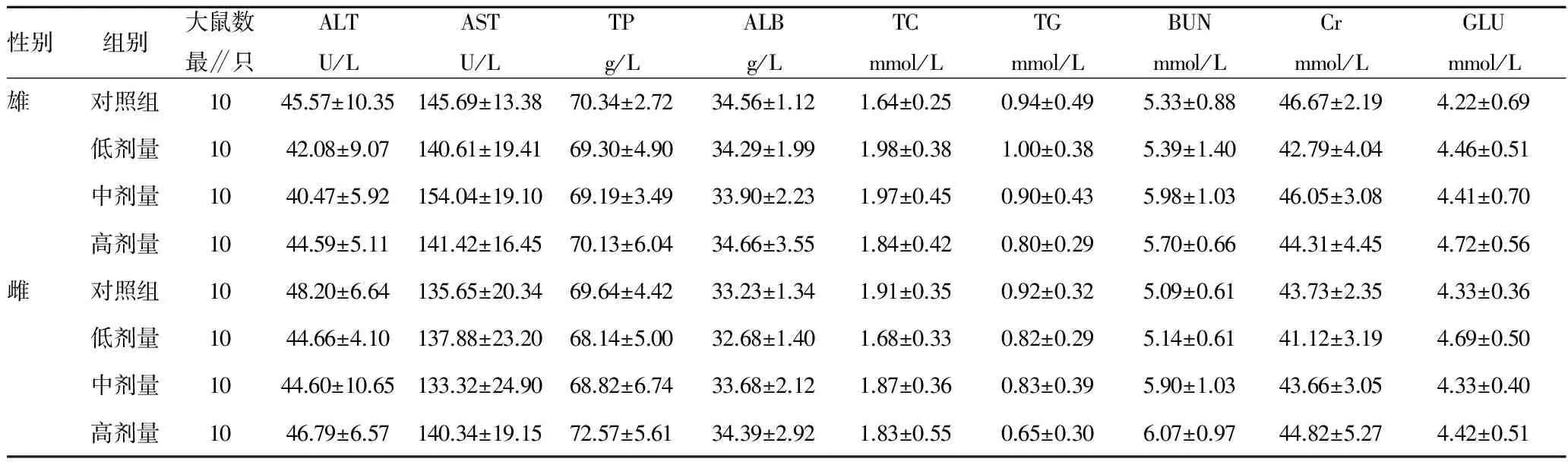
表4 壳聚糖胶囊对大鼠生化指标的影响
注:表中数据为平均值±标准误。ALT为谷丙转氨酶;AST为谷草转氨酸;TP为总蛋白;ALB为白蛋白;TC为胆固醇;TG为甘油三酯;BUN为尿素氮;Cr为肝酐;GLU为血糖。
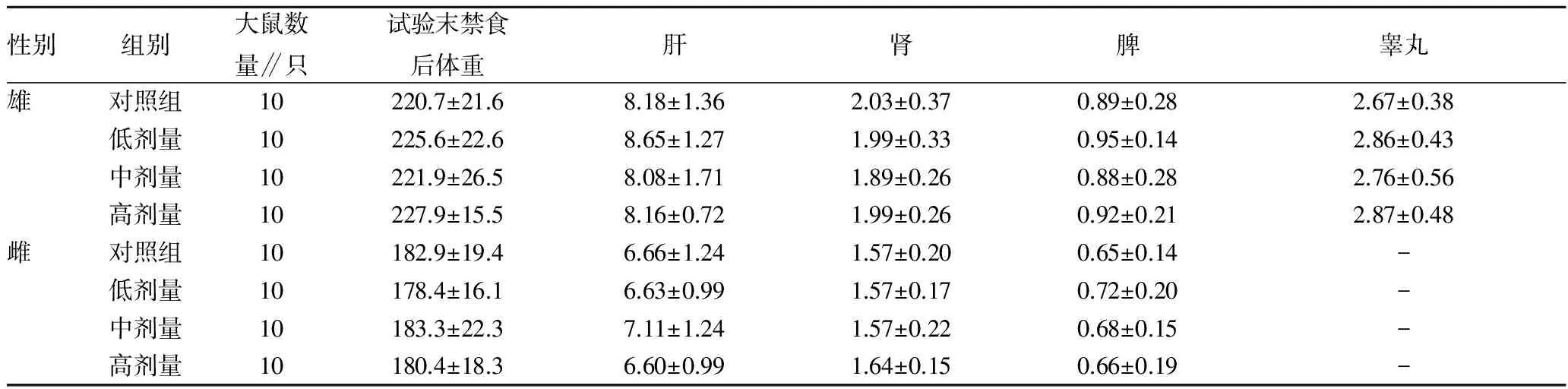
表5 壳聚糖胶囊对大鼠体重及脏器重量的影响 g
注:表中数据为平均值±标准误。
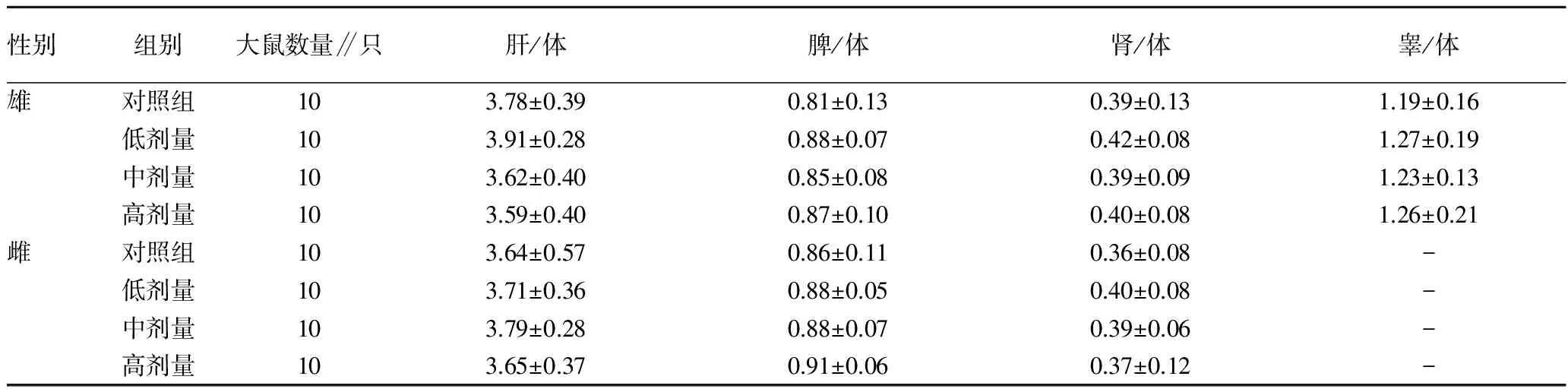
表6 壳聚糖胶囊对大鼠脏器/体重比值的影响 %
注:表中数据为平均值±标准误。
谢无明显影响;大鼠的血常规、血生化指标、脏器重量及脏器/体重比值与对照组比较,无显著性差异(P>0.05),脏器组织未出现明显异常病理学改变。可见在该试验条件下,受试物30 d喂养对大鼠未产生明显毒副作用。
[1] 郭开宇,赵谋明.甲壳素/壳聚糖的研究进展及其在食品工业中的应用[J].食品与发酵工业,2000,26(1):59-64.
[2] 马宁,汪琴,孙胜玲,等.甲壳素和壳聚糖化学改性研究进展[J].化学进展,2004,16(4) :643-653.
[3] 李树品,康战燕,苏学艳.壳聚糖与人体生理机能调节[J].山东科学,1998,11(1):57-62.
[4] 刘丽红.壳聚糖及其衍生物在医药中的应用[J].福建化工,2001(1):13-14.
[5] 中华人民共和国卫生部.保健食品检验与评价技术规范[S].北京:中华人民共和国卫生部,2003:961-1001.
[6] 王莹,徐艺玫,杜勇,等.月见草油软胶囊大鼠30天喂养试验观察[J].疾病预防控制通报,2013(4):89-91.
Thirty Days Feeding Experiment of Chitosan Capsule on Rats
WU Dan et al
(Jiangxi Provincial Center for Drug Evaluation, Nanchang, Jiangxi 330046)
[Objective] To evaluate the toxicology and safety of chitosan capsule. [Methods] Setting low (0.83 g/kg·bw), medium (1.67 g/kg·bw) and high (3.33 g/kg·bw) dose groups and control group; feeding rats for 30 days; observing growth of rats, body weight change and the average intake; calculating food utilization rate, organ weight, and organ/body weight ratio; analyzing biochemical indexes and blood routine indexes; performing gross anatomy and histopathological analysis. [Results] During the experiment, there were no significant differences between the control group and experimental group (P>0.05). There were no abnormal changes associated with chitosan capsules in gross anatomy and histopathological analysis. [Conclusion] There is no obvious side effect of chitosan capsule on rats.
Chitosan; Capsule; Rat; Toxicology; Feeding experiment
吴丹(1983- ),女,江西临川人,主管技师,硕士,从事保健食品研究。
2014-05-04
S 816.4
A
0517-6611(2014)15-04671-02

