有机溶剂稀释与气相色谱-燃烧-同位素质谱(GC-C-IRMS)联用测定食醋中乙酸的δ13C
钟其顶,王道兵,孟 镇,熊正河,王 敏
(1. 天津科技大学,天津 300457;2. 中国食品发酵工业研究院,北京 100027;3.全国食品发酵标准化中心,北京 100027)
食醋是日常生活中的重要食材之一,根据工艺不同可分为酿造醋和配制醋,其中酿造醋[1]根据发酵原料不同,可以分为粮食醋和水果醋。近年来,果醋饮料由于独特的风味和保健作用在世界发达国家受到欢迎,被称作“第四代黄金饮品”。在利益驱动下,部分不法商家通过虚假标注食醋来获取最大市场利益,如将普通食醋虚假标注为果醋。因此,需要建立一种食醋原料溯源的分析方法,以推动食醋市场公平竞争,保护消费者利益。
目前,依据国家标准或行业标准中的物理化学等常规指标只能判定食醋的基本质量,难以有效溯源食醋的发酵原料[2-4]。据报道,产品中碳-13比值(δ13C)与其原料有密切关联,碳同位素技术已被广泛用于原料溯源及产品真实性鉴别[5-13],因此通过测定乙酸中δ13C可溯源食醋的原料来源[14-16]。醋中有机物除乙酸外,还有多种醇、醛、酯类化合物,为避免受到其他有机物的影响,测定乙酸中δ13C时需先提纯乙酸[16]。目前测定食醋中乙酸δ13C主要有两种方法:一种是通过微蒸馏系统提纯食醋中乙酸[16],再采用元素分析仪-同位素质谱(EA-IRMS)进行测定,该方法采用的微蒸馏系统设备昂贵、操作步骤复杂,需尽力避免在蒸馏过程中乙酸的碳同位素分馏影响;另一种是利用气相色谱-燃烧-稳定同位素比值质谱(GC-C-IRMS)测定单体有机物中碳同位素组成[17],考虑到食醋中含水量高达90%以上,且含水量大的样品不能直接进入气相色谱仪,因此需先采用顶空-固相微萃取技术[15-16]萃取食醋中乙酸[18-19],然后用GC-C-IRMS分析测定,但该萃取过程存在同位素分馏作用,且随着固相微萃取头使用次数增加而导致效率降低,进而影响测量的稳定性和准确度,因此该方法至今未被推广应用。
摆脱对复杂前处理步骤的依赖,实现食醋中乙酸的GC直接进样,是利用GC-C-IRMS技术测定乙酸碳同位素的关键。考虑到食醋中乙醇含量在1.19~3.37 g/L之间[20],而乙酸含量高于35 g/L[1],出于增加样品中有机相比例和降低碳同位素测定时信号强度的目的,本研究采用乙醇作为稀释剂[21],利用GC-C-IRMS直接测定食醋中乙酸的碳同位素组成。
1 实验部分
1.1 仪器
Triplus自动进样器,Trace GC气相色谱仪,燃烧转化装置,Delta V Advantage稳定同位素比值质谱仪(δ13C测定内精度≤0.065‰,线性测定范围2~10 V):均为美国Thermo-Fisher公司产品。
1.2 试剂
氦气:纯度大于99.999%;乙醇:国产色谱纯;冰乙酸:国产分析纯,经EA-IRMS标定得δ13CVPDB= -26.41±0.15‰;果醋:2011年FIT-PTS第2轮国际比对样品;6种市售食醋和1个工业醋酸的详细信息列于表1。
1.3 色谱条件
Wax毛细管柱(30 m×0.25 mm×0.25 μm);载气为氦气;柱流速1.2 mL/min;进样口温度300 ℃;升温程序:起始温度120 ℃,保持1 min,以15 ℃/min 升温至200 ℃,保持2 min;进样体积1 μL;分流比20∶1。
1.4 乙酸转化条件
燃烧转化装置(IsoLink)中配备陶瓷(Al2O3)氧化管(填料为CuO,NiO和Pt),工作温度为1 000 ℃,将乙酸转化成CO2。
1.5 样品前处理
根据稳定同位素比值质谱仪的测定线性范围(2~10 V)及色谱条件,用乙醇将食醋样品稀释至乙酸含量约8 g/L。

表1 市售食醋和工业醋酸的详细信息及乙酸碳同位素数据(n=3)Table 1 Details of vinegar samples and acetic acid with isotope ratios measured by GC-C-IRMS(n=3)
注:*原材料代指商品标签所列的原料信息
2 结果与分析
2.1 保留时间的确定
同位素质谱测定乙酸δ13C前,需通过燃烧炉装置将乙酸转化成CO2,为了避免稀释用乙醇溶剂进入燃烧炉影响乙酸转化率,需要准确测定乙醇和乙酸在气相色谱分离中的保留时间;再根据乙醇溶剂保留时间设定反吹(backflush)参数,确保乙醇溶剂全部通过反吹排出。
将乙醇和乙酸的标准品混合物置于顶空进样瓶,取进样瓶上层的乙醇和乙酸混合气体注入GC-C-IRMS进行测定,得到乙醇和乙酸的44、45和46离子流图,示于图1。

图1 GC-C-IRMS测定乙醇和乙酸的44,45和46离子流图Fig.1 Ions chromatography of acetic acid and ethanol 44,45,46 determinated by GC-C-IRMS
由图1可见,乙醇与乙酸可有效分离,保留时间分别为309 s和523 s,可设置在200~400 s期间打开反吹,将乙醇溶剂峰成功排出,从而消除乙醇溶剂对乙酸δ13C测定的影响。
2.2 乙醇稀释法测定乙酸δ13C准确性研究
根据稳定同位素测定要求,测定复杂样品中某一种组分时,必须通过前处理技术将待测组分进行分离、提纯、转化特定气体(如CO或CO2),再进入稳定同位素质谱进行测定。如前面提及的微蒸馏系统提纯食醋中乙酸和固相萃取技术萃取浓缩食醋中乙酸,均属于食醋样品的前处理手段。本研究拟采用乙醇直接稀释后,经毛细管气相色谱柱分离提纯食醋中乙酸。为了验证乙醇稀释前处理技术的稳定性和准确性,模拟配制不同乙酸浓度的水溶液,测定结果列于表2。
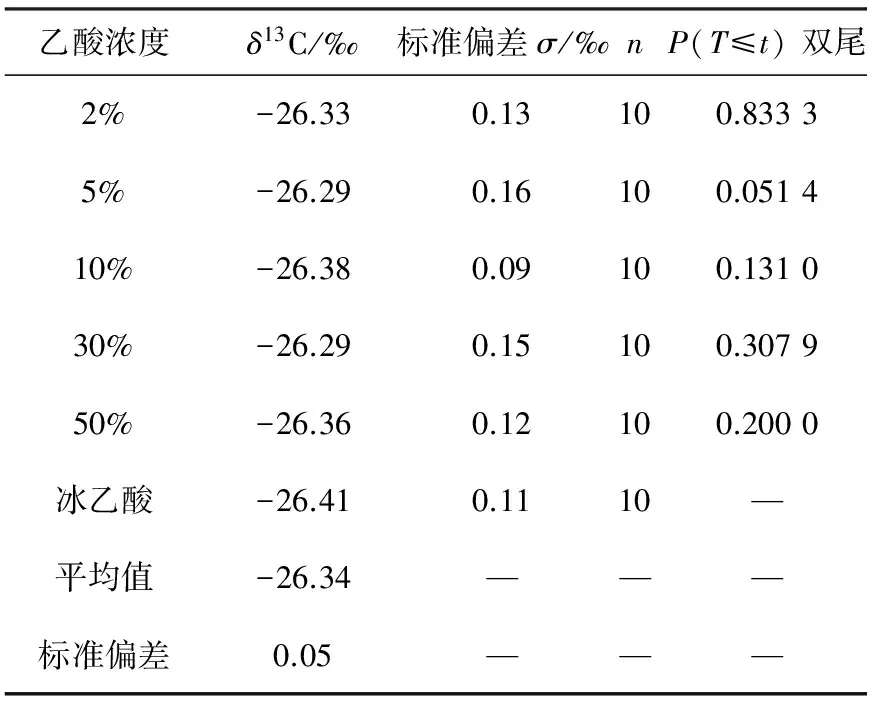
表2 不同浓度乙酸水溶液中乙酸δ13C测定结果Table 2 δ13C-values of acetic acid in acetic acid-water solution with different contents
注:α=0.05时,t双尾临界为2.262 2;P为双层检验概率
从表2可见,5%乙酸溶液中乙酸δ13C的测定结果稳定在-26.28‰~-26.40‰之间,与冰乙酸(δ13C=-26.41‰)十分接近。分别对不同浓度的乙酸溶液同冰乙酸测定值进行t检验分析,P均大于0.05,说明溶液中乙酸δ13C与冰乙酸的测定值无显著性差异,因此,该方法可以用来测定浓度为2%~100%的乙酸溶液。
2.3 食醋中乙酸δ13C测定
选择实际食醋样品进行测定,44、45和46离子谱图示于图2。
从图2可见,食醋样品的乙酸峰对称均匀,与其他杂峰明显分离,避免了未知物质对乙酸δ13C测定的干扰。
2.4 稳定性
2.4.1重复性分析 选择特定食醋样品,重复测定10次,验证该方法的重复性,结果列于表3。

图2 果醋样品乙酸δ13C分析图谱Fig.2 Chromatogram of δ13C of acetic acid in fruit vinegar

表3 食醋中乙酸δ13C重复性测定结果Table 3 Repeatability of δ13C-values of acetic acid in vinegar
由表3可知,本方法连续10次测定食醋样品中乙酸δ13C的标准偏差1σ=0.13‰,不仅满足文献[18]所述的纯乙酸δ13C稳定性的标准偏差σ范围为0.1‰~0.4‰,而且达到稳定同位素质谱精度测试要求小于0.2‰。
2.4.2再现性分析 选择某食醋样品为实验对象,分别置于4个溶剂瓶A、B、C、D中,其中A、B、C和D分别在第1天、第3天、第5天、第7天进行测定,结果列于表4。
结果表明,该方法的标准偏差为0.05‰,再现性较好,能满足重复测定的要求(小于0.2‰)。
2.5 准确性验证
实验室在2011年参加由欧盟联合研究中心(JRC)支持的稳定同位素实验室间能力验证计划(FIT-PTS)。实验室按照本研究所建立的乙醇溶剂稀释法结合气相色谱-同位素质谱(GC/IRMS)测定欧盟邮递的以水果为原料的食醋中乙酸δ13C,结果列于表5。
由表5可见,通过不同时间的再现性测试,样品中乙酸的δ13C均十分稳定,平均值为-25.66,不同天数12次测定的标准偏差为0.06‰,符合测定要求。本实验室向欧盟提交了果醋中乙酸δ13C的测试结果(实验室编号D6),并得到了数据反馈,列于表6和图3(除D6外,其余7个实验室均采用微蒸馏装置将乙酸从食醋中提纯后,再用EA-IRMS进行测定)。

表4 食醋中乙酸δ13C再现性测定结果Table 4 Reproducibility of δ13C-values of acetic acid in vinegar

表5 果醋中乙酸δ13C重复性测定结果Table 5 Repeatability of δ13C-values of acetic acid in fruit vinegar
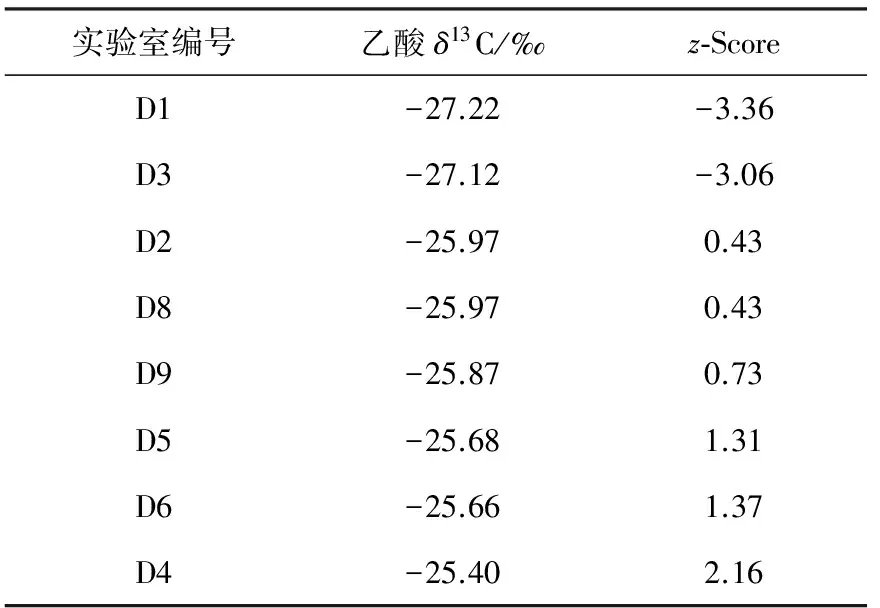
表6 FIT-PTS国际实验室比对结果Table 6 Results of FIT-PTS inter-laboratory comparison study

图3 FIT-PTS项目中果醋样品乙酸δ13C的标准得分(z-Score)图Fig.3 z-Score for δ13C of acetic acid in vinegar
由表6和z-score可知,编号为D1、D3和D4的实验室测定结果明显偏离(≤-2σ或≥2σ),超出正常波动测定范围。剔除上述3个离散数据后,其余数据的平均值为-25.83‰,1σ=0.15‰,与本方法测得的结果相差0.17‰,达到国际实验室间比对的能力验证范围(小于0.3‰)。通过本次国际间比对实验说明,当前采用微蒸馏提纯食醋中乙酸的方法在不同实验室间仍存在较大偏差,稳定性和操作误差仍有待提高;同时,本研究所建立的GC-C-IRMS方法适用于食醋中的乙酸同位素测定,结果准确、操作简便快捷。
2.6 食醋样品分析
应用本方法测定表1中列出的市售食醋样品及工业醋酸中乙酸δ13C。结果表明,食醋的原料不同时,乙酸δ13C也有差异,B与C均为米醋,但B中加入了食用醋酸使得乙酸δ13C偏正,该食用醋酸可能由玉米等C3植物发酵而来;D与E均为老陈醋(3年),乙酸δ13C不同可能是由于不同产品中原料(配比)不尽相同;G为工业醋酸,其δ13C最偏负。由此可知,根据食醋中乙酸δ13C可溯源其发酵原料,也可定性鉴别食醋中是否含有工业醋酸。
3 结论
采用乙醇作为稀释溶剂,基于毛细管气相色谱柱分离技术,可在不引起食醋中乙酸碳同位素分馏的情况下进行分离纯化,通过燃烧炉和稳定同位素质谱实现对食醋中乙酸δ13C的准确测定。该方法的精密度和稳定性好、准确性高、操作简便快速,适合推广应用,为我国进一步规范食醋和果醋市场提供技术支撑。
参考文献:
[1] GB 18187—2000 酿造食醋 [S].北京:中国标准出版社,2000.
[2] 王 慧.电子舌在食醋品质检测及食醋发酵过程监控中的应用[D].镇江:江苏大学,2009.
[3] 李先端,马志静,张丽宏.酿造醋和配置醋质量分析与鉴别[J].中国食物与营养,2011, (2):27-31.
LI Xianduan, MA Zhijing, ZHANG Lihong, et al. Quality analysis and distinction about brewed vinegar and prepared vinegar [J].Food and Nutrition in China, 2011, (2):27-31(in Chinese).
[4] 刘晓伟. 酿造食醋原汁含量检测方法研究[D].中南林业科技大学,2010.
[5] SUHAJ M, KOREKOVSKM. Study of some European cheeses geographical traceability by pattern recognition analysis of multielemental data [J]. Eur Food Res Technol, 2008, 227(5):1 419-1 427.
[6] 费晓庆,吴 斌,沈崇钰,等. 液相色谱/元素分析-同位素比值质谱联用法鉴定蜂蜜掺假[J].色谱,2011,29(1):15-19.
FEI Xiaoqing, WU Bin, SHEN Chongyu, et al, Honey adulteration detection using liquid chromatography/elemental analysis-isotope ratio mass spectrometry [J]. Chinese Journal of Chromatography, 2011, 29(1):15-19(in Chinese).
[7] CAMIN F, PERINI M, COLOMBARI G, et al. Influence of dietary composition on the carbon, nitrogen, oxygen and hydrogen stable isotope ratios of milk[J]. Rapid Commun Mass Spectrom, 2008, 22(11):1 690-1 696.
[8] RODRIGUES C I, MAIA R, MIRANDA M, et al.
Stable isotope analysis for green coffee bean: A possible method for geographic origin discrimination[J]. Journal of Food Composition and Analysis, 2009, 22(5): 463-471.
[9] ANDREA A, ALESSANDRO B, GIANCARLO C, et al. Natural origin of ascorbic acid: Validation by13C NMR and IRMS[J]. Food Chemistry, 2008, 112(3): 715-720.
[10] GUO B L, WEI Y M, PAN J R, et al. Stable C and N isotope ratio analysis for regional geographical traceability of cattle in China[J]. Food Chemistry, 2010, 118(4): 915-920.
[11] SPITZKE M E, FAUHL-HASSEK C. Determination of the13C/12C ratios of ethanol and higher alcohols in wine by GC-C-IRMS analysis[J]. European Food Research and Technology, 2010, 231(2): 247-257.
[12] CAMIN F, LARCHER R, PERINI M, et al. Ch-
aracterisation of authentic Italian extra-virgin olive oils by stable isotope ratios of C, O and H and mineral composition[J]. Food Chemistry, 2010, 118(4): 901-909.
[13] MARDEGAN S F, ANDRADE T M B, de SOU-
SA NETO E R, et al. Stable carbon isotopic composition of Brazilian beers: A comparison between large- and small-scale breweries[J]. Journal of Food Composition and Analysis, 2013, 29(1): 52-57.
[14] SCHMID E R, GRUNDMANN H, FOGY I,et al.
Intramolecular13C/12C isotope ratios of acetic acid of biological and synthetic origin [J]. Biological Mass Spectrometry, 1981, 8(10): 496-499.
[15] REMAUD G, GUILLOU C, VALLET C,et al. A coupled NMR and MS isotopic method for the authentication of natural vinegars[J]. Fresenius' Journal of Analytical Chemistry,1992,342(4/5):457-461.
[16] THOMAS F, JAMIN E. H-NMR and13C-IRMS analyses of acetic acid from vinegar,18O-IRMS analysis of water in vinegar: International collaborative study report [J]. Analytica Chimica Acta,2009,649(1):98-105.
[17] SERRA F, JANEIRO A, CALDERONE G, et al.
Inter-laboratory comparison of elemental analysis and gas chromatography combustion isotope ratio mass spectrometry (GC-C-IRMS). Part I : d13C measurements of selected compounds for the development of an isotopic Grob-test[J]. J Mass Spectrom, 2007,42(3):361-369.
[18] HATTORI R, YAMADA E, SHIBATA H, et al.
Measurement of the isotope ratio of acetic acid in vinegar by HS-SPME-GC-TC/C-IRMS [J]. Journal of Agricultural and Food Chemistry, 2010, 5 (1):7 115-7 118.
[19] 李心清,黄代宽,章炎麟,等. 针式微萃取结合GC-IRMS测定水溶液中甲酸、乙酸的稳定碳同位素组成[J]. 地球化学, 2008, 37(6): 549-555.
LI Xinqing, HUANG Daikuan, ZHANG Yanlin, et al. Measurement of stable carbon isotopic compositions of formic and acetic acids in aqueous solution by needle trap coupled with GC-IRMS[J]. Geochimica, 2008, 37(6): 549-555(in Chinese).
[20] 李艳青,付大友,王 蓉. 食醋中乙醇含量的测定[J]. 四川理工学院学报:自然科学版,2009,2(1):72-74.
LI Yanqing, FU Dayou, WANG Rong. Determination of alcohol content in vinegar[J]. Journal of Sichuan University of Science & Engineering (Nature Science Edition), 2009, 2(1): 72-74(in Chinese).
[21] CALDERONE G, NAULET N, GUILLOU C, et al.
Characterization of European wine glycerol: Stable carbon isotope approach[J]. J Agric Food Chem, 2004, 52 (19): 5 902-5 906.

