妇科止带片微生物限度检查的方法学验证研究
杨春杰,丁连峰,马 凯,刘超祥
(1.安徽济人药业有限公司;2.亳州职业技术学院,安徽 亳州 236800)
妇科止带片微生物限度检查的方法学验证研究
杨春杰1,丁连峰1,马 凯1,刘超祥2
(1.安徽济人药业有限公司;2.亳州职业技术学院,安徽 亳州 236800)
目的 建立妇科止带片微生物限度检查方法。方法 采用薄膜过滤法进行细菌数计数,采用平皿法进行霉菌和酵母菌计数,采用常规法进行控制菌的检查。结果 大肠埃希菌、白色念珠菌、黑曲霉菌回收率皆在 80%以上;金黄色葡萄球菌、枯草芽孢杆菌回收率皆在95%以上;阴性菌对照组均无生长。结论 该法可以作为妇科止带片的微生物限度检查方法。
妇科止带片;微生物限度检查法;薄膜过滤法;平皿法;方法学验证
妇科止带片具有清热燥湿、收敛止带,用于慢性子宫颈炎、子宫内膜炎、阴道黏膜炎等引起的湿热型赤白带症。该片剂具有中等抗菌活性,使微生物限度检查结果不准确,给临床使用带来隐患;为保证微生物限度检查方法及结果的有效性,对具有抗菌活性的药品进行微生物限度检查,应首先消除其抗菌活性,并通过实验验证抗菌活性去除效果[1-2]。本实验在对妇科止带片进行微生物限度检查时采用薄膜过滤的方法,建立对妇科止带片的微生物限度检查方法,该方法可有效地消除妇科止带片的抑菌作用。
1 仪器与材料
仪器:YJA型均浆仪(台州市椒江五星试压设备有限公司),NS01-75D4型专用滤膜(孔径:0.45 μm),NS01-D7型双联导液管套装及 NS01-D5型可重复消毒薄膜过滤器,SPX-150B生化培养箱(上海博迅实业有限公司),MJX-160B霉菌培养箱(上海博迅实业有限公司),HPX-9082MBE电热恒温培养箱(上海博迅实业有限公司),AR5120电子分析天平(奥豪斯国际贸易有限公司)。
样品:妇科止带片(规格:每片0.36 g,安徽济人药业有限公司)。
培养基:玫瑰红钠琼脂培养基(批号1210183)、营养琼脂培养基(批号 130118)、营养肉汤培养基(批号121022)、改良马丁琼脂培养基 (批号010520)、胆盐乳糖培养基(批号1301173)、麦康凯琼脂培养基(批号130304)、4-甲基伞形酮葡糖苷酸(批号121022)、胆盐硫乳琼脂培养基 (批号130129)、四硫磺酸钠亮绿培养基(批号1301242)、三糖铁琼脂培养基(批号121022)。以上培养基均由北京三药科技开发公司生产,灵敏度实验符合《中国药典》2010年版规定,配制后的pH需符合规定,若不相符需进行调整[3-4]。试剂:无菌氯化钠—蛋白胨缓冲液(pH=7.0,北京三药科技开发公司生产),氯化钠(分析纯,上海市申翔化学试剂有限公司生产),聚山梨酯80(上海市申宇医药化工有限公司生产)。
菌种:大肠埃希菌(Escherichia coli)[CMCC (B)44 102]、金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26 003]、枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63 501]、白色念珠菌(Candida albicans)[CMCC(F)98 001]、黑曲霉(Aspergillus niger)[CMCC(F)98 003]、乙型副伤寒沙门菌(Salmonella paratyphi B)[CMCC(B)50094](中国食品药品检定研究院)。
2 方法与结果
参照《中国药典》2010版微生物限度检查法实验[5]。
2.1 菌液制备
2.1.1 细菌菌液的制备 接种金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌、乙型副伤寒沙门菌的新鲜培养物至营养肉汤培养基中,经30~35℃培养18~24 h。接种白色念珠菌的新鲜培养物至改良马丁培养基中,23~28℃培养 24~48 h。上述培养物用质量分数为0.9%无菌氯化钠溶液稀释10倍,白色念珠菌至 10-5、黑曲霉菌至 10-4、金黄色葡萄球菌至 10-7、大肠埃希菌至 10-7、枯草芽孢杆菌至10-5和乙型副伤寒沙门菌至 10-8。制成每 1 mL含菌数约为50~100 cfu(菌落形成单位)的菌悬液,备用,菌落计数结果见表1。

表 1 试验用菌检查(菌落计数平均值,cfu·mL-1)
2.1.2 真菌菌液的制备 接种黑曲霉菌的新鲜培养物至改良马丁培养基中,23~28℃培养5~7 d,加3~5 mL含0.05%(v/v)聚山梨酯80的0.9%无菌氯化钠溶液,将黑曲霉孢子洗脱,吸出孢子至无菌试管内,用含0.05% (v/v)聚山梨酯80的0.9%无菌氯化钠溶液稀释,用标准比浊管比浊,其浊度与标准比浊管相当后,取1 mL稀释后的孢子悬液,用0.05% (v/v)聚山梨酯80的0.9%无菌氯化钠溶液10倍稀释至10-4,制成每1 mL含菌数约为50~100 cfu的菌悬液,备用。上述各株菌的培养物均为第三代的培养物。
2.2 菌液检验
2.2.1 细菌菌液的检验 取上述金黄色葡萄球菌至10-7、枯草芽孢杆菌至10-5、大肠埃希菌至 10-7、乙型副伤寒沙门菌至10-8的稀释液各1 mL,分别用45℃营养琼脂培养基 20 mL注皿,各平行测定两皿。30~35℃培养48 h,计数,应约为50~100 cfu·mL-1。
2.2.2 真菌菌液的检验 取上述白色念珠菌至10-5的稀释液及上述黑曲霉菌至 10-4孢子悬液各 1 mL,分别用45℃玫瑰红钠琼脂培养基20 mL注皿,各平行测定两皿,23~28℃培养,逐日观察计数,应约为50~100 cfu·mL-1。
2.3 细菌、霉菌及酵母菌计数方法的验证 供试液制备:取供试品 10 g置无菌的匀浆罐中,加入45℃无菌氯化钠—蛋白胨缓冲液(pH=7.0)至 100 mL,匀浆2 min(3 000 r·min-1),制成质量浓度为100 g·L-1的供试液。
(1)平皿法:试验组:取供试液1 mL加入平皿后,加入上述相应的 50~100 cfu·mL-1的试验菌 1 mL,然后每皿注入20 mL营养琼脂培养基或玫瑰红钠琼脂培养基,摇匀,在规定温度培养,观察结果。
菌液组:取上述50~100 cfu·mL-1的试验菌各1 mL,然后每皿注入20 mL营养琼脂
培养基或玫瑰红钠琼脂培养基,摇匀,在规定温度培养,观察结果。
供试品对照组:取供试液1 mL加入平皿后,然后每皿注入 20 mL营养琼脂培养基或玫瑰红钠琼脂培养基,摇匀,在规定温度培养,观察结果。按如下公式计算试验组的加菌回收率(公式1):
加菌回收率%=(试验组菌落数均值 -供试品对照组菌落数均值)/菌液组菌落数均值 ×100%。
(2)培养基稀释法:试验组:取供试液分别按每皿0.5 mL、每皿0.2 mL加入平皿后,加入上述相应的50~100 cfu·mL-1的试验菌菌液 1 mL,然后每皿注入20 mL营养琼脂培养基或玫瑰红钠琼脂培养基,摇匀,在规定温度培养,观察结果。
菌液组:同平皿法。
供试品对照组:除不加菌液外,同试验组测定方法,置规定温度培养,观察结果。按公式1计算试验组的加菌回收率。
(3)薄膜过滤法:试验组:取供试液10 mL以500 r·min-1离心5 min后,取上清液 1 mL加入薄膜过滤器(滤膜先用水冲洗液润湿)中,用500 mL无菌氯化钠—蛋白胨缓冲液 (pH=7.0)冲洗,每次100 mL,在最后一次冲洗液中加入上述相应的50~100 cfu·mL-1的试验菌 1 mL,冲洗完毕后,滤干,取出滤膜贴于营养琼脂培养基或玫瑰红钠琼脂培养基上,置规定温度培养,观察结果。
菌液组:除不加供试液外,同试验组操作,置规定温度培养,观察结果。
供试品对照组:除不加菌液外,同试验组操作,置规定温度培养,观察结果。
按公式1计算试验组的加菌回收率。
2.4 控制菌检查方法的验证
2.4.1 大肠埃希菌:按常规法 试验组:取质量浓度为100 g·L-1供试液10 mL加入100 mL胆盐乳糖培养基中,加入上述50~100 cfu·mL-1的大肠埃希菌菌液1 mL,置30~35℃培养18~24 h,按相应的控制菌的检查法检查。
阴性对照组:取稀释液 10 mL加入 100 mL胆盐乳糖培养基中,置30~35℃培养18~24 h,按相应的控制菌的检查法检查。
阳性对照组:取上述50~100 cfu·mL-1的大肠埃希菌菌液1 mL加入100 mL胆盐乳糖培养基中,置30~35℃培养18~24 h,按相应的控制菌的检查法检查。
供试品组:取质量浓度为100 g·L-1供试液供试液10 mL加入100 mL胆盐乳糖培养基中,置30~35℃培养18~24 h,按相应的控制菌的检查法检查。
阴性菌对照组:阴性对照菌采用金黄色葡萄球菌,方法同试验组,阴性对照菌不得检出。
2.4.2 沙门菌:按常规法 试验组:取供试品10 g,加入200 mL的营养肉汤培养基中,混匀,加入上述50~100 cfu·mL-1的乙型副伤寒沙门菌菌液1 mL,置30~35℃培养18~24 h,按相应的控制菌的检查法检查。
阴性对照组:取200 mL的营养肉汤培养基,置30~35℃培养 18~24 h,按相应的控制菌的检查法检查。
阳性对照组:取上述50~100 cfu·mL-1的乙型副伤寒沙门菌菌液 1 mL,置 30~35℃培养 18~24 h,按相应的控制菌的检查法检查。
供试品组:取供试品 10 g加入 200 mL的营养肉汤培养基中,置 30~35℃培养 18~24 h,按相应的控制菌的检查法检查。
阴性菌对照组:阴性菌对照组采用金黄色葡萄球菌,方法同试验组,阴性对照菌不得检出;实验结果见表2。
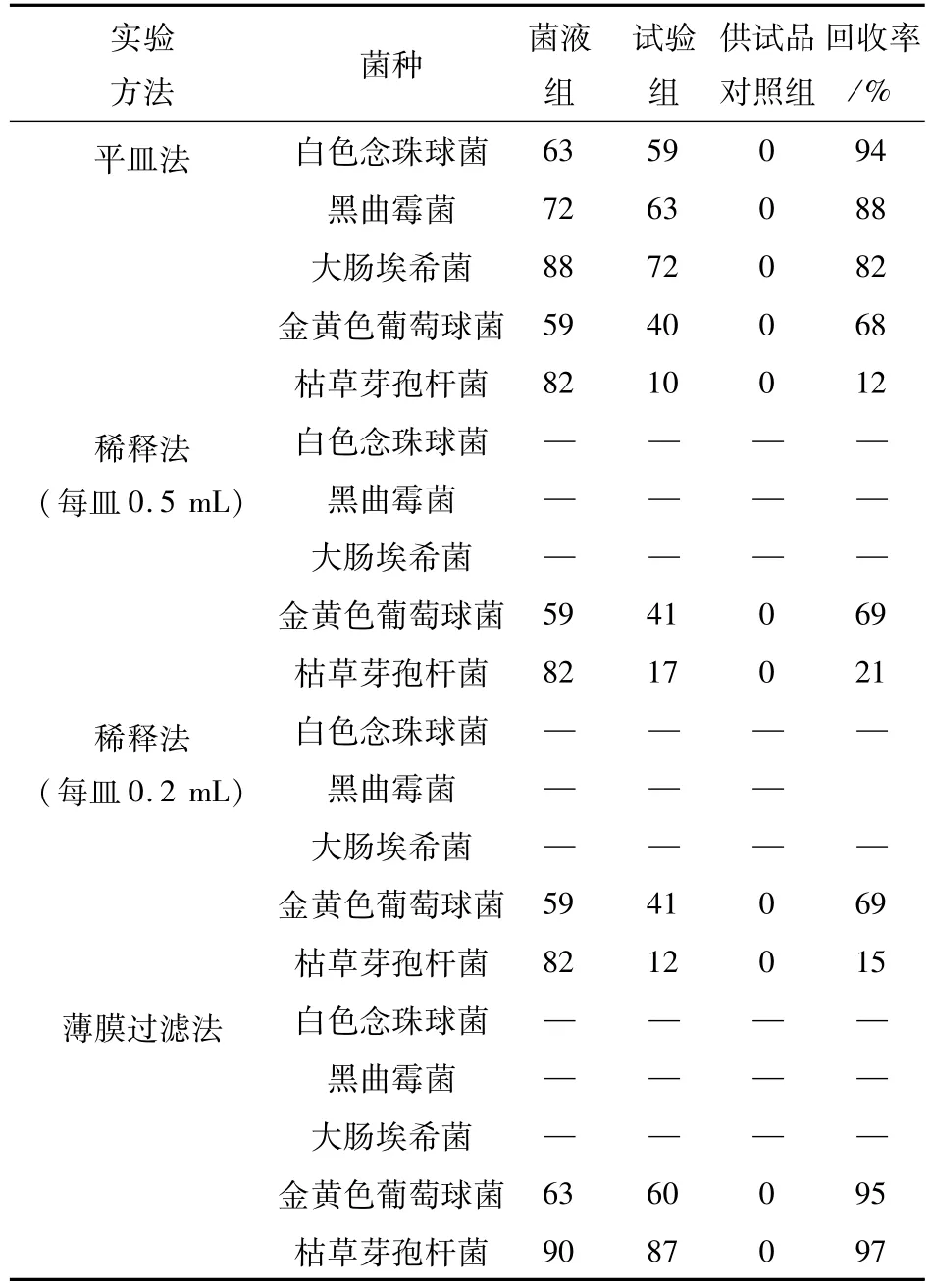
表2 不同菌种计数方法的验证(cfu)

表3 控制菌检查方法的验证结果
3 讨论
在细菌、霉菌和酵母菌数检查的方法验证试验中,平皿法对大肠埃希菌、白色念球菌、黑曲霉菌的回收率均高于80%;采用平皿法及培养基稀释法每皿0.2 mL、每皿0.5 mL对金黄色葡萄球菌、枯草芽孢杆菌的回收率不能达到 70%,采用薄膜过滤法对金黄色葡萄球菌、枯草芽孢杆菌的回收率高于95%。结合细菌、霉菌和酵母菌的验证实验结果,当采用薄膜过滤法时能满足细菌检查的基本要求,采用平皿法时能满足霉菌和酵母菌检查的基本要求。
实验时稀释液及培养基的温度对实验结果存在影响,应使稀释液及培养基温度约在45℃。温度过低不能充分溶解样品及稀释,温度过高容易杀害实验中验证用菌,均影响检验结果[6]。
实验中加入相应菌液的意义在于明确采用的实验方法是否可以将药品抑菌作用消除,如果加入菌液生长良好,则说明供试品在该检验条件下无抑菌作用或抑菌作用基本可以忽略不计,可以照此实验条件继续进行验证。如果相应菌株生长微弱、缓慢或不生长,则说明此试验条件不能完全除去药品的抑菌作用,不能照此实验条件继续进行验证,应进行进一步调整以达到完全去除供试品抑菌作用[7]。
从表3可以看出阴性菌对照组中阴性菌未检出,控制菌大肠埃希菌和沙门菌的检查可采用常规法。
综合分析,妇科止带片微生物限度检查标准如下:取本品10 g,加无菌氯化钠—蛋白胨缓冲液(pH =7.0)至100 mL,制成质量浓度为 100 g·L-1的供试液。取该供试液 10 mL以 500 r·min-1离心5 min后,取上清液1 mL采用薄膜过滤法以每次100 mL冲洗总量为400mL的无菌氯化钠—蛋白胨缓冲液 (pH=7.0),滤干后取膜贴于营养琼脂培养基上培养进行细菌数测定;取质量浓度为 100 g·L-1的供试液1 mL用平皿法进行霉菌和酵母菌计数;取质量浓度为100 g·L-1的供试液 10mL按常规法进行大肠埃希菌的检查,取供试品10 g按常规法进行沙门菌的检查。
[1] 潘友文.现代医药工业微生物实验室质量管理与验证技术[M].北京:中国协和医科大学出版社,2004:179-185.
[2] 杨 静.药品微生物限度检查法的影响因素分析[J].中国药事,2008,22(12):133-135.
[3] 马绪荣,苏德模.药品微生物学检验手册[M].北京:科学出版社,2001:403-413.
[4] 纪绍梅,严德喜.微生物培养基质控与图解[M].北京:北京科学技术出版社,2006:18-23.
[5] 国家药典委员会.中国药典:一部[S].北京:中国医药科技出版社,2010:79-88.
[6] 李云龙.中国药品检验标准操作规范[S].北京:中国医药科技出版社,2010:354-355.
[7] 刘 鹏,马仕洪.普卢利沙星薄膜衣片微生物限度检查法的建立[J].中国药事,2013,27(4):413-415.
Methodological validation method for microbial limit test of fukezhidai tablets
YANG Chun-jie,DING Lian-feng,MA Kai,et al
(Anhui Jiren Pharmaceutical Industries Co.,Ltd,Bozhou,Anhui 236800,China)
Objective To establish a microbial limit test for fukezhidai tablets.Methods We used membrane filtration method for bacterium,plate method for fungus and yeast test,conventional test method for control bacteria examination.Results The recovery rates of Escherichia coli,Candida albicans and Aspergillus niger were all more than 80%and more than 95%for Staphylococcus aureus and Bacillus subtilis.Negative control group had no growth.Conclusions The method can be used to examine microbial limit of fukezhidai tablets.
fukezhidai tablets;microbial limit test;membrane filtration method;plate method;methodological validation
10.3969/j.issn.1009-6469.2014.03.015
2013-08-25,
2013-12-23)
杨春杰,男,副研究员,研究方向:中药制剂,E-mail:yangchunjie8@126.com

