萃取法分离柠檬酸的研究进展
鞠辉,杨慧茹,魏琦峰,任秀莲,董慧栓
(哈尔滨工业大学(威海)海洋科学与技术学院,山东 威海 264209)
萃取法分离柠檬酸的研究进展
鞠辉,杨慧茹,魏琦峰,任秀莲,董慧栓
(哈尔滨工业大学(威海)海洋科学与技术学院,山东 威海 264209)
柠檬酸是世界上产量最大发酵产品之一,是一种重要的有机酸。本文较全面地总结了近年来液-液萃取法和液膜萃取法分离纯化柠檬酸的原理和优缺点,详细讨论了这两种体系的发展现状况以及亟待解决的问题,这两种方法均具有污染小、萃取率高、成本低等优点,但是由于发酵液中含有蛋白质、多糖等乳化剂,使得这两种均有易乳化的缺点,并且液膜萃取法操作复杂。基于这两种方法的不足之处,提出了将离子液体运用到柠檬酸的萃取体系中,具有很大的发展空间,既保证了萃取法本身的优势,又克服了易乳化的缺点,同时离子液体可以循环使用,能源效率高,分离成本低。
柠檬酸;萃取法;分离;提取
柠檬酸(又称枸橼酸),化学名为2-羟基丙烷-1,2,3-三羧酸,是一种天然的果酸[1],是世界上除酒精发酵外产量最大的发酵产品[2],用途十分广泛,主要用于食品行业,化工中常将其运用到湿法冶金中的浸出剂[1]、提取果胶[3]或甲壳素[4]等。每年世界上有机酸生物制品的产量超过170万吨,其中柠檬酸生物制品占重要地位。据统计,柠檬酸生物制品量将以每年高达5%的增长率上升[5]。目前,常用微生物发酵法生产柠檬酸发酵液,因此后期分离提取则是关键部分,寻找经济而合理的分离纯化柠檬酸的方法一直是人们关注的热点。本文对萃取法分离提取柠檬酸的各种方法进行综述和评述。
1 液-液萃取法分离纯化柠檬酸
液-液萃取柠檬酸的基本原理是相似相容原理:利用原料液中柠檬酸和其他成分在有机相中溶解度的差异,将柠檬酸从水相转移到有机相而达到分离的目的。液-液萃取法有其自身的特点:在提取过程中不会产生大量废渣,有利于环保;萃取率高;可连续性操作;萃取剂可以反复使用,生产成本较低。
在柠檬酸的萃取过程中,由于其亲水性较强,一般采用化学萃取法。化学萃取法按萃取机理可分为:中性络合萃取和离子缔合萃取。按萃取剂种类分为:磷氧类萃取剂和胺类萃取剂。通常萃取体系中包含主体萃取剂、相调节剂和稀释剂三部分,主体萃取剂的作用是与被分离物柠檬酸发生反应,生成络合物等;相调节剂可以调节萃取体系的极性,从而增加了络合物在有机相中的溶解度,并且防止第三相的形成;稀释剂的作用是改善有机相的物理性质,降低萃取体系的成本。
1.1 磷氧类萃取剂对柠檬酸的络合萃取
磷氧类萃取剂一般为中性有机磷类和亚砜类,P=O官能团氧原子上有孤对电子,而被分离物柠檬酸中的—COOH中氢原子为裸露的原子核,二者以氢键结合形成缔合物实现络合萃取[6],其与羧酸的反应可表示为式(1)。

江玉明等[7]研究了以中性磷类TRPO和TBP作萃取剂,分别与柠檬酸形成的萃合物结构式为C6H8O7·2TRPO·H2O和C6H8O7·3TBP·2H2O,实验结果显示TRPO对柠檬酸的萃取能力高于TBP;金寄春等[8]使用80%石油亚砜甲苯溶液萃取柠檬酸,6% NaCl水溶液作为反萃剂,其萃取率高于相同条件下磷酸三丁酯的萃取率,同时,石油亚砜萃取含Ca2+、Mg2+和 Fe3+的柠檬酸时能选择性萃取柠檬酸,但Fe3+会同时被石油亚砜萃取。
1.2 胺类萃取剂对柠檬酸的络合萃取
伯胺、仲胺和叔胺属于中强的Lewis碱性萃取剂,与Lewis酸类有机物的中性分子作用生成离子对萃合物,进入有机相[6]。叔胺与羧酸反应表示如式(2)。

例如 Bayazit等[9]对两种胺类萃取剂三月桂胺和Amberlite LA-2进行对比,其中三月桂胺为长链叔胺,Amberlite LA-2为仲胺的混合物,分别使用甲基异丁基酮、甲苯、环己烷、异辛醇、1-辛醇作为相调节剂,结果显示,30% Amberlite LA-2、20% 1-辛醇的萃取体系,萃取效率最高,达到99.05%。
季铵盐属于强碱性萃取剂,本身含有阳离子R4N+,所以能直接与Lewis酸性有机物的阴离子进行阴阳离子交换,形成萃合物,完成萃取分离过程[6]。季铵盐与羧酸反应表示如式(3)。
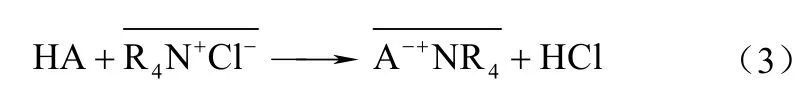
例如Uslu等[10]采用体积比为1∶1的三辛基甲基氯化铵-1-丙醇(或1-辛醇或1-癸醇)体系萃取柠檬酸,起始浓度为 1.775 mol/L的三辛基甲基氯化铵-1-丙醇体系可使柠檬酸的萃取率达到69.76%。当只改变稀释剂的种类,萃取率变化为:1-丙醇≫1-辛醇>1-癸醇>(1-丙醇+1-辛醇)>(1-丙醇+1-癸醇)>(1-辛醇+1-癸醇),结果显示随着脂肪链碳数的逐渐增大,溶剂的萃取能力下降。
王志华等[11]采用伯胺N1923-煤油-A1416体系萃取柠檬酸,实验结果说明有机相中有 N1923· (2/3)H3A和N1923·H3A两种萃合物,且以前者为主,即萃合物中N1923∶H3A=1.5∶1(摩尔比),所以在H3A的摩尔分数为0.42时,有机相中柠檬酸的平衡浓度达到极大值。Heyberger等[12]研究在叔胺体系中第三相的形成条件,使用1-辛醇或者氯仿与正庚烷的混合物作为二元稀释剂,在25 ℃无水体系中进行,当1-辛醇的质量分数在13%以上或者氯仿质量分数在21%以上时,则没有第三相的形成,并且1-辛醇的效果优于氯仿。除了这两类萃取剂外,Lintomen等[13]使用酯类萃取剂三辛酸甘油酯和醇类稀释剂,利用实验所得数据进行模拟,得到的模型与实验数据偏差低于1.28%。
萃取剂对萃取率有直接的影响,同时相调节剂也对萃取率有影响。本文作者在萃取柠檬酸发酵液时发现:使用正辛醇或异辛醇作为相调节剂,相同条件下前者萃取率更高,且分层时间更短。当主体萃取剂浓度一定时,相调节剂占萃取剂体积分数超过45%时,对萃取率基本没有影响[14]。Inci等[15]使用环己烷、2,2,4-三甲基戊烷、1-丁醇、甲苯、甲基异丁基酮和乙酸乙酯作为相调节剂进行研究,其中使用57% 2,2,4-三甲基戊烷、甲基异丁基酮和初始浓度1.74 mol/L的三辛基甲基氯化铵体系时,萃取率最高。Prochazka等[16]对甲基异丁基酮、氯仿和1-辛醇这3种相调节剂进行比较,实验结果显示,甲基异丁基酮可以在较高的酸溶液中超载胺,而后两者则不能,并且随着胺浓度的增加,柠檬酸的萃取率增加,而温度升高,柠檬酸的萃取率则降低。
通常研究者使用萃取法从柠檬酸发酵液中分离提取柠檬酸,Ali等[17]利用 K2HPO4缓冲溶液或者K2HPO4-甲醇溶液从土壤中萃取柠檬酸,实验结果显示土壤中有机表面地平线中柠檬酸的浓度高于淋溶层,并且柠檬酸的含量高于其他低分子量酸的含量。
2 液膜萃取法分离纯化柠檬酸
液膜萃取法主要分为乳化液膜(emulsion liquid membrance,ELM)和支撑液膜(SLM)两种方法,其基本分离原理是根据原料液和反萃相被分离组分柠檬酸的浓度梯度,将柠檬酸从原料液进入膜相,再转入反萃相,而得到柠檬酸或柠檬酸盐。
2.1 乳化液膜分离法
在乳状液膜法ELM中,有机相中加入反萃相,进行高速搅拌,形成W/O型乳化液,分散于原料液中,由于乳化液中萃取剂对原料液中柠檬酸具有高选择性,使柠檬酸与膜内相萃取剂反应得到络合物,推动力为浓度梯度,使得络合物向内相传递,与反萃相接触进行反应,得到柠檬酸或柠檬酸盐,由图1所示。
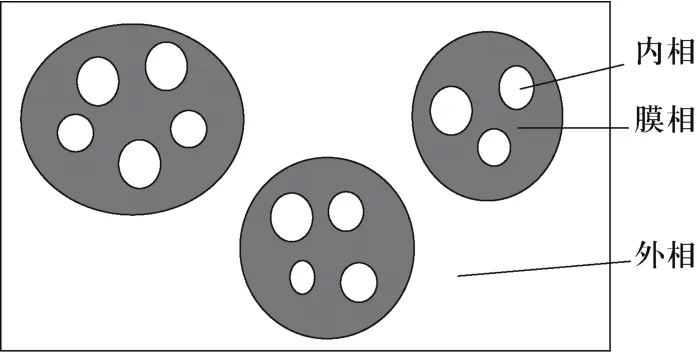
图1 乳状液膜示意图
乳状液膜根据成膜流体的不同,分为(W/O)/W和(O/W)/O两种,柠檬酸萃取通常为(W/O)/W型。乳化液通常由载体、调节剂、乳化剂组成,其中载体为主体催化剂,与被分离物质柠檬酸发生反应,转移柠檬酸;调节剂是使生成的柠檬酸络合物更好地溶入有机相,同时调节有机相的黏度;乳化剂是一种使形成的乳化液更稳定的表面活性剂,同时可以提高液膜传质速率和选择性。该方法[18-19]可以将柠檬酸在膜的两侧同时进行萃取与反萃取,但是存在操作复杂、乳液易于溶胀、破乳困难以及稳定性问题等缺点。
Yordanov等[20]采用Alamine 336作为载体,氯仿做调节剂,C9232作为乳化剂,NaOH作为反萃剂,最终在内相可以得到浓缩15倍的柠檬酸钠。实验过程中若使用醇类作为调节剂,乳液有明显的破乳现象,调节剂的浓度增加到一定程度,会导致有机相黏度增加,使得原料液与乳化液分离困难,故选择体积分数为 8%的氯仿。朱亦仁等[21-22]采用正三辛胺为载体,表面活性剂Span-80和LMA-1为乳化稳定剂,Na2CO3为反萃剂,其中LMA-1对柠檬酸的提取率比Span-80高,并且乳液溶胀较小。
2.2 支撑液膜分离纯化法
支撑液膜分离法是将有机相固定于多孔膜材料中,即支撑体(溶剂和流动载体),原料液和反萃剂分别在膜两侧,通过支撑液膜内的流动载体对被迁移物质柠檬酸的选择性,首先载体与原料液中柠檬酸反应,生成络合物,因膜两侧存在浓度梯度,使生成络合物从膜的原料液侧扩散到反萃相侧,与反萃相发生反应而解萃,解萃后生成的柠檬酸离子进入反萃相,而载体则反扩散到膜的原料液侧,继续与原料液中的柠檬酸反应,如图2。

图2 支撑液膜示意图
该方法优点是具有更高的选择性,过程需要的有机溶剂很少,萃取和反萃过程结合在一起[22],有机相利用率很高,但渗透压的存在是 SLM不稳定的重要原因之一;由于膜孔径的改变,使得膜的寿命短[23],对孔径要求严格。
Juang等[24-25]利用三辛胺作为载体,二甲苯作为稀释剂,疏水的聚偏氟乙烯作为多孔膜,水或者Na2CO3溶液作为反萃剂,实验结果显示当温度和三辛胺浓度升高时,溶质的传质速率增加,但低温、高浓度三辛胺以及水作为反萃剂时,柠檬酸的分离效率更好。Miyako等[26]利用酶催化反应驱动支撑液膜,使有机酸更容易通过液膜,实验得出水相 pH值为6.3时酶活性较高;原料液中超过体积分数65%的乙醇,会使酶变性;异辛醇为液膜相;Candida rugosa酶作为酯化反应的催化剂;原料液中含有酯类催化剂;反萃相中含有酯水解催化剂,最终可以达到对有机酸选择性的分离。
为了解决乳状液膜法和支撑液膜法的缺点,Ren等[27]研究的中空纤维更新液膜法,其操作简单,传质速率高,能耗低,过程稳定,两相之间无泄漏,没有二次污染,萃取剂消耗少,无破乳问题等,并且可以从稀溶液中同时提取浓缩柠檬酸。Juang等[28]采用无分散膜萃取柠檬酸,通过亲水性平面多微孔膜或者亲水性中空纤维膜,将溶质从水溶液转移到含络合载体的有机相,该方法克服了许多液-液萃取的缺点,例如溶剂损失、乳状液的形成以及在反应器和混合器中产生的溢流和负载问题。这种方法操作更简单,成本更低。中空纤维组件可以串联或者并联,通过改变纤维和组件的长度和直径来改变接触面积。这样膜过程不仅可以从水中除掉复合物,而且可以在产品一侧进一步处理浓缩这些物质。
为了改善支撑液膜法稳定性差、寿命短的缺点,可以将离子液体作为支撑液膜的溶剂[29-30]。离子液体由有机阳离子和有机或无机阴离子组成[31]。该液体热稳定性强、离子传导性强、不易燃[32]。离子液体具有一个很重要的物理性质,可以通过改变离子液体中烷基碳链的长度,增加阳离子的疏水性,从而降低它的水溶性,而且阴离子的选择也对离子液体的性质有很大改变[30]。研究者将支撑离子液膜用于分离提取有机酸,例如乙酸[33]和乳酸[31]。还有将电渗析和离子液体有效地结合起来,有机酸的收率能达到99%,离子液体可以循环使用,能源效率高,分离成本低[34]。
3 发展前景
近年来,随着人们消费水平的不断提高,对柠檬酸的需求逐年增加,因此分离提取柠檬酸已成为研究的热点。萃取法在分离提取方面具有一定的优势,例如工艺简单,适合工业化;整个过程节能环保,符合国家发展趋势。目前,使用萃取法分离提取柠檬酸面临的主要问题有以下几个方面。
(1)选择合适的萃取剂。柠檬酸发酵液中组成复杂,选择对柠檬酸选择性较高的萃取体系至关重要,同时其要求无毒、萃取率高、易分层、回收利用率高。
(2)在传统萃取法的基础上加入新的元素。传统萃取法有一定的不足,研究人员可以将新的理念与传统萃取法相结合,比如柠檬酸的分离提取中离子液体尚未得到应用,将其运用到分离提取柠檬酸中,可能会有很大的发展空间。
[1] Larba R,Boukerche I,Alane N,et al. Citric acid as an alternative lixiviant for zinc oxide dissolution[J]. Hydrometallurgy,2013,134-135:117-123.
[2] Vendruscolo F,Albuquerque P M,Streit F,et al. Apple pomace:A versatile substrate for biotechnological applications[J]. Critical Reviews in Biotechnology,2008,1(28):1-12.
[3] Vriesmann L C,Teó filo R F,Petkowicz C L. Extraction and characterization of pectin from cacao pod husks (Theobroma cacao L.) with citric acid[J]. LWT-Food Science and Technology,2012,49(1):108-116.
[4] Setoguchi T,Kato T,Yamamoto K,et al. Facile production of chitin from crab shells using ionic liquid and citric acid[J]. International Journal of Biological Macromolecules,2012,50(3):861-864.
[5] Gurpreet S D,Satinder K B,Surinder K,et al. Bioproduction and extraction optimization of citric acid from Aspergillus niger by rotating drum type solid-state bioreactor[J]. Industrial Crops and Products,2013,41:78-84.
[6] 戴猷元,秦炜,张瑾,等. 有机物络合萃取化学[M]. 北京:化学工业出版社,2008: 42-54.
[7] 江玉明,苏元复. 三烷基氧膦萃取柠檬酸的萃合物的结构和性能研究[J]. 华东化工学院学报,1985,11(1):1-8.
[8] 金寄春,苏克曼. 石油亚砜萃取柠檬酸的研究[J]. 华东化工学院学报,1989,15(6):788-794.
[9] Bayazit S S,Uslu H,Inci I. Comparative equilibrium studies for citric acid by amberlite LA-2 or tridodecylamine (TDA)[J]. J. Chem. Eng. Data,2009,54(7):1991-1996.
[10] Uslu H,Inci I,Kirbaslar S I,et al. Extraction of citric acid from aqueous solution by means of a long chain aliphatic quaternary amine/diluent system[J]. J. Chem. Eng. Data,2007,52(5):1603-1608.
[11] 王志华,高自立,孙思修,等. 伯胺N1923萃取柠檬酸的研究[J].高等学校化学学报,1992,13(9):1153-1156.
[12] Heyberger A,Prochfizka J,Volaufova E. Extraction of citric acid with tertiary amine-third-phase formation[J]. Chemical Engineering Science,1998,53(3):515-521.
[13] Lintomen L,Pinto R T P,Batista E,et al. Liquid-liquid equilibrium of the water+citric acid+short chain alcohol+tricaprylin system at 298.15K[J]. J. Chem. Eng. Data,2001,46(3):546-550.
[14] Ju H,Wei Q F,Ren X L,et al. Study on solvent extraction of citric acid from fermentation broth[J]. Advances in Chemical EngineeringⅢ,2013,781-784.
[15] Inci I,Uslu H. Investigation of diluent effect on extraction of citric acid by trioctyl methyl ammonium chloride+organic solutions[J]. J. Chem. Eng. Data,2005,50(3):1103-1107.
[16] Prochazka J,Heyberger A,Volaufova E. Amine extraction of hydroxycarboxylic acids. 3. Effect of modifiers on citric acid extraction[J]. Ind. Eng. Chem. Res.,1997,36(7):2799-2807.
[17] Ali T,Bylund D,Essén S A,et al. Liquid extraction of low molecular mass organic acids and hydroxamate siderophores from boreal forest soil[J]. Soil Biology & Biochemistry,2011,43(12):2417-2422.
[18] Sayed M S E.Uranium extraction from gattar sulfate leach liquor using aliquat-336 in a liquid emulsion membrane process[J]. Hydrometallurgy,2003,68(1-3):51-56.
[19] Pataik P R. Liquid emulsion membranes:Principles,problems and applications in fermentation processes[J]. Biotechnology Advances,1995,13(2):175-208.
[20] Yordanov B,Boyadzhiev L. Pertraction of citric acid by means of emulsion liquid membranes[J]. Journal of Membrane Science,2004,238(1-2):191-197.
[21] 林立,金美芳,温铁军,等. 乳化液膜提取柠檬酸及其溶胀的研究[J]. 水处理技术,1995,21(5):331-336.
[22] 朱亦仁,崔玉民.表面活性剂对液膜法提取柠檬酸影响的研究[J]. 膜科学与技术,2002,22(6):20-23.
[23] Yang X J,Fane A G,Soldenhoff K. Comparison of liquid membrane processes for metal separations:Permeability,stability and selectivity[J]. Ind. Eng. Chem. Res.,2003,42(2):392-403.
[24] Juang R S,Huang R H,Wu R T. Separation of citric and lactic acids in aqueous solutions by solvent extraction and liquid membrane processes[J]. Journal of Membrane Science,1997,136(1-2):89-99.
[25] Juang R S,Chen L J. Transport of citric acid across a supported liquid membrane containing various salts of a tertiary amine[J]. Journal of Membrane Science,1997,123(1):81-87.
[26] Miyako E,Maruyama T,Kamiya N,et al. Transport of organic acids through a supported liquid membrane driven by lipase-catalyzed reactions[J]. Journal of Bioscience and Bioengineering,2003,96(4):370-374.
[27] Ren Z,Zhang W,Li H,et al. Mass transfer characteristics of citric acid extraction by hollow fiber renewal liquid membrane[J]. Chemical Engineering Journal,2009,146(2):220-226.
[28] Juang R S,Chen J D,Huan H C. Dispersion-free membrane extraction:Case studies of metal ion and organic acid extraction[J]. Journal of Membrane Science,2000,165(1):59-73.
[29] Antonia P R,Francisco J H F ,Francisca T A,et al. On the importance of the nature of the ionic liquids in the selective simultaneous separation of the substrates and products of a transesterification reaction through supported ionic liquid membranes[J]. Journal of Membrane Science,2008,307(2):233-238.
[30] Joan F B,Edward J M. Ionic liquids:Innovative fluids for chemical processing[J]. AIChE Journal,2001,47(11):2384-2389.
[31] Martak J,Schlosser S,Vlckova S. Pertraction of lactic acid through supported liquid membranes containing phosphonium ionic liquid[J]. Journal of Membrane Science,2008,318(1-2):298-310.
[32] Francisco J H F,Antonia P R,et al. A novel application of supported liquid membranes based on ionic liquids to the selective simultaneous separation of the substrates and products of a transesterification reaction[J]. Journal of Membrane Science,2007,293(1-2):73-80.
[33] Kouki N,Tayeb R,Zarrougui R,et al. Transport of salicylic acid through supported liquid membrane based on ionic liquids[J]. Separation and Purification Technology,2010,76(1):8-14.
[34] Lopez A M,Hestekin J A. Separation of organic acids from water using ionic liquid assisted electrodialysis[J]. Separation and Purification Technology,2013,116:162-169.
Progress in citric acid separation by extracting
JU Hui,YANG Huiru,WEI Qifeng,REN Xiulian,DONG Huishuan
(School of Marine Science and Technology,Harbin Institute of Technology,Weihai 264209,Shandong,China )
Citric acid is an important organic acid and one of the largest amounts of fermentation products in the world. In the paper,it is comprehensively synopsized for the principles,advantages and disadvantages about the liquid-liquid extraction and liquid membrane extraction. The current development of two systems and problems need to be solved now are discussed in detail. They have little pollution,high extraction efficiency and low cost,but they are all easy to emulsify due to emulsifiers,proteins,polysaccharides contained in fermentation broth,meanwhile liquid membrane extraction method is complicated. Based on these shortages,ionic liquid applied to the citric acid extraction system is proposed. And the idea ensures the extraction keep its advantages,but also overcome its emulsification,while ion liquid can be recycled,which will increase its energy-efficiency,and reduce the cost of separation.
citric acid;extraction method;separation;extraction
O 69
A
1000-6613(2014)02-0285-05
10.3969/j.issn.1000-6613.2014.02.003
2013-08-05;修改稿日期:2013-10-31。
鞠辉(1989—),女,硕士研究生。E-mail juhuihit@163.com。
联系人:魏琦峰,博士,教授,研究生导师,研究方向为分离提取、电化学。E-mail weiqifeng163@163.com。

