维持性血液透析患者左室肥厚的相关因素分析
李春红 田 洁 王洪玲 赵继红
维持性血液透析患者左室肥厚的相关因素分析
李春红 田 洁 王洪玲 赵继红
目的 探讨维持性血液透析(MHD)患者左室肥厚的影响因素。方法对本透析中心60例维持性血液透析患者,行心脏彩超检查了解左心室肥厚(LVH)情况,60例患者中,共有43例(71.7%)患者存在LVH(LVH组),17例为非LVH患者(非LVH组)。收集2组临床资料并进行血红蛋白(HGB)、血肌酐(Cr)、甲状旁腺素(iPTH)、白蛋白(ALB)、三酰甘油(TG)、胆固醇(CHO)、钙(Ca)、磷(P)、晚期氧化蛋白产物(AOPP)、C反应蛋白(CRP)指标检测。结果与非LVH组相比,LVH组年龄、收缩压、iPTH、AOPP水平均明显升高(P<0.05),BMI及其他生化指标差异均无统计学意义。左室心肌质量指数(LVMI)与年龄、收缩压、iPTH、AOPP呈正相关(r分别为0.240、0.293、0.288 和0.363),与其他指标均无相关性。多重线性回归分析显示,收缩压、iPTH、AOPP是LVMI的影响因素。结论LVH在MHD患者多发,收缩压、iPTH和AOPP在LVH发病中起重要作用。
肾透析;肥大,左心室;血压;甲状旁腺素;维持性血液透析;晚期氧化蛋白产物
心血管并发症是血液透析患者死亡的主要原因[1],左心室肥厚(left ventricular hypertrophy,LVH)在维持性血液透析(maintenance hemodialysis,MHD)患者中有很高的发生率,同时是MHD患者心血管病死率最重要的预测因子[2]。LVH发生机制复杂,本研究对规律血液透析的患者进行心脏彩超检查,同时记录其临床及生化指标,旨在探讨MHD患者LVH的相关危险因素。
1 对象与方法
1.1 研究对象 选择2010年10月—12月于我透析中心行规律性血液透析治疗的患者60例,排除合并原发性梗阻性心肌病、瓣膜狭窄患者。其中男35例,女25例,年龄21~77岁,平均(57.9±11.8)岁,透析时间7~126个月,平均(42.8± 5.10)个月。原发病分别为:慢性肾小球肾炎24例,糖尿病肾病15例,多囊肾7例,高血压肾小动脉硬化9例,其他及不明病因5例。60例患者中,43例(71.7%)患者存在LVH (LVH组),17例(28.3%)为非LVH患者(非LVH组)。
1.2 方法
1.2.1 治疗方法 所有患者每周透析3次,每次4~4.5 h,血流量200~280 mL/min,透析液流量500 mL/min。使用碳酸氢盐透析液,透析液钙离子浓度为1.25 mmol/L或1.5 mmol/L。应用聚砜膜(Fresenius F6)、三醋酸纤维膜(130 G)及聚甲基丙烯酸甲酯膜(B3-1.6A)透析器透析。规律透析基础上给予常规药物治疗。
1.2.2 各指标检测方法 采集病史包括年龄、血压、体质指数(BMI)、透析龄。透析前空腹采血,白蛋白(ALB)、三酰甘油(TG)、胆固醇(CHO)、肌酐(Cr)、钙(Ca)、磷(P)采用日本日立TOSHIBA-1 20全自动生化分析仪进行检测,血红蛋白(HGB)采用ADVIA2120全自动血细胞分析仪检测。甲状旁腺素(iPTH)采用化学发光法检测。C反应蛋白(CRP)采用免疫透射比浊法,试剂盒购自芬兰Orion Diagnoctica公司。晚期氧化蛋白产物(AOPP)采用分光光度计方法检测。心脏超声(美国Philips IE-33型)均由同一位训练有素的超声检查专业人员操作。测定左室内径(LVD)、左房内径(LAD)、左室后壁厚度(LVPWT)、室间隔厚度(IVST),左室心肌质量指数(LVMI)采用公式{1.04×[(IVST+LVPWT+LVD)3-LVD3]-13.6}/体表面积(BSA)计算。LVH定义为LVMI男性>131 g/m2,女性>110 g/m2[3]。
1.3 统计学方法 采用SPSS 13.0统计软件包。所有计量资料均采用±s表示,组间比较采用两独立样本的t检验,LVMI与其他指标的相关分析采用Pearson法,LVMI影响因素分析采用多重线性回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 2组临床资料比较 与非LVH组相比,LVH组年龄、收缩压、iPTH、AOPP和LVMI水平均明显升高,差异有统计学意义(P<0.05),BMI及其他生化指标差异均无统计学意义,见表1。
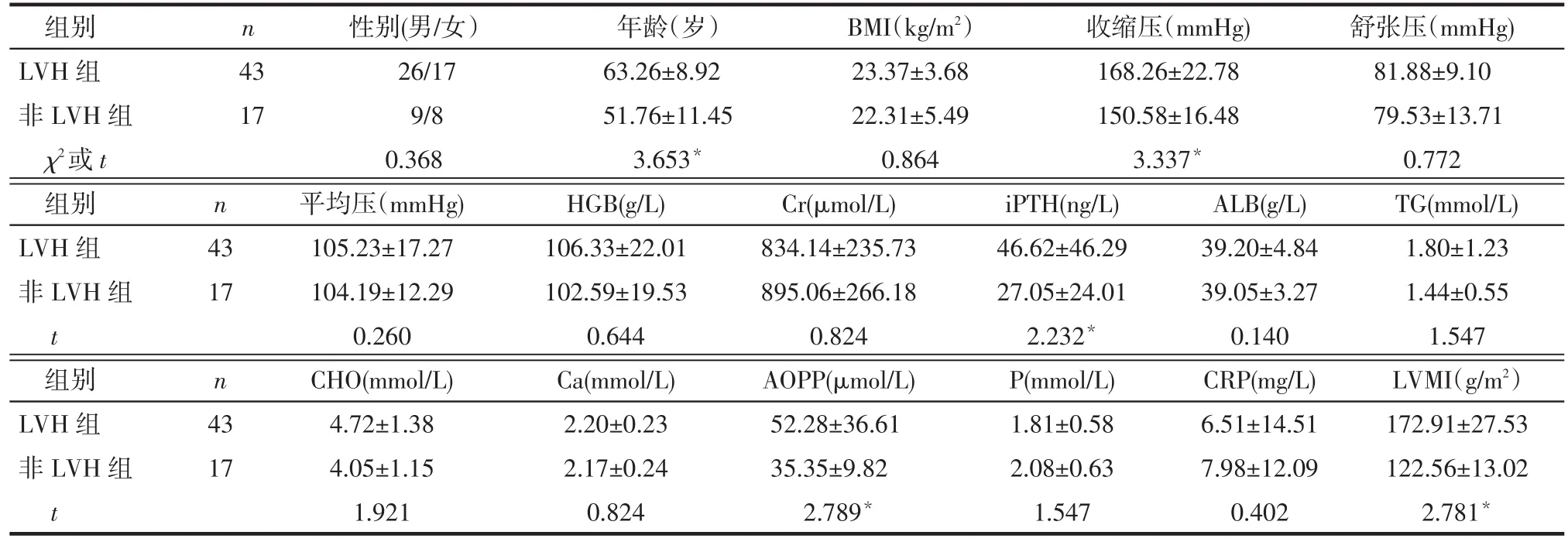
Tab.1 Comparison of clinical parameters between two groups表1 2组患者临床资料比较
2.2 相关与回归分析结果 LVMI与年龄、收缩压、iPTH、AOPP呈正相关(r分别为0.240、0.293、0.288 和0.363,P<0.05),与其他指标均无相关性。多重线性回归分析显示,收缩压、iPTH、AOPP是LVMI的影响因素,见表2。
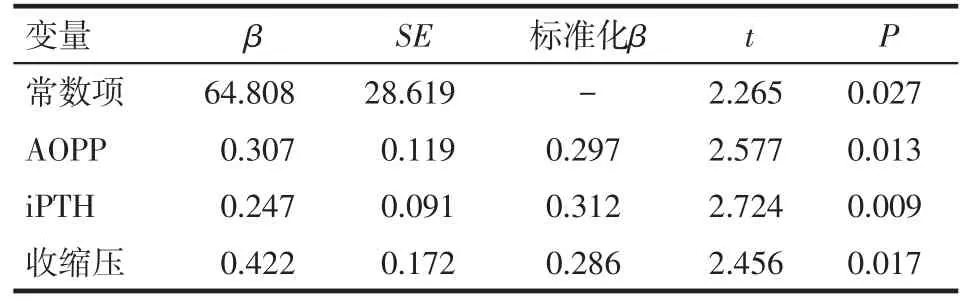
Tab.2 Regression Analysis of LVMI in Hemodialysis Patients表2 MHD患者影响LVMI的回归分析
3 讨论
心血管疾病是慢性肾脏病(CKD)患者最常见的并发症,是导致慢性肾衰竭患者首要的死亡原因,占CKD患者全部死亡原因的40%~50%[4]。有报道显示,维持性血液透析患者心血管疾病的病死率为38.1%,大部分为心源性猝死,这与结构性心脏病(左室肥厚和心肌纤维化)有关[5]。据报道,MHD患者LVH发生率高达71%[6]。本研究中左心室肥厚发生率71.7%,与文献报道一致。
CKD患者LVH的发生机制比较复杂,传统理论认为高容量负荷、高血压及贫血等一般性因素不论在尿毒症还是非尿毒症患者,均是引起心脏病变的重要原因。本研究结果显示,收缩压是MHD患者LVMI的影响因素。这与参考文献[7]观点一致。高血压增加了心脏的后负荷,加重LVH的发生。有研究发现积极且较长时间的降压治疗可能能够减轻MHD患者的LVMI[8],但何种降压药物更有利,却少见报道。本研究因条件所限未涉及,仍需进一步证实。鉴于收缩压对LVMI的影响,降压治疗尤其是降收缩压的治疗可能在延缓LVH进展中起作用。本研究中血红蛋白与LVH无相关,考虑可能与本组患者贫血状况改善较好有关。
事实上,MHD患者即使严格控制血压、纠正贫血,LVH的发生率仍然高达60%~90%[9],说明可能有其他因素参与LVH的发展。研究发现,持续性PTH增高可以升高血压,增加心肌收缩阻力,促进心肌细胞肥大和心肌纤维间质化,造成左心室肥厚;促进钙磷在血管壁以及心肌沉积,导致心肌和心脏瓣膜钙化[10]。Qing等[11]对尿毒症模型鼠的研究发现,PTH可提高细胞内钙离子浓度及胰岛素样生长因子浓度,从而刺激蛋白质合成,导致心肌细胞肥大。有研究认为,高水平的PTH在MHD患者左室肥厚和左室射血分数降低过程中起重要作用,是MHD患者左室肥厚的独立预测因子,并增加其左室肥厚相关的心血管死亡率[12]。本研究提示左室肥厚与iPTH水平呈正相关,与文献报道一致。但本研究未发现LVH与钙磷的关系,不除外与含钙的磷结合剂的应用有关。
慢性肾脏病患者存在氧化应激,体内产生大量的活性氧,它们可以直接引起心肌细胞的损害,进一步引起LVH[13]。AOPP是氧化应激的新型标志物,本研究中亦观察到AOPP为LVMI的影响因素,提示AOPP参与了MHD患者LVH发病的过程,具体机制尚不明确。有研究显示,CRP水平可预示MHD患者存在心肌肥厚和心肌重塑,CRP与LVMI呈正相关,是导致LVH的危险因素[14]。本研究中未观察到CRP与LVMI的相关性,考虑可能与病例数较少有关。
[1]Lyu WL,Teng J,Ding XQ,et al.Comparison of survival in patients on hemodialysis and peritoneal dialysis[J].Chin J Nephrol,2010,26: 252-257.[吕文律,滕杰,丁小强,等.血液透析和腹膜透析患者生存比较[J].中华肾脏病杂志,2010,26:252-257.]doi:10.3760/ cma.j.issn.1001-7097.2010.04.003.
[2]Nakamura S,Sasaki O,Nakahama H,et al.Left ventricular hypertrophy is a risk factor independent of hypertension in survival of hemodialyzed patients[J].Ren Fail,2002,24(2):175-186.doi:10.1081/ JDI-120004094.
[3]Levin A,Singer J,Thompson CR,et al.Prevalent left ventricular hypertrophy in the predialysis population:identifying opportunities for intervention[J].Am J Kidney Dis,1996,27:347-354.doi:10.1016/S0272-6386(96)90357-1.
[4]Al-Dadah A,Omran J,Nusair MB,et al.Cardiovascular mortality in dialysis patients[J].Adv Perit Dial,2012,28:56-59.
[5]Cerasola G,Nardi E,Palermo A,et al.Epidemiology and pathophysiology of left ventricular abnormalities in chronic kidney disease:a review[J].J Nephrol,2011,24(1):1-10.doi:10.5301/JN.2010.2030.
[6]Takeda A,Toda T,Iwamoto H,et al.Long-term evolution and changing associations of left ventricular hypertrophy after starting hemodialysis[J].Nephron Clin Pract,2008,110(1):c126.doi: 10.1159/000163845.
[7]Ishimitsu T,Nakano N,Sudo Y,et al.Predictive significance of blood pressure values for the incidence of cardiovascular events in chronic hemodialysis patients[J].Hypertens Res,2008,31:1703-1709.doi:10.1291/hypres.31.1703.
[8]Kutlay S,Dincer I,Sengul S,et al.The long-term behavior and predictors of left ventricular hypertrophy in hemodialysis patients[J].Am J Kidney Dis,2006,47:485-492.doi:10.1053/j.ajkd.2005.12.029.
[9]Chang ST,Chen CC,Chen CL,et al.Changes of the cardia architectures and functions for chronic hemodialysis patients with dry weight determined by echocardiography[J].Blood Purif,2004,22: 351-359.doi:10.1159/000080031.
[10]Wang AY,Woo J,Wang M,et al.Association of inflammation and malnutrition with cardiac valve calcification in continuous ambulatory peritoneal dialysis patients[J].J Am Soc Nephrol,2001,12(9): 1927-1936.
[11]Qing DP,Ding H,Vadgama J,et al.Elevated myocardial cytosolic calcium impairs insulin-like growth factor-l-stimulated protein synthesis in chronic renal failure[J].J Am Soc Nephrol,1999,10(1): 84-92.
[12]Randon RB,Robde LE,Comerlato L,et al.The role of secondary hyperparathyroidism in left ventricular hypertrophy of patients and chronic hemodialysis[J].Braz J Med Bioc Res,2005,38:1409-1416.doi:10.1590/S0100-879X2005000900016.
[13]Hambali Z,Ahmad Z,Arab S,et al.Oxidative stress and its association with cardiovascular disease in chronic renal failure patients[J].Indian J Nephrol,2011,21(1):21-25.doi:10.4103/0971-4065.75218.
[14]Monfared A,Salari A,Kazemnezhad E,et al.Association of left ventricular hypertrophy with high-sensitive C-reactive protein in hemodialysis patients[J].Int Uroc Nephrol,2013,45:1679-1686.doi:10.1007/s11255-012-0375-x.
(2013-12-16收稿 2014-08-19修回)
(本文编辑 魏杰)
Related Factors of Left Ventricular Hypertrophy in Maintenance Hemodialysis Patients
LI Chunhong,TIAN Jie,WANG Hongling,ZHAO Jihong Nephrology Department,the Third Central Hospital of Tianjin,Tianjin 300170,China
ObjectiveTo explore potential related factors of left ventricular hypertrophy in maintenance hemodialysis(MHD)patients.MethodsSixty patients were enrolled in the study.Echocardiography was performed to exam LVH indexes.There are forty-three patients with LVH(LVH group),and seventeen patients without LVH(non-LVH group).Clinical data were collected to exam the levels of hemoglobin(HGB),creatinine(Cr),parathyrin(iPTH),albumin(ALB),triglyceride(TG),cholesterol(CHO),calcium(Ca),phosphorus(P),advanced oxygen protein products(AOPP)and C reactive protein (CRP).ResultsCompared with non-LVH group,age,BP,iPTH,AOPP were higher in LVH group patients while BMI and other biochemistry index does not show any statistical difference.Multiple linear stepwise regressions analysis shows that SBP,iPTH and AOPP are correlated factors to left ventricle mass index(LVMI).ConclusionLVH is prevalent in MHD patients.BP,iPTH and AOPP are the risk factors for LVH.
renal dialysis;hypertrophy,left ventricular;blood pressure;parathyroid hormone;maintenance hemodialysis;advanced oxygen protein products
R692
A
10.3969/j.issn.0253-9896.2014.12.024
天津市第三中心医院肾内科(邮编300170),天津市人工细胞重点实验室

