吲哚美辛对荷Lewis肺癌小鼠抗肿瘤作用的相关研究
王存德 张利娟 龚 泉 李雪芹 董 蕙
吲哚美辛对荷Lewis肺癌小鼠抗肿瘤作用的相关研究
王存德 张利娟 龚 泉 李雪芹 董 蕙
目的探索吲哚美辛对荷Lewis肺癌小鼠肿瘤生长的抑制作用。方法建立C57小鼠Lewis肺癌皮下移植瘤模型并随机分组,各组分别以吲哚美辛和生理盐水连续灌胃16天,观察各组小鼠的出瘤时间、用药前后瘤体大小及变化,绘制瘤体生长曲线。结果吲哚美辛干预组的肿瘤体积小于生理盐水对照组(P<0.05),肿瘤抑制率高于生理盐水对照组(P<0.05)。结论吲哚美辛对荷Lewis肺癌小鼠肿瘤生长具有显著的抑制作用。
吲哚美辛;Lewis肺癌;小鼠
恶性肿瘤严重威胁着人类健康与生命,伴随着人们对恶性肿瘤发生、发展过程认识的逐步深入,在恶性肿瘤的治疗中靶向治疗发挥着越来越重要的作用,其中成为研究者们最为关注的焦点是以肿瘤血管为靶点的治疗策略[1]。近年来研究发现,吲哚美辛具有抑制促血管生因子(如VEGF)表达的作用,从而阻断肿瘤血管的生成,抑制肿瘤的生长[2]。本研究应用吲哚美辛作用于荷瘤小鼠,初步探索吲哚美辛抗肿瘤生长的作用。
1 资料与方法
1.1 试剂与药品 吲哚美辛、二甲基亚砜(DMSO)购自Sigma公司,RPMI 1640培养基粉剂及胎牛血清均购于Gibco公司。
1.2 实验动物及细胞 Lewis小鼠肺癌细胞株购自美国典型培养物保藏中心(ATCC),SPF级C57小鼠购自湖南斯莱克景达实验动物有限公司。
2 方法
2.1 细胞培养与接种 首先将 Lewis细胞株用含10%胎牛血清的RPMI 1640培养基培养,当细胞贴壁长满单层后用0.25%胰蛋白酶消化,将培养液吹打混匀,1000rpm×5min离心,收集细胞用无菌 PBS稀释,在显微镜下计数后将浓度调整至1×106~7/ml,取0.2ml细胞悬液接种于C57小鼠右侧腋后线皮下,观察肿瘤的生长,待体积达1000mm3左右时移植至小鼠右侧腋窝附近皮下。
2.2 造模与分组 选择生长良好、瘤体无破溃的荷瘤小鼠,断颈法处死,在超净工作台内完整剥离瘤体,用无菌生理盐水清洗血渍,清除中心坏死组织,充分匀浆以制备瘤细胞悬液,加生理盐水调整细胞悬液浓度至1×106~7/ml。每只小鼠取0.2ml悬液接种于右侧腋后线皮下,构建荷瘤小鼠22只(接种操作在 30min内完成)。10d后肿瘤体积达到 100~200mm3时,将建立好的小鼠模型随机分为吲哚美辛干预组和生理盐水对照组,吲哚美辛干预组 16只小鼠,每天以吲哚美辛灌胃;生理盐水对照组 6只,每天以生理盐水灌胃。其中,吲哚美辛干预组又分为高剂量组和低剂量组,低剂量组每天以吲哚美辛2mg/kg灌胃,高剂量组每天以吲哚美辛4mg/kg灌胃。观察各组小鼠的出瘤时间、给药前后瘤体的大小及变化,同时观察给药前后各组小鼠的整体状况,如饮食量、体重、皮肤色泽、反应灵敏度及活动能力等。
2.3 给药剂量与方法 分组当天开始灌胃给药,每天1次,连续16天(给药剂量采用人与动物剂量换算法确定)。吲哚美辛干预组:吲哚美辛分别按2mg/kg/d和4mg/kg/d灌胃给药;生理盐水对照组:生理盐水每天0.2ml/10g灌胃。
2.4 计算方法 每四天测量一次,具体方法为用药前后用毫米游标卡尺测量肿瘤长、宽最大垂直直径,并按如下公式计算肿瘤体积:肿瘤体积(mm3)=(肿瘤长径×肿瘤短径2)/2,同时绘制各组小鼠肿瘤生长曲线。用药结束后两天断颈法处死小鼠,分离瘤体并称重,通过下列公式计算两组肿瘤抑制率:肿瘤抑制率%=(1―吲哚美辛干预组平均瘤重/生理盐水对照组平均瘤重)×100%。
3 结果
3.1 一般情况观察 造模前各组小鼠一般状况良好,生理盐水对照组与吲哚美辛干预组小鼠平均体重分别为(17.67±1.48)g、(17.72±0.89)g,两组初始体重无统计学差异(P>0.05),具有可比性。实验过程中动态观察发现生理盐水对照组小鼠进食、饮水情况基本正常,但反应较为迟钝,活动状况较植瘤前明显减少;吲哚美辛干预组小鼠反应较生理盐水对照组灵敏,饮水、进食及活动等状况良好。实验完成时22只小鼠均存活,但吲哚美辛组小鼠有粪便中带血及轻度腹泻的情况。
3.2 各组肿瘤体积动态变化 吲哚美辛干预组﹑生理盐水对照组C57小鼠Lewis肺癌移植瘤的体积变化情况见表1和图1。从表1和图1可以看出,自用药后第4天起,生理盐水对照组肿瘤体积大于吲哚美辛干预组,且统计结果表明差异有显著性(P<0.05);从表2及图2可以看出,吲哚美辛低剂量组与高剂量组肿瘤体积比较无统计学差异(P>0.05)。
表1 吲哚美辛干预组、生理盐水对照组对C57小鼠Lewis肺癌移植肿瘤体积变化比较(±s)

表1 吲哚美辛干预组、生理盐水对照组对C57小鼠Lewis肺癌移植肿瘤体积变化比较(±s)
注:与生理盐水对照组比较,*P<0.05
组别 n d0 d4 d8 d12 d16肿瘤体积(mm3)生理盐水对照组 6 84.92±15.39 162.04±39.38 351.12±39.68 944.62±79.84 1638.43±256.63吲哚美辛干预组 16 83.82±14.26 121.24±14.12* 207.93±15.92* 685.07±69.39* 1258.48±133.41*P 0.877 0.048 0.032 0.015 0.013
表2 吲哚美辛低剂量组与吲哚美辛高剂量组肿瘤体积的动态变化比较(±s)

表2 吲哚美辛低剂量组与吲哚美辛高剂量组肿瘤体积的动态变化比较(±s)
注:吲哚美辛低剂量组与高剂量比较,P>0.05
组别 n d0 d4 d8 d12 d16肿瘤体积(mm3)吲哚美辛低剂量组 8 83.07±16.19 120.90±15.76 211.14±16.97 678.05±76.01 1262.47±168.08吲哚美辛高剂量组 8 84.57±13.13 121.57±13.37 204.72±15.20 692.09±66.54 1254.47±99.26 P 0.841 0.928 0.439 0.700 0.909
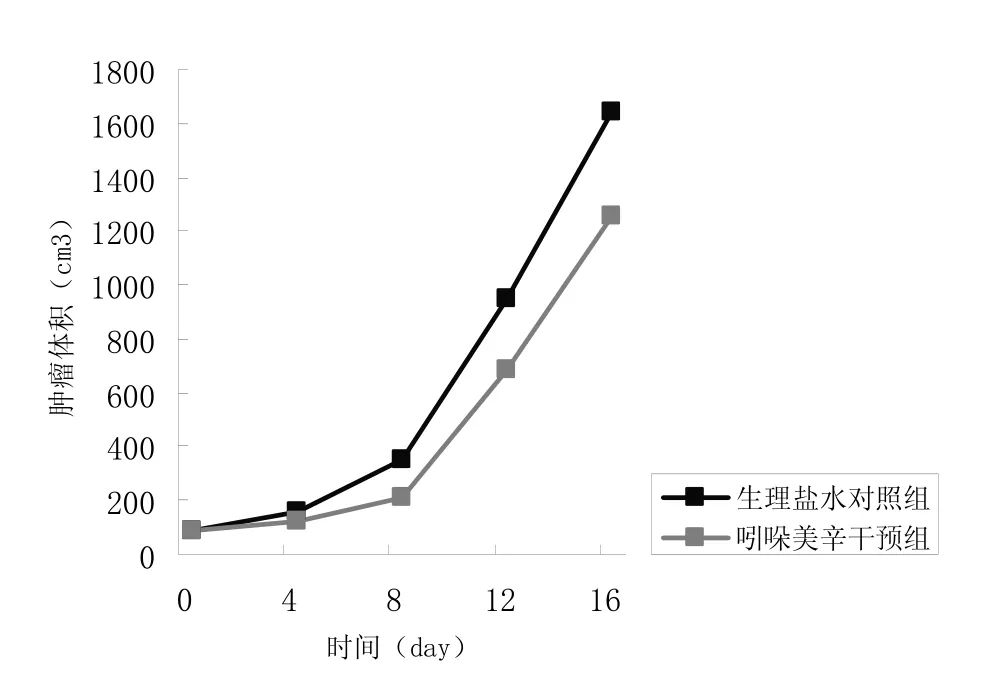
图1 吲哚美辛干预组与生理盐水对照组肿瘤生长曲线

图2 吲哚美辛低剂量组与吲哚美辛高剂量组肿瘤生长曲线
3.3 肿瘤抑制率 吲哚美辛干预组与生理盐水对照组对C57小鼠Lewis肺癌移植瘤生长抑制作用,结果见图3及表3。结果表明,吲哚美辛干预组肿瘤瘤重较生理盐水对照组轻,差异有统计学意义(P<0.05)。吲哚美辛干预组的肿瘤平均抑制率为12.6%,其中吲哚美辛低剂量组、吲哚美辛高剂量组的肿瘤平均抑制率分别为 13.3%、11.9%。吲哚美辛高剂量组的肿瘤平均抑制率和肿瘤重量与低剂量组相比较,差异均无统计学意义(P>0.05)。

图3 吲哚美辛干预组与生理盐水对照组移植瘤重量比较
表3 吲哚美辛低剂量组与生理盐水对照组肿瘤重量(±s)与抑瘤率(%)比较
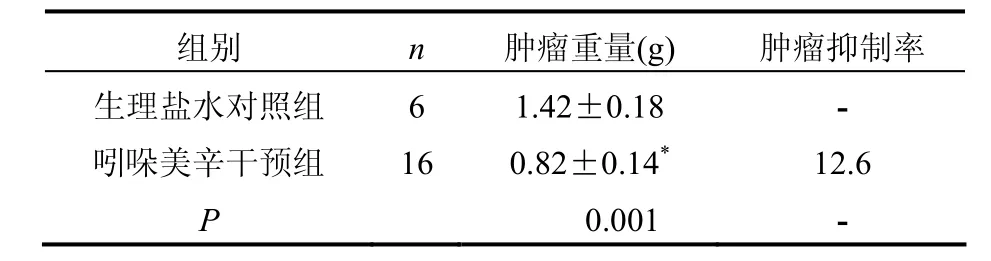
表3 吲哚美辛低剂量组与生理盐水对照组肿瘤重量(±s)与抑瘤率(%)比较
注:与生理盐水对照组比较,*P<0.05
组别 n 肿瘤重量(g) 肿瘤抑制率生理盐水对照组 6 1.42±0.18 -吲哚美辛干预组 16 0.82±0.14* 12.6 P 0.001 -
4 讨论
在专家、学者多年的不断努力之下,恶性肿瘤的治疗已经取得了若大的进步,并有了一定的疗效,但对恶性肿瘤的整体治愈率依然存在一定的差异[3]。目前对于加强恶性肿瘤的临床和基础研究,最现实的意义就是寻找有效的治疗方法和经济实用的治疗药物[4]。研究发现,很多肿瘤的发生、发展与慢性炎症有着紧密的联系。炎症反应就像一把双刃剑,除了可以引起抗肿瘤反应之外,更多的是促进了肿瘤细胞的增殖、转移和肿瘤血管的生成。研究表明,肿瘤细胞的增殖、坏死和凋亡可刺激局部微环境内的巨噬细胞释放炎症介质,进而刺激内皮细胞产生趋化因子、细胞因子、黏附分子及生长因子等,吸引更多的巨噬细胞、嗜酸性粒细胞、淋巴细胞、肥大细胞和中性粒细胞的聚集,其将释放各种生长因子、基质金属蛋白水解酶和趋化因子等以促进内皮细胞增殖、迁移,并水解组织间质成分,从而促进组织重建、血管生成、肿瘤生长和转移,研究者称之为炎症依赖性或炎症性血管生成[5-6]。炎性血管生成的理论为抗肿瘤生成提供了新的策略,使用天然或合成的抗炎药物来抑制肿瘤血管新生,从而抑制肿瘤的生长和转移成为了一个可行的途径。
吲哚美辛(IN)又称消炎痛,是NSAIDs中常见的一种药物。本研究初步探索了吲哚美辛对荷Lewis肺癌小鼠肿瘤抑制的作用。本研究表明,应用吲哚美辛后,吲哚美辛干预组与生理盐水对照组相比,肿瘤体积均有不同程度的缩小,且差异具有显著的统计学意义(P<0.05);然而,吲哚美辛低剂量组与高剂量组相比,小鼠肿瘤体积无明显差异(P>0.05)。对肿瘤抑制率的统计分析发现,吲哚美辛干预组的肿瘤抑制率与生理盐水对照组比较有显著的统计学意义(P<0.05);而吲哚美辛低剂量组与高剂量组相比,肿瘤抑制率无明显差异(P>0.05)。上述结果表明,应用吲哚美辛对小鼠Lewis肺癌肿瘤生长有明显的抑制作用,而吲哚美辛低剂量组与高剂量组其肿瘤抑制作用无明显的差异。研究认为,本文所涉及的吲哚美辛用药剂量是由人类用药剂量换算而来的,吲哚美辛对肿瘤的抑制作用是否存在剂量依赖性,以及其抑制肿瘤的最佳剂量仍需进一步研究探索。
本研究从生活中极为常见的非甾体类抗炎药物吲哚美辛出发,以荷Lewis肺癌小鼠为研究对象,初步证实了吲哚美辛具有显著的抗肿瘤作用。本研究结果为日后进一步研究联合抗炎药物抗肿瘤机制,特别是对研究抗肿瘤血管生成等方面提供了大量的参考信息。
[1] Ferrara N,Kerbel RS.Angiogenesis as a therapeutic target[J]. Nature,2005,438(7070):967-974.
[2] Folkman J.Tumor angiogenesis:therapeutic implications[J].N Engl J Med,1971,285(21):1182-1186.
[3] Mahmud SM,Franco EL,Aprikian AG,et al.Use of nonsteroidal anti-inflammatory drugs and prostate cancer risk:a meta-analysis[J]. Int J Cancer,2010,127(7):1680-1691.
[4] Lanas A.Nonsteroidal anti-inflammatory drugs and cyclooxygenase inhibition in the gastrointestinal tract:a trip from peptic ulcer to colon cancer[J].Am J Med Sci,2009,338(2):96-106.
[5] Scapini P,Morini M,Tecchio C,et al.CXCL1/macrophage inflammatory protein-2-induced angiogenesis in vivo is mediated by neutrophil-derived vascular endothelial growth factor-A[J].J Immunol, 2004,172(8):5034-5040.
[6] Benelli R,Morini M,Carrozzino F,et al.Neutrophils as a key cellular target for angiostatin:implications for regulation of angiogenesis and inflammation[J].FASEB J,2002,16(2):267-269.
The related study on Antitumor effect of Indomethacin on mice Bearing Lewis lung Cancer
Wang Cunde Zhang Lijuan Gong Quan Li Xueqin Dong Hui
ObjectiveTo prove the effects of indomethacin on inhibiting tumor growth of rats' Lewis pulmonary tumor(LLC).MethodsLLC transplant model was built to set up control group and indomethacin group.Each group were lavaged with indomethacin and saline for 16 days.To observe the tumor growth time,tumor size,and changes before and after treatment,and draw the tumor growth curve.ResultsThe tumor volume of Indomethacin group less than the saline control group(P<0.05),and the tumor control rate is higher than the saline control group(P<0.05).ConclusionsIndomethacin have the significant inhibition effect on the tumor growth of transplanted rats' Lewis pulmonary tumor.
Indomethacin;Lewis pulmonary tumor;Rat
R734.2
A
1673-5846(2014)02-0037-04
云南省肿瘤医院昆明医科大学第三附属医院姑息医学科,云南昆明 650118

