PCD方案与VAD方案治疗多发性骨髓瘤的临床观察
李 青 李玉明
PCD方案与VAD方案治疗多发性骨髓瘤的临床观察
李 青 李玉明
目的:探讨硼替佐米+环磷酰胺+地塞米松(PCD方案)和长春新碱+表阿霉素+地塞米松(VAD方案)治疗多发性骨髓瘤的临床疗效及不良反应。方法:回顾天津市第一中心医院血液科2011年1月至2013年1月收治的多发性骨髓瘤患者41例,依治疗方案不同分为PCD组及VAD组,分析两组患者的疗效及不良反应。结果:PCD组治疗后部分缓解及以上的有效率达42.9%,而VAD组仅15.0%,差异有统计学意义(P<0.05),在初治患者中反应良好的患者(CR和VGPR)PCD组为50.0%,VAD组7.7%,差异有统计学意义(P<0.05),两组患者在疱疹感染、血细胞减少及乏力腹胀等方面的不良反应无明显差异,但PCD组的神经毒性的发生率较VAD组高,差异有统计学意义(P<0.05)。结论:PCD方案治疗多发性骨髓瘤疗效优于VAD方案,特别是对于初治患者PCD方案能明显提高缓解率,但治疗过程中应注意硼替佐米的神经毒性,必要时应减量应用。
多发性骨髓瘤 治疗 不良反应
多发性骨髓瘤是浆细胞恶性增殖性疾病,多见于中老年患者,发病率约占血液系统恶性肿瘤的10%,缓解率低。近年来,随着蛋白酶体抑制剂硼替佐米的广泛应用,临床疗效有所提高,本文回顾性比较硼替佐米+环磷酰胺+地塞米松(PCD方案)和长春新碱+表阿霉素+地塞米松(VAD方案)治疗多发性髓瘤的疗效及相关不良反应,为今后多发性骨髓瘤的治疗选择提供参考依据。
1 材料与方法
1.1 临床资料
回顾天津市第一中心医院血液科2011年1月至2013年1月收治的多发性骨髓瘤患者41例,所有患者的诊断及分期均参照国际通用标准[1-2],将患者按照治疗方案的不同分为两个治疗组,两组患者在性别、年龄及疾病分型分期等方面的差异无统计学意义(表1,P>0.05)。
1.2 方法
1.2.1 化疗方案 PCD组:硼替佐米1.1~1.3 mg/m2·d,d1、4、8、11皮下注射,环磷酰胺400 mg/m2·d,d1、4、8、11静脉注射,地塞米松40 mg/d,d1、2、4、5、8、9、11、12静脉注射,d21~28为1个疗程。VAD组:长春新碱0.4 mg/ d d1~4持续静脉泵入,表阿霉素15 mg/m2·d,d1~4持续泵入,地塞米松20 mg/m2·d口服d1~4,d9~12,d17~20,d28~35为1个疗程。
1.2.2 疗效及不良反应评估 两组患者完成2~4个疗程后进行评估,疗效评估参照国际骨髓瘤工作组(IMWG)判断,不良反应评估标准参照WHO毒副反应分级标准。
1.3 统计学方法
采用SPSS 19.0软件进行统计学处理,计数资料的比较采用卡方检验或Fisher's精确概率法检验。P<0.05为差异有统计学意义。
2 结果
2.1 疗效
两组患者的疗效见表2,PCD组有效率(CR+VGPR+ PR)达42.9%,VAD组仅为15.0%,差异有统计学意义,PAD组中有3例达到完全缓解,而VAD组无一例达完全缓解。
2.2 分组疗效
所有患者中初治的多发性骨髓瘤患者21例,复发难治患者20例(表3,4),初治患者中PCD组有效率为75.0%,VAD组15.4%,差异有统计学意义(P=0.010),其中治疗反应良好的患者(CR+VGPR)PCD组50.0%,VAD组7.7%,差异有统计学意义(P=0.047),提示对于初治患者PCD方案的治疗有效率及缓解率均高于VAD方案。
2.3 不良反应
PCD组患者的神经毒性发生率高于VAD组(42.9%vs.10.0%),差异有统计学意义(P=0.043),其他不良反应如带状疱疹、消化道反应及血细胞减少的发生率PCD组亦稍高于VAD组,但差异无统计学意义。

表1 两组患者的一般资料比较Table 1 Comparison of baseline information of two groups
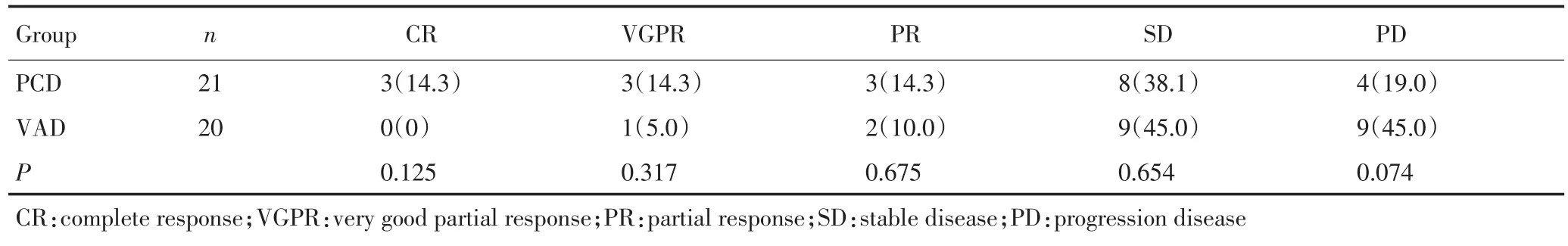
表2 两组患者的总体疗效比较 例(%)Table 2 Comparison of overall response rates of two groups n(%)
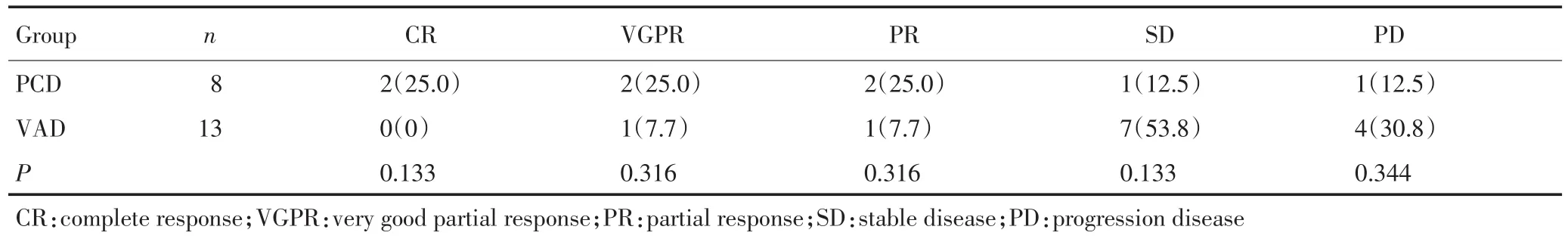
表3 两种方案对初治患者的疗效比较 例(%)Table 3 Efficacy comparison of newly diagnosed patients in the two groups n(%)
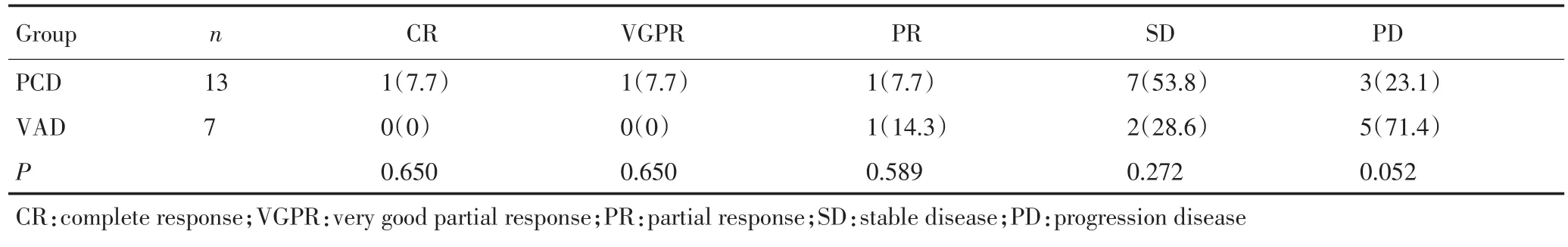
表4 两种方案对复发难治患者的疗效比较 例(%)Table 4 Efficacy comparison of relapsed/refractory patients in the two groups n(%)
3 讨论
多发性骨髓瘤的主要治疗手段为化疗,以往的治疗目标主要为达到或尽量延长平台期,而近年国内外多项研究表明,让患者尽早达到更高程度的缓解对延长患者的生存甚至治愈疾病至关重要,疗效达CR及VGPR是影响患者总生存的独立预后良好的因素[3-5]。随着蛋白酶体抑制剂硼替佐米的出现,多发性骨髓瘤的治疗缓解率从10%上升到了30%左右,同时有研究显示,硼替佐米与多种化疗药物有协同抗肿瘤效应[6-8],因此已成为临床治疗多发性骨髓瘤的一线用药[9],有报道[10]硼替佐米联合地寨米松、沙利度胺及阿霉素等药物对复发、难治及初治MM患者治疗有效率和缓解率可分别高达93%及64%。VAD方案作为传统的一线治疗方案目前国内指南仍在推荐应用,虽然其有效率不及含有硼替佐米的方案,但仍有其自身优势,如价格低廉、起效迅速、肾功能不全患者无需减量,因此目前仍有一定比例的患者选择应用。本观察中显示以硼替佐米为主的PCD方案较传统的VAD方案治疗有效率明显提高,特别是对于初治的多发性骨髓瘤患者,缓解率75%,完全缓解率达25%,另外13例复发难治的多发性骨髓瘤患者应用PCD方案治疗后有效率(CR+VGPR+PR)为23.1%,提示对传统化疗药物耐药的骨髓瘤患者对硼替佐米的治疗仍然敏感。
硼替佐米的不良反应包括乏力腹胀、血细胞减少、周围神经毒性等,其中神经毒性是硼替佐米临床应用的主要剂量限制因素,其具体的发生机制在人体中尚未得到证实,因此临床的防治措施主要依赖药物剂量的调整而不是发病机制的干预[11],目前APEXⅢ期临床研究提示早期调整用药剂量及周期,不影响疗效,能缓解周围神经病变[12]。另有研究表明,皮下注射硼替佐米能够减少药物的神经毒性,且不影响其疗效[13]。本观察中PCD组神经毒性发生率为42.9%,明显高于VAD组,有1例患者因麻痹性肠梗阻终止了硼替佐米的治疗,其他患者均为Ⅰ~Ⅱ级不良反应,经营养神经等对症治疗或减量应用硼替佐米后恢复正常。
本研究提示,无论对于初治还是复发难治的多发性骨髓瘤患者,PCD方案的有效率及完全缓解率均高于传统的VAD化疗方案,常见的不良反应为神经毒性,临床治疗中应注意密切观察,及时调整用药剂量。
1 Mckenna RW,Kyle RA,Kuehl WM,et al.WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues[M].Lyon:IARC Press,2008:200-208.
2 The Chinese medical doctor association branch of haematology department physicians,hematology branch of Chinese Medical Association.Diagnosis and treatment guideline of multiple myeloma in China [J].Chinese Journal of Internal Medicine,2013,52(9):791-795.[中国医师协会血液科医师分会,中华医学会血液学分会.中国多发性骨髓瘤诊治指南[J].中华内科杂志,2013,52(9):791-795.]
3 Ludwig H,Beksac M,Blade J,et al.Current Multiple Myeloma-Treatment Strategies with Novel Agents:A European Perspective[J]. Oncologist,2010,15(1):6-25.
4 Moreau P,Attal M,Pegourie B,et al.Achievement of VGPR to induction therapy is an important prognostic factor for longer PFS in the IFM 2005-01 trial[J].Blood,2011,117(11):3041-3044.
5 Liang ZY,Ren HY,Cen XN,et al.Bortezomib-based chemotherapy for patients with multiple myeloma:a single center experience[J]. Chinese Journal of Hematology,2014,35(3):225-230.[梁赜隐,任汉云,岑溪南,等.硼替佐米为基础的化疗方案治疗多发性骨髓瘤患者的疗效及预后因素分析[J].中华血液学杂志,2014,35(3):225-230.]
6 Rajkumar SV.Treatment of multiple myeloma[J].Nat Rev Clin Oncol,2011,20(8):479-490.
7 Neri P,Ren L,Gratton K,et al.Bortezomib-induced"BRCA-ness" sensitizes multiple myeloma cells to PARP inhibitors[J].Blood,2011, 118(24):6368-6379.
8 Yuan ZG,Jin J,Huang XJ,et al.Different dose combinations of bortezomib and dexamethasone in the treatment of relapsed or refractory myeloma:an open-label,observational,multi-center study in China[J].Chin Med J(En91),2011,124(19):2969-2974.
9 Bensinger WI,Jagannath S,Vescio R,et al.Phase 2 study of two sequential three-drug combinations containing bortezomib,cyclophos-phamide and dexamethasone,followed by bortezomib,thalidomide and dexamethasone as frondine therapy for multiple myeloma[J].Br J Haematol,2010,148(4):562-568.
10 Manoehakian R,Miller KC,Chanan-Khan AA.Clinical impact of bortezomib in frontline regimens for patients with multiple myeloma [J].Oncologist,2007,12(8):978-990.
11 Gu HT,Su GG,Gao GX,et al.Efficacy comparison between standard and reduced doses of bortezomib combined with adriamycin and dexamethasone in the treatment of patients with multiple myeloma[J].Chinese Journal opf Hematology,2013,34(7):622-625.[顾宏涛,舒汩汩,高广勋,等.标准和减低剂量硼替佐米联合阿霉素及地塞米松治疗多发性骨髓瘤疗效比较[J].中华血液学杂志,2013, 34(7):622-625.]
12 Richardson PG,Sonneveld P,Schuster MW,et al.Reversibility of symptomatic peripheral neumpathy with bortezomib in the phaseⅢAPEX trial in relapsed multiple myeloma:impact of a dose modification guideline[J].Br J Haematol,2009,144(6):895-903.
13 Arnulf B,Pylypenko H,Grosicki S,et al.Updated survival analysis of a randomized phaseⅢstudy of subcutaneous versus intravenous bortezomib in patients with relapsed multiple myeloma[J]. Haematologica,2012,97(12):1925-1928.
(2014-05-08收稿)
(2014-06-11修回)
(本文编辑:郑莉)
Clinical observation on PCD and VAD regimens for multiple myeloma
Qing LI,Yuming LI
Yuming LI;E-mail:lijiaos@yahoo.com.cn
Objective:To compare the efficacy and adverse effects of bortezomib+cyclophosphamide+dexamethasone(PCD)and vincristine+adriamycin+dexamethasone(VAD)regimens in multiple myeloma(MM).Methods:A total of 41 patients with MM were analyzed retrospectively and divided into two groups according to their treatment protocols:PCD group(21 cases)and VAD group(20 cases).Clinical effects and adverse effects were observed in both groups.Patients accepted two to four cycles of PCD or VAD regimens.Results:In the PCD group,three patients achieved complete remission(CR),three patients had very good partial remission(VGPR),three patients were under partial remission(PR),eight patients had stable disease status(SD),and four patients had progressive disease(PD).In the VAD group,none achieved CR,one patient had VGPR,two patients were under PR,nine patients had SD status,and nine patients had PD.The rate of patients who achieved efficacy(CR+VGPR+PR)in the PCD group was 42.9%,which was higher than that of the VAD group(15.0%).The rate of newly diagnosed patients who achieved good efficacy(CR+VGPR)in the PCD group was 50%,which was higher than that of the VAD group(7.7%).The incidence of herpes infection,cytopenia,fatigue,and gastrointestinal symptoms was similar in the two groups,whereas the incidence of neurotoxicity in the PCD group was higher than that of the VAD group.Conclusion:The response rate of PCD is higher compared with that of conventional VAD chemotherapy,especially in newly diagnosed MM.PCD may improve CR and VGPR rates and may bring about more severe toxicities,such as neuropathy.
multiple myeloma,therapy,adverse effects

10.3969/j.issn.1000-8179.20140930
李青 主治医师。研究方向为血液内科。
天津市第一中心医院血液科(天津市300192)
李玉明 lijiaos@yahoo.com.cn
Department of Hematology,The First Center Hospital,Tianjin 300192,China.
E-mail:15522388022@163.com

