核磁共振、乳腺钼靶、彩超对早期乳癌影像诊断的对比分析
罗 义,魏成刚,李阳敏
(1.南充市中心医院普外三科;2.南充市中心医院妇科,四川 南充 637000)
本刊网址:http://www.nsmc.edu.cn 作者投稿系统:http://noth.cbpt.cnki.net 邮箱:xuebao@nsmc.edu.cn
乳腺癌是女性最常见的恶性肿瘤之一,具有发病隐匿、预后差等特点。据统计,全球每年约有120余万妇女患乳腺癌,50 万妇女死于乳腺癌。我国妇女乳腺癌的发病率目前正以每年3% ~4%的增长率急剧上升,发病人群逐渐趋于年轻化,而迄今为止仍没有有效控制乳腺癌发病的一级预防措施。早发现,早治疗是治疗乳腺癌的关键[1],对降低乳腺癌死亡率和提高5 年生存率具有举足轻重的作用。因此,着力提高对早期乳腺癌的检出能力对提高患者生存率不失为一种有价值的策略。医学影像学技术是乳腺癌征象与病灶检测的主要手段,既方便又无创,常见影像学检查方法有乳腺钼靶X 线摄影、超声、CT、MRI 等,特别是MRI 自应用于临床乳腺疾病诊断以来,在乳腺癌诊断方面发挥了重要作用[2]。而由于乳腺X 线摄影对微钙化敏感性及其经济性,在乳腺癌普查中发挥巨大作用[3]。本研究拟探讨影像检查对早期乳腺癌的诊断价值。
1 临床资料与方法
1.1 临床资料
2009年3月至2012 年3 月经临床触诊检查怀疑乳腺癌而行MRI、乳腺钼靶、彩超检查,采用乳腺影像报告和数据系统(breast imaging reporting and data system,BI RADS)分类为Ⅲ类、Ⅳ类及Ⅴ类者共70 例。
1.2 检查及分析方法
1.2.1 MRI 检查 ①采用GE EXCITE HD1.5T 超导MRI 扫描仪和乳腺专用相控阵表面线圈,患者取俯卧位,双乳自然下垂。患者均采用飞利浦1.5T 超导MRI 扫描仪进行检查。患者取俯卧位,双乳对称自然悬于线圈洞穴内,阵列乳腺专用表面线圈或相控阵表面线圈,平扫T2WI 采用快速反转恢复自旋回波脂肪抑制序列(repetitiontime,TR,重复时间;echotime,TE,回波时间。TR/TE4200/90ms)。反转恢复STIR 序列(TR/TI/TE9999/150/60ms)。T1WI 选择二维FLASH 序列(TR/TE450/5ms,反转角90°),层厚3 ~5 mm、层距8 ~10 mm。若扫描一侧乳腺,以矢状位最常用。检查双侧乳腺多用冠状位和横断位。检查时须注意调整相位编码的方向,胸壁后加预饱和带,使用流动代偿技术,附加心电呼吸门控感应器以消除呼吸心跳伪影。乳腺增强MRI 检查选择动态扫描方式,采用二维快速梯度回波序列(2DFSPGR)加脂肪抑制技术,TR/TE 为200/5 ms,翻转角80°,FOV32×32,矩阵256 ×160,激发次数1,对比剂用量0.2 mmol/kg,速度2.5 ~3.0 mL/s,于10 s 内快速注入,分别在注射前、注射时、注射后1、2、4、7 min 扫描,根据病灶大小选取ROI。通过相关软件计算早期强化率、强化峰值,并绘制出时间-信号强度百分比曲线。平扫和动态增强扫描采用频率选择脂肪抑制技术,对双侧乳腺分别进行匀场、调整中心频率,以达到脂肪抑制最佳效果。②MRI 表现分析:分析每个乳腺病灶的MRI 形态学表现,包括病灶形状(圆形、类圆形、分叶状不规则形)、病灶边缘(光整、不光整)、病灶数目(单灶、多灶、多中心),并分析病灶内部强化(环状强化、非环状强化)、TSIC 类型(渐进型、平台型、廓清型)、早期强化率、对比剂注入后3 min 内强化峰值及ADC 值。所有病例的MRI 形态学特征及动态增强指标均由2 名有经验的影像科医师采用双盲法判定,共分为BI RADSⅠ~Ⅴ类,并通过讨论取得共识,作出评分、分类及诊断。
1.2.2 乳腺钼靶检查 ①使用设备:采用GE Senographe2000D 全野,数字化乳腺机,常规头尾位、CC 位、内外斜位摄片MLO 位。②MG 图像分析:分析指标包括病灶数目、病灶形态(圆形、椭圆形、分叶状、不规则)、病灶边缘(清晰、模糊、小分叶、浸润、星芒状)、病灶的密度(高密度、等密度、低密度)、含脂肪密度、钙化情况(恶性钙化、良性钙化、不定性钙化)、是否有结构扭曲及局灶性不对称等改变。所有病例的图像均分别由上述2 名有经验的影像科医师采用双盲法判定,共分为BI RADSⅠ~Ⅴ类,若意见不同,则通过讨论取得共识,再作出判断。
1.2.3 彩超检查 图像分析,分析指标包括病灶数目、病灶形态(不规则、病灶边缘清晰、模糊)、钙化情况(恶性钙化、良性钙化、不定性钙化)、局灶性不对称等改变。所有病例的图像均分别由上述2 名有经验的影像科医师采用双盲法判定,共分为BI RADSⅠ~Ⅴ类,若意见不同,则通过讨论取得共识,再作出判断。
1.3 统计学分析
本研究所有数据采用SPSS15.0 统计学软件进行统计学分析,实验数据用表示,采用t 检验,比较结果P <0.05 为差异有统计学意义。
2 结果
所有病例经病理诊断64 例为乳腺癌,对乳腺核磁共振、乳腺彩色多普勒超声、乳腺钼靶X 射线影像结果分别按照BI-RADS 及BI-RADS2US 进行分级比较。
影像检查结果见表1,MRI BI-RADS 分类以Ⅳ类及Ⅴ类为正确诊断,MRI 对乳腺癌的检出率为92.2%(59/64)。
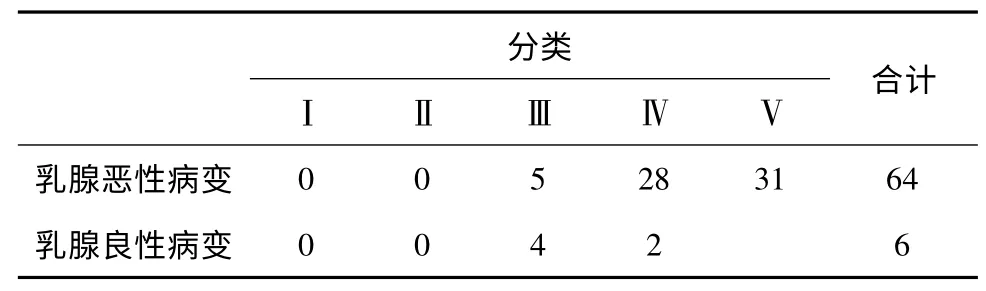
表1 70 例乳腺疾病的MRI BI-RADS 分类
乳腺MRI 对乳腺病变具有很高的敏感性,尤其对于致密型乳腺内的肿瘤、乳腺癌术后复发及乳房成形术后乳腺组织内有无癌瘤等的检出率高(图1、图2)。早期乳腺癌X 线检查特点,见图3。
图1 X 钼靶检查未发现病灶
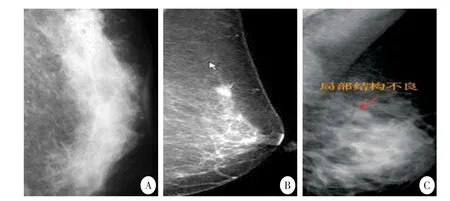
图3 早期乳腺癌X 线检查特点
由表2 可见,X 线BI-RADS 分类以Ⅳ类及Ⅴ类为阳性诊断,X 线对乳腺癌的检出率为78.1%(50/64)。
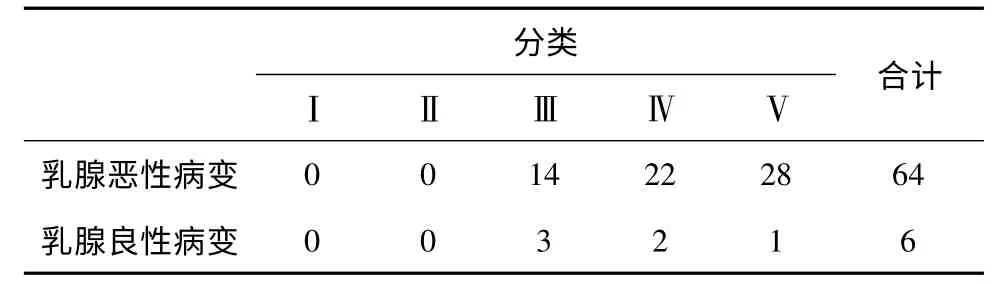
表2 70 例乳腺疾病的X 线BI-RADS 分类
由表3 可见,彩超BI-RADS 分类以Ⅳ类及Ⅴ类为阳性诊断,X 线对乳腺癌的检出率为73.4%(47/64)。
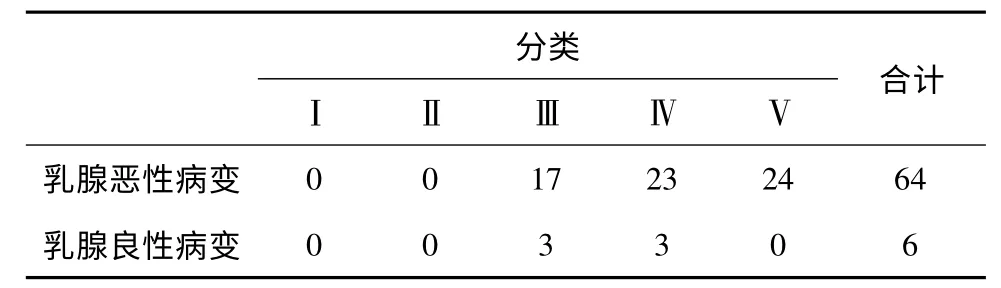
表3 70 例乳腺疾病的彩超BI-RADS 分类
MRI、乳腺钼靶和彩超对早期乳腺癌的检出率、灵敏度见表4,分别为92.2%和83.2%;78.1%和93.40%;73.4%和63.5%。MRI 高于乳腺钼靶和彩超组,差异有统计学意义(P <0.05)。
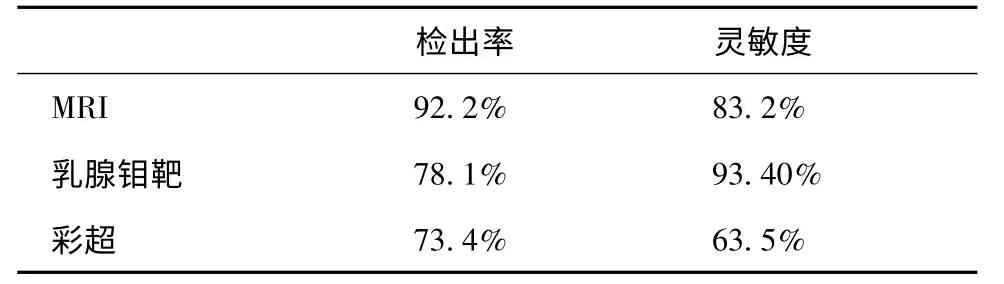
表4 MRI、乳腺钼靶和彩超对早期乳腺癌的检出率、灵敏度
3 讨论
研究表明,乳腺X 检查是发现乳腺早期肿瘤最重要的有效手段,检出临床隐匿乳腺癌和微小癌[4-5]。自从90 年代起欧美发达国家陆续开展乳腺X 线摄影筛查后,早期乳腺癌的诊断率猛增了4倍[6]。乳腺X 线能检出以钙化点为主要表现的乳腺癌,可以发现波长小、超声不能显示的钙化病灶影,这是其他设备无法替代的。而CR 乳腺钼靶摄影与普通X 线摄影相比更具有独特的优点,它最大限度减低了X 线照射剂量,可减少患者辐射损伤,因此可广泛应用于乳腺检查[7]。CR 密度分辨率高,提高病灶的对比度和清晰度,尤其对于较小病灶的发现,更利于疾病的早期诊断。但对于腺体致密的妇女,乳腺钼靶的敏感性降低,早期检出浸润性小叶癌的能力不足,对多灶癌的发现能力有限。也有研究指出乳腺钼靶检查对浆液性乳腺炎极易误诊为乳腺癌,以及X 线显示圆形肿块的单纯癌则易误诊为良性病[8]。因此,X 线检查有一定局限性。
乳腺超声检查无放射性损伤,能清楚分辨层次,不受位置限制,可提供肿瘤周围血流分布及血运情况。而且对纤维腺体丰富的致密型乳腺其价值尤高于X 线摄影检查,容易在强回声的乳腺纤维腺体层中分辨出表现为低回声的肿瘤病灶[9],并可了解腋窝及锁骨上淋巴结转移情况,可弥补乳腺X 线摄影在这方面的缺陷,因此,可与乳腺靶X 检查相互补充[10]。但老年患者的乳腺组织萎缩明显,在超声检查时乳腺与脂肪间层次不清,表现为低回声的脂肪颗粒可掩盖体积很小的肿瘤而无法确定有无占位[11]。而在有乳头溢液或血性溢液的情况下,部分肿瘤体积较小或沿乳腺导管分布未形成明确肿物,超声检查不易区别肿瘤与因肿瘤阻塞而引起扩张或有淤积物的乳腺导管,可进一步行乳管镜检查。
MRI 具有很高的软组织分辨力,动态增强检查对乳腺癌的诊断有较高的敏感性和准确性,国内胡静等[12]报道,MRI 对早期乳腺癌的诊断正确率可达94.4%,明显高于乳腺钼靶及彩超。作为最新的乳腺疾病检查手段,MRI 检查技术可以实现多平面、多参数成像检查的目标,具有高敏感性,三维成像使病灶定位更准确,显示更直观,对乳腺高位、深位病灶显示较好等特点,而且对多中心、多灶性病变的检出、临近胸壁的侵犯及腋窝、胸骨后、纵隔淋巴结转移的显示较为敏感等特点,为乳腺癌的分期和治疗提供了可靠依据。作为对高危患者检查的首选技术,其在疑难病例确诊、肿瘤病灶范围评估和化疗疗效评价以及手术方式选择等方面也发挥着不可替代的作用[13]。不过MRI 也有局限性,如价格昂贵、操作复杂、检查时间长、影像易受呼吸心脏搏动伪影的影响,且对钙化的显示不如钼靶[14]。
乳腺癌的早诊方法很多,乳腺核磁共振在早期乳癌检查中有较高的敏感性和准确性,但任何单项检查都有局限性,依成像原理不同,各有其优缺点。应根据具体情况和技术条件进行选择。
[1] 汪秀玲.乳腺影像诊断现状及进展[J].中华现代影像杂志,2005,2(6):515 -517
[2] 赵亚娥,胡 进,汪登斌,等.MRI 对小乳腺癌的诊断价值[J].外科理论与实践,2011,16(2):116 -170
[3] 谢 坪,何远智,付 凯,等.乳腺癌X 线表现分析[J].实用放射学杂志,2006,22(3):346 -348
[4] Smith-Bindman R,Chu P,Miglioretti DL,et al.Physician predictors of mammographic accuracy[J].J Natl Cancer Inst,2005,97(5):358 -367
[5] Rawal R,Lorenzo Bermejo J,Hemminki K.Risk of subsequent invasivebreast carcinoma after in situ breast carcinoma in a population covered by national mammographic screening[J].Br J Cancer,2005,92(1):162
[6] Patani N,Khaled Y,Al Reefy S,et al.Ductal carcinoma in-situ:an update for clinical practice[J].Surg Oncol,2011,20(1):e23 -31
[7] 蔡 丰,张 涛,郭章留,等.数字乳腺X 线机与传统乳腺X 线机的临床应用对比研究[J].中华放射学杂志,2002,36(11):981 -984
[8] 王双坤.早期乳腺癌的影像学检查方法[J].继续医学教育,2006,20(25):201 -203
[9] 汪登斌.乳腺导管原位癌的影像学研究[J].磁共振成像,2012,2(3):109 -113
[10] Warner E,Plewes DB,Hill KA,et al.Surveillance of BRCA1 and-BRCA2 mutation carriers with magnetic resonance imaging,ultrasound,mammography,and clinical breast examination[J].JAMA,2004,292(11):1317 -1325
[11] 高雅军.彩色多普勒超声及乳腺钼靶X 射线影像检查在乳腺原位癌早期诊断的对比分析[J].中华妇幼临床医学杂志,2012,2(8):43 -46
[12] Hu J,Wang DB,Jiang TT,et al.Analysis of MR findings in ductal breast carcinoma in situ[J].J Surg Concept Pract,2010,15(4):112 -116
[13] 赵琼惠,马雪华,杜 勇.乳腺钼靶X 线误诊分析[J].川北医学院学报,2001,28(5):48 -49
[14] 周 群,刘文新,于寅尧.动态增强联合钼靶X 线摄影对隐匿性乳腺癌的诊断价值[J].吉林医学,2012,24(33):714 -716

