高离子浓度溶液环境对修饰的β-环糊精主客体相互作用影响的研究
弓韬,梁文婷,董川*,杨成
(1.山西医科大学 基础医学院,山西 太原 030001;2.山西大学 环境科学研究所,山西 太原 030006;3.四川大学 化学学院,四川 成都 610064)
现代化学发展到今天,超分子化学由于其独特的性质受到人们日益关注。环糊精(Cyclodextrin,CD)作为一个经典的超分子主体分子,具有亲水性的外表和疏水性的内腔,可以通过主客体相互作用将尺寸适宜的分子包结在内,显著地改善被包结小分子的溶解度、稳定性等理化性质。环糊精及其衍生物的分子识别的一个重要特征是疏水相互作用,因此探讨水溶液中环糊精及其衍生物的构象,对于进一步考察环糊精衍生物的分子识别和催化机理有着重要意义。环糊精的内腔除了具有疏水性之外还具有手性,非手性的客体分子被包结后可以产生诱导的圆二色(ICD)信号。因此,圆二色光谱也成为一种研究环糊精主客体相互作用和包结能力的强有力手段。在环糊精边缘修饰的发色团与环糊精手性空腔的相互作用可以产生圆二色信号,我们就可以利用这种诱导的圆二色(ICD)信号来判定发色团在溶液中的空间位置和方向,并且研究对客体分子的识别和包结能力[1-3]。
环糊精主体对客体分子的包结现象的研究,通常是在纯水溶液或者水和有机溶剂的混合溶液中。这是由于适量有机溶剂,可以使得通过环糊精主体进行包结催化的反应在较低的温度下进行,但是在有机溶剂的存在下,环糊精对客体分子的包结作用会由于客体分子的疏溶剂作用减弱而大大减小,因而选择一种既能在低温下进行研究又能保持相对较强的包结作用的溶剂环境是非常有意义的[4-7]。基于此考虑,盐溶液引起了我们的关注,其中氯化锂(LiCl)和氯化钠(NaCl)两种溶液由于其可以达到的冰点温度低(根据CRC理化手册[8]提供的数据,我们可知质量分数为14%的LiCl溶液冰点可达-21℃;质量分数为22%的NaCl溶液冰点可达-19℃),且溶液无色、低毒性、易获得,成为我们研究考察的对象。本文利用圆二色光谱法研究了在不同溶液环境中,3种环糊精衍生物6-O-(邻-甲氧基苯甲酰)-β-环糊精(1)、6-O-(间-甲氧基苯甲酰)-β-环糊精(2)、6-O-(对-甲氧基苯甲酰)-β-环糊精(3)的构型变化及对环辛烯客体分子的包结现象并计算了包结稳定常数,并探讨了质量分数14%LiCl和质量分数22%NaCl两种高离子浓度溶液环境对环糊精主客体相互作用的影响,通过这3种修饰环糊精与客体分子相互作用的圆二色光谱可以看到在高离子浓度溶液环境中的,环糊精主体对客体分子的包结能力明显强于体积分数50%乙醇溶液,但与纯水相比有明显下降,这是由于高离子浓度环境对主体分子的发色团和客体分子都有着很强的疏溶剂作用,二者产生了竞争包结。
1 实验部分
β-环糊精衍生物1-3按文献方法[4-5]合成,其结构经元素分析,1H NMR,13C NMR和质谱鉴定。环辛烯经过蒸馏、氧化铝柱纯化。乙醇、LiCl、NaCl均为分析纯产品,分别配制成体积分数为50%的乙醇溶液、14%的LiCl溶液、22%的NaCl溶液待用。实验中所用水均为Milli-Q水。
光谱实验分别在JASCO J-720S圆二色光谱仪和JASCO V-560紫外光谱仪上测定。所使用样品池均为常规1 cm矩形石英池,测定温度为25℃。环糊精与客体分子形成主-客体包结物的包结稳定常数通过圆二色光谱滴定法测定,即固定主体化合物的浓度,改变客体分子的浓度,根据主体包结客体前后的光谱变化,通过曲线拟合的方法计算包结物的稳定常数[9]。

Fig.1 Structure of cyclodextrin derivatives 1-3 and cyclooctene图1 环糊精衍生物1-3和环辛烯结构示意图
2 结果与讨论
2.1 主体分子1-3在不同溶液中的紫外吸收和圆二色光谱
取相同浓度的主体分子,分别溶解在50%乙醇、纯水、14%LiCl和22%NaCl水溶液中,测定其紫外吸收光谱和圆二色光谱。为了消除主体分子浓度的影响而准确表示溶液对圆二色光谱的影响,我们将圆二色强度单位由摩尔椭圆度(θ)换算成摩尔吸收系数差(Δε)表示,如图2所示。其中不同的溶液分别由不同颜色的线表示:50%乙醇水溶液(黑色线)、纯水(红色线)、14%LiCl水溶液(绿色线)和22%NaCl水溶液(蓝色线)。

Fig.2 UV-vis and CD spectral of 1(a),2(b)and 3(c)in different aqueous solutions at 25 ℃,the concentration of 1-3 is 0.086 mmol/L图2 主体分子1(a)、2(b)和3(c)在不同水溶液中的紫外可见(上)和圆二色(下)光谱,检测温度为25℃,主体分子1-3的浓度均为0.086 mmol/L
从吸收光谱(图2上图)来看,在不同溶液中,主体分子1-3的特征吸收峰的位置没有明显位移。但从圆二色光谱(图2下图)看,在不同溶液中,相同的主体分子却表现出很明显的变化。从图2a所示的圆二色图谱看出,主体分子1在纯水中,它在245 nm处有一个相对较强的负Cotton效应峰,其可归属于1La带;在297 nm处有一个非常弱的负Cotton效应峰,应归属为1Lb带。根据Kajtar等人提出的扇形规则[10](如图3a所示),在客体(或取代基)发色团包结到环糊精的手性空腔后,如果它的电跃迁矩平行于环糊精的对称轴,则该跃迁对应的诱导圆二色Cotton效应为正值;相反,如果电跃迁矩垂直于环糊精的对称轴,则其对应的诱导圆二色Cotton效应为负值。由此可见,在纯水中,修饰在环糊精分子第一面上的发色团仅有很少一部分横向包结在环糊精空腔内或者仅仅是掩盖在环糊精第一面的边缘,而由于发色团在50%乙醇溶液中溶解性增加,其1La带和1Lb带均表现出更加明显的负的Cotton效应峰(如图3a所示)。相反,在14%LiCl溶液中,其1La带和1Lb带表现出减弱负的 Cotton效应峰;而在22%NaCl水溶液中,发色团的1La带表现出正的Cotton效应峰,1Lb带的Cotton效应峰几乎消失,这表明在高离子强度的盐溶液环境中,由于疏水作用,发色团的1La带变得与扇形的纵轴更加平行(如图3a所示)。

Fig.3 (a)The sector rule applied toβ-cyclodextrin derivatives in different solvent.(b)Proposed conformations of 2 in different aqueous solutions.The big circle,ellipse and ellipse around small circle indicate the ethanol molecule,H 2 O molecule and aquo ions,respectively图3 (a)溶液中β-环糊精衍生物的圆二色变化遵循的扇形规则 (b)主体分子2在不同溶液中可能的构象。其中,大圆形代表乙醇分子,椭圆形代表水分子,椭圆形围绕小圆形表示盐水合离子
对于主体分子2,除了在50%乙醇溶液中,归属于1La带的248 nm处有一个弱的负Cotton效应峰,在纯水、14%LiCl和22%NaCl水溶液中则表现为越来越强的正的Cotton效应峰;而在归属为1Lb带的295 nm处,在50%乙醇溶液和纯水中Cotton效应峰几乎消失,14%LiCl和22%NaCl水溶液中则表现出一个非常弱的负Cotton效应峰。
虽然主体分子3与主体分子1、2仅仅是苯环上的甲氧基取代位置的不同,但是由于其电子跃迁有很大的不同,其紫外吸收光谱有很大的差异。观察其圆二色光谱,在270 nm处,除了在50%乙醇溶液中Cotton效应峰几乎消失,在纯水、14%LiCl和22%NaCl水溶液中则表现为越来越强的正的Cotton效应峰。
对比各个主体在纯水溶液中的圆二色光谱可以看出,主体分子1、2、3都为结构相似的简单修饰环糊精,但仅仅由于苯环上甲氧基取代的位置不同,就可能导致的发色团处于环糊精空腔的位置并不相同,处于邻位的甲氧基取代基会产生较大的位阻,从而影响发色团深入到环糊精空腔,而处于对位的甲氧基取代基则有较大的旋转自由度,可以较深地伸入到环糊精的空腔中。而极性从弱到强的溶液环境,使得发色团的芳香环与环糊精母体空腔分别产生了未包结、较弱的自包结和较强的自包结形式。而改变盐溶液阳离子的种类并未产生明显的作用,而仅仅是离子浓度表现出了明显的影响(如图3b所示)。
2.2 主体分子1-3在不同溶液中与环辛烯的主客体相互作用
主体分子1-3在不同溶液环境中分别具有未包结、浅包结和深包结三种形式,为了考察不同溶液环境及不同取代基构象对客体分子包结能力的影响,我们选用环辛烯作为模型客体分子,采用圆二色谱滴定法测定了主体化合物与模型客体分子环辛烯在25℃时的光谱变化,主体分子2的圆二色滴定图谱如图4所示。根据公式(1),我们选取波长λ=217 nm处的圆二色光谱变化数据,拟合了不同溶液中的包结稳定常数Ks,结果列于表1。

公式中,[G]0代表客体分子的总浓度,[CD]0代表环糊精的总浓度,θ1代表只有环糊精(CD)存在时的摩尔椭圆率,θx代表任意浓度时环糊精CD 与客体G的摩尔椭圆率,θs代表客体完全包结时的摩尔椭圆率[9]。
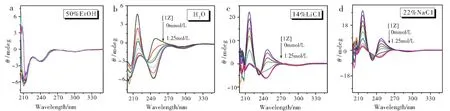
Fig.4 CD spectral changes of 2 (0.086 mmol/L)in different solutions at 25 ℃(a)2 in 50%EtOH aqueous solutions upon increasing the concentration of 1Z from 0 to 3.0 mmol/L (b)2 in pure water upon increasing the concentration of 1Z from 0 to 1.25 mmol/L.(c)2 in 14%LiCl aqueous solution upon increasing the concentration of 1Z from 0 to 1.25 mmol/L and(d)2 in 22%NaCl aqueous solution upon increasing the concentration of 1Z from 0 to 1.25 mmol/L图4 0.086 mmol/L的主体分子2随着客体分子浓度增加在不同溶液中的圆二色光谱变化,测量温度25℃.(a)50%乙醇溶液中,环辛烯浓度从0到3.0 mmol/L。(b)纯水中,环辛烯浓度从0到1.25 mmol/L。(c)14%LiCl溶液中,环辛烯浓度从0到1.25 mmol/L.(d)22%NaCl溶液中,环辛烯浓度从0到1.25 mmol/L
如图4a所示,缓慢加入客体分子环辛烯之后,在50%乙醇溶液中,在加入客体分子的过程中,未表现出明显的圆二色信号变化,这是由于溶液环境极性较低,修饰在环糊精上的发色团几乎未被包结在环糊精的空腔内,因此在加入客体分子后,发色团所处的位置构象并未发生明显变化。但从图4b-4d可以看出,在极性较强的水溶液及盐溶液中,客体分子的加入引起了明显的圆二色信号变化,表明主体分子上的发色团在加入客体分子后,其位置和环境发生了显著的变化。根据圆二色滴定光谱,我们计算出在不同溶液环境中,主体分子1-3对客体分子的1∶1包结常数,如表1所示。从包结稳定常数我们看到,对于主体分子1-3在纯水中的包结稳定常数都远大于在其他溶液环境中的包结稳定常数,这表明对于客体分子,在纯水有很强的疏溶剂作用力,使得客体分子能稳定的包结在环糊精空腔内。而在盐溶液环境中,高离子强度使得疏溶剂效应不但作用于客体分子使其包结于环糊精的空腔内,而且强有力的作用于主体分子的发色团,使其与客体分子存在一定竞争包结的作用,从而使得包结稳定常数显著减小。

表1 不同溶液环境中25℃下主体分子1-3对环辛烯的包结稳定常数KSTable 1 Stability constant(KS)for the 1∶1 inclusion complexation of cyclooctene with 1-3 in different solvent at 25 ℃
综上所述,我们利用圆二色光谱法,通过对比在不同溶液环境中环糊精衍生物的构象及对环辛烯分子的包结能力,研究高离子强度溶液环境对环糊精主客体相互作用的影响,首次探讨了β-环糊精衍生物在高离子浓度溶液环境中的分子识别能力。结果表明,通过这3种修饰环糊精与环辛烯分子相互作用的构型变化,可以看出与纯水相比,在高离子强度溶液环境中的主体分子对客体分子包结能力有所减弱,推断其原因有可能是高离子浓度对主体分子上修饰的发色团的疏溶剂作用影响了环糊精主体对客体分子的包结能力,但是,与有机溶剂-水混合溶液相比,β-环糊精衍生物与客体分子在高离子浓度溶液中仍保持了较高的包结稳定常数,为进一步拓展环糊精在高离子浓度溶液环境中的应用提供了基础。
[1] Lehn J M.Comprehensive Supramolecular Chemistry[M].Amsterdam:Elsevier Science Ltd,1996.
[2] Inoue Y.Asymmetric Photochemical Reactions in Solution[J].ChemRev,1992,92:741-770.
[3] Tong L H,Hou Z J,Inoue Y,etal.Novel Acyclic Receptors Foraromatic Amines Using Peptidic Frameworks[J].JChem Soc,PerkinTrans2,1992:1253-1257.
[4] Lu R,Yang C,Cao Y,etal.Enantiodifferentiating Photoisomerization of Cyclooctene Included and Sensitized by Aroyl-beta-cyclodextrins:a Critical Enantioselectivity Control by Substituents[J].JOrgChem,2008,73:7695-7701.
[5] Yang Lu R,Cao C,Wang Y,etal.Supramolecular Enantiodifferentiating Photoisomerization of Cyclooctene with Modified β-cyclodextrins:Critical Control by a Host Structure[J].ChemCommun,2008,3:374-376.
[6] Liang W,Yang C,Nishijima M,etal.Cyclodextrin Nanosponge-Sensitized Enantiodifferentiating Photoisomerization of Cyclooctene and 1,3-Cyclooctadiene[J].BeilsteinJOrgChem,2012,8:1305-1311.
[7] Liang W,Yang C,Zhou D,etal.Phase-controlled Supramolecular Photochirogenesis in Cyclodextrin Nanosponges[J].ChemCommun,2013,49:3510-3512.
[8] David R.Lide.CRC Handbook of Chemistry and Physics,90th Edition Internet Version[M].Boca Raton:Taylor &Francis Group,2010.
[9] Inoue Y.Yamamoto,Wada K,Everitt T,Gao S,etal.Inclusion Complexation of(Cyclo)Alkanes and (Cyclo)Alkanols with 6-O-modified Cyclodextrins[J].JChemSoc,PerkinTrans,1998,2:1807-1816.
[10] Kajtar M,Horvath-Toro C,Kuthi E,etal.A Simple Rule for Predicting Circular Dichroism Induced in Aromatic Guests by Cyclodextrin Hosts in Inclusion Complexes[J].ActaBiochimBiophysAcadSciHung,1982,110:327-355.

