AIDS抗病毒药物的不良反应
王辉,周伯平
·专题综述·
AIDS抗病毒药物的不良反应
王辉,周伯平
目前已有超过25种抗HIV药物在临床使用,尽管抗病毒药物的耐受性和安全性在不断完善,但药物不良反应仍然是影响AIDS患者服药依从性及导致抗病毒治疗失败的重要原因,了解药物不良反应尤为重要。随着抗病毒治疗新药的涌现,服用新药引起的不良反应尚须进一步观察。
获得性免疫缺陷综合征;抗逆转录病毒治疗,高效;抗病毒药
1987年第一种抗反转录病毒药物齐多夫定(AZT或ZDV)问世,但并没有为AIDS患者带来明显的益处,这种核苷类反转录酶抑制剂(nucleoside reverse transcriptase inhibitors,NRTIs)虽然对HIV复制起到一定的抑制作用,但是几乎所有服药者在治疗12周后出现病毒反弹。之后,又有几种新的NRTIs进入临床,使用2种NRTIs联合治疗可加强抗病毒作用,且疗效维持时间更长,但是仍不能长期维持疗效。20世纪90年代中后期抗病毒治疗进入一个新时期,随着蛋白酶抑制剂(protease inhibitors,PIs)的应用,1种PIs┼2种NRTIs联合疗法具有非常强大的抗病毒作用,可使HIV RNA在血浆中检测不到,且可长期维持疗效,这种合理有效的联合用药被称为高效抗反转录病毒治疗(highly active antiretroviral therapy,HAART)。随后经过多年的实践证明,一些不包括PIs的组合,如1种非NRTIs(non-NRTIs,NNRTIs)┼2种或3种NRTIs[其中必须包括阿巴卡韦(abacavir,ABC)],或1种整合酶抑制剂(integrase inhibitors,INSTIs)┼2种NRTIs也可达到相同或相似效果。HAART的出现将AIDS这个“世纪绝症”转变为可防可治的慢性病。目前,临床已有超过25种针对HIV各个阶段的不同类型的药物,抗病毒治疗组合也向毒性更低、效果更好、服用更方便、服用次数更少的方向发展。当前在发达国家,抗病毒治疗组合一线药物推荐2种NRTIs┼1种NNRTIs或PIs或INSTIs,而发展中国家的一线方案则推荐2种NRTIs┼1种NNRTIs[1]。尽管抗病毒药物有良好的耐受性及安全性,但用药后产生不良反应的报道也较常见,有时药物不良反应是导致患者服药依从性差及治疗失败的重要原因。目前,有些抗病毒药物因其不良反应已逐渐退出治疗组合(如司他夫定、地丹诺辛和茚地那韦),而与此同时,有些新上市药物的不良反应因应用时间有限还不能完全了解[如德特格韦(dolutegravir)]。但无论何种药物组合均有其优缺点。在长期临床用药中应权衡利弊,根据患者的实际情况选择合理方案。
1 抗病毒药物的分类及名称(表1)
2 AIDS抗病毒药物的不良反应
2.1 骨髓抑制骨髓抑制是服用AZT的常见不良反应,通常发生在服药后的数周至数月,临床表现为贫血(常常为大细胞性)及中性粒细胞缺乏。避免的措施为开始HAART前检测血常规,勿与其他有骨髓抑制作用的药物如更昔洛韦、利巴韦林及磺胺类药物同时使用。并做好服药后的随访检查,定期监测血常规的变化情况。
2.2 心血管系统的不良反应HIV感染会增加心血管疾病(cerebrovascular disease,CVD)的风险,因此通过抗病毒治疗(antiretroviral therapy,ART)降低病毒载量有助于减少HIV感染者并发CVD的风险。但是,ART又能增大患者出现心肌梗塞(myocardial infarction,MI)的风险,这种风险的增加与抗病毒药物的种类有关[2]。有报道在服用PIs及NRTIs药物ABC和dd I数年或数月后会增大MI或心血管事件发生的危险,发生率为3~6/1000[3]。吸烟、高龄、高脂血症、高血压、糖尿病家族史及有冠状动脉疾病史的患者在ART后会增加CVD发生的危险。因此,患者在接受ART前应评估CVD的危险因子,根据具体情况选择对脂代谢影响小的抗病毒药物组合;ART后监测血糖和血脂;通过戒烟、减肥及运动改变生活方式。
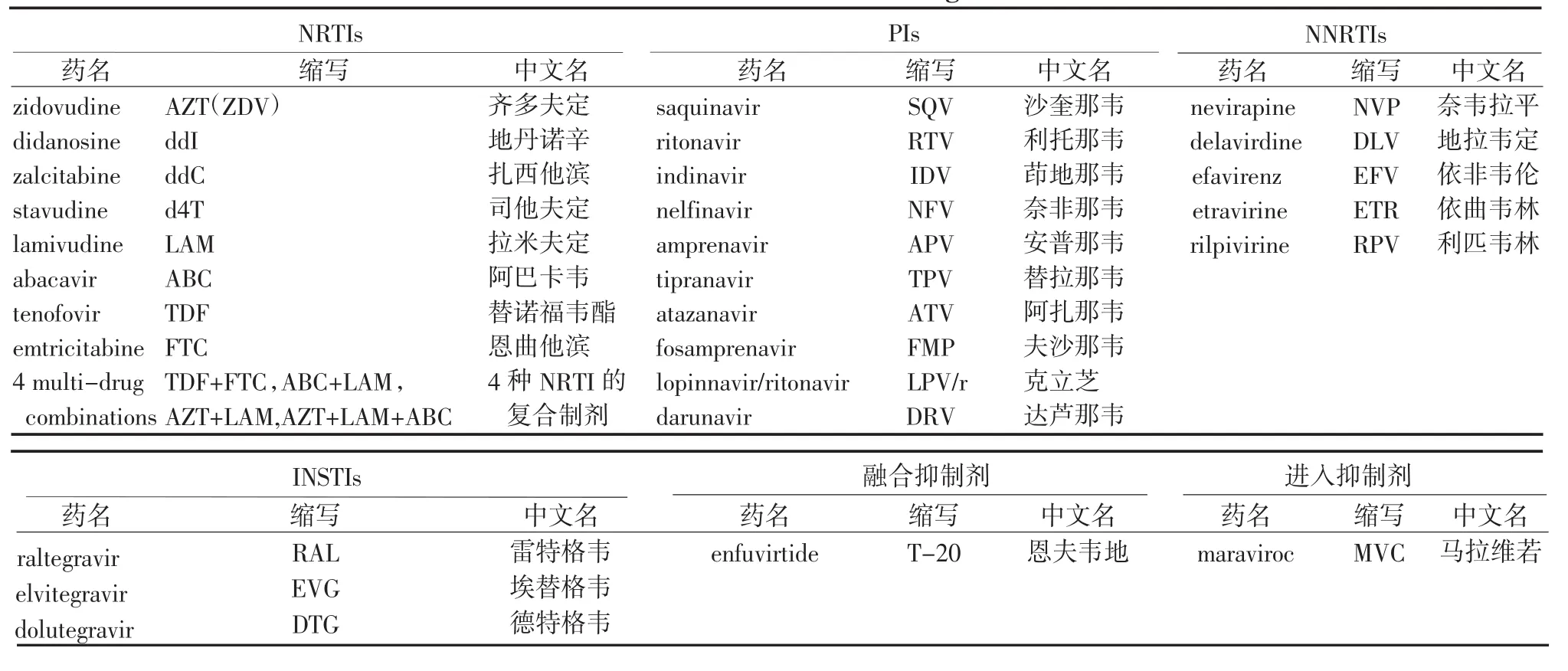
表1 AIDS抗病毒药物的分类与名称Table 1 Names and classes of antiviral agents for AIDS
2.3 中枢神经系统不良反应有近50%的患者在服用EFV后会立即出现嗜睡、多梦、失眠、怪梦、头晕、注意力无法集中、抑郁、幻觉、精神失常甚至自杀念头,大多数症状会在服药2~4周后减退或消失[4]。服药前有精神疾患的患者应尽量避免使用EFV,研究显示有些患者具有CYP2B6酶的基因多态性从而血药浓度超高,药物不良反应也较严重[5]。EFV应在睡前或睡前2~3 h服用,空腹服药会降低药物的血药浓度,在服药的前2~4周应避免从事机械操作。
2.4 消化道不良反应几乎所有患者在服用AZT、dd I及PIs后都会出现不同程度的恶心、呕吐、腹痛及腹泻等消化道不良反应。通常出现在治疗的前2个月内,但大多数并不严重,可对症处理,随着时间的推移将逐渐好转。服药时如同时进食,可以减少某些消化系统的药物不良反应,除非药物有特别指出进食限制(如ddI和EFV应空腹服药)。
2.5 肝毒性(药物性肝炎及无症状的转氨酶升高)
所有NNRTIs在服药后的最初3个月、所有PIs在服药后的数周至数月、大多数NRTIs在服药后的数月至数年内以及进入抑制剂(又称CCR5抑制剂)MVC在用药后都会出现不同程度的肝损伤;使用NNRTIs出现的肝损伤往往伴皮疹和嗜酸性粒细胞升高,严重时还会引起肝衰竭;而使用NRTIs因其线粒体毒性,在导致肝损伤的同时常伴高乳酸血症;TPV/r或其他PIs也能导致不同程度的肝损伤[6]。男性CD4+T细胞计数≥400个/mm3,女性CD4+T细胞计数≥250个/mm3的患者使用NVP会增加发生肝毒性的危险;另外合并慢性乙型肝炎、丙型肝炎、酒精成瘾、基线转氨酶升高及同时服用其他肝损伤类药物的患者,应密切监测服药后肝功能的变化,如转氨酶升高超过正常5~10倍,应立即停药,待肝功能恢复正常后更换其他类型的药物组合,切勿再次使用同类肝损伤类药物。
2.6 高脂血症除ATV之外的所有PIs及d4T、EFV和NVP在开始服药后的数周至数月后均可导致血脂升高。PIs会引起血清总胆固醇(TC)、甘油三酯(TG)及低密度脂蛋白(LDL)升高,其中LPV/r会引起TG单指标升高,所有RTV强化的PIs都有使LDL和TG升高的不良反应,只有ATV引起的高脂血症程度较轻。而NNRTIs如EFV和NVP则会引起TC和LDL升高,伴轻度TG和高密度脂蛋白升高,血脂升高程度EFV>NVP。NRTIs中d4T和AZT则会引起LDL、TC和TG升高,血脂升高程度d4T>AZT>ABC>TDF。
研究显示PIs中DRV和ATV相对较少引起血脂异常;而NVP对血脂代谢的影响低于ATV/r;使用Kivexa(ABC┼LAM)组合的患者血脂升高的幅度高于使用Truvada(TDF┼FTC)的患者;INSTIs中RAL和进入抑制剂MVC较少引起血脂异常[7]。
2.7 皮肤或全身超敏反应大约5%~8%的患者在服用ABC后1~6周内会出现超敏反应,临床表现为高热、播散性皮疹、精神萎靡、黏膜受损、头痛和腹痛等,研究显示HLA-B5701筛查阳性的患者发生ABC超敏反应的几率较大[8]。抗病毒治疗前应常规筛查HLA-B5701,阳性患者应避免使用ABC。注意对已发生过超敏反应的患者应避免再次使用ABC。
服用EFV和NVP(尤其是NVP)后也会引起皮疹,一般发生在治疗开始的1~4周。如果是EFV导致的轻度皮疹,多数会在皮疹出现后3~5 d自动消失。而NVP引起的皮疹多较重,约1%的患者甚至会出现Stevens-Johnson综合征[4]。出现重度皮疹的患者应立即停药,待皮疹恢复后选用其他类药物治疗。
2.8 肾毒性HAART对HIV感染者的肾功能及慢性肾病发病率的总体作用至今仍存争议,数项队列研究已证实HAART对肾功能存在正面作用。事实上,引入新型抗反转录病毒药物方案后病毒被持续抑制与慢性肾脏病(chronic kidney disease,CKD)的发病率下降及肾小球滤过率评估值的显著改善相关。然而,HAART本身可导致肾毒性作用,且HIV感染者如长期应用抗反转录病毒药物可能通过数种发病机制导致肾功能不全的发生[9]。
PIs中IDV最常见与肾毒性反应相关,包括肾结石、小管内药物沉积、结晶尿、排尿困难、血尿、肾绞痛、乳头坏死、肾萎缩、急性间质性肾炎及急慢性肾功能衰竭。早在开始IDV治疗后1周时即可发生,且在肾脏和尿道的任何结构处可能形成由IDV组成的尿结晶。接受IDV治疗的患者中约20%存在结晶尿,其中有3%可进一步发展至肾结石[9]。可见与RTV、SQV和LPV/r治疗相关的肾结石和急性肾损伤报道,但肾损伤的病因仍不十分明确。虽然在临床研究中ATV不与尿石症或结晶尿相关,但在接受ATV治疗的患者中有数个肾结石及间质性肾炎的病例报道。
NNRTIs肾毒性的数据非常有限,因为在对照试验中NVP、EFV和ETV通常表现出安全的肾脏特性。
NRTIs相关的肾毒性在临床试验中一般不常见,以NRTIs为基础的治疗可能导致线粒体毒性,20%~30%接受NRTIs治疗的HIV感染者可因线粒体损伤而导致无症状性高乳酸血症,在少数情况下也可导致严重的乳酸酸中毒和急性肾功能衰竭。
目前,TDF相关的药物诱导的肾脏毒性反应引人注目,数篇病例报告及研究发现TDF治疗可诱导潜在肾脏毒性反应,其中大多数包括伴Fanconi综合征的近端肾小管病变及肾源性尿崩症[9]。TDF是最常见的与Fanconi综合征相关的抗反转录病毒药物,Fanconi综合征很可能导致钙磷调节紊乱、急性肾功能衰竭和骨软化症及骨折。另外,对TDF临床试验的数据分析提示,肾小球滤过率轻度下降可能散在发生[9]。在接受TDF治疗的患者中高龄、低体重、TDF血浆浓度高及同时合用ddI、APV或RTV加强的PIs,以及ABCC2基因多态性的患者CKD风险会明显升高。因此应用TDF的患者应该考虑对肾功能和肾小管功能不全标记物进行长期监测,尤其是那些存在合并疾病(如之前已患肾脏疾病、高血压及糖尿病)或存在致病因素(包括高龄和同时接受加强PIs或其他肾毒性药物治疗)的患者。
至今尚无证据表明融合抑制剂(T-20)、进入抑制剂(MVC)或INSTIs(RAL)存在潜在的肾毒性作用。
2.9 外周神经炎主要由NRTIs中的d4T、dd I和ddC引起,常发生在服药后的数周至数月后,发病率为12%~52%[4]。临床表现显示为逐渐进展的过程,一开始患者会出现肢体末端感觉异常或麻木,继而会出现双足及小腿疼痛,然后逐渐进展到外周神经病变。上肢很少受累,部分患者可表现为乏力或虚弱。
2.10 胰腺炎服用dd I后会有1%~7%的患者出现胰腺炎不良反应,若ddI联合d4T、TDF、利巴韦林和羟基脲应用时胰腺炎发病率会明显升高4~5倍[4]。因目前dd I已退出临床,由其引起的胰腺炎已少见。
2.11 脂肪代谢障碍脂肪代谢异常包括脂肪萎缩和脂肪沉积2个方面,是临床上长期服用抗病毒药物治疗后常见的不良反应,通常在治疗后的数月或数年后出现。
服用含有胸苷类似物的NRTIs(如AZT或d4T)会导致脂肪丢失,多发生在面部、四肢及臀部,这种现象会在更换其他NRTIs后得以部分恢复。而服用PIs和NNRTIs则会引起脂肪沉积,多发生在腹部、上背部、乳房及皮下组织,观察性研究发现不同组合的抗病毒药物引起脂肪沉积的可能性相似,更换药物并不能使脂肪沉积的程度有所改变。
另有研究显示服用EFV┼NRTIs较PIs┼NRTIs出现脂肪萎缩的危险性更高,分析原因是因为PIs能部分改善由NRTIs诱导的细胞凋亡,而EFV因能释放更多炎性细胞因子或其线粒体毒性而增加NRTIs对脂肪细胞的毒性[10]。
避免选择含有胸苷类似物的NRTIs可防止患者出现脂肪萎缩,而脂肪沉积是长期抗病毒治疗后不可避免的不良反应。
2.12 骨质疏松及骨坏死到目前为止尚不清楚AIDS患者的骨坏死是抗病毒药物的不良反应还是由HIV感染引起。AIDS进展期、糖尿病、高脂血症、老年患者、酒精成瘾及激素使用史都是骨坏死的危险因素,服用TDF和骨坏死的关系还有争议。
有服用TDF和d4T后出现骨质疏松的报道,临床也观察到服用TDF能导致骨密度降低,发生率明显高于健康人群[11-12]。骨质疏松一般在服药后的数月至数年后出现,一般无症状,如骨痛即有发生骨折的危险。低体重、妇女、老人、吸烟、饮酒、性机能减退、甲状腺功能亢进、使用激素及服用TDF都是发生骨质疏松的危险因素。
2.13 胰岛素依赖及糖尿病超过3%~5%的AIDS患者在服用含胸苷类似物的NRTIs(如d4T或AZT)及一些PIs数周至数月后会出现胰岛素耐受或糖尿病[4]。临床上会出现多尿、烦渴、多食、疲劳、乏力及血糖升高等。有家族性糖尿病的患者应尽量避免选择含有胸苷类似物的NRTIs。
2.14 乳酸酸中毒所有NRTIs都可能导致乳酸酸中毒,尤其是d4T、dd I和AZT,随着d4T和dd I逐渐退出市场,抗病毒药物引起的乳酸酸中毒临床较少见,但一旦发生则有致命的危险。抗病毒药物引起的乳酸酸中毒多发生在治疗后的8~9个月,如患者出现无缘由的疲惫乏力、呼吸加快、恶心、呕吐、腹痛、肌肉疼痛及体重减轻等症状时,须考虑乳酸酸中毒,并及时进行血乳酸浓度、动脉血pH值和血碳酸氢根离子的检测。确诊为乳酸酸中毒后须立即停药。妊娠为高危因素,应避免给予含有胸苷类似物的d4T和dd I,并须密切监测血乳酸的变化。
2.15 出血PIs会诱发血友病患者发生皮下出血。有报道TPV/r会引起颅内出血,一般发生在用药1年后,如果患者有中枢神经损伤、外伤性头痛、近期接受过神经外科手术、高血压、酒精依赖、同时服用抗凝及抗血小板因子类药物(包括维生素E)及血友病,建议避免选用PIs[13-14]。
2.16 免疫重建炎性综合征免疫重建炎性综合征是在抗病毒治疗后发生的因机体的快速免疫重建而对已存在的病原体的特异性免疫反应,可在抗病毒治疗后的1~120 d内发生,发病率约16%[1]。免疫重建炎性综合征通常发生于开始治疗时CD4+T细胞计数较低且伴机会性感染的患者,这些机会性感染和肿瘤包括分枝杆菌(结核和非结核)、病毒(巨细胞病毒、疱疹病毒、HBV、HCV和引起进行性多发性脑白质病变的JC病毒)、真菌(隐球菌和念珠菌)以及肿瘤(卡波西氏肉瘤和淋巴瘤)。临床表现为发热、淋巴结肿大及原有感染在治疗中加重或原先隐匿的感染出现。在较高的CD4+T细胞基数时开始抗病毒治疗可减少免疫重建炎性综合征的发生;治疗前常规筛查机会性感染;对有机会性感染的患者应适当延迟开始抗病毒治疗的时间。
经过全世界科学家近30年的不断努力,抗反转录病毒药物在疗效和安全性方面都得到了改善,但在还没有疫苗的情况下,预防及减少长期服药后不良事件的发病率仍是主要方向[15-16]。
[1]Maartens G,Celum C,Lewin SR.HIV infection:epidemiology, pathogenesis,treatmentand prevention[J].Lancet,2014,384(9939): 258-271.
[2]DAD Study Group,Friis-Møller N,Reiss P,et al.Class of antiretroviral drugs and the risk ofmyocardial infarction[J].N Engl J Med,2007,356(17):1723-1735.
[3]DAD Study Group,Sabin CA,Worm SW,et al.Use of nucleoside reverse transcriptase inhibitors and risk ofmyocardial infarction in HIV-infected patients enrolled in the D:A:D study:amulti-cohort collaboration[J].Lancet,2008,371(9622):1417-1426.
[4]Paul ES,Calvin JC,Daniel RK.HIV Essentials[EB/OL].[2014-08-20].http://yuedu.baidu.com/ebook/ccf753d380eb6294dd886ce0. html.
[5]Rodriguez-Novoa S,Barreiro P,Rendón A,et al.Influence of 516G>T polymorphisms at the gene encoding the CYP450-2B6 isoenzyme on efavirenz plasma concentrations in HIV-infected subjects[J].Clin Infect Dis,2005,40(9):1358-1361.
[6]Chan-Tack KM,Struble KA,Birnkrant DB.Intracranial hemorrhage and liver-associated deaths associated with tipranavir/ritonavir:review of cases from the FDA's Adverse Event Reporting System[J].AIDSPatient Care STDS,2008,22(11):843-850.
[7]沈银忠.抗反转录病毒治疗对血脂代谢及心血管系统的影响[J].中国艾滋病性病,2013,19(1):81-85.
[8]Mallal S,Phillips E,Carosi G,etal.HLA-B*5701 screening for hypersensitivity to abacavir[J].N Engl JMed,2008,358(6):568-579.
[9]Maggi P,Bartolozzi D,Bonfanti P,et al.Renal complications in HIV disease:between present and future[J].AIDSRev,2012,14 (1):37-53.
[10]de Waal R,Cohen K,Maartens G.Sys tematicreview of antiretroviral-associated lipodystrophy:lipoatrophy,but not central fat gain,is an antiretroviral adverse drug reaction[J].PLoSOne,2013, 8(5):e63623.
[11]Assoumou L,Katlama C,Viard JP,etal.Changes in bonemineral density over a 2-year period in HIV-1-infected men under combined antiretroviral therapy with osteopenia[J].AIDS,2013,27(15): 2425-2430.
[12]Lucey JM,Hsu P,Ziegler JB.Tenofovir-related Fanconi's syndrome and osteomalacia in a teenager with HIV[EB/OL].[2014-08-20].http://www.ncbi.nlm.nih.gov/pubmed/?term=Tenofovir-related+Fanconi's+syndrome+and+osteomalacia+in+a+teenager+ with+HIV.
[13]Kort JJ,Aslanyan S,Scherer J,et al.Effects of tipranavir, darunavir,and ritonavir on platelet function,coagulation,and fibrinolysis in healthy volunteers[J].Curr HIV Res,2011,9(4):237-246.
[14]Chan-Tack KM,Struble KA,Birnkrant DB.Intracranial hemorrhage and liver-associated deaths associated with tipranavir/ritonavir:review of cases from the FDA′s Adverse Event Reporting System[J].AIDSPatient Care STDS,2008,22(11):843-850.
[15]汪习成,王玉,董兴齐.AIDS治愈临床研究及展望[J].传染病信息,2014,26(4):198-201.
[16]李文刚,赵敏.AIDS抗病毒治疗研究进展[J].传染病信息,2014,26(4):247-250.
(2014-08-26收稿 2014-09-30修回)
(责任编委 赵敏 本文编辑 陈玉琪)
Adverse reactions of antiretroviral agents for treatment of AIDS
WANG Hui,ZHOU Bo-ping
Department of Infectious Diseases,Shenzhen Third People's Hospital,Shenzhen,Guangdong 518112,China
More than 25 kinds ofantiretroviralagents have been approved in clinicaluse.Although the tolerability and safety of antiretroviral agents have improved substantially,adverse reactions remain one of the most common causes of medication noncompliance and treatment failure in AIDSpatients.So,it isofgreat importance to know quitewell the adverse reactions of antiretroviral agents for clinicians.As the novel antiretroviral agents continue to be approved in use,their adverse reactions should be observed further.
acquired immunodeficiency syndrome;antiretroviral therapy,highly active;antiviral agents
R512.91
A
1007-8134(2014)06-0369-04
518112,深圳市第三人民医院感染科(王辉、周伯平)

