低浓度鼠李糖脂单糖脂在近中性溶液中的聚集行为
谈 菲,刘智峰,钟 华,曾光明,袁兴中 (湖南大学环境科学与工程学院;环境生物与控制教育部重点实验室,长沙 410082)
低浓度鼠李糖脂单糖脂在近中性溶液中的聚集行为
谈 菲,刘智峰,钟 华*,曾光明,袁兴中 (湖南大学环境科学与工程学院;环境生物与控制教育部重点实验室,长沙 410082)
研究了临界胶束浓度(CMC)附近鼠李糖脂单糖脂在近中性溶液中的聚集体粒径分布.结果发现,单鼠李糖脂在低于CMC和高于CMC时均能形成聚集体,根据粒径大小分为粒径在5000nm左右的大粒子、200~500nm的中等粒子和40nm左右的小粒子.当pH≤7且浓度低于CMC时,中等粒子的粒径随单鼠李糖脂浓度增大而减小,且聚集体在分布上由大粒子向小粒子转变.随着pH值升高,中等粒子的粒径也同样由大变小,且分布上大粒子和中等粒子均向小粒子转变.该结果被认为是聚集体中的单鼠李糖脂分子密度和分子的离解性质随浓度或pH变化所致.
单鼠李糖脂;聚集体;临界胶束浓度;离解
生物表面活性剂是一种具有亲水和亲油性的两亲性分子,具有增溶、分散、润湿、渗透特性.鼠李糖脂是铜绿假单胞菌的次级代谢产物,具有表面活性剂的通性,在液相环境中浓度增加能发生聚集.由于生物表面活性剂具有良好的环境友好性及生物可利用性,在越来越多的生活和工业(如材料、生命、制药等)领域得到应用研究[1-4].
在浓度和溶液pH值变化时,生物表面活性剂所形成的聚集体的结构也会发生变化.Imura等[5]发现在高浓度时,随浓度继续升高,甘露糖赤藻糖醇脂依次形成海绵晶格、双连续立方晶格和膜结构.Ishigami等[6]研究了鼠李糖脂单糖脂和二糖脂在水或磷酸缓冲液中的聚集行为,结果发现在pH 4.3~5.8时,其聚集物主要以双层膜的胶囊(Vesicle)形式存在于液相中;当pH值升高至6.0~6.5,溶液中出现了鼠李糖脂分子的双层膜结构(Lamella),并伴随有脂状颗粒物的存在;随着溶液pH值升高至6.8以上,聚集物发生了有膜结构和脂状颗粒物向胶束(Micelle)的转化.Champion等[7]用冷场透射电镜进一步确定了在不同pH值的水溶液中60mmol/L鼠李糖脂聚集物的原始形态,并发现了随着pH值的升高,聚集物依次发生了双层膜或管状结构、大型双层膜或单层膜胶囊、小型单层膜胶囊以及胶束的转化.
以上关于鼠李糖脂在溶液中聚集形态的研究集中在较高的鼠李糖脂浓度范围内(均高于CMC),而对CMC附近的鼠李糖脂的聚集行为鲜有涉及.而鼠李糖脂作为一种高效的表面活性剂,在CMC附近即表现出较强的表面活性,Zhang等[8]研究表明,浓度低于CMC的鼠李糖脂单糖脂对烃类就表现出了较强的增溶作用.另一方面鼠李糖脂相对于一般的化学表面活性剂生产成本要高,使其在低浓度下发挥作用可提高其应用潜力,弥补生产成本高的不足.鼠李糖脂属于阴离子表面活性剂,不同pH值下鼠李糖脂的离解度不同,前人研究[9]表明即使在适合微生物生长的中性pH值附近,pH值的变化也可能显著影响鼠李糖脂在水溶液中的形态.因此,在近中性pH环境中浓度在CMC附近鼠李糖脂聚集行为的研究对它在有机污染生物修复中的应用具有实际意义.基于此,本文针对鼠李糖脂中重要的一类——鼠李糖脂单糖脂(简称“单鼠李糖脂”)在无机盐溶液中的聚集行为进行了研究,考察了近中性pH条件下(6~8),浓度在CMC附近单鼠李糖脂的聚集体粒径差异,以求进一步揭示低浓度鼠李糖脂的聚集行为.
1 材料与方法
1.1 试剂
本研究采用的生物表面活性剂为单鼠李糖脂,采用Zhong等[10]的方法制得,主要成分为RhaC10C10、RhaC10C12-H2和RhaC10C12(物质的量比0.80:0.08:0.12).实验用纯水由Lanconco Water Pro PS纯水机(Kansas, USA)制取,电阻率18.2MΩ·cm.其他试剂均为分析纯.
1.2 单鼠李糖脂CMC的测定
作为背景溶液的MSM溶液成分包括NaNO3(0.20%), KH2PO4(0.15%), Na2HPO4·12H2O (0.15%), MgSO4(0.01%), FeSO4·7H2O (0.001%).
称取一定量的膏状单鼠李糖脂溶解至MSM溶液中,并用MSM稀释成不同浓度的单鼠李糖脂溶液,溶液的表面张力采用界面张力仪(JZ-200A,承德仪器厂)之Du Noüy环法于30℃下进行测定.在单鼠李糖脂浓度0~70μmol/L范围内表面张力测定的灵敏度<2μmol/L,并且连续3次测定误差在±0.1mN/m之内.通过溶液表面张力与单鼠李糖脂浓度之间的关系曲线得到该生物表面活性剂在MSM中的CMC.
1.3 单鼠李糖脂粒径测定
通过微量注射器用20%的NaOH将不同浓度的单鼠李糖脂MSM溶液的pH值调至8.0.将溶液通过0.22μm的微孔滤膜(Millex-HV系列,Millipore Products, Billerica, Ma., U.S.)过滤,以除去溶液中灰尘等大颗粒杂质.滤液在带有纸盖的小烧杯中静置2h使其中的单鼠李糖脂聚集体重新达到分配平衡,然后测定聚集体的粒径分布.据以往类似实验结果,在pH 8.0时溶液中单鼠李糖脂聚集体的粒径远小于0.22μm(后面的实验结果也证实了这一点),因此可以认为过滤对单鼠李糖脂聚集体没有截留.之后用微孔滤膜过滤后的20% HNO3溶液通过微升级移液枪逐步调节单鼠李糖脂的pH值至各目标值,在每个目标值下,溶液静置2h使单鼠李糖脂聚集体重新达到分配平衡后,进行粒径测定.由于硝酸浓度很高,加入硝酸溶液的体积相对于单鼠李糖脂溶液体积可忽略不计,故认为调节时单鼠李糖脂浓度不变.粒径测定仪器为Zetasizer Nano ZEN3600 (Malvern Instruments, Malvern, U.K.)微粒粒径测定仪.测定基于溶液微小粒子的动态光散射原理,其激光源为633nm的He-Ne激光灯,工作功率4.0mW.样品由边长约1mm的DTS-0012四棱柱聚苯乙烯样品池盛装,样品池插入恒温测样室中30℃下进行测定,散射光于与光路呈173°角处由接收器收集.粒子粒径通过累计量法进行计算,最终数据由仪器自带软件在SOP模式下分析获得.最终得到的粒子粒径为体积平均粒径,各类粒子所占百分比为体积百分比.
2 结果与讨论
2.1 单鼠李糖脂溶液CMC
表面活性剂的临界胶束浓度CMC是指溶液中表面活性剂分子开始大量形成胶束时的表面活性剂浓度[11].当表面活性剂的浓度高于CMC时,溶液中的表面活性剂分子由于疏水基的范德华力作用将会发生聚集,形成亲水基在表面、疏水基在核心的胶束结构,使溶液系统的能量达到最低状态.在溶液和空气的相界面生物表面活性剂分子也达到饱和,增加其浓度不会使溶液的表面张力继续降低.在单鼠李糖脂浓度低于CMC时,溶液表面张力γst(mN/m)和浓度C(μmol/L)的对数值符合线性关系γst=b-alnC;当单鼠李糖脂浓度高于CMC时,溶液表面张力和液相浓度的关系用常数方程γst=γst0表示,其中γst0通过表面张力数据的标准方差最小化计算得到[12].
由图1可见,在单鼠李糖脂浓度低于CMC时随浓度升高,溶液的表面张力急剧下降,直至单鼠李糖脂浓度降低至CMC时,表面张力将不再随单鼠李糖脂浓度变化,维持在一个稳定值.低于CMC和高于CMC时,溶液表面张力γst和单鼠李糖脂浓度C之间的关系分别为γst=69.8-7.379lnC (C≤70μmol/L)和γst=35.4 (C≥80μmol/L),联立上述两个方程得出单鼠李糖脂的CMC为75μmol/L,这与之前Mata-Sandovala等[13]的研究结果一致.
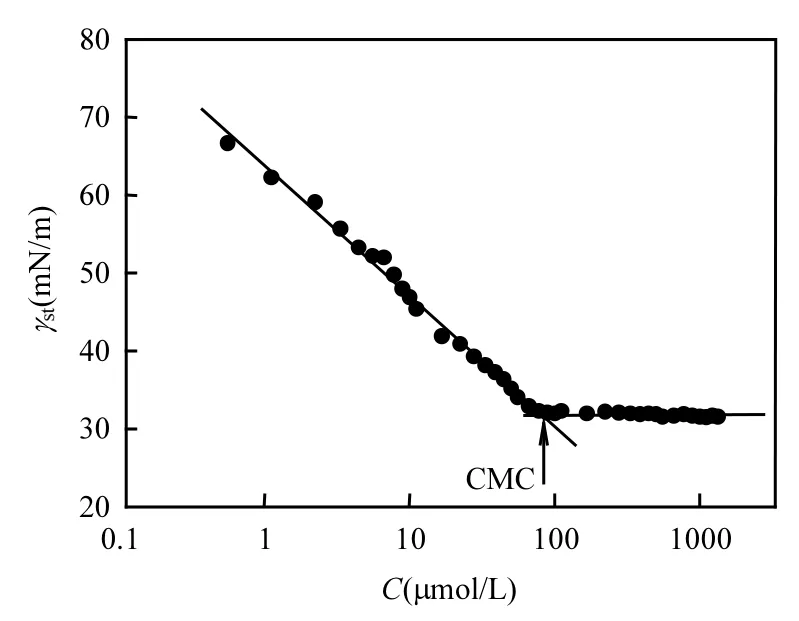
图1 MSM溶液中鼠李糖脂浓度与表面张力之间关系Fig.1 Relationship between surface tenstion and concentration of monorhamnolipid in MSM
2.2 单鼠李糖脂在MSM溶液中的粒径分布
由图2可见,不同pH值和浓度下单鼠李糖脂可以是1个、2个或3个粒径范围的聚集体.通过对Zetasizer Nano ZEN3600仪器软件对图线的积分分析,可以得到每类聚集体的平均粒径及其体积占所有粒子总体积的百分比.
单鼠李糖脂在MSM中的聚集体可能的形态共有3种,分别粒径5000nm左右的大粒子c、粒径200~500nm的中等粒子b和粒径40nm左右的小粒子a,且即使在浓度低于CMC (75μmol/L)时也检测到了聚集体的存在.由图3可见,在各pH值下,随着单鼠李糖脂浓度的增加,大粒子c粒径保持5000nm左右没有明显变化,中等粒子b在浓度低于CMC时随浓度的增加粒径减小,在高于CMC时基本不变.除了pH=6.0的情况,小粒子a的粒径随浓度没有明显变化(左图).对于粒子的分布,在某一pH值下,随着浓度的增加,一般地有大粒子c和中等粒子b的体积百分比减小,而小粒子a的体积百分比增加(右图).由于分子中羧基的存在, 单鼠李糖脂属阴离子表面活性剂,在水溶液中能够离解,它在常温下的离解平衡常数Ka=10-5.6[6],在实验pH 6.0, 6.5, 7.0, 7.5, 8.0时,单鼠李糖脂在MSM中的离解度分别为71.5%, 88.8%, 96.2%, 98.8%,和99.6%.不考虑无机盐等其他因素的影响,在固定pH下,单鼠李糖脂的离解度是一定的,其粒径的变化由浓度的变化引起.随着浓度的升高,粒子的粒径减小,粒子表面单位面积单鼠李糖脂分子密度增加,同时小粒子的数目增加,这对于系统的热力学稳定性有利.
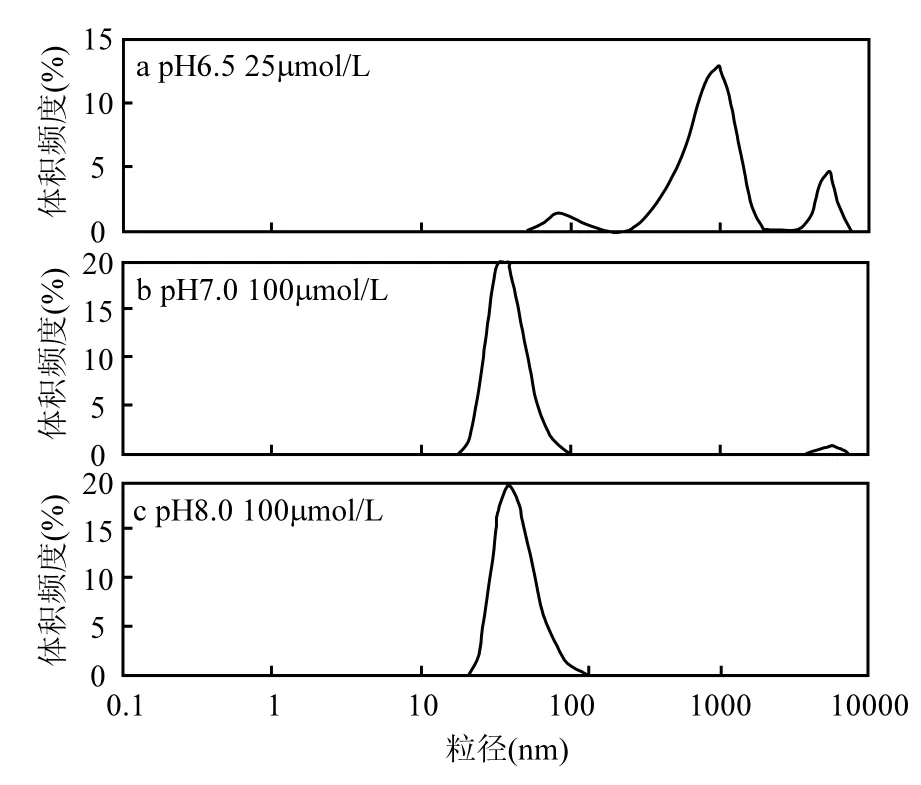
图2 不同pH和浓度条件下单鼠李糖脂在MSM溶液中的聚集体体积频度分布Fig.2 Size volume distribution of monorhamnolipid aggregates under different conditions of pH and rhamnolipid concentration
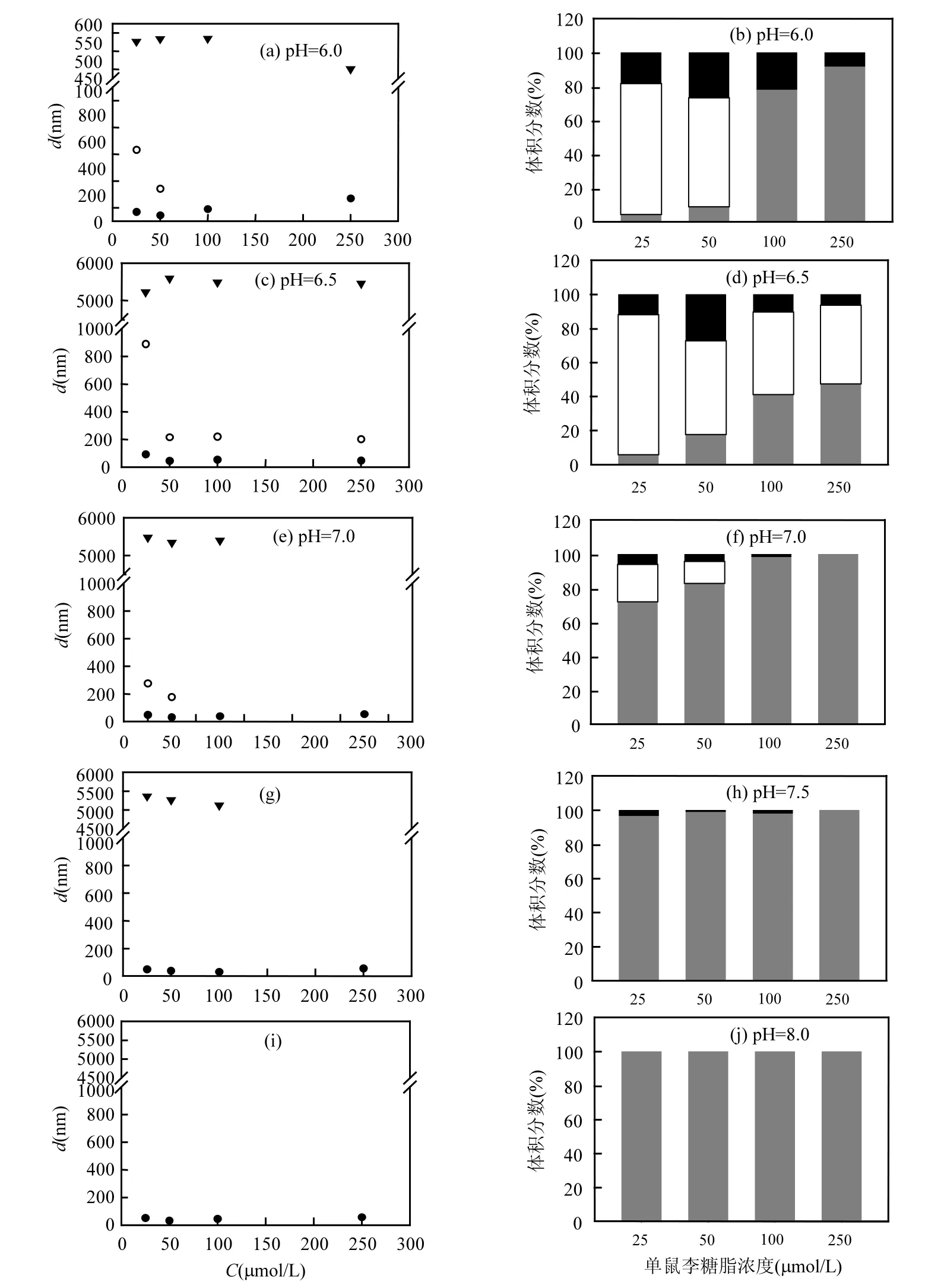
图3 单鼠李糖脂在不同pH值的MSM溶液中的聚集体粒径及体积分布Fig.3 Size of co-aggregates and volume distribution in MSM of monorhamnolipid with different pH
由于单鼠李糖脂的离解度受溶液pH值的影响较大,pH值对单糖脂聚集体的粒径分布有较大影响.各浓度下,大粒子c的体积百分比基本随pH值的增加而降低,至pH 8.0时完全消失;中等粒子b的体积百分比基本随pH值的增加而降低,在pH 6.5至pH 7.0段降低迅速,并且在pH7.5时完全消失;小粒子a的体积百分比随pH值的增大而增加,直至pH8.0时聚集体完全以小粒子形式存在(右图).随着MSM溶液pH值的增大,溶液中离子态的单鼠李糖脂比例增加,聚集体表面单鼠李糖脂分子之间的静电斥力增大,使得胶团曲率变大,粒径变小,同时也促进了大粒子向小粒子的转化.因此,随着pH的增加,单糖脂的粒子b的粒径在各浓度下都有减小的一般规律,同时大粒子和中等粒子向小粒子转化.Champion等研究表明,在高浓度(60mmol/L)的单鼠李糖脂溶液中,随pH值从6.0增大到8.0,其聚集形态发生了由大型双层膜胶囊、大型单层膜胶囊、小型单层膜胶囊直至胶束的变化[14].而本研究显示,在低浓度下(CMC左右),随着pH值的增加其聚集形态也发生了由大到小的变化,与之一致.
以上结果表明,对于生物表面活性剂鼠李糖脂单糖脂,在其浓度低于CMC时溶液中形成了多种粒径的聚集体.一般认为,低分子表面活性剂形成的胶束粒径在10nm以下,但本研究中的单鼠李糖脂在低浓度范围内能够形成粒径达5000nm的大型聚集体结构,而在高浓度范围内,却没有发现粒径小于10nm的聚集体.这与单鼠李糖脂分子结构有关.单鼠李糖脂的亲水基/疏水基比例较小,在分子构型上可能形成了和磷脂分子POPE类似的亲水基位于顶角的正三角形结构[14],这样的构型使得单糖脂分子在溶液中形成的聚集体表面曲率更小,疏水基之间的作用更强,形成的聚集体粒径也比较大.因此低于CMC形成的这种聚集体很可能不是实际意义上的胶束结构,而是其它的结构形式,如与磷脂分子或甘露糖赤藻糖醇酯等生物表面活性剂分子类似,形成双层膜和胶囊结构[15-16].
3 结论
3.1 在浓度低于和高于CMC时,单鼠李糖脂在溶液中均能形成聚集体,但两种聚集体结构上可能存在差别.
3.2 随着浓度和pH值的增加,聚集体的粒径均有由大变小的一般规律,且小粒径聚集体的体积百分比增加,这分别是单鼠李糖脂聚集体分子密度的改变以及单鼠李糖脂的离解引起的分子电性变化所导致的结果.
[1] 彭子原,袁兴中,彭 馨,等.生物表面活性剂逆胶束中漆酶催化性能的研究 [J]. 中国环境科学, 2013,33(6):1091-1096.
[2] Zeng G M, Chen M, Zeng Z T. Risks of neonicotinoid pesticides [J]. Science, 2013,340(6139):1403.
[3] Zeng G M, Chen M, Zeng Z T. Shale gas: surface water also at risk [J]. Nature, 2013,499(7457):154.
[4] 王 静,曾光明,刘智峰,等.表面活性剂对热带假丝酵母降解十六烷的影响 [J]. 中国环境科学, 2009,29(8):822-827.
[5] Imura T, Ohta N, Inoue K, et al. Naturally engineered glycolipid biosurfactant leading to distinctive self-assembled structures [J]. Chem. Eur., 2006:2434-2440.
[6] Ishigami Y, Gama Y, Nagahora H, et al. The pH-sensitive conversion of molecular aggregates of rhamnolipid biosurfactant. Chem. Lett., 1987:763-766.
[7] Champion J T, Gilkey J C, Lamparski H, et al. Electron microscopy of rhamnolipid (biosurfactant) morphology: effects of pH, cadmium, and octadecane [J]. J. Colloid. Interface. Sci., 1995,170:569-574.
[8] Zhang Y, Miller R M. Enhanced octadecane dispersion and biodegradation by a pseudomonas rhamnolipid surfactant (biosurfactant). Appl. Environ. Microbiol., 1992,58:3276-3282.
[9] 汪小娅,曹玉华,潘 红,等.鼠李糖脂的合成及pH值对其表面活性和微乳结构的影响 [J]. 物理化学学报, 2009,25(8):1567-1571.
[10] Zhong H, Zeng G M, Liu J X, et al. Adsorption of monorhamnolipid and dirhamnolipid on two Pseudomonas aeruginosa strains and the effect on cell surface hydrophobicity [J]. Appl. Environ. Microbiol., 2008,79:671-677.
[11] 陈宗淇,王光信,徐桂英.胶体与界面化学 [M]. 北京:高等教育出版社, 2001:180-182.
[12] Yuan X Z, Ren F Y, Zeng G M, et al. Adsorption of surfactants on a Pseudomonas aeruginosa strain and the effect on cell surface lypohydrophilic property [J]. Appl. Environ. Microbiol., 2007,76: 1189-1198.
[13] Mata-Sandovala J C, Karnsb J, Torrents A. High-performance liquid chromatography method for the characterization of rhamnolipid mixtures produced by Pseudomonas aeruginosa UG2 on corn oil [J]. J. Chromatogr. A, 1999,864:211-220.
[14] Aranda F J, Espuny M J, Marqués A, et al. Thermodynamics of the interaction of a dirhamnolipid biosurfactant secreted by Pseudomonas aeruginosa with phospholipid membranes [J]. Langmuir, 2007,23,2700-2705.
[15] Kitamoto D, Ghosh S, Ourisson G, et al. Formation of giant vesicles from diacylmannosylerythritols, and their binding to concanavalin A [J]. Chem. Commun., 2000,861-862.
[16] Kell H, Holzwarth J F, Boettcher C, et al. Physicochemical studies of the interaction of the lipoheptapeptide surfactinwith lipid bilayers of L-α-dimyristoyl phosphatidylcholine [J]. Biophys. Chem., 2007,128:114-12.
Aggregation of monorhamnolipid with concentrations near CMC in neutral solution.
TAN Fei, LIU Zhi-feng,ZHONG Hua*, ZENG Guang-ming, YUAN Xing-zhong (College of Envirnmental Science and Engineering, Key Laboratory of Environmental Biology and Pollution Control, Ministry of Education, Hunan University, Hunan 410082, China). China Environmental Science, 2014,34(11):2912~2916
Size distribution of monorhamnolipid aggregates in neutral pH solutions with rhamnolipid concentration near critical micelle concentration (CMC) was studied. Aggregates were formed when rhamnolipid concentration was either below or above CMC. Three types of aggregates which were large (d=5000nm), medium (d=200~500nm) and small (d=40nm) in size were found. When pH was below 7.0 and the rhamnolipid concentration was below CMC, size of the medium-size aggregates decreased with increasing rhamnolipid concentration, and large-size and medium-size aggregates transformed into small-size aggregates. With the increase of solution pH, size of the medium-size aggregate also decreased, and large-size and medium-size aggregates transformed into small-size aggreqates. These observations were assumed to result from change of density and dissociation degree of monorhamnolipid molecule in the aggregates with rhamnolipid concentration and solution pH.
monorhamnolipid;agreegates;critical micelle concentration;dissociation
X131.2
A
1000-6923(2014)11-2912-05
谈 菲(1991-),女,湖南长德人,湖南大学环境科学与工程学院硕士研究生,主要从事水环境污染生物修复技术研究.
2014-04-27
国家自然科学基金资助项目(50908081,51039001, 51378192,51308200,51378190)
* 责任作者, 讲师, zhonghua@hun.edu.cn

