新兴污染物BP-3和BP-4的好氧生物降解性能
张 弘,殷浩文,周忠良,陈晓倩,刘 敏
(1. 华东师范大学 生命科学学院,上海 200062;2. 上海市检测中心 生物与安全实验室,上海 201203)
新兴污染物BP-3和BP-4的好氧生物降解性能
张 弘1,殷浩文2,周忠良1,陈晓倩2,刘 敏2
(1. 华东师范大学 生命科学学院,上海 200062;2. 上海市检测中心 生物与安全实验室,上海 201203)
[摘要]采用欧洲经济合作与发展组织(OECD)的生物降解测试标准方法——301F测压呼吸计量法,考察了2-羟基-4-甲氧基二苯甲酮(BP-3)和2-羟基-4-甲氧基二苯甲酮-5-磺酸(BP-4)的好氧生物降解性能,并研究了降解动力学及共代谢现象。实验结果表明:BP-3和BP-4的可生物降解率分别为68.36%和41.34%;根据OECD快速降解性判定标准,BP-3划归为易快速降解物质,而BP-4为不易快速降解物质;两种物质的生物降解可用一级动力学描述,半衰期分别为1.986 d和2.806 d;根据欧盟法规《化学品的注册、评估、授权和限制》(REACH法规),BP-3和BP-4均非持久性物质;与苯甲酸钠共存时,BP-3和BP-4的降解过程均表现出共代谢现象。
[关键词]2-羟基-4-甲氧基二苯甲酮;2-羟基-4-甲氧基二苯甲酮-5-磺酸;好氧生物降解;301F测压呼吸计量法;半衰期;共代谢
2-羟基-4-甲氧基二苯甲酮(BP-3)和2-羟基-4-甲氧基二苯甲酮-5-磺酸(BP-4)是两种生产量较大[1-2]、使用较多的二苯甲酮类紫外线吸收剂[3],常用于生产化妆品、沐浴露、洗发露等个人护理用品,能有效防止紫外线对人体的伤害[4]。随着人们的广泛使用,BP-3和BP-4被大量释放到水环境中[5]。近年来,中国、瑞士、美国等很多国家在污水等环境介质中检测出这两种物质[6-8]。环境中检出的紫外吸收剂与药品统称为PPCPs类新兴污染物。相关的研究结果表明,作为PPCPs类的BP-3和BP-4对生物体具有内分泌干扰效应及生殖毒性[9-11]。
微生物降解作用是自然界中有机物最终矿化的唯一途径[12],是决定有机污染物环境归宿的关键。研究BP-3和BP-4的生物降解有助于深入了解它们的迁移转化规律,不仅为控制污染、保护环境提供理论依据,还可为研制环境友好型防晒剂提供参考,同时也有助于为有效处理含防晒剂的有机废水提供思路。截至目前,国内未见有关BP-3和BP-4生物降解的报道。
本工作采用欧洲经济合作发展组织(OECD)提出的生物降解测试标准方法—301F测压呼吸计量法(OECD-301F 法)[13]研究BP-3和BP-4的好氧生物降解性能,并考察其降解动力学以及共代谢现象。
1 实验部分
1.1 试剂、材料和仪器
BP-3:纯度为99%; BP-4:纯度为97%;苯甲酸钠:纯度为98%;甲醇:分析纯;乙腈:分析纯;四氢呋喃:分析纯。
接种物:采自上海某城市污水处理厂曝气池的新鲜活性污泥。
BP-3溶液:BP-3质量浓度为0.030~0.225 mg/L的甲醇溶液;BP-4溶液:BP-4质量浓度为0.052~0.520 mg/L的甲醇溶液。
301F无机培养基以及苯甲酸钠母液的制备方法参见文献[13](OECD标准)。
OxiTop OC 110 WTW 型BOD呼吸计:德国WTW公司; Acquity UPLC型超高效液相色谱系统:Waters公司。
1.2 实验方法
OECD-301F 法是以受试物在一定时间内被微生物氧化所需要的耗氧量(BOD,mg/L)[13]为指标,研究化学品的生物降解性的经典方法,其结果反映的是化学品在环境中最终转化为无机物的程度。因其方法规范严格且具有良好的实验重现性和精确性,而被国外许多实验室采用[14]。设备感测探头可以在28 d内连续记录360个BOD数据,为降解动力学的分析提供足够的数据支持[15]。
按照文献[13],采用BOD呼吸计进行OECD-301F 法实验。将添加不同组分的反应瓶分组,每组3个平行样,启动感测探头后在22 ℃培养箱中避光培养28 d。根据反应体系内的氧气消耗量,通过电化学分析过程得出BP-3和BP-4的BOD。
OECD-301F 法规定:受试物的浓度为理论需氧量 (受试物完全氧化时所需的耗氧量,ThOD)50.0~100.0 mg/L或质量浓度为100 mg/L,接种物浓度(以活性污泥悬浮固体计)为30 mg/L[13]。本实验兼顾方法规定以及污染物的实际环境浓度,设置BP-3的质量浓度为30.00 mg/L( ThOD=65.1 mg/ L),BP-4的质量浓度为32.00 mg/L( ThOD=51.5 mg/L),参比物苯甲酸钠的质量浓度为100.00 mg/L( ThOD=167.0 mg/L)。实验方案见表1。
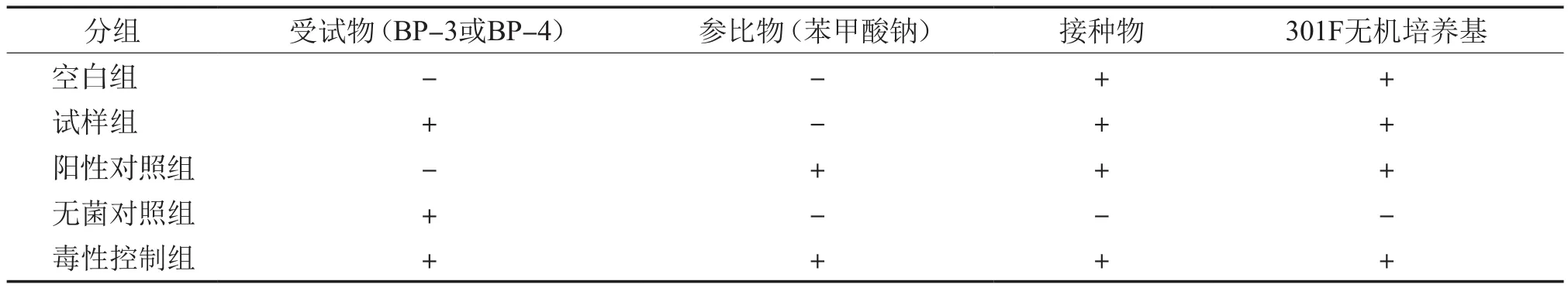
表1 实验方案
设置空白组的目的是为得到不含受试物时的接种物微生物的BOD;设置阳性对照组的目的是为了以苯甲酸钠为参比物,验证活性污泥的有效性;设置无菌对照组的目的是考察是否存在非生物转化;设置毒性控制组的目的是为了考察受试物对微生物是否存在严重毒性抑制,以确保降解结果的可信度[13]。
根据BOD数据,按式(1)计算受试物的可生物降解率(α,%),以此来间接表征受试物的最终可生物降解程度[13]。
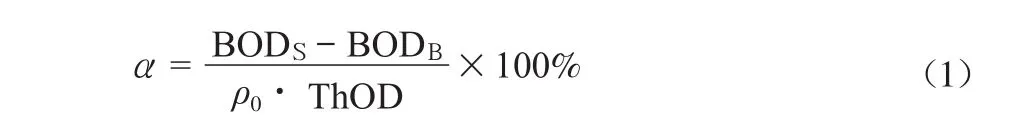
式中:BODS为试样组生物需氧量的平均值,mg/ L;BODB为空白组生物需氧量的平均值,mg/L;ρ0为受试物的初始质量浓度,mg/L。
1.3 BP-3和 BP-4 的超高效液相色谱分析方法
检测器:二极管阵列检测器(PDA);色谱柱:Waters BEH C18(50.0 mm ×2.1 mm×1.7μm)。柱温:40 ℃;进样体积:2 μL;体积流量:0.4 mL/min;检测波长:285 nm(BP-3), 320 nm(BP-4)。
BP-3的测定:流动相为不同体积分数的甲醇-水溶液。梯度洗脱顺序:0~0.5 min,10%(甲醇体积分数,下同);0.5~3.5 min,100%;3.5~7.0 min,10%。取250 mL含BP-3的混合洗脱液分3次加入100 mL 四氢呋喃,超声处理30 min,磁力搅拌5 min。取10 mL混合溶液,加入10 mL四氢呋喃,混匀后取1.8 mL 二次混合溶液,13 000 r/min离心10 min,取上清液100 μL,甲醇稀释100倍,用超高效液相色谱仪测定BP-3的质量浓度。
BP-4的测定:流动相为不同体积分数的乙腈-水溶液。梯度洗脱顺序为: 0~0.5 min,10%(乙腈体积分数,下同);0.5~3.5 min,100%;3.5~3.7 min,10%;3.7~7.0 min,10%。取1.8 mL混合溶液,以13 000 r/min的转速离心10 min,取上清液100 μL,以体积分数为50%的乙腈-水溶液稀释100倍,用超高效液相色谱仪测定BP-4的质量浓度。
按式(2),由测定得到的质量浓度计算BP-3和BP-4的初级降解率(β,%)。初级降解率表征的是有机物分子的原始结构发生改变的程度。

式中:ρN为无菌对照组的受试物质量浓度,mg/L;ρS为试样组的受试物质量浓度,mg/L。
2 结果与讨论
2.1 BP-3和BP-4的好氧生物降解性能
阳性对照组及试样组中苯甲酸钠、 BP-3及BP-4的生物降解曲线见图1。
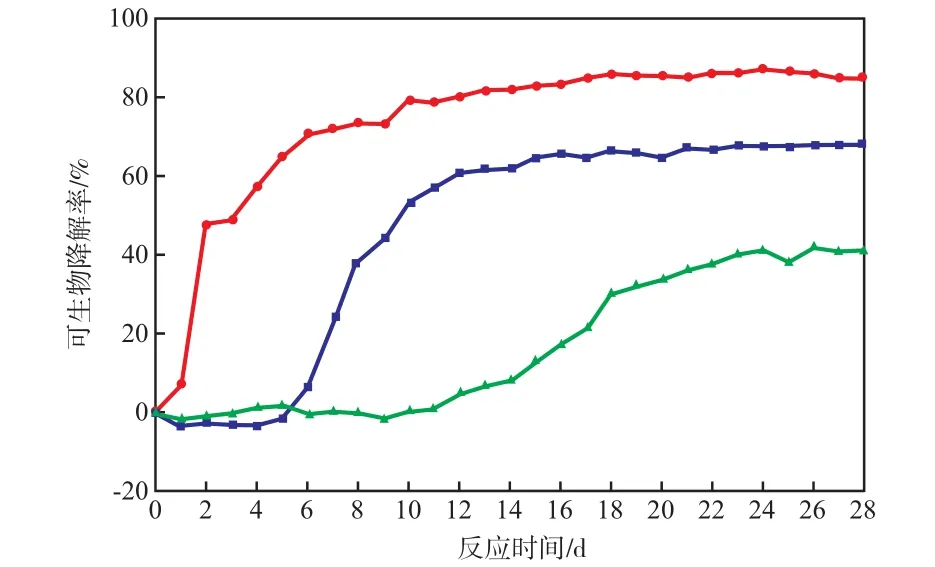
图1 阳性对照组及试样组中苯甲酸钠、 BP-3及 BP-4的生物降解曲线· 苯甲酸钠;■ BP-3;▲ BP-4
根据OECD标准,阳性对照组的参比物在14 d时的可生物降解率要达到60%[13]。由图1可见,在测试第5天,阳性对照组的苯甲酸钠可生物降解率即达到65.00%,已满足质量控制要求,体现了实验的有效性。
由图1中BP-3的降解曲线可见:BP-3的可生物降解率首先经历大约6 d的迟滞期,该期间可生物降解率为负值,即受试物的BOD比空白低,说明微生物的呼吸受到BP-3的抑制,原因是微生物进入新环境时需要诱导特定的代谢酶,或具备降解BP-3能力的微生物需要足够的增殖时间[16];但是通过几天的驯化后,微生物便能把BP-3作为碳源加以利用,使其得以迅速降解,第13天的BP-3可生物降解率超过60%,之后达到稳定期,第28天时BP-3可生物降解率达到 68.36%。依据OECD快速生物降解性判定标准[13],BP-3达到严格定义上的通过水平,可判定其为易生物降解物质。美国毒理学数据库Toxnet有资料记载,采用标准OECD-301C MITI(I)法[13](与OECD-301F 法类似)对BP-3进行快速生物降解实验,其可生物降解率仅达4%,并没有达到通过水平。这与本研究得到的结果存在明显差异。笔者推断原因可能是OECD-301C MITI(I)法的接种物不同于OECD-301F法,前者接种物源于实验室驯化污泥[13],而后者则来自于污水处理厂的新鲜活性污泥。Forney等[17]的研究结果表明,在实验室驯化前后,新鲜活性污泥的微生物群落结构发生明显改变,微生物种群多样性减少,因此OECD-301C MITI(I)法规定使用的接种物可能使原本存在的BP-3高效降解菌在驯化过程中丢失。就接种物来看,本研究采用的方法结果更具代表性,更能反映实际环境中的降解效果。
由图1中BP-4的降解曲线可见: BP-4的降解迟滞期较BP-3长,为15 d;而在第28天,BP-4的可生物降解率仅为41.34%,没有达到通过水平,因此判定BP-4不易生物降解,说明BP-4在环境中只能部分降解。但该结果并不表示BP-4在环境中一定持久存在,若要证明这一点,需进行更高层次的模拟实验。
从分子结构看,BP-4仅比BP-3在苯环上多1个磺酸基团。王奕等[18]认为磺酸基增大了生物反应的位阻效应,削弱了微生物攻击碳核的能力,阻碍了芳香族化合物的降解;另外由于极性比BP-3强,BP-4主要分布在水相,对污泥的亲和力较弱,减少了微生物与其反应的接触面积。这两个因素可能是BP-4比BP-3难降解的原因。
2.2 BP-3和BP-4的初级降解
分别取第28天的无菌对照组、试样组溶液进行测定,生物降解前后BP-3和BP-4质量浓度的变化见表2。
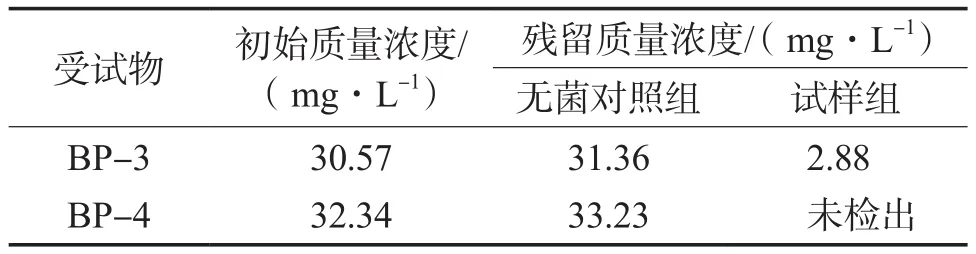
表2 生物降解前后BP-3和BP-4质量浓度的变化
由表2可见:无菌对照组的BP-3和BP-4的残留质量浓度与初始质量浓度基本一致,表明BP-3和BP-4在去离子水中稳定,不易水解;在BP-3试样组中,其残留质量浓度为2.88 mg/L,根据公式(2)计算得出其初级降解率为90.78%,说明BP-3基本完成初级降解。该初级降解率之所以高于由BOD计算得到的可生物降解率,是由于后者反映的是有机物完全转变成无机小分子的程度,而前者仅代表化合物原始结构的变化程度。Balmer等[19]对瑞士某污水处理厂进出水中的BP-3进行了测定,BP-3初级降解率为93%~100%,与本方法测得的初级降解率结果基本一致。另外从图1中BP-3的生物降解曲线也可看出,BP-3降解的中间产物在环境中的保留时间也应该较短,对环境的影响小。
由表2还可见:在BP-4试样组中未检出BP-4,可认为其初级降解率为100%,然而由BOD计算得到的可生物降解率却很低(见图1),说明BP-4生成了不易进一步转化的中间产物。通常,在好氧条件下,微生物对芳香族化合物的典型降解途径是通过合成加氧酶在邻位和间位的C—C键上形成C—O键,以推动苯环裂解,最后生成CO2和H2O[20]。BP-4的苯环上有1个磺酸基,这是钝化反应的基团,因此在BP-4分子结构中最难打开的是磺酸基所连接的苯环。笔者根据以上两点推断了BP-4生物降解反应的可能顺序及中间产物(见图2)。
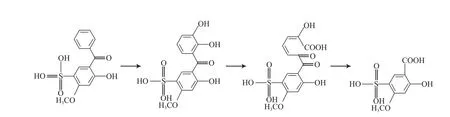
图 2 BP-4生物降解反应的可能顺序及中间产物
2.3 BP-3和BP-4的生物降解动力学分析
参考 Stasinakis等[21]的301F降解阶段动力学研究方法,以最终BOD(BODult)表征发生彻底降解的有机物的浓度,用BODult与t时刻BOD测定值的差值(BODr)表征t时刻的有机物残余浓度,将BODr随时间t变化的数据采用不同函数进行拟合。拟合结果表明,用指数函数拟合的相关系数最高(R>0.9)。BP-3和BP-4的生物降解动力学参数见表3。由表3可见,BP-3和BP-4的生物降解均符合一级反应动力学模型;BP-3和BP-4的半衰期分别为1.986 d和2.806 d。根据欧盟法规《化学品的注册、评估、授权和限制》(REACH法规)对物质在水环境中是否具备“持久性”的判定依据(物质在淡水中半衰期大于40 d则具备持久性),该两种物质均不会持久存在。因为该标准是针对实际环境下的半衰期,所以BP-4是否为持久性物质尚需更多数据支持。

表3 BP-3和BP-4的生物降解动力学参数
2.4 毒性控制组中的共代谢过程
阳性对照组、毒性控制组及试样组中苯甲酸钠、BP-3和BP-4的生物降解曲线分别见图3、图4。由图3、图4可见,第14天时,毒性控制组混合样的可生物降解率均大于OECD法规定的质量控制要求,说明在所设浓度条件下BP-3和BP-4对微生物的正常代谢基本是无毒的。
由图3、图4还可见,在实验最后一天(即第28天),毒性控制组混合样的可生物降解率分别为78.67%和67.09%,这比BP-3或BP-4单独存在的试样组的可生物降解率有所提高。由于OECD-301F法实验中的无机培养基本身并不含碳源,笔者推断可生物降解率的提高可能是因为共代谢作用[22]。

图3 阳性对照组、毒性控制组及试样组中苯甲酸钠及BP-3的生物降解曲线· 阳性对照组的苯甲酸钠;■ 毒性控制组的苯甲酸钠和BP-3;▲ 试样组的BP-3
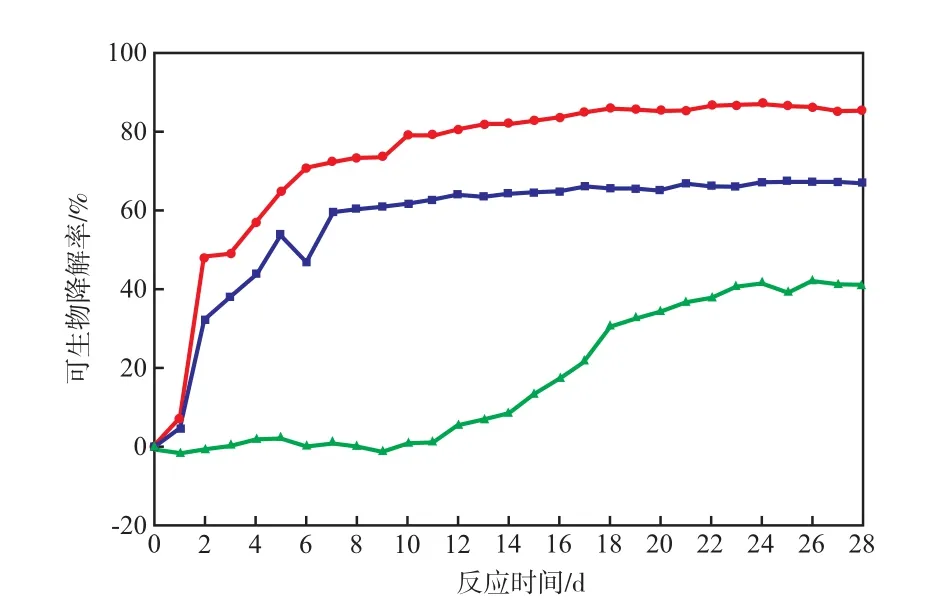
图4 阳性对照组、毒性控制组及试样组中苯甲酸钠及BP-4的生物降解曲线· 阳性对照组的苯甲酸钠;■ 毒性控制组的苯甲酸钠和BP-4;▲ 试样组的BP-4
3 结论
a)在好氧条件下,微生物对BP-3或BP-4的降解均需要一段适应时间。以BOD作为表征即时降解程度的参数,BP-3或BP-4的可生物降解率分别为68.36%和41.34%。根据OECD降解性判定标准,前者为易降解物质,后者为难降解物质。但BP-4比BP-3的初级降解程度略高,存在较稳定的中间产物。
b)BP-3和BP-4的生物降解可用一级反应动力学方程描述,拟合方程分别为BODr= 88.049e-0.349t和BODr= 68.087e-0.247t,半衰期分别为1.986 d 和2.806 d。依据REACH法规,BP-3和BP-4不属于持久性物质,但仍需进一步实验确定BP-4是否具有持久性。
c) BP-3和BP-4分别与苯甲酸钠共存时的生物降解均可能存在共代谢现象。
参考文献
[1] National Institutes of Health,U.S. Department of Health & Human Services. HSDB:2-Hydroxy-4-methoxybenzophenone[DB/OL]. [2014-03-03]. http://toxnet. nlm.nih.gov/cgi-bin/sis/search/a?dbs+hsdb:@term+@ DOCNO+4503.
[2] National Institutes of Health, U.S. Department of Health & Human Services. HSDB: Sulisobenzone [DB/OL]. [2014-03-03]. http://toxnet.nlm. nih.gov/cgi-bin/sis/search/a?dbs+hsdb:@term+@ DOCNO+7422.
[3] Landers M,Law S,Storrs F J. Contact urticaria, allergic contact dermatitis, and photoallergic contact dermatitis from oxybenzone[J]. Am J Cont Derm,2003,14(1):33 - 34.
[4] Negreira N,Rodríguez I, Rodil R,et al. Assessment of benzophenone-4 reactivity with free chlorine by liquid chromatography quadrupole time-of-flight mass spectrometry[J]. Anal Chim Acta ,2012,743:101-110.
[5] Zenker A,Schmutz H, Fent K. Simultaneous trace determination of nine organic UV-absorbing compounds(UV filters) in environmental samples [J]. J Chromatogr A,2008,1202 :64 - 74.
[6] 马永明,渠志华,刘克明,等. 城市再生水生产工艺中典型紫外防晒剂的去除[J]. 生态毒理学报,2006,1(3):278 - 282.
[7] Fent K,Zenker A,Rapp M . Widespread occurrence of estrogenic UV filters in aquatic ecosystems in Switzerland[J]. Environ Pollut,2010,158:1817 - 1824.
[8] Zucchi S,Bluthgen N,Ieronimo A,et al. The UV-absorber benzophenone-4 alters transcripts of genes involved in hormonal pathways in zebrafish (Danio rerio) eleuthero-embryos and adult males [J]. Toxicol Appl Pharmaco, 2011,l250:137 - 146.
[9] Brausch J M,Rand G M.A review of personal care products in the aquatic environment: Environmentalconcentrations and toxicity [J]. Chemosphere,2011,82:1518 - 1532.
[10] Schmutzler C,Bacinski A,Gotthardt I,et al. The ultraviolet filter benzophenone 2 interferes with the thyroid hormone axis in rats and is a potent in vitro inhibitor of human recombinant thyroid peroxidase[J].Endocrinology,2008,148( 6) :2835 - 2844.
[11] Schlumpf M,Cotton B,Conscience M,et al.In vitro and in vivo estrogencity of UV screens[J].Environ Health Perspect,2001,109: 239 - 244.
[12] 鲁亢,杨尚源,梁志伟,等. 选矿废水中黄药自然降解特性的研究[J]. 应用生态学报,2013,24(2):597 - 606.
[13] OECD. OECD Guidelines for the Testing of Chemicals,Section 3:Degradation and Accumulation [DB/OL]. [2014-03-03]. http://www. oecd-ilibrary.org/environment/test-no-301-readybiodegradability_9789264070349-en;jsessionid= 5283q9ltf0ia6.x-oecd-live-01.
[14] Guhl W,Steber J. The value of biodegradation screening test results for predicting the elimination of chemicals’organic carbon in waste water treatment plants[J]. Chemosphere,2006,63:9 - 16.
[15] Richterich K,Steber J. The time-window—an inadequate criterion for the ready biodegradability assessment of technical surfactants[J]. Chemosphere,/CN 103951156 A,2014-07-30 2001,44:1649 - 1654.
[16] Foulk J A,Bunn J M. Factors influencing the duration of lag phase during in vitro biodegradation of compression-molded, acetylated biodegradable soy protein films[J]. Food Eng,2007,79:438 - 444.
[17] Forney L J,Liu W T,Guckert J B,et al. Structure of microbial communities in activated sludge: Potential implications for assessing the biodegradability of chemicals [J]. Ecotoxicol Environ Saf,2001,49:40 - 53.
[18] 王奕,杨凤林,张兴文,等. 化学品生物降解性的评价与预测[J]. 化工环保, 2002, 22(4):209 - 212.
[19] Balmer M E,Buser H R,Müller M D,et al. Occurrence of some organic UV filters in wastewater,in surface waters,and in fish from Swiss lakes[J]. Environ Sci Technol,2005,39(4):953 - 962.
[20] 孙艳,钱世钧.芳香族化合物生物降解的研究进展[J]. 生物工程进展,2001,21(1):42 - 45.
[21] Stasinakis A S,Thomaidis N S,Nikolaou A,et al. Aerobic biodegradation of organotin compounds in activated sludge batch reactors[J]. Environ Pollut ,2005,134:431 - 438.
[22] 董春娟,吕炳南,陈志强. 处理生物难降解物质的有效方式——共代谢[J]. 化工环保. 2003,23(2):82 - 85.
[中图分类号]X172
[文献标志码]A
[文章编号]1006 - 1878(2014)05 - 0423 - 06
[收稿日期]2014 - 02 - 17;
[修订日期]2014 - 07 - 09。
[作者简介]张弘(1989—),男,安徽省六安市人,硕士生,主要研究方向为水生生态毒理学。电话 021-38831500,电邮 zhanghong8907@163.com。
[基金项目]上海市技术性贸易措施应对专项(13TBT012)。
Aerobic Biodegradability of Emerging Contaminants BP-3 and BP-4
Zhang Hong1,Yin Haowen2,Zhou Zhongliang1,Chen Xiaoqian2,Liu Min2
(1. School of Life Sciences, East China Normal University, Shanghai 200062, China;2. Bioassay and Safety Assessment Laboratory, Shanghai Academy of Public Measurement, Shanghai 201203, China)
Abstract:The aerobic biodegradabilities of 2-hydroxy-4-methoxybenzophenone(BP-3) and 2-hydroxy-4-methoxybenzophenone-5-sulfonic acid(BP-4) were studied by 301F manometric respirometry method, the OECD standard method for biodegradability test. Their degradation kinetics and co-metabolic phenomena were also explored. The experimental results show that: The biodegradation rates of BP-3 and BP-4 are 68.36% and 41.34% respectively; According to the OECD criterion of ready biodegradability, BP-3 is an easily degradable substance while BP-4 is difficult to be biodegraded ultimately; The biodegradation of the two substances can be described by the first order kinetics, and their half-lives are 1.986 d and 2.806 d respectively; According to the REACH rule,BP-3 and BP-4 are both non persistent substances; BP-3 and BP-4 can both co-metabolized with sodium benzoate during the degradation process.
Key words:2-hydroxy-4-methoxybenzophenone; 2-hydroxy-4-methoxybenzophenone-5-sulfonic acid;aerobic biodegradation; 301F manometric respirometry method; half-life; co-metabolism

