熊胆粉中熊去氧胆酸结晶条件
陈 正, 王伯初*, 祝连彩, 刘绍勇, 薛东升
(1.重庆大学生物工程学院 生物流变学与技术教育部重点实验室, 重庆 400030;2.上海凯宝药业股份有限公司, 上海 201418)
熊胆粉中熊去氧胆酸结晶条件
陈 正1, 王伯初1*, 祝连彩1, 刘绍勇2, 薛东升2
(1.重庆大学生物工程学院 生物流变学与技术教育部重点实验室, 重庆 400030;2.上海凯宝药业股份有限公司, 上海 201418)
目的 对熊胆粉中熊去氧胆酸的结晶及重结晶过程加以控制,以提高熊胆粉提取物产率及质量。方法 通过溶解度实验确定了结晶及重结晶的最佳起始条件,再采用不同的降温方法对该过程进行梯度控温的优化研究。结果 以70 ℃和 30 ℃做为结晶及重结晶的始末温度; 筛选出最佳的结晶控温条件为控温 8 h, 前 5 h 每 1 h 降温 2 ℃, 后 3 h每1 h降温10 ℃, 重结晶工艺控温条件与结晶控温条件一致。 应用该结晶工艺, 与原工艺相比, 熊胆粉提取物产率提高 2.38%, 转化率提高 12.35%, 熊去氧胆酸量提高 5.83%, 鹅去氧胆酸量基本保持不变。 结论 本研究所建立的结晶工艺,可显著提高熊胆粉中熊去氧胆酸的产率和质量。
熊去氧胆酸;梯度降温;结晶过程;熊胆粉
熊胆粉属国家卫生部批准的一类新药[1], 为粉末、不规则碎片或颗粒,呈棕黄色,绿黄色或深棕色。具有消炎镇痛、清热解毒、平肝明目等功效[2-3]。熊胆 粉 的 主 要 成 分 为 牛 磺 熊 去 氧 胆 酸(TUDCA) 和牛磺鹅去氧胆酸 ( TCDCA)[4], 经水解后可得熊去氧胆酸 (UDCA)、 鹅去氧胆酸 (CDCA), 现入药的熊胆粉提取物的主要成分为熊去氧胆酸[5], 鹅 去 氧 胆 酸 是 熊 去 氧 胆 酸 的 差 向 异构体[6]。
熊胆粉除了含有胆汁酸类成分外,还含有胆固醇、 蛋白质、 色素等非胆汁酸类成分[7]。 由于熊胆粉成分的复杂性,鹅去氧胆酸和熊去氧胆酸的性质又极为相似,使得熊去氧胆酸制备难度较大。目前的工艺主要是通过醇提、水解、酸沉、结晶及重结晶等方法提纯熊胆粉提取物,使最终熊胆粉提取物 (以下简称精品) 中熊去氧胆酸含有量高于73%, 鹅去氧胆酸含有量低于 15%, 从而达到配方药的标准。本实验室通过对目前企业熊胆粉提取工艺过程的分析和研究发现,影响熊去氧胆酸量主要原因是结晶过程控制不佳:将经过醇提、水解制得的熊胆粉粗提取物用乙酸乙酯提取浓缩后,在30 ℃条件下静置结晶, 无恒定的初始温度条件和降温控制,使工艺结晶条件易受外界环境气候的影响。从而导致最终提取的转化率 (以下转化率都是指熊去氧胆酸) 低下, 约为 49.54%, 产率低约为 19.96%。 本实验在此基础上对熊胆粉结晶及重结晶过程进行控制研究。
1 仪器与试药
1.1 仪 器 优 普 UPT系 类 超 纯 水 器 ( UPT-I-10T, 成都超纯科技有限公司), ACQUITY UPLC型高效液相色谱仪 ( 上海 waters公司),ACQUITY UPLC ELSD型蒸发光散射检测器 (上海 waters公司)。
1.2 材料 熊胆粉 (上海凯宝药业股份有限公司提供,批号为 s111103)。
1.3 试剂 氢氧化钠 (重庆市川东化工集团有限公司, 分析纯), 盐酸 (重庆市川东化工集团有限公司, 分析纯), 乙酸乙酯 (成都市科龙化工试剂厂,分析纯),甲醇 (成都市科龙化工试剂厂,分析 纯 ), 甲 醇 ( Merck 公 司, 色 谱 纯 ), 50 mmol/L醋酸铵水溶液 (Merck 公司, 色谱纯), 熊去氧胆酸 (中国食品药品检定研究院, 批号110755-9003,20 mg)、鹅去氧胆酸 (中国食品药品检定研究院, 批号 110806-200704, 30 mg)
2 方法与结果
2.1 方法
2.1.1 溶解度试验 结晶及重结晶的过程中所涉及到的溶剂均为乙酸乙酯,所以通过测定熊去氧胆酸、鹅去氧胆酸在乙酸乙酯中的溶解度以确定结晶及重结晶的最佳起始温度。
采用文献[8]中的综合法测定溶解度。 精确称取一定量的熊去氧胆酸固体粉末,然后向三颈瓶中缓慢加入少量的乙酸乙酯,搅拌,保持温度在70℃, 粉末未溶解完全, 继续搅拌, 如果不溶解再少量多次加入溶剂,直至固体颗粒消失,停止搅拌,静置,无固体颗粒析出,则缓慢降温,每次降温5℃,用同样的方法测出各个温度梯度下的溶解度。然后再反向操作,精确移取一定量的乙酸乙酯,向三颈瓶中缓慢加入少量熊去氧胆酸固体粉末, 搅拌, 保持温度25℃, 溶液澄清, 继续多次少量添加熊去氧胆酸,直至固体颗粒出现,继续搅拌,不溶,静置,缓慢升温,每次升温5℃,用同样的方法测出各个温度梯度下的溶解度。将前一种方法重复2次,3次数据结果取平均值可得熊去氧胆酸溶解度结果。用相同的方法测定鹅去氧胆酸的溶解度值。
2.1.2 搅拌试验 在结晶工艺步骤前添加搅拌过程, 时间为 15 min, 与原工艺重结晶的搅拌时间一致。
2.1.3 结晶及重结晶温度梯度控制 根据结晶原理分析,以控温速率为因素,设置三个梯度的控温方式,将结晶及重结晶过程的控温方式设计如下:①控温 8 h (先按 2 ℃/h 降温, 控温 5 h; 再按 10℃/h 降温, 控温 3 h); ②控温 6 h (先按 5 ℃/h降温,控温 4 h; 再按 10 ℃/h 降温, 控温 2 h);③控温 4 h (按 10 ℃/h 降温, 4 h), 详见表 1。
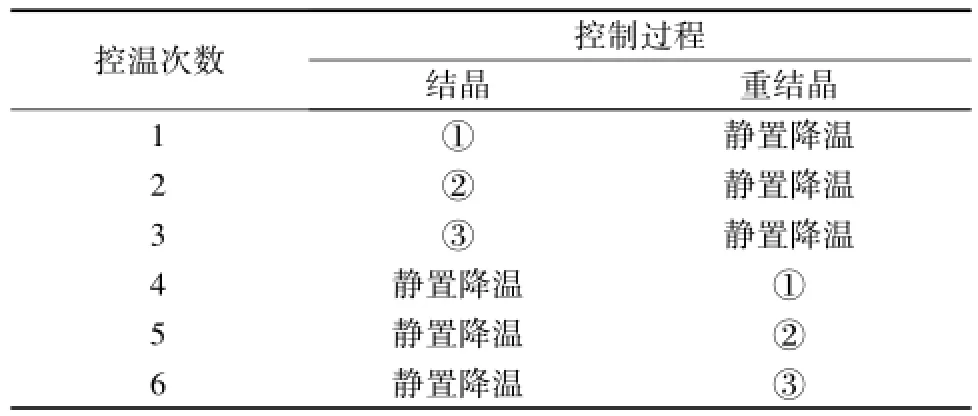
表1 不同控温方式试验的设计Tab.1 Design of different tem Perature con trol tests
2.1.4 熊去氧胆酸和鹅去氧胆酸的测定
2.1.4.1 色谱条件[9]welch ultimate XB-C18色谱柱 ( 4.6 mm×250 mm); 流动相为甲醇 (A) -50mM醋酸铵水溶液 (B); 线性梯度洗脱为A相0 ~15 min, 40%→90%; 15.01 min, 90%→40%; 25 min, 40%; 体积 流 量 1.0 mL/min; 柱 温 40 ℃;ELSD漂移管温度 45 ℃;雾化气体积流量 25 Psi;增益500。
2.1.4.2 对 照 品 溶 液 制 备 分 别 精 密 称 取0.010 5 g熊去氧胆酸、0.010 4 g鹅去氧胆酸对照品于10 mL量瓶中, 用甲醇溶解并定容,分别制成质量浓度为熊去氧胆酸 1.0 mg/mL鹅去氧胆酸 1.0 mg/mL对照品贮备液。
2.1.4.3 供试品溶液制备 分别精密称取新旧工艺熊胆粉提取物 0.010 2 g和 0.010 1 g供试品于10 mL量瓶中, 用甲醇溶解并定容, 均制成质量浓度为 1.0 mg/mL供试品贮备液。
2.1.4.4 标准曲线的测定 精密量取各对照品贮备液 1.0 mL于 10 mL量瓶中, 再用甲醇稀释至刻度, 制成质量浓度分别为熊去氧胆酸 0.10 mg/m L,鹅去氧胆酸 0.10 mg/mL的混合对照品溶液。 分别进样 3 次, 依次为 2、 4、6、 8、10 μL,得图谱,经计算可得回归方程。
2.1.4.5 样品的测定 精确量取各供试品贮存液2.0 m L于 10 mL量瓶中, 再用甲醇定容至刻度,制成质量浓度均为 0.2 mg/mL。
进样量均为8 μL, 得图谱。
2.2 结果与讨论
2.2.1 溶解度试验 从图 1 可以看出熊去氧胆酸、鹅去氧胆酸在乙酸乙酯中的溶解度随着温度的增加而线性地增加,其中随着温度的升高鹅去氧胆酸线性增加速度更显著,通过斜率可以得出同一个温度条件下鹅去氧胆酸溶解度比熊去氧胆酸大 10倍左右。 此实验结果与文献[9]所做的实验结果基本一致。

图1 熊去氧胆酸、鹅去氧胆酸在乙酸乙酯中的溶解度Fig.1 UDCA and CDCA in ethyl acetate: the solubility of values
结晶始末温度的确定 首先设置的起始温度应低于乙酸乙酯的沸点 77℃; 其次降温的终止温度为30 ℃, 一个较大的温度范围有利于下一步控温结晶的实施;最后温度越高,熊去氧胆酸和鹅去氧胆酸的溶解度差异越大,便于提高熊去氧胆酸量降低鹅去氧胆酸量。 所以选择 70 ℃作为控温的起始最佳温度。为了保证结晶的稳定性,将终止温度设定在 30 ℃ (与原工艺一致), 整个控温过程置于水浴中,维持整个体系结晶的平衡稳定性,使得工艺不会随着外界条件的变化而不稳定。
2.2.2 搅拌对熊胆粉提取物产率的影响 见表 2。在未将控制初始温度统一前 (均低于70 ℃),初始温度易受环境气候的影响,使得结晶的范围不稳定,通过初始温度的添加确定了结晶温度范围。

表2 搅拌对熊胆粉提取物产率的影响Tab.2 M ixing of bear bile Powder's influence on the extraction rate of Products
由表2可得出实验的结果良好,但由于原料所加入的量规模均较小,所以导致最终提高的产量不是很显著,但经3次重复试验平均值可得出产率仍提高 0.2%左右。
2.2.3 结晶及重结晶温度梯度控制 根据结晶原理分析,以控温速率为因素,设置3个梯度的控温方式, 结晶及重结晶过程的控温方式结果如表3,表4。
经过3次重复, 经 t检验后, 可得结晶条件下1、 2、 3 中, 1 与 3 比较有统计学意义, 而 2 与 3比较无统计学意义,但考虑到结晶过程控温的基本规律是初始要慢,结晶后期要快。且1的平均值仍然高于 2, 1的控制条件相对精细, 所以选择 1作为结晶最佳条件。重结晶条件下4与5、 6比较,有统计学意义,所以选择4作为重结晶的最佳条件。

表3 不同控温方式试验的平均产率Tab.3 Productivities of sam Ples in different tem Peratures

表4 不同控温方式试验控温产率 t检验Tab.4 Test of sam Ple Productivities in d ifferent tem Peratures
最终可得出在结晶控温和重结晶控温均以控温8 h的条件最佳,得到产率最高,因此选用此结晶及重结晶条件作为最优化条件进行试验。

表5 新旧工艺熊胆粉提取物产率对比Tab.5 Com Parison of bear bile Powader extraction rate between the old Process and the new one
由表5可得出实验的结果良好,3次原工艺平均产率为 19.96%, 而通过两次控温实验产率最终平均 产 率 可 以 达 到 22.34%, 比 原 工 艺 提 高了 2.38%。
2.2.4 梯度控温工艺对熊胆粉提取物质量的影响
2.2.4.1 熊去氧胆酸、 鹅去氧胆酸的标准曲线
见表6。

表6 熊去氧胆酸、 鹅去氧胆酸标品回归方程、 线性范围及相关系数Tab.6 Regression equation, linear range and correlation coefficient of UDCA and CDCA reference standards
其中x表示实际进样量取对数, y表示为熊去氧胆酸、鹅去氧胆酸各自所对应的峰面积取对数。通过相关系数可知,该分析方法的线性关系良好,可用于样品中熊去氧胆酸和鹅去氧胆酸的检测。
2.2.4.2 梯度控温结晶工艺对熊胆粉提取物质量的影响 经过优化后的工艺,熊去氧胆酸量提高5.83%, 熊去氧胆酸转化率提高 12.35%, 而鹅去氧胆酸的量基本保持不变,符合配方药标准,说明该结晶过程控温工艺具有较好的效果。 见表7。
3 讨论
3.1 结晶产生的因素主要涉及到在很宽的的温度和溶液过饱和度范围内进行,且结晶成核过程与二次成核、 晶 粒 附 聚等 伴 随 现象 有 关[10-12]。 本 研 究中初始温度的添加统一了初始结晶标准,使得结晶过程的初始温度得到控制,不会随着外界温度的变化而不稳定。

表7 新旧工艺熊胆粉提取物中熊去氧胆酸、 鹅去氧胆酸量及转化率对比Tab.7 Com Parison of UDCA and CDCA content and conversion contrast between the old Process and the new one
3.2 通过增加搅拌过程, 便于溶质在溶剂中充分溶解,有利于二次成核,避免因浓度过大,初次非均相成核析出过多的物质中含有大量的杂质。结晶的晶核形成模式大体分为初级成核和二次成核。其中初级成核速率过快,使得工艺难以控制,所以在工业过程应尽量避免。二次成核为大多数工艺结晶过程的主要来源。二次成核是一个复杂的现象,影响的因素主要包括过饱和度、冷却速度、搅拌程度等[13]。
3.3 对结晶和重结晶的过程进行控温控制, 一方面符合二次成核的原理,另一方面也满足了结晶控温过程中先慢后快的原则。其原因在于初期晶面小,介稳区窄,易爆发成核,如果冷却速度快,会导致晶体在换热表面生长。结晶后期,由于有大量的晶体存在,晶体有足够的机会在晶体表面生长,过饱和度比较容易消耗掉。因此后期的降温速率可以加快[14]。
3.4 通过对结晶及重结晶过程控制, 最终选取了初始温度为 70 ℃, 搅拌 15 min, 终止温度 30 ℃,结晶控温8 h, 重结晶控温8 h, 最终达到对熊胆粉提取优化。使产率提高 2.38%, 熊去氧胆酸转化率提高 12.35%,熊去氧胆酸量提高 5.83%,鹅去氧胆酸量保持稳定,符合配方药标准对工业生产具有参考价值。
[ 1 ] 连常宝.熊胆粉的药理作用及临床应用研究概述[J].海峡药学, 2008, 20(8): 71-75.
[ 2 ] 王巍巍.熊胆粉的药效学研究[J].黑龙江医药, 2010,23(2): 196-198.
[ 3 ] 姜英芝, 刘春芳, 王同州, 等.熊胆粉的药用价值[J].中国林副特产, 2004, 71(4): 30-31.
[ 4 ] Lepercq P, Gerard P, Beguet F, et al.Epimerization of chenodeoxycholic acid to ursodeoxycholic acid by Clostridium baratii isolated from human feces[ J] .FEMS Microbiol Lett,2004, 235(1): 65-72.
[5] 李富善,黄晓玲.痰热清注射液的作用机理和临床应用[J].青海医药杂志, 2011, 41(5): 78-79.
[ 6 ] 王永金, 杨泽民.红外光谱鉴定熊胆的研究[J].沈阳药学院学报, 1989, 6(3): 157-163.
[7] 吴革林, 吴修红, 董阗伟, 等.熊胆(粉) 非胆汁酸类成分研究进展[ J] .中医药学报, 2011, 39(3) : 90-92.
[8] 胡程耀, 黄 培.固体溶解度测定方法的近期研究进展[ J] .药物分析杂志, 2010, 30(4) : 761-766.
[9] 王 珏.痰热清注射液质量控制研究 [D].杭州: 浙江大学, 2010.
[10] 叶铁林.化工结晶过程原理及应用[M].北京: 北京工业大学出版社, 2006: 4-5.
[11] Rauls M, Bartosch K, Kind M, et al.The influence of impurities on crystallization kinetics-a case study on ammonium sulfate[ J] .JCryst Growth, 2000, 213(1/2) : 116-128.
[12] Demo P, Kozisek Z.Transient nucleation[ J] .Thermochimica Acta, 1996, 280/281: 101-126.
[13] 刘家祺.传质分离过程[M].北京: 高等教育出版社,2005: 237-243.
[14] Mersmann A.Crystallization Technology Handbook [ M] .Second edition.Germany: Technical University of Munich Garching, 1995: 35-64.
Crystallization of ursodeoxycholic acid from bear bile Powder
CHEN Zheng1, WANG Bo-chu1*, ZHU Lian-cai1, LIU Shao-yong2, XUE Dong-sheng2
(1.Key Laboratory of Biorheological Science and Technology, Ministry of Education; College of Bioengineering, Chongqing University, Chongqing 400030, China; 2.Shanghai Kaibao Pharmaceutical Company Limited, Shanghai, 201418, China)
AIM To control the crystallization and recrystallization process in ursodeoxycholic acid extracted from bear bile powder, as well as their improvement in yield and quality.M ETHODS The optimal initial conditions of crystallization and recrystallization were obtained by the solubility experiments.The extraction from bear bile powder processwas improved by differentmethods of gradient temperature controlling.RESULTS The initial and final temperature of crystallization and recrystallization was70 ℃ and 30 ℃ , respectively.Itwas screened out that the best condition for the crystallization and recrystallization was 8 h.In the first5 hours, the temperature decreased at the rate of2 ℃ per hour.In the following 3 hours, the temperature decreased at the rate of 10 ℃ per hour instead.Comparing with the original process, the extract rate of bear bile powder products increased by 2.38%.The conversion rate increased by 12.35%.The content of ursodeoxycholic acid increased by 5.83%, and chenodeoxycholic acid content kept steady.CONCLUSION The established crystallization process can significantly improve the yield and quality of bear bile powder extract.
ursodeoxycholic acid; temperature gradient; crystallization process; bear bile powder
R284.2
: A
: 1001-1528(2014)01-0061-05
10.3969/j.issn.1001-1528.2014.01.015
2013-03-12
中央高校基本科研业务费资助 (CDJXS11230051)
陈 正 (1986—) , 男, 硕士生, 研究方向: 中药提取工艺过程。 Tel: 13658314964, E-mail: aijiaying_03@163.com
*通信作 者: 王 伯 初 ( 1962—) , 男, 教 授, 研 究 方 向: 生 物 制 药 工 程、 天 然 药 物。 Tel: ( 023 ) 65112840, E-mail: wangbc2000 @126.com

