银菊散结口服液质量标准研究
付庆霞, 王建成, 任继东
(1.山东临沂市人民医院, 山东 临沂 276003; 2.山东临沂市食品药品检验检测中心, 山东 临沂 276001)
银菊散结口服液质量标准研究
付庆霞1, 王建成2, 任继东1
(1.山东临沂市人民医院, 山东 临沂 276003; 2.山东临沂市食品药品检验检测中心, 山东 临沂 276001)
目的 建立银菊散结口服液 (金银花、 菊花、 桔梗、 玄参等) 的质量标准。 方法 采用薄层色谱法对金银花、菊花、 桔梗进行定性鉴别; 并采用 HPLC法同时测定金银花与菊花中绿原酸及木犀草苷、 玄参中哈巴俄苷、 菊花中3,5-O-二咖啡酰基奎宁酸。 结果 薄层色谱斑点清晰; 绿原酸、 木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸分别在 0.082 4 ~0.824 μg、 0.103 9 ~1.039 μg、 0.048 ~0.48 μg、 0.185 6 ~1.856 μg范围内呈良好线性关系 (r分别为0.999 8、 0.999 9、 0.999 9、 0.999 9), 平均回收率分别为 100.67%、 99.42%、 99.79%、 99.89%, RSD分别为0.75%、 1.46%、 0.81%、 0.63%。 结论 该方法可准确用来定性、 定量检测, 具有简便、 准确及专属性强的特点,可用于银菊散结口服液的质量控制。
银菊散结口服液; 绿原酸; 木犀草苷; 哈巴俄苷; 3,5-O-二咖啡酰基奎宁酸; TLC; HPLC
银菊散结口服液是临沂市人民医院经山东省食品药品监督管理局批准生产的中药制剂 (鲁药制字 Z20110003), 由金银花、 菊花、 桔梗、 玄参等中药组方,具有解毒清热,散结消瘿的作用,临床用于瘿病,甲状腺肿瘤、单纯性甲状腺肿大、甲状腺机能亢进、甲状腺机能减退、亚急性甲状腺炎、慢性淋巴细胞性甲状腺炎 (桥本甲状腺炎) 见上述证候者; 亦用于 “乳癖”、 “症瘕” 及 “经断前后诸证”,乳腺增生、卵巢囊肿、子宫腺肌病及更年期综合征见于上述证候者。通过多年的临床使用,疗效可靠,大大填补了目前甲状腺类疾病治疗的市场空白。为控制药品的内在质量,对处方中的金银花、桔梗进行了薄层色谱鉴别,并采用高效液相色谱法测定了制剂中的绿原酸、木犀草苷、哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸的量, 所建立的方法操作简便、分离效果好、重复性好,专属性强,可以有效地控制本品的质量。
1 仪器与试药
Agilent1260 高效液相色谱仪, DAD二极管阵列检测器, Agilent Chemistation 色谱工作站, KQ3200型超声波清洗器 (昆山市超声仪器有限公司), XS-205 型电子分析天平 (瑞士梅特勒公司)。
绿原酸、木犀草苷、哈巴俄苷、3,5-O-二咖啡酰 基 奎 宁 酸 对 照 品 ( 批 号: 110753-200413、111720-200501、 111730-201106、 111782-201203 )。金银花、 桔梗、 菊花对照药材 ( 批号为 121028-200507、121028-200909、 121384-201103)。 对照品与对照药材均购自中国食品药品检定研究院。
银菊散结口服液由临沂市人民医院委托鲁南厚普有限公司生产 (批号分别为 1107201、 1107202、1107203)。
乙腈 (色谱纯, 山东禹王实业有限公司化工分公司), 娃哈哈纯净水 (杭州娃哈哈集团), 甲醇 (分析纯,山东禹王实业有限公司)。 其他均为分析纯。
2 薄层色谱鉴别
2.1 金银花与菊花的薄层鉴别[1]取本品 5 mL置10 mL量瓶中, 加乙醇至刻度, 摇匀,离心, 取上清液作为供试品溶液。另取绿原酸对照品,加甲醇制成每 1 m L含 0.1 mg的溶液, 作为对照品溶液。 再取金银花对照药材 0.2 g,加甲醇 5 mL,放置 12 h,滤过, 取滤液作为金银花对照药材溶液。最后, 取菊花对照药材 1 g, 加石油醚 (30 ~60 ℃) 20 m L, 超声处理 10 min, 弃去石油醚, 药渣挥干, 加稀盐酸 1 mL与乙酸乙酯 50 mL, 超声处理 30 min, 滤过,滤液蒸干, 残渣加甲醇 2 mL使溶解,作为菊花对照药材溶液。照 《中国药典》2010 年版一部附录Ⅵ B薄层色谱法试验, 吸取供试品溶液 15 μL, 对照品溶液与对照药材溶液各10 μL, 上述四种溶液分别点于同一硅胶 G薄层板,以乙酸丁酯-甲酸-水 (7 ∶2.5 ∶2.5) 的上层溶液为展开剂,展 开,取 出,晾 干,置 紫 外 光 灯(365 nm) 下检视。 供试品色谱中, 在与对照品、对照药材色谱相应的位置上,显相同颜色的荧光斑点。缺金银花、菊花阴性样品无相应斑点,见图1。
2.2 桔梗的薄层鉴别[1]取本品 20 m L, 加 7%硫酸乙醇 5 mL, 加热回流3 h, 放冷, 用三氯甲烷振摇提取2 次, 每次 20 m L, 合并三氯甲烷液, 加水3 mL洗涤, 弃去洗液, 三氯甲烷液用无水硫酸钠脱水, 滤过,滤液蒸干, 残渣加甲醇1 m L使溶解,作为供试品溶液。 另取桔梗对照药材 1 g, 加 7%硫酸乙醇-水 (1 ∶3) 20 mL, 同法制成对照药材溶液。照薄层色谱法试验,吸取上述两种溶液各10 μL,分别点于同一硅胶 GF254薄层板上, 以三氯甲烷-乙醚 (1 ∶1) 为展开剂, 展开, 取出,晾干,置紫外光灯 (254 nm) 下检视。 供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。 缺桔梗阴性样品无相应斑点, 见图2。
3 4 种成分的同时测定[2-13]
3.1 色 谱 条 件 Agilent ZORBAX SB-C18色 谱 柱(5 μm, 4.6 mm×250 mm, 柱号 880975-902); 以乙腈为流动相 A, 0.4%磷酸溶液为流动相 B, 梯度洗脱, 0 ~30 min (9% ~18%A), 30 ~33 min(18% ~25%A), 33 ~36 min (25%A), 36 ~38 min (25% ~30%A), 38 ~40 min ( 30%A),40 ~50 min (30% ~50%A), 50 ~60 min (50% A)。 柱温 30 ℃; 绿原酸、 木犀草苷、 3,5-O-二咖啡酰基奎宁酸检测波长为 348 nm, 哈巴俄苷为278 nm; 体积流量 1 mL/min; 理论塔板数按绿原酸峰计算不低于 1 000、 木犀草苷峰不低于20 000,哈巴俄苷峰不低于 20 000, 3,5-O-二咖啡酰基奎宁酸峰不低于 20 000。 色谱图见图3 ~4。
3.2 对照品溶液的制备 精密称取绿原酸、 木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸对照品10.30、 12.99、 6.00、 23.20 mg, 置 250 mL量瓶中, 加80%甲醇制成混合对照品溶液, 即得。
3.3 供试品溶液的制备 取装量项下的本品, 精密吸取 5 m L, 置 10 mL量瓶中, 加 50%甲醇至刻度,摇匀,滤过,取续滤液即得。
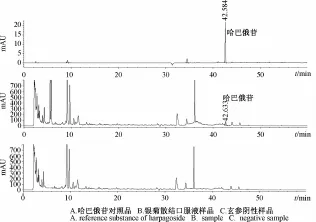
图 3 哈巴俄苷测定 HPLC图谱 (278 nm)Fig.3 HPLC chromatograms of harpagoside(278 nm)
3.4 阴性样品溶液的制备 分别按处方比例及制剂制备工艺制备不含金银花、菊花、玄参的阴性样品, 再按 “3.3”项下方法制备,即得。
3.5 专属性试验 取对照品溶液、 供试品溶液和阴性样品溶液各 10 μL, 分别注入液相色谱仪测定,结果金银花、菊花、玄参阴性样品分别在绿原酸、 木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸相应保留时间处未见色谱峰,表明阴性样品对检测无干扰。 见图3~4。
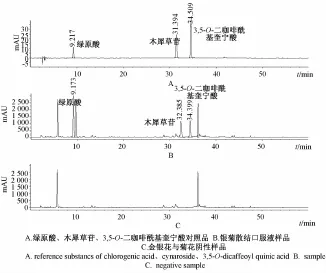
图 4 绿原酸、 木犀草苷、 3,5-0-二咖啡酰基奎宁酸测定HPLC图谱 (348 nm)Fig.4 HPLC chromatograms of ch lorogenic acid, cynaroside and 3,5-0-dicaffeoyl quinic acid(348 nm)
3.6 线性关系考察 分别精密吸取绿原酸、 木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸对照品混合溶液 1、 2、 4、 8、 10、 20 μL, 注入高效液相色谱仪,以进样量为横坐标,峰面积为纵坐标,其回归方程及线性范围见表1。
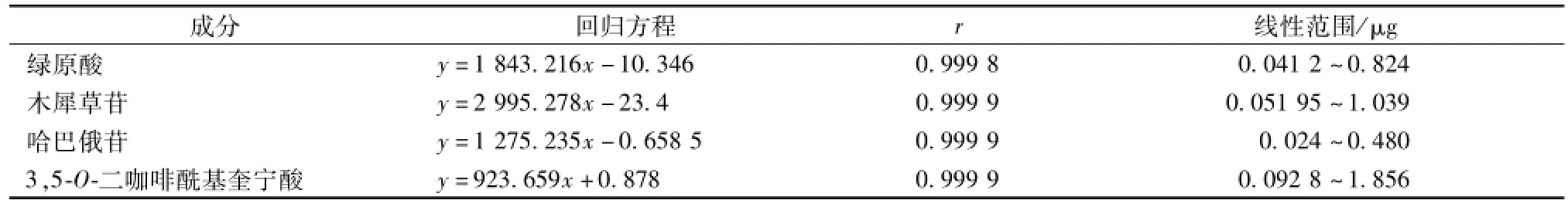
表1 回归方程和线性范围Tab.1 Regression equations and linear ranges
3.7 稳定性试验 精密吸取同一份供试品溶液,在上述色谱条件下于 1、 2、 3 日分别进样分析, 记录各色谱峰面积值,并计算绿原酸、木犀草苷、哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸的 RSD, 分别为0.85%、 0.76%、 1.12%、 1.03%, 结果表明供试品溶液在3日内基本稳定。
3.8 重复性试验 分别取同一批次样品, 按照“3.3”项下的方法制备供试品溶液, 在上述色谱条件下测定4种成分,平行操作6份,并计算绿原酸、 木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸的 RSD, 分别为 1.20%、 1.40%、 0.95%、 3,5-O-二咖啡酰基奎宁酸为 1.16%, 表明本方法重复性试验良好。
3.9 精密度试验 按照上述色谱条件, 精密吸取“3.3” 项下的方法制备的供试品溶液 10 μL, 注入高效液相色谱仪中,连续进样6次,计算绿原酸、木犀草苷、 哈巴俄苷、 3,5-O-二咖啡酰基奎宁酸峰面积 的 RSD, 分 别 为 0.20%、 0.45%、 0.68%、0.23%, 表明仪器精密度良好。
3.10 加样回收率试验 精密量取不同批次已知含有量的银菊散结口服液样品各 1 mL, 平行操作 6份,每份分别精密加入适量的固体对照品或对照品溶液, 置 100 mL量瓶中, 加 50%甲醇稀释至刻度,摇匀,取对照品溶液、加样回收供试品溶液各5 μL, 分别注入液相色谱仪, 测定, 计算加样回收率, 结果见表2。
3.11 样品测定 取 3 批银菊散结口服液, 按“3.3” 项下方法制备供试品溶液, 精密吸取10 μL注入高效液相色谱仪中,在上述相同色谱条件下记录4种成分的峰面积值,通过回归方程计算4种化合物的质量浓度, 结果见表3。
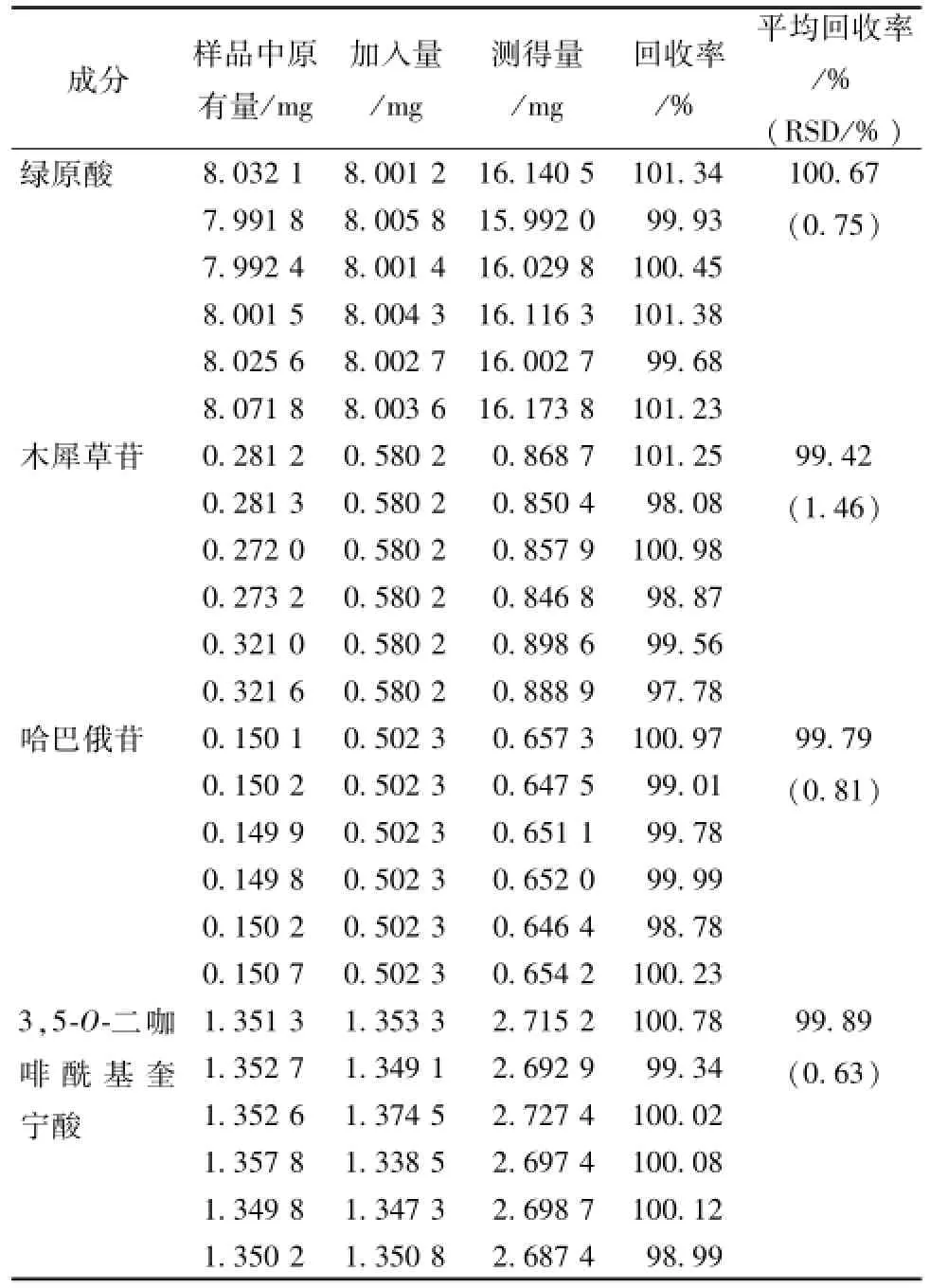
表2 4种化合物回收率测定结果Tab.2 Resu lts of recovery tests for four com ponents
4 讨论
4.1 色谱条件的选择 通过 DAD检测器光谱扫描与同时开通8个通道检测,其最大吸收波长分别为327 nm、 350 nm、 278 nm、 348 nm, 经过系列实验,未能整合同一波长下4种成分同时测定,故在参考文献的基础上, 绿原酸、木犀草苷、 3,5-O-二咖啡酰基奎宁酸选择 348 nm作为检测波长, 因哈巴俄苷在 348 nm出现倒峰, 故选择 278 nm作为检测波长, 根据 AgilentDAD检测器的特殊功能, 可并列开通 348 nm、 278 nm两个通道同时检测 4 种成分,从而达到4种成分同时检测的效果。为保证4种成分同时检出,采用了梯度洗脱,此两个波长下,基线平稳,峰面积较大,色谱峰的峰形均较好。
4.2 提取条件的选择 为保证 4 种成分的同时检出,根据处方中的药材量及实际检测过程中的检测浓度,仅对银菊散结口服液样品稀释2倍,可大大减少前处理环节、提高检验效率、节约试剂及降低检验成本。
4.3 金银花与桔梗的定性鉴别 根据配制工艺,对绿原酸的鉴别采用直接取样稀释的方式。因金银花与菊花中皆有绿原酸,故在定性鉴别中采用金银花和菊花对照药材,保证处方中金银花与菊花的投料, 同时, 在成分定量测定中, 加入菊花的 3,5-O-二咖啡酰基奎宁酸指标的测定, 可对菊花进行定性鉴别。在桔梗的薄层色谱定性鉴别中,参考《中国药典》采用酸溶液水解皂苷的方式提取, 与桔梗对照药材对比,充分显示出多个斑点的一致性,说明该提取方式对鉴别有效、可操作。
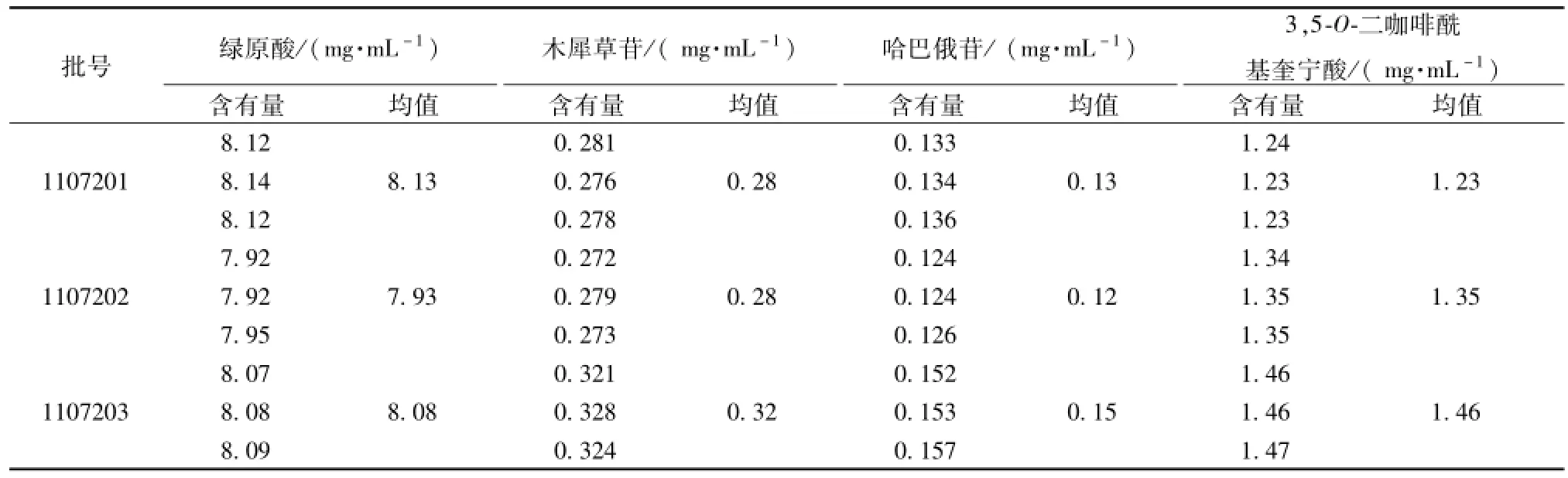
表 3 绿原酸、 木犀草苷、 哈巴俄苷、 3,5-0-二咖啡酰基奎宁酸测定结果 (n=3)Tab.3 Determ ination results of chlorogenic acid, cynaroside, harpagoside and 3,5-0-dicaffeoyl quinic acid( n=3)
4.4 本实验对以消瘿化结汤为处方基础所开发的院内医疗机构制剂银菊散结口服液,进行了质量标准控制研究。为保证处方的投料,采用了薄层色谱定性鉴别,利用高效液相色谱法两个波长通道梯度洗脱方式同时测定本品中金银花与菊花中绿原酸、木犀草苷与菊花中 3,5-O-二咖啡酰基奎宁酸以及玄参中哈巴俄苷的量,作为4种成分的定量分析,经稳定性、精密度、重复性和回收率试验,证明该方法所建立的检测方法专属、简便、可行,检测结果准确、可靠,可起到全面多维度控制制剂质量的作用。
参考文献:
[ 1 ] 国家药典委员会.中华人民共和国药典: 2010 年版一部[S].北京: 中国医药科技出版社, 2010: 205, 259.
[ 2 ] 李 萍, 金红星, 贾 静.HPLC法同时测定金银花中三种成分的含量[ J] .天津医药, 2009, 37(6) : 519-520.
[3] 施 法, 侯 峰.金银花中3种成分含量的超高速液相色谱法同 时测定 [ J].时珍国 医 国 药, 2010, 21 (11 ):3014-3015.
[ 4 ] 辛 华, 丰 杰, 程若敏, 等.HPLC测定不同产地金银花中绿原酸和木犀草苷[J].中国实验方剂学杂志, 2011,17(2): 60-63.
[5] 闵春艳,游本刚,许琼明,等.正交试验比较金银花药材中绿原酸与木犀草苷的乙醇提取工艺[J].中成药, 2011,33(10): 1815-1818.
[ 6 ] 王伟影, 王建伟.HPLC同时测定金银花中 3 种化学成分的含量[J].中华中医药学刊, 2013, 31(2): 405-407.
[ 7 ] 包小红, 周 娟, 伍丕娥.HPLC法测定玄麦甘桔颗粒中甘草酸和哈巴俄苷[J].中成药, 2011, 33(4): 625-628.
[ 8 ] 张雪梅, 王 瑞, 安 睿, 等.HPLC同时测定玄参中 5种成 分 的 含 量 [ J].中 国 中 药 杂 志, 2011, 36 (6 ):709-711.
[ 9 ] 白云娥, 袁鹏飞, 王庆辉, 等.HPLC-UV波长转换法测定玄参药材及饮片中哈巴苷与哈巴俄苷的含量[J].中国中药杂志, 2011, 36(19): 2697-2701.
[10] 刘宏宇, 钮正睿, 蔡铁全.浙江产玄参不同采收季节哈巴俄苷和肉桂酸含量变化分析 [ J].中国 药师, 2012, 15(5): 613-616.
[11] 魏庆华, 王 勤.HPLC测定增液承气口服液中哈巴苷和哈巴俄苷含量[J].中国实验方剂学杂志, 2012, 18(7): 81-83.
[12] 沈 智, 张文婷, 黄琴伟, 等.RP-HPLC法测定菊花中3,5-O-双咖啡酰基奎宁酸、 木犀 草苷 和绿原 酸[ J] . 中草药, 2010, 26(10): 810-812.
[13] 马桂云, 马艳玲, 吕 洁, 等.不同干燥方法对菊花含量的影 响 [ J].中 国 中 医 药 现 代 远 程 教 育, 2012, 10(22): 99.
Quality standard for Yinju Sanjie Oral Liquid
FU Qing-xia1, WANG Jian-cheng2, REN Ji-dong1
(1.Linyi People's Hospital, Linyi276003, China; 2.Linyi Institute for Drug and Food Control, Linyi 276001, China)
Yinju Sanjie Oral Liquid; chlorogenic acid; cynaroside; harpagoside; 3,5-O-dicaffeoyl quinic acid; TLC; HPLC
R927.2
: A
: 1001-1528(2014)05-0986-05
10.3969/j.issn.1001-1528.2014.05.022
2013-07-01
付庆霞 (1978—), 女, 主管中药师, 硕士, 从事中药制剂与中药质量控制研究。 Tel: 13969991383

