艾叶挥发油提取工艺的优化
赵志鸿 耿 楠 黄勇勇 吴 芳 李锦玉 王桂芳 张壮丽 张小俊
1.郑州大学医药科学研究院,河南郑州 450052;2.河南省肝病药理重点实验室,河南郑州 450052;3.郑州大学药学院,河南郑州 450001;4.郑州大学临床医学系,河南郑州 450001
艾叶为菊科多年生草本植物艾(Artemisia argyi Lévl.et Vant.)的干燥叶,全国各地区均产,资源丰富。 现代研究显示,其主要含有挥发油、甾萜类、黄酮类、香豆素类、多糖及一些小分子成分等[1-3],其中挥发油、黄酮类为主要有效成分[4-6]。艾叶是我国历史悠久且临床常用的中药材[7],有温经止血、散寒止痛、降湿杀虫等[8]功效,现代实验表明其具有增强免疫抗感染、平喘镇咳、护肝利胆、止血与抗凝血及抗自由基等作用[9-11],挥发油是艾叶的主要药效成分群之一,提取方法和工艺是挥发油质量和药理活性的保证,对于艾叶资源的开发利用也具有重要意义。本课题组前期研究发现艾叶挥发油具有抗乙肝病毒作用,并对其化学成分进行了分析[12],为将其研制成抗乙肝病毒新药,研究挥发油的提取工艺。水蒸气蒸馏法适合工业生产推广,环保、经济。 本文以正交试验法[13-14]对艾叶挥发油水蒸气蒸馏法提取工艺进行优化, 可提高挥发油的收率和质量,降低成本,具有良好的应用前景。
1 材料与方法
1.1 材料
1.1.1 药材
艾叶产地河南省驻马店,由河南省中医学院药学院生药学科董诚明教授鉴定为菊科植物艾(Artemisia argyi Lévl.et Vant.)的干燥叶。使用时粉碎使通过二号至三号筛,混合均匀。
1.1.2 仪器及试剂
挥发油提取器 (相对密度小于1 型);KDM-4 型电子可调自动恒温仪(山东菏泽市仪器制刷厂制造);电子天平AR1530(梅特勒-托利多仪器上海有限公司制造);蒸馏水(自制)。
1.2 方法
1.2.1 艾叶挥发油的提取方法
参照《中国药典》2010 年版一部附录ⅩD 挥发油测定法(甲法)[15]。 取粉碎的艾叶约100.00 g,精密称定,加蒸馏水适量,浸泡,加热提取,收集挥发油,计算挥发油得率,密封,冷藏保存。艾叶挥发油得率计算公式:挥发油得率(%)=A/B×100%。
1.2.2 单因素试验
分别考察料液比、浸泡时间和提取时间对艾叶挥发油得率的影响。
1.2.2.1 料液比的影响 取粉碎的艾叶约100 g, 精密称定,加蒸馏水,料液比(W/V)分别为:1∶8、1∶10、1∶12、1∶14、1∶16,浸泡2 h,提取3 h,各条件分别平行3次,考察不同的料液比下艾叶挥发油的得率。
1.2.2.2 浸泡时间的影响 取粉碎的艾叶约100 g,精密称定,加蒸馏水,料液比(W/V)1∶12,浸泡时间分别取:0、1、2、4、6 h,提取3 h,各条件分别平行3 次,考察不同的浸泡时间下艾叶挥发油的得率。
1.2.2.3 提取时间的影响 取粉碎的艾叶约100 g,精密称定,加蒸馏水,料液比(W/V)1∶12,浸泡2 h,提取时间分别为:1、2、3、4、5 h, 各条件分别平行3 次,考察不同的提取时间时下叶挥发油的得率。
1.2.3 正交试验及最优提取条件的验证
1.2.3.1 因素水平设计 由单因素试验结果选择考察因素为提取时间(A)、料液比(B)和浸泡时间(C),各因素分别设3 个水平,考察指标为挥发油得率,设计三因素三水平的正交试验。 见表1。

表1 正交试验因素水平表
1.2.3.2 正交试验设计 取粉碎的艾叶约100 g, 精密称定,按表2 设计的L9(34)正交表进行试验。
1.2.3.3 最优工艺条件验证试验 以优选出的提取条件进行试验,重复3 次,以RSD 值小于5%为必要条件,确定优化条件下艾叶挥发油的得率。
1.2.4 统计学方法
采用统计软件SPSS 15.0 对实验数据进行分析[16-17],计量资料数据以均数±标准差()表示,采用单因素方差分析进行数据比较,采用t 检验。 以P <0.05 为差异有统计学意义。

表2 L9(34)正交试验表
2 结果
2.1 单因素试验结果与分析
2.1.1 料液比的影响
料液比(W/V)分别为:1∶8、1∶10、1∶12、1∶14、1∶16时,对应的挥发油得率依次为:(0.350±0.017)%、(0.424±0.013)%、(0.421±0.016)%、(0.414±0.021)%、(0.408±0.014)%,二者关系见图1。

图1 料液比与挥发油得率的关系
由图1 试验结果看出:在浸泡2 h、提取时间为3 h 的提取条件下, 料液比各水平间的挥发油得率由高到低依次为:1∶10>1∶12>1∶14>1∶16>1∶8。料液比为1∶10 时得率最高,为(0.424±0.013)%,与料液比1∶8 比较,差异有统计学意义(P <0.05),而与1∶12、1∶14、1∶16 之间比较,差异无统计学意义(P >0.05),即料液比为1∶10、1∶12、1∶14、1∶16 对挥发油的得率并无太大影响,但由于料液比在1∶10、1∶12 时挥发油得率较高,且综合考虑工业生产成本,选择正交试验中料液比的各水平为1∶10、1∶12、1∶14。
2.1.2 浸泡时间的影响
浸泡时间分别为:0、1、2、4、6 h,对应的挥发油得率依次为:(0.343±0.021)%、(0.378±0.014)%、(0.425±0.013)%、(0.417±0.012)%、(0.365±0.022)%, 二者关系见图2。

图2 浸泡时间与挥发油得率的关系
由图2 试验结果看出:料液比1∶12、提取时间为3 h 的提取条件下, 依艾叶挥发油得率高至低顺序的浸泡时间为:2 h>4 h>1 h>6 h>0 h。 艾叶经浸泡后提取较不浸泡挥发油得率提高。 其中浸泡2 h 的得率最高,为(0.425±0.013)%,约高于不浸泡时得率的23.91%,与浸泡4 h 比较,差异无统计学意义(P >0.05),浸泡时间超过4 h 后,挥发油得率显著降低,差异有统计学意义(P <0.05),浸泡1、2、4 h 挥发油得率较高。 因此,在正交试验中浸泡时间水平选择为1、2、4 h。
2.1.3 提取时间的影响
提取时间分别为1、2、3、4、5 h, 对应的挥发油得率依次为:(0.312±0.012)%、(0.365±0.019)%、(0.412±0.014)%、(0.418±0.014)%、(0.420±0.016)%, 二者关系见图3。
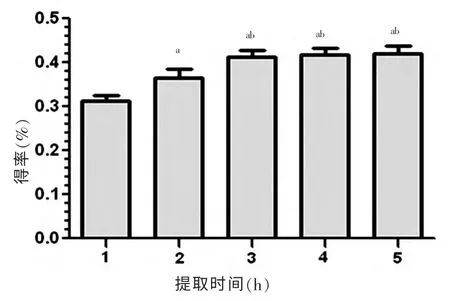
图3 提取时间与挥发油得率的关系
由图3 试验结果看出:在料液比1∶12、浸泡时间为2 h 的条件下,提取时间各水平间的挥发油得率由高到低依次为:5 h>4 h>3 h>2 h>1 h。 挥发油得率随着提取时间的增加而增加, 提取时间由1 h 增至3 h时,得率由(0.312±0.012)%增至(0.412±0.014)%,增加约32.05%,且3、4、5 h 得率显著增加,与2 h 比较,差异均有统计学意义(均P <0.05)。 3 h 后得率间的增加差异无统计学意义(P >0.05),5 h 比3 h 仅增加约1.94%,综合考虑成本,正交试验中提取时间选择1、2、3 h 三个水平。
2.2 正交试验结果与分析
2.2.1 正交试验
正交试验结果见表3, 利用正交试验软件对表3中的数据进行方差分析,结果见表4。

表3 L9(3)4 正交试验结果与分析

表4 方差分析表
由表3 得知,RA=0.096、RB=0.007、RC=0.021 各因素主次顺序为A>C>B,即直观分析:A 是最重要因素,对结果影响最大,其次是C,B 是最次要因素。 方差分析结果表明: 对艾叶挥发油得率的影响,A 差异有统计学意义(P <0.05),B 和C 差异无统计学意义(P >0.05)。 两者结果一致,提取时间是艾叶挥发油得率的主要影响因素。
根据挥发油提取条件的优选原则, 由表3 可知:kA3>kA2>kA1,kB1>kB3>kB2,kC3>kC2>kC1确定艾叶挥发油的最优提取工艺为A3B1C3,即料液比选择1∶10,浸泡4 h,提取3 h。
2.2.2 验证试验
由表5 结果显示,在优选的提取条件下,艾叶挥发油平均得率为0.416%,RSD=2.64%(n=3), 实验重复性好,结果可靠。

表5 最优提取工艺(A3B1C3)下的验证试验
3 讨论
通过单因素试验考察并选择正交试验各因素水平,用正交试验对艾叶挥发油水蒸气蒸馏法提取工艺进行了优选, 对优选出的最佳工艺条件进行了验证,证明重复性好,方法可行,结果可靠。
挥发油常见的提取方法有水蒸气蒸馏法、 微波法、溶剂回流法、超临界流体萃取法等,其中水蒸气蒸馏法是分析植物中挥发性成分的传统提取技术,操作简便、效率较高,适合工业生产推广,环保、经济[18-19]。
以水蒸气蒸馏法提取艾叶挥发油时,挥发油由水介质慢慢浸出,随水蒸气蒸出,因此应适当选择艾叶与水的比例。水量少时,水散作用进行不彻底,艾叶不能被充分浸泡,蒸气量生成的就少,得油率将受到影响,试验中当料液比为1∶8 时,上述原因使得挥发油得率不高;料液比为1∶10、1∶12、1∶14、1∶16 时,挥发油得率较高,分析原因可能是水量增大,水与挥发油两者的接触界面浓度差增大,更利于挥发油的扩散和溶解,从而使传质速率得到提高;若加水量过多,会增加耗能,从而使工业生产成本增加,因此试验中料液比的水平为1∶10、1∶12、1∶14。
艾叶挥发油得率随提取时间的增加而增加,3 h前挥发油得率增加明显,3 h 后得率增加缓慢,与艾叶挥发油不断蒸出后含量的减少有关。
艾叶是我国传统中药,挥发油是其诸多药理活性的主要有效成分群,艾叶挥发油质量的稳定是其药理活性的保证,因此其提取工艺的研究具有应用价值[20-21],尤其水蒸气蒸馏法提取,环保、经济,适合推广。
[1] 宋川.艾叶生药及其化学成分研究[D].昆明:云南中医学院,2013.
[2] 段蓉.艾叶化学成分的提取、分离与含量测定研究[D].天津:天津中医药大学,2011.
[3] 吉双,张予川,刁云鹏,等.艾叶的化学成分[J].沈阳药科大学学报,2009,26(8):617-619.
[4] 刘先华,周安,刘碧山,等.艾叶挥发油体内外抑菌作用的实验研究[J].中国中医药信息杂志,2006,13(8):25-26.
[5] 侯迎迎.艾叶乙酸乙酯部位抗乙肝病毒活性研究及成分分析[D].郑州:郑州大学,2013.
[6] 程慧.艾叶中黄酮类化合物研究进展[J].光明中医,2014,29(9):2015-2016.
[7] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:83.
[8] 梅全喜,高玉桥.艾叶化学及药理研究进展[J].中成药,2006,28(7):1030-1032.
[9] 张袁森,张琳,倪娜,等.艾叶的体外凝血作用实验研究[J].天津中医药,2010,27(2):156-157.
[10] 费新应,余珊珊,韦媛,等.蕲艾提取液抑制免疫性肝损伤大鼠肝纤维化作用的观察[J].实用肝脏病杂志,2009,12(1):11-13.
[11] 周英栋,费新应.艾叶的药理作用研究[J].湖北中医杂志,2010,32(11):75.
[12] 赵志鸿,黄勇勇,张小俊,等.河南驻马店产艾叶挥发油的GC-MS 分析[J].郑州大学学报:理学版,2013,45(2):80-84.
[13] 刘瑞江,张业旺,闻崇炜.正交试验设计和分析方法研究[J].实验技术与管理,2010,27(9):52-55.
[14] 姜丽红,田汝芳,马宏伟,等.正交试验优选藏茵香挥发油的提取与包合工艺[J].中药工艺与制剂,2014,25(23):2139-2140.
[15] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:附录63.
[16] 方积乾.生物医学研究的统计方法[M].北京:高等教育出版社,2007:541-553.
[17] 李艳玲,范艳花,陶偌偈.SPSS16.0 软件在化学正交试验中的应用[J].化学教学,2011,6(1):17-19.
[18] 温悦.挥发油提取方法研究概况[J].中国药业,2010,19(12):84-85.
[19] 张丽珍,詹晓如,胡奕勤,等.四味清口含片中挥发油的微波-超声辅助协同提取工艺研究[J].中国现代医生,2013,51(35):27-30.
[20] 张小俊,赵志鸿,张壮丽,等.艾叶顶空萃取的挥发油指纹图谱[J].中成药,2014,36(6):1222-1249.
[21] 王绪颖,陈彦,张振海,等.化学与药效学指标相结合改进痛经宝颗粒中挥发油提取工艺[J].中国实验方剂学杂志,2011,17(9):15-21.

