睾酮对自发性高血压大鼠肾脏结构和功能的影响
易东 谈世进 金俊 张臻
睾酮对自发性高血压大鼠肾脏结构和功能的影响
易东 谈世进 金俊 张臻
目的研究睾酮对自发性高血压大鼠(spontaneously hypertensive rats,SHR)肾脏结构和功能的影响。方法分别将18只10周龄的SHR及Wistar⁃Kyoto rats(WKY大鼠)进行卵巢切除,并随机分为卵巢切除(ovariectomized,OVX)组,卵巢切除后雌激素补充组(OVX+EB)和卵巢切除后雄激素补充组(OVX+TP),分别给予茶油0.5 ml/(kg·2 d)、苯甲酸雌二醇(estradiol benzoate,EB)0.25 mg/(kg·2 d)、丙酸睾酮(testosterone propionate,TP)3 mg/(kg·2 d)肌肉注射,持续8周。分别在实验初,第4和第8周末用尾部套囊法测定尾动脉收缩压(SBP)。在第8周末代谢笼收集大鼠24 h尿液,ELISA法检测尿微量白蛋白(urinalmicroalbumin,MAU)和尿肌酐浓度,计算蛋白肌酐比值。麻醉处死大鼠,ELISA法检测血清睾酮、雌二醇及孕酮浓度。分离右肾,称量,切片、HE染色观察肾病理改变。结果各组与实验初SBP相比,SHR及WKY OVX组及OVX+TP组4周末和8周末SBP逐渐升高(P<0.05),OVX+EB组SBP改变不明显(P<0.05)。和对应的OVX组8周末SBP相比,SHR及WKY大鼠OVX+TP组SBP明显升高(P<0.05),OVX+EB组SBP明显降低(P<0.05)。和对应的OVX组大鼠相比,补充雄激素均能显著增加SHR及WKY肾脏质量(P<0.05)及肾指数(P<0.05)。同时OVX及OVX+TP组均出现不同程度肾小管损伤,OVX+TP大鼠肾小管损伤较OVX组更严重,尤其是SHR。分别与SHR+OVX组和WKY+OVX+TP组相比,SHR+OVX+TP组MAU浓度和尿蛋白肌酐比值均显著升高(P<0.01),而WKY+OVX+TP组仅MAU浓度升高(P<0.01),蛋白肌酐比值无明显改变(P>0.05)。结论生理剂量的睾酮可以加重卵巢切除SHR肾结构改变和功能损伤,血压升高是其可能的机制之一。
雄激素;雄激素受体;肾功能;高血压
雄激素在生殖、分化、生长、发育及维持机体正常的生理稳态方面均起着极为重要的作用。近些年的研究发现,性激素能通过多种机制影响机体肾脏结构和功能的改变,引起了男女慢性肾病(chronic kidney dis⁃ease,CKD)发病率和进展速度的显著差异,表现为男性CKD发病率较女性高[1⁃2]。目前大量研究表明雌激素可能对肾脏起保护作用,其主要机制包括下调肾素、血管紧张素转换酶和血管紧张素Ⅱ等血管收缩因子的表达,促进一氧化氮(NO)等血管舒张因子合成和释放,抑制氧化应激水平,抑制胶原合成并促进胶原降解等[3⁃4]。而雄激素对肾脏结构和功能的研究则相对较少,本研究通过给卵巢切除自发性高血压大鼠(sponta⁃neously hypertensive rats,SHR)肌注生理剂量的丙酸睾酮来研究雄激素对肾脏结构和功能的影响,并探索可能的机制。
1 材料与方法
1.1 实验动物 8周龄的SPF级SHR及WKY大鼠各18只,体质量(120±10)g,由北京维通利华实验动物技术有限公司提供。
1.2 主要试剂 丙酸睾酮(中国药品生物制品检定所,生产批号100008),苯甲酸雌二醇(中国药品生物制品检定所,生产批号100006),睾酮、雌二醇、孕酮、尿肌酐及微量白蛋白ELISA试剂盒均由碧云天生物研究所提供。
1.3 主要仪器 电子天平,高速低温离心机,切片机(德国SLEE公司,型号CUT5062),显微镜,酶标仪(美国BioTek公司,型号ELx800),BP98A型尾动脉血压计(北京软隆科技有限责任公司)。
1.4 实验方法
1.4.1 实验模型与分组:分别将18只SHR及WKY大鼠随机分为3组,卵巢切除(ovariectomy,OVX)组、卵巢切除后雌激素补充(OVX+EB)组及雄激素补充(OVX+TP)组,每组6只,OVX组作为阴性对照,OVX+EB作为阳性对照。为区分SHR及WKY大鼠,各组名称分别记为:WKY+OVX,WKY+OVX+EB,WKY+OVX+TP;SHR+OVX,SHR+OVX+EB,SHR+OVX+TP。适应性喂养2周后开始实验。氯胺酮50 mg/kg腹腔注射麻醉大鼠后,背部固定,酒精喷雾消毒湿润毛发并去毛,在距剑突下约3 cm侧腹部处用75%酒精消毒,正中切口依次切开皮肤、皮下组织、腹部肌肉至腹膜,切口1.5 cm长,止血钳分开切口,镊子移开腹内组织,在腰椎两侧、肾后方找到一小球状物即卵巢,结扎卵巢动脉及输卵管,切除卵巢。将腹腔内容物复位,然后逐层缝合。术后连续3 d腹腔注射青霉素钠40万U,防止术后感染,然后开始实验,记作实验初。
1.4.2 动物饲养与给药:所有大鼠均给以标准饲料喂养,自由摄食,自由饮水,OVX+EB组给予苯甲酸雌二醇0.25mg/(kg·2 d)肌肉注射,OVX+TP组给予丙酸睾酮3 mg/(kg·2 d)肌肉注射[5]。OVX组给予肌肉注射相同剂量的注射用茶油,均持续8周。
1.4.3 大鼠尾动脉血压测定:分别在大鼠卵巢切除前,开始给药后第4周末及第8周末,采用尾部套囊法测定各组大鼠清醒状态下尾动脉收缩压(SBP),每只连续测3次,取平均值。
1.4.4 大鼠尿液收集与尿肌酐、微量白蛋白测定:在第8周末将大鼠放入清洁的代谢笼,收集24 h尿液,注入15 ml EP管,以4000 r/min的速度离心15 min,弃去底部残渣,按商家说明书采用ELISA法测定尿液肌酐及微量白蛋白浓度。
1.4.5 血清中性激素浓度测定:在第8周末,禁食8 h,称量体质量,颈椎脱臼法处死大鼠,迅速剖开腹腔,采用BD惰性分离胶促凝管下腔静脉采血,上下摆动数次后放入4℃冰箱中1~2 h,取出以4000 r/min的速度离心10 min,取血清。按商家说明书采用ELISA法测定血清睾酮、雌二醇及孕酮浓度。
1.4.6 单侧肾质量及肾指数测定:处死大鼠后,分离周围结缔组织及包膜,取出右侧肾脏,称量其质量记作单侧肾质量,计算其与禁食后体质量比值,即为肾指数。
1.4.7 肾脏形态学:将称量好的肾脏放入10%的中性福尔马林溶液中固定。石蜡包埋,普通切片机将肾脏切成10μm的薄片,HE染色,高倍镜观察肾脏病理形态改变。
1.5 统计学处理 所有计量数据以均数±标准差表示,数据分析采用SPSS 19.0统计软件。各组间均数比较采用单因素方差分析(one⁃way ANOVA),满足方差齐性的多重比较采用LSD法,不满足方差齐性的两两比较采用近似t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 各组大鼠血清性激素水平比较 各组大鼠血清睾酮、雌二醇及孕酮浓度如表1所示。与OVX组相比,补充雄激素后睾酮及补充雌激素后雌二醇的浓度均对应地显著升高(P<0.01)。OVX组和OVX+TP组雌二醇浓度,OVX组和OVX+EB组睾酮浓度差异均无统计学意义(P>0.05)。SHR的睾酮,雌二醇及孕酮水平与对应的WKY大鼠相比,均无明显差异(P>0.05),同时各组大鼠孕酮水平无明显差异(P>0.05)。
表1 各组大鼠血清性激素浓度比较(±s,n=6)

表1 各组大鼠血清性激素浓度比较(±s,n=6)
注:与OVX组比较,∗∗P<0.01
组别睾酮(nmol/L)雌二醇(pmol/L)孕酮(nmol/L)WKY+OVX 0.67±0.19 40.8±8.8 6.5±2.1 WKY+OVX+EB 0.56±0.18 326.8±35.4∗∗10.4±2.8 WKY+OVX+TP 11.70±3.20∗∗53.2±10.3 8.6±3.1 SHR+OVX 0.65±0.15 52.5±8.4 7.8±2.6 SHR+OVX+EB 0.77±0.22 284.9±30.8∗∗9.8±3.8 SHR+OVX+TP 12.61±3.42∗∗66.4±9.9 9.2±3.2
2.2 各组大鼠尾动脉SBP比较 SHR及WKY大鼠卵巢切除前组内SBP无明显差异(P>0.05)。和本组实验初SBP相比,SHR及WKY大鼠OVX组血压逐渐上升,8周末血压均显著高于实验初SBP(P<0.01),WKY大鼠血压反应较快,而SHR则变化幅度较大。SHR及WKY大鼠OVX+EB组整个实验过程中SBP变化无统计学差异(P>0.05),而OVX+TP组第4周末和第8周末SBP均显著高于对应组实验初的SBP(P<0.01)。与4周末SBP相比,SHR+OVX+TP第8周末SBP进一步升高(P<0.01),而WKY+OVX+TP变化无统计学意义(P>0.05)。和各自的OVX组相比,雄激素和雌激素干预4周对WKY和SHR SBP的影响均不明显(P>0.05),干预8周后雌激素能显著抑制卵巢切除引起的SBP升高(P<0.05),而丙酸睾酮干预则能进一步升高WKY及SHR的SBP(P<0.05),且以WKY大鼠更明显,可能与SHR实验初SBP较高且随着时间逐渐升高的特点有关。见表2。
表2 各组大鼠尾动脉SBP变化比较(±s,mmHg,n=6)

表2 各组大鼠尾动脉SBP变化比较(±s,mmHg,n=6)
注:与OVX组比较,∗P<0.05,∗∗P<0.01;与实验初比较,△P<0.05,△△P<0.01;与4周末比较,▲P<0.05,▲▲P<0.01
组别实验初4周末8周末WKY+OVX 133.7±3.6 141.9±5.0△145.6±6.7△△WKY+OVX+EB 132.3±6.4 135.4±5.2 133.1±4.8∗∗WKY+OVX+TP 130.5±7.1 151.3±8.3△△162.2±7.7∗∗△△SHR+OVX 171.3±6.1 179.2±7.6 190.3±4.7△△▲SHR+OVX+EB 180.1±6.4 181.0±6.5 182.8±4.6∗SHR+OVX+TP 173.5±5.1 188.0±5.0△△197.6±3.7∗△△▲▲
2.3 各组大鼠肾脏形态学比较 检测大鼠单侧肾质量、肾指数及肾脏病理切片改变以明确有无结构改变。大鼠单侧肾质量及肾指数结果见表3。卵巢切除后补充雌激素对SHR及WKY大鼠单侧肾质量及肾指数均无影响(P>0.05),而补充雄激素后SHR及WKY大鼠单侧肾质量及肾指数均明显升高(P<0.05)。HE染色结果如图1所示,各组肾小球结构完整,无明显纤维化或间质增生。卵巢切除大鼠肾小管出现上皮细胞脱落,管型形成,刷状缘脱落等改变,而雌激素补充后可以逆转这些损伤,雄激素干预后可以加剧WKY及SHR卵巢切除引起的肾小管损伤,表现为病变更广泛、密集,出现典型的管型。且SHR+OVX组及OVX+TP组病变均较对应的WKY大鼠严重。
2.4 各组大鼠肾功能比较 各组大鼠肾功能结果见表3。与OVX组相比,补充雌激素后显著降低SHR微量白蛋白和蛋白肌酐比值(P<0.01),而WKY大鼠无明显改变(P>0.05),雄激素干预后显著升高SHR微量白蛋白浓度和蛋白肌酐比值(P<0.01),且明显高于补充雄激素的WKY大鼠(P<0.01)。与WKY+OVX相比,WKY+OVX+TP仅微量白蛋白明显升高(P<0.01),蛋白肌酐比并无明显改变(P>0.05)。
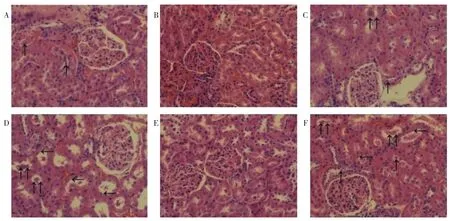
图1 各组大鼠高倍镜下肾脏病理表现
表3 各组大鼠肾大体结构及功能相关参数的比较(±s,n=6)
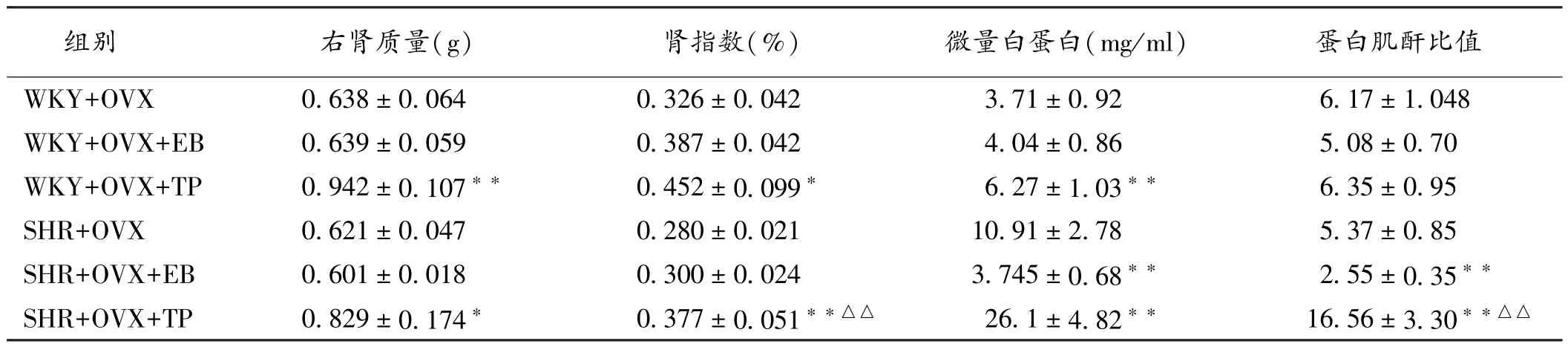
表3 各组大鼠肾大体结构及功能相关参数的比较(±s,n=6)
注:与相应的OVX组比较,∗P<0.05,∗∗P<0.01;与WKY+OVX+TP组比较,△△P<0.01
组别右肾质量(g)肾指数(%)微量白蛋白(mg/ml)蛋白肌酐比值WKY+OVX 0.638±0.064 0.326±0.042 3.71±0.92 6.17±1.048 WKY+OVX+EB 0.639±0.059 0.387±0.042 4.04±0.86 5.08±0.70 WKY+OVX+TP 0.942±0.107∗∗0.452±0.099∗6.27±1.03∗∗6.35±0.95 SHR+OVX 0.621±0.047 0.280±0.021 10.91±2.78 5.37±0.85 SHR+OVX+EB 0.601±0.018 0.300±0.024 3.745±0.68∗∗2.55±0.35∗∗SHR+OVX+TP 0.829±0.174∗0.377±0.051∗∗△△26.1±4.82∗∗16.56±3.30∗∗△△
3 讨论
与高血压发病的性别差异一样,男性CKD的发病率较同年龄的女性高且进展速度快,雄激素可能促进肾脏结构改变和功能减退。本研究中对卵巢切除的SHR及WKY大鼠补充生理剂量的雌激素和雄激素,结果显示补充雌激素可以降低SBP,逆转卵巢切除引起的肾小管损伤,降低SHR蛋白肌酐比值和微量白蛋白浓度,证明生理剂量的雌激素可以保护肾脏结构和功能。而雄激素则相反,可以升高SHR的SBP,增加单侧肾质量,肾指数,加剧卵巢切除引起的肾损伤,同时升高微量白蛋白浓度和蛋白肌酐比值,即可能加剧卵巢切除后SHR的肾损伤。血压升高可以引起肾脏结构和功能的改变,补充雄激素能显著升高SHR及WKY大鼠的血压,可能是雄激素促进肾损伤的机制之一。
雄激素的生物作用主要是通过雄激素受体(an⁃drogen receptor,AR)实现的,AR广泛分布于肾小球和肾小管[6]。雄激素和AR相互结合后即可以通过其基因作用和非基因作用来影响肾脏的结构和功能。研究表明高盐饮食上调雄性大鼠肾皮质血管紧张素原(an⁃giotensinogen,ATO)mRNA和蛋白水平,引起明显的血压升高和肾损伤,去势可以阻断高盐诱导的雄性大鼠血压升高和肾损伤,补充雄激素可以升高血压并增加肾损伤和肾内ATO表达[7]。雄激素可以直接上调近端小管肾素⁃血管紧张素⁃醛固酮系统(renin⁃angiotensin⁃aldosterone system,RAAS),增加肾小管重吸收,促进水钠潴留,升高血压,诱导或加重肾损伤[8]。同时大量研究证实心血管系统及肾脏局部的RAAS多个成分均有明显的性别差异,且雄激素可以上调RAAS表达和活性,最终引起血管紧张素Ⅱ浓度升高[9],后者引起强烈的血管收缩,引起肾小球内压力升高,诱导肾小球损伤。
雄激素还参与花生四烯酸的代谢,研究表明与雌性SHR相比,雄性SHR血压明显升高,肾脏细胞色素P450 4A蛋白表达上调,20⁃羟基廿碳四烯酸(20⁃hydroxyeicosatetraenoic acid,20⁃HETE)生成增加,而睾丸切除和AR阻断剂氟他胺均能降低血压,下调肾脏CYP450 4A及20⁃HETE,表明雄激素可以通过上调CYP450 4A基因表达,促进20⁃HETE合成,后者可以导致细胞去极化和钙离子内流,引起血管收缩增强,血压升高[10⁃11]。此外,CYP450 4A表达升高促进20⁃HETE合成后可以降低一氧化氮合酶(endothelial nitric oxide synthase,eNOS)的表达和磷酸化,抑制内皮依赖性血管舒张,增加阴离子的生成,引起血压升高和蛋白尿增加,而20⁃HETE合成抑制剂可以通过促进内皮蛋白激酶Akt,AMPK和eNOS磷酸化,改善内皮依赖性血管舒张,降低肾脏氧化应激和肾损伤[11]。即雄激素可以通过对花生四烯酸代谢的调节,影响局部血管舒缩、NO的生成和氧化应激状态,引起肾脏血流动力学改变和肾损伤。
此外,研究表明雄激素可以上调肾皮质NADPH氧化酶表达,后者促进超氧阴离子生成,诱导血压升高和氧化应激,而抑制NADPH氧化酶可以抑制氧化应激[12]。雄激素还可以和AR结合后通过JNK/c⁃Jun促进肾近端小管细胞凋亡[5]。而氧化应激过度和细胞凋亡增多均能引起肾脏结构改变和功能损伤。
总之,雄激素可以通过影响RAAS,花生四烯酸代谢,氧化应激,细胞凋亡等多种途径影响肾脏的结构和功能,参与慢性肾病的发病和调节。本研究中对卵巢切除SHR补充生理剂量的雄激素可以升高动脉收缩压,增加单侧肾质量及肾指数,加重肾小管损伤,增加微量白蛋白浓度和蛋白肌酐比值,即生理剂量的雄激素可以加剧卵巢切除SHR肾结构改变和功能损伤,动脉收缩压的改变是其可能的机制之一,雄激素引起肾脏结构和功能改变的确切机制还有待更深入的研究。
[1] de Munter JS,Agyemang C,van Valkengoed IG,et al.Sex difference in blood pressure among South Asian diaspora in Europe and North America and the role of BMI:ameta⁃ana⁃lysis[J].JHum Hypertension,2011,25(7):407⁃417.
[2] 黄燕,顾宁,庞家华.老年高血压患者血压节律变化与靶器官损害的关系[J].实用老年医学,2012,26(5):401⁃403.
[3] Dokras A.Cardiovascular disease risk in women with PCOS[J].Steroids,2013,78(8):773⁃776.
[4] 景秀菊,祁秀娟,刘建新,等.雌激素及精氨酸对去卵巢大鼠血清一氧化氮水平的影响[J].实用老年医学,2013,27(3):229⁃232.
[5] Yu Y,Shen Z,Zhou X,et al.Effects of steroid hormones on morphology and vascular endothelial growth factor expression in female bladder[J].Urology,2009,73(6):1210⁃1217.
[6] Reckelhoff JF,Zhang H,Granger JP.Testosterone exacerbates hypertension and reduces pressure⁃natriuresis in male spon⁃taneously hypertensive rats[J].Hypertension,1998,31(1 Pt 2):435⁃439.
[7] Akishita M,Hashimoto M,Ohike Y,et al.Low testosterone level is an independent determinant of endothelial dysfunction inmen[J].Hypertens Res,2007,30(11):1029⁃1034.
[8] Yaron M,Greenman Y,Rosenfeld JB,et al.Effect of testoste⁃rone replacement therapy on arterial stiffness in older hypo⁃gonadalmen[J].Eur JEndocrinol,2009,160(5):839⁃846.
[9] Empen K,Lorbeer R,Dorr M,et al.Association of testosterone levels with endothelial function in men:results from a population⁃based study[J].Arteriosclerosis,2012,32(2):481⁃486.
[10]Yu J,Akishita M,Eto M,et al.Androgen receptor⁃dependent activation of endothelial nitric oxide synthase in vascular en⁃dothelial cells:role of phosphatidylinositol 3⁃kinase/akt pathway[J].Endocrinology,2010,151(4):1822⁃1828.
[11]Simoncini T,Mannella P,Fornari L,et al.Dehydroepiandros⁃teronemodulates endothelial nitric oxide synthesis via direct genomic and nongenomic mechanisms[J].Endocrinology,2003,144(8):3449⁃3455.
[12]Forstermann U,Munzel T.Endothelial nitric oxide synthase in vascular disease:from marvel to menace[J].Circulation,2006,113(13):1708⁃1714.
Effect of testosterone on kidney structure and function in spontaneously hypertensive rats
YIDong,TAN Shi⁃jin,JIN Jun,ZHANG Zhen.Department ofGeriatrics,Affiliated Sixth People's Hospital,Shanghai Jiaotong University,Shanghai 200233,China
ObjectiveTo investigate the effectof testosterone on kidney structure and function in spontaneously hy⁃pertensive rats(SHR).M ethodsEighteen SHR and Wistar⁃Kyoto rats(WKY)of ten weeks old were ovariectomized and assigned to three groups randomly:ovariectomized(OVX)group,estrogen supplement after ovariectomy(OVX+EB)group and androgen supplement after ovariectomy(OVX+TP)group.They accepted intramuscular injection of tea oil 0.5 ml/(kg·2 d),estradiol benzoate(EB)0.25 mg/(kg·2 d)and testosterone propionate(TP)3 mg/(kg·2 d)respec⁃tively for 8 weeks.The tail artery systolic blood pressure(SBP)wasmeasured at the beginning,4th and 8th week of the study respectively by tail cuffmethod.The ratswere put intometabolic cages and the urine of 24 hourswas collected,then the urinary albumin and urinary creatinine concentration were detected by ELISA,and the ratio of protein to creatinine was calculated.At last,all the ratswere anesthetized and killed,blood and tissue samples collected,and then the concentra⁃tions of serum testosterone,estradiol and progesterone were detected by ELISA.The right kidney weightwasmeasured and pathological changes were observed.ResultsCompared with SBP at the beginning of our study,SBP of OVX and OVX+TP ofWKY or SHR increased continuously during 8 weeks experiment(P<0.05).The changes in OVX+EB group were not significant(P>0.05).Compared with SBP of corresponding OVX group at 8th week,SBP of OVX+TP group ofWKY or SHR was significantly increased,while SBP in OVX+EB group was decreased(P<0.05).Meanwhile,TP intervention in⁃creased the single kidney weight(P<0.05)and the ratio of kidney to body weight(P<0.01)of both SHR orWKY.OVX and OVX+TP group of SHR or WKY showed glomerular and renal tubular injury.What'smore,the changes in OVX+TP group weremore serious than those in OVX group,especially for SHR.Urinary albumin concentration and the ratio of pro⁃tein to creatinine of OVX+TP group of SHR wasmuch higher than those in OVX group of SHR and OVX+TP group ofWKY(P<0.01).While TP supplement only increased urinary albumin concentration in WKY significantly(P<0.01),but had no effect on the ratio of protein to creatinine(P>0.05).ConclusionsPhysiological dose of testosterone can aggravatethe changes of renal structure and function impairment of ovariectomized SHR and elevated blood pressuremight be one of the possiblemechanisms.
androgen;androgen receptor;renal function;hypertension
R 544.1
A
10.3969/j.issn.1003⁃9198.2014.02.010
2013⁃07⁃30)
200233上海市,上海交通大学附属第六人民医院老年科

