喹唑啉类衍生物的合成及杀菌活性研究
吴瑛
(岳阳职业技术学院,湖南岳阳 414000)
喹唑啉类衍生物的合成及杀菌活性研究
吴瑛
(岳阳职业技术学院,湖南岳阳 414000)
在作物的生长过程中常常会用到杀菌剂,为了寻找并筛选具有较高杀菌活性的化合物,本文利用生物等排原理及亚结构连接法,将具有优良生物活性的喹唑啉等结构引入化合物中,并对其生物活性进行检测,以获得对部分植物病原真菌具有较高活性和应用价值的杀菌剂。
喹唑啉;合成;杀菌活性;研究
0 引言
为了保证农作物的增产增收,发展农药是很重要的一方面。含喹唑啉类化合物的杀菌剂之所以受到关注,是由于这些化合物具有抗菌、抗微生物、抗炎、抗疟等活性。例如化合物1-1具有抗烟草花叶病毒(TMV)活性。化合物1-2能抑制玉米大斑病菌。

1-1
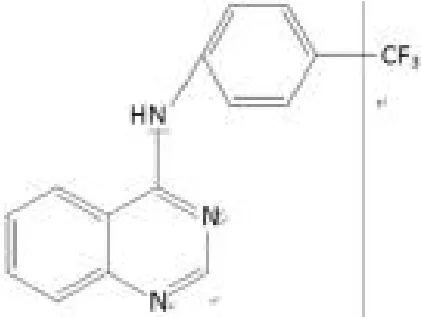
1-2
化合物1-3有一定的抑制克鲁斯氏椎体虫半胱氨酸蛋白酶的活性。化合物1-4具有抗炎活性。

1-3
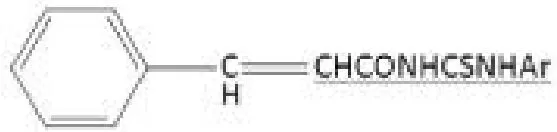
1-4
化合物1-5具有抗烟草花叶病毒活性,化合物1-6能高效抑制双子叶植物的生长,而对单子叶植物的生长具有促进作用[1]。
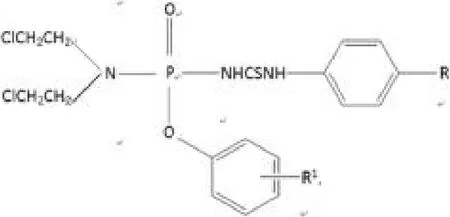
1-5

1-6
化合物1-7具有一定的杀菌活性,化合物1-8对大肠杆菌、枯草杆菌、变形杆菌有很强的抑制作用。

1-7
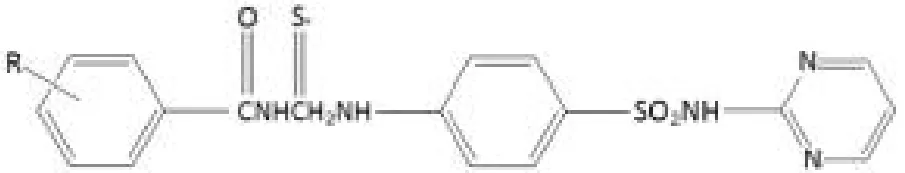
1-8
本文将对两个系列化合物4-苯甲酰肼基喹唑啉及N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲进行研究,目的在于获得具有较高活性的杀菌剂。
1 实验

所用试剂为化学纯或分析纯。
仪器:400型400MHZ核磁共振仪;VarioELIII CHNSO元素分析仪;X4型熔点测定仪;Trace EMS2000(finnigan)质谱仪;NICOLET公司的NEXUS470型红外光谱仪。

1.2.1 取代苯甲酰肼的制备
0.15 mol芳香酸加到50ml无水C2H5OH、30mL苯(环己烷)及8mLH2SO4的混合溶液中,加热回流24h,用水分离器分水。反应完毕后将反应物倒入盛有150g碎冰的烧瓶中,边搅拌边缓慢加入K2CO3至无气体溢出。用乙醚萃取,收取有机层,用无水MgSO4干燥,蒸去乙醚,粗品直接用于肼解。
将上述芳香乙酯加入到0.35mol85%的水合肼和40mL无水C2H5OH中并回流2h,冷却、抽滤后得到白色固体,产率为53%。
1.2.2 第一系列物质4-苯甲酰肼基喹唑啉合成
由邻氨基苯甲酸经过关环、氯化后得到4-氯喹唑啉(Ⅰ)。取代的苯甲酸酯化、肼解,所得产物与(Ⅰ)反应后得目标化合物Ⅱa-Ⅱg[2]。具体合成路线如下:

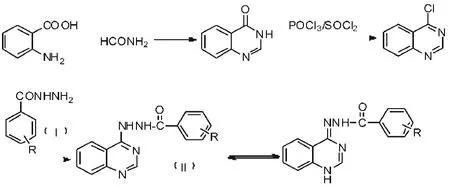
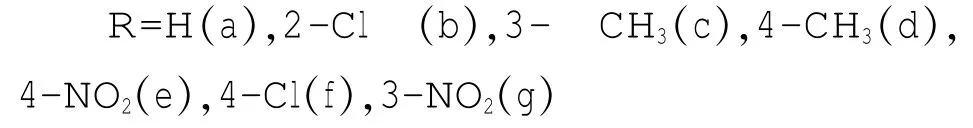
合成方法为:于三颈烧瓶中加入30mL三氯甲烷和0.4g4-氯喹唑啉及2.8mol取代苯甲酰肼,2.5mmol的三乙胺和少量的4-二甲氨基吡啶。加热回流5h,冷却,过滤,用乙醇重结晶即得所需化合物。1.2.3第二系列物质N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲合成
邻氨基苯甲酸经关环、氯化,生成4-氯喹唑啉,再与硫氰酸钾反应后再与苯甲酰肼反应便得到目标化合物Ⅱa-Ⅱg[3]。具体合成路线如下:
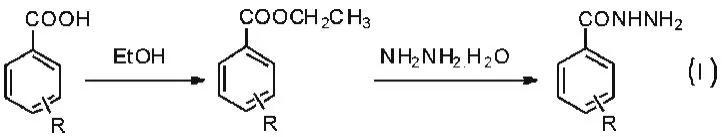
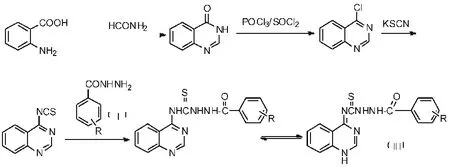

合成方法为:于三颈烧瓶中加入5mmol4-氯喹唑啉、6mmol硫氰酸钾和20mL无水乙腈,反应9h,然后过滤除氯化钾,加入4mmol取代苯甲酰肼,70℃状况下反应9h,所得物质用丙酮洗涤,再用乙醇重结晶[4]。
2 化合物的合成条件

在反应过程中,用二氯甲烷、三氯甲烷、乙腈作溶剂,实验证明在相同温度及条件下,用三氯甲烷产率最高。

在反应中适量减少苯甲酰肼量,原因在于它与目标化合物极性相近,取代苯甲酰肼过量会增加了产物的提纯难度。因此采用4-氯喹唑啉过量的方法,当两者的摩尔比为1∶1.2时较为合适。
3 目标化合物的理化性质及波谱数据

目标化合物IIa~IIg:的分子式、物理性质、产率及1HNMR,IR,元素分析和质谱等数据如下:
IIa4-苯甲酰肼基喹唑啉:黄色固体,产率71.8%;m.p.238℃~240℃1HNMR(d6-DMSO,400MHz)δ:11.76(s,1H,NH)10.71(s,1H,N=CH),10.0(s,1H, NH),7.52~8.19(m,9H,ArH),v:3424(N-H),3208(NH),1722(C=0),1604(C=N)cm-1;MS(m/z,%)264(0.77),159(2.35),129(15.18),112(11.53),105(28.41),102 (100),90(12.72),86(29.27),77(41.51),76(52.13);Anal.Calcd.for C15H12N4O:C68.17 H4.58 N21.20; found C 68.02,H 4.37,N21.28.
IIb4-(2-氯)苯甲酰肼基喹唑啉:黄色固体,产率75.7%.m.p.244℃~245℃1 HNMR(d6-DMSO, 400MHz)δ:11.75(s,1H,NH)10.70(s,1H,N=CH),10.0(s,1H,NH),7.53~8.19(m,8H,ArH);IR(KBr), v:3389(N-H),3318(N-H),1665(C=0),1614(C=N) cm-1;MS(m/z,%)298(1.47),159(2.44),139 (27.95),128(15.14),112(20.72),102(100),90 (12.73),86(29.17),77(13.23),76(52.13);Anal. Calcd.for C15H11ClN4O:C60.37 H3.71 N18.75; found C 60.08,H 3.43,N18.85.
IIc4-(3-甲基)苯甲酰肼基喹唑啉:黄色固体,产率64.5%.m.p.235℃~237℃1 HNMR(d6-DMSO,400MHz)δ:11.88(s,1H,NH),10.70(s,1H, N=CH),10.0(s,1H,NH),7.43~8.21(m,8H, ArH)2.36(s,3H,CH3),v:3422(N-H),3342(N-H), 1653(C=0),1604(C=N)cm-1;MS(m/z,%)278(0.90),159(2.25),129(17.48),118(29.73),112(10.26),102(100),92(43.92),90(11.75),86(28.17),76 (50.63);Anal.Calcd.for C16H14N4O:C69.07 H5.08 N20..2;found C 69.25,H 5.11,N20.20.
IId4-(4-甲基)苯甲酰肼基喹唑啉:黄色固体,产率70.4%.m.p255℃~258℃1HNMR(d6-DMSO,400MHz)δ11.97(s,1H,NH),10.70(s,1H, N=CH),10.0(s,1H,NH),7.43~8.21(m,8H,ArH)2.36(s,3H,CH3),v:3422(N-H),3338(N-H),1655 (C=0),1604(C=N)cm-1;MS(m/z,%)278(1.27),159 (2.55),129(14.48),118(27.24),112(12.26),102 (100),91(42.02),90(10.65),86(23.17),76 (50.23);Anal.Calcd.for C16H14N4O:C69.07 H5.08 N20.12;found C 69.12,H 5.00,N20.21.
IIe4-(4-硝基)苯甲酰肼基喹唑啉:黄色固体,产率50.2%.m.p.256℃~258℃1 HNMR(d6-DMSO,400MHz)δ:11.78(s,1H,NH),10.70(s,1H,N= CH),10.1(s,1H,NH),7.53~8.47(m,8H,ArH);IR (KBr),v:3402(N-H),3318(N-H),1674(C=0), 1634(C=N)cm-1;MS(m/z,%)309(0.84),159 (2.66),150(23.71),123(18.79),129(14.46),112(12.23),102(100),90(10.12),76(49.93);Anal. Calcd.for C15H11N5O3:C58.27 H3.58 N22.65; found C 58.39,H 3.42,N22.51.
IIf4-(4-氯)苯甲酰肼基喹唑啉:黄色固体,产率63.4%.m.p.259℃~261℃1 HNMR(d6-DMSO, 400MHz)δ:11.72(s,1H,NH),10.66(s,1H,N=CH),9.79 (s,1H,NH),7.51~8.17(m,8H,ArH)IR(KBr)v:3358(NH),3317(N-H),1665(C=0)1626(C=N),1237(C=S)cm-1. MS(m/z,2.36(s,3H,CH3),v:3422(N-H),3338(N-H), 1655(C=0),1614(C=N)cm-1;MS(m/z,%)298(1.47),159 (2.44),139(27.98),129(15.14),112(22.36),102 (100),90(12.72),86(29.17),77(14.53),76(52.13);Anal.Calcd.forC15H11ClN4O:C60.37H3.78 N18.72;found C 60.16,H 3.60,N18.91.
IIg4-(3-硝基)苯甲酰肼基喹唑啉:黄色固体,产率52.3%.m.p.247℃~249℃1 HNMR(d6-DMSO, 400MHz)δ:11.79(s,1H,NH),10.70(s,1H,N=CH),10.1 (s,1H,NH),7.50~8.41(m,8H,ArH)IR(KBr),v:3403 (N-H),3318(N-H),1675(C=0),1634(C=N)cm-1;MS (m/z,%)308(0.83),159(2.66),150(23.71),123 (18.79),129(14.46),112(12.23),102(100),90 (10.15),76(49.93);Anal.Calcd.for C15H11N5O3: C58.39,H3.42 N22.50;found C 58.38,H 3.42,N22.45.
目标化合物IIa~IIg:的分子式、物理性质、产率及1 HNMR,IR,元素分析和质谱等数据如下:
IIa N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:黄色固体,产量50.8%.m.p238℃~240℃1 HNMR(d6-DMSO,400MHz)δ:11.73(s,1H,NH),10.75(s,1H,N= CH),10.07(s,1H,NH),7.53~8.21(m,9H,ArH);IR (KBr),v:3412(N-H),3320(N-H),1655(C=0),1609 (C=N)cm-1;Anal.Calcd.for C16H13N50S:C52.17 H3.28 N22.80;found C 52.38,H 3.15,N22.06.
IIb(2-氯)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:黄色固体,产率47.3%.m.p.244℃~246℃1HNMR(d6-DMSO,400MHz)δ:11.79(s,1H,NH),10.76(s,1H,N=CH),10.08(s,1H,NH),7.49~ 8.20(m,8H,ArH),IR(KBr)v:3397(N-H),3310 (N-H),1659(C=0)1612(C=N)cm-1.Anal.Calcd. for C16H12ClN5OS:C53.72 H3.38 N19.60;found C53.45,H3.42,N19.88.
IIc(3-甲基)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:黄色固体,产率49.7%.m.p.235℃~237℃1HNMR(d6-DMSO,400MHz)δ:11.77(s,1H,NH), 10.76(s,1H,N=CH),10.10(s,1H,NH),7.41~ 8.20(m,8H,ArH)2.38(s,3H,CH3),IR(KBr)v:3424(N-H),3317(N-H),1659(C=0)1615(C=N)cm-1.Anal.Calcd.forC17H15N5OS:C60.52H4.48 N20.76;found C60.28,H4.52,N20.99.
IId(4-甲基)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:黄色固体,产率51.2%.m.p.255℃~258℃1HNMR(d6-DMSO,400MHz)δ:11.77(s,1H,NH), 10.76(s,1H,N=CH),10.09(s,1H,NH),7.41~8.20(m, 8H,ArH)2.36(s,3H,CH3),IR(KBr)v:3427(N-H), 3317(N-H),1658(C=0)1614(C=N)cm-1.MS(m/z,2.36 (s,3H,CH3),v:3422(N-H),3338(N-H),1655(C=0), 1614(C=N)cm-1;Anal.Calcd.for C17H15N5OS: C60.52 H4.48 N20.76;found C60.27,H4.62,N20.89.
IIe(4-硝基)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:橘黄色固体,产量42.3%.m.p.256℃~258℃1HNMR(d6-DMSO,400MHz)δ:11.84(s,1H,NH)10.83 (s,1H,N=CH),10.11(s,1H,NH),7.50~8.47(m,8H, ArH),IR(KBr)v:3405(N-H),3324(N-H),1657(C= 0)1621(C=N)cm-1.Anal.Calcd.for C16H12N6O3S: C52.17 H3.28 N22.81;found C52.33,H3.22,N22.89.
IIf(4-氯)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:黄色固体,产率43.6%.m.p.244℃~246℃1HNMR(d6-DMSO,400MHz)δ11.77(s,1H,NH),10.76 (s,1H,N=CH),10.09(s,1H,NH),7.50~8.20(m,8H, ArH),IR(KBr)v:3395(N-H),3317(N-H),1655(C=0)1608(C=N)cm-1.Anal.Calcd.for C16H12ClN5OS: C53.71 H3.38 N19.57;found C53.96,H3.26,N19.73.
I
Ig(3-硝基)-N-苯甲酰肼基-N·-(4-喹唑啉基)硫脲:橘黄色固体,产量45.6%.m.p.247℃~ 249℃1HNMR(d6-DMSO,400MHz)δ:11.82(s,1H, NH)10.79(s,1H,N=CH),10.11(s,1H,NH), 7.50~8.45(m,8H,ArH),IR(KBr)v:3404(N-H), 3318(N-H),1652(C=0)1619(C=N)cm-1.Anal. Calcd.for C16H12N6O3S:C52.28 H3.36 N22.59.
4 化合物的杀菌活性检测
4.1.1 供实验用的植物病原菌
4.1.2 实验方法
葡萄糖20g、水1000mL、琼脂30g、马铃薯260g配成培养基,在培养皿中,在一个大气压下高温灭菌30min,趁热加入待测样品后配成浓度为50PPm的液体,摇匀后倒入培养皿中,冷却后取菌琼脂片,放入各培养皿中,菌丝面向下,然后放入恒温培养皿箱中进行培养(温度27℃,时间3天),然后测量菌斑的直径并空白对照[5]。
4.1.3 计算方法


4.2.1 化合物的测试结果
化合物杀菌活性的测试结果见表1、表2。
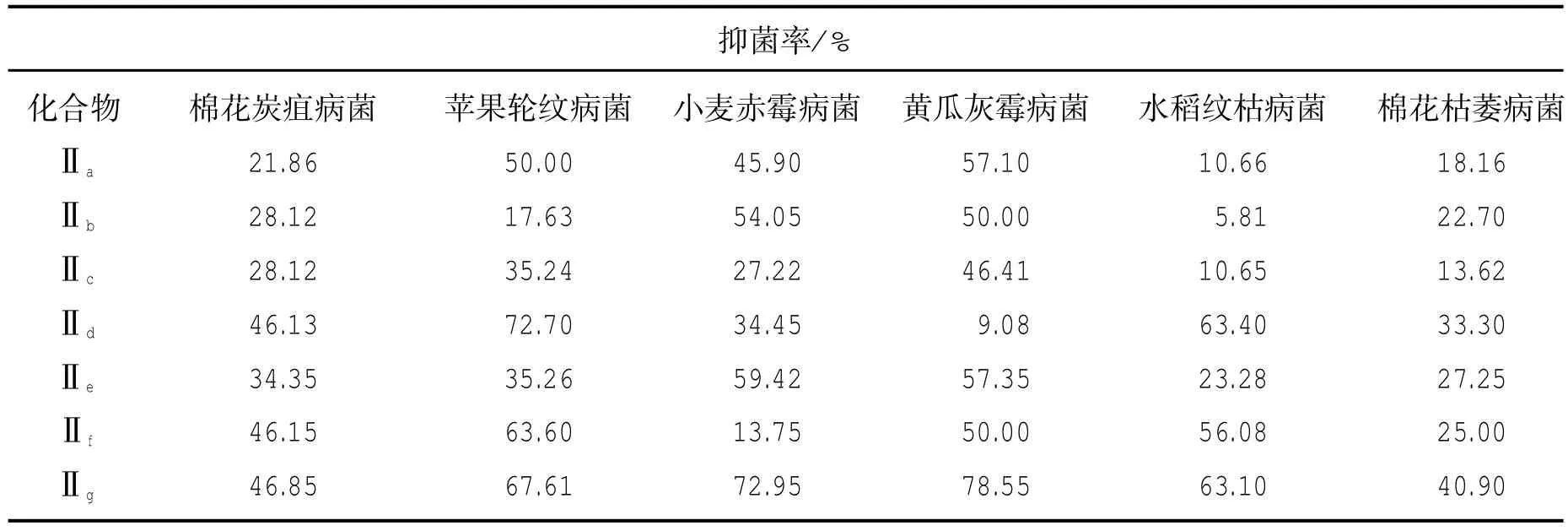
表1 第1系列化合物的杀菌活性测试结果

表2 第2系列化合物的杀菌活性测试效果
4.2.2 杀菌活性测试结果分析
实验证明:在化合物中引入硫脲结构后,活性有所增强。所有化合物对黄瓜灰霉病菌Botrytis cinereapers的选择性是较好的。苯环上有吸电子基团的抑菌活性比有供电子基团的抑菌活性强[6]。
[1]李秀文.含1,3,4-噁二唑或喹唑啉类衍生物的合成与杀菌活性研究[D].武汉:华中师范大学,2006.
[2]孙光文.N-(5-芳基-1,3,4-噁二唑-2-基)-N’-取代芳氧乙酰基硫脲的合成及杀菌活性的研究[D].武汉:华中师范大学,2006.
[3]王芬华,覃章兰.N-(5-芳基-1,3,4-噁二唑-2-基)-N'-α-萘乙酰基硫脲的合成及杀菌活性[J].农药学学报,2004,09 (30).
[4]刘军虎,刘勇,蹇军友,等.含1,2,4-三唑类席夫碱的新型喹唑啉类化合物的合成及抗菌活性研究[J].有机化学,2013(2).
[5]高元磊,林选福,韩菲菲,等.N-[3-(4-喹唑啉基)氨基-1H-吡唑-4-甲酰基]醛腙类衍生物的合成及抗菌活性研究[J].有机化学,2011(10).
[6]陈舒忆,吕同杰.喹唑啉类化合物的合成及抗菌活性研究[J].有机化学,2013(2).
(责任编校:马余平)
Study on Synthesis and Fungicidal Activity of Quinazoline
WU Ying
(Yueyang Vocational and Technical College,Yueyang,Hunan 414000)
Bactericidal agent is useful in crop breeding.In order to find out and screen compounds which possess high bactericidal activity,based on the bioisosterism and the method of metastructure conjunction,the paper inducted the Quinazoline metastructure to some compounds,then tested their bioactivity,and got the fungicide with high activity and application value to part of the plant pathogenic fungi.
Quinazoline;synthesis;bactericidal activity;research
R 914
A
1672-738X(2014)06-0074-05
2014-06-20
2013年湖南省教育厅一般资助课题(13C981)
吴瑛(1966—),女,湖南平江人,化学教授。主要研究方向:有机化学。

