新型哌啶基对甲苯磺酸叔铵盐离子液体的制备及其催化合成柠檬酸三丁酯
郭剑桥,丁 嘉,黄媛媛,汪青松,虞 宁,李 工*
(1.常州大学石油化工学院,江苏 常州 213164; 2.溧阳江南绝缘粉末厂,江苏 常州 213371)
柠檬酸三丁酯(TBC)为生物可降解无毒增塑剂,具有增塑效率高、相容性好、耐寒、耐光、抗霉挥发性小等优良性能,还可用于聚氯乙烯、聚丙烯和各种纤维素树脂的增塑剂、蛋白质类溶液的消泡剂等,用途非常广泛[1]。传统合成TBC的方法主要为浓硫酸催化酯化法,但该工艺存在副反应多、产品色泽深、后处理工艺复杂、设备腐蚀严重和废酸环境污染等弊端。目前,开发以硫酸氢盐、盐酸盐、有机酸、固体超强酸、杂多酸等为催化剂替代浓硫酸的新工艺的研究十分活跃[2-6]。这些催化剂虽然在一定程度上克服了传统质子酸催化剂存在的缺陷,但它们不同程度的存在相对活性低、表面易积碳、酸性位密度低和酸强度分布不均等缺陷,从而限制了它们的应用。离子液体具有稳定性高、可重复使用、可调变性能等特殊性能[7],其用途之一是可以作为催化剂使用,并可根据反应的需要来改变和修饰离子液体的阴、阳离子[8-11],使其具有灵活的可调变酸性,且可以循环使用[12]。
笔者利用离子液体的可设计性特点,参考文献[13-14]设计合成了两种Brønsted酸性的对甲苯磺酸叔铵盐离子液体[HMILS]OTs和HMIBL[OTs]2,并将其作为催化剂用于催化柠檬酸和正丁醇的酯化反应,考察离子液体的结构、反应条件对酯化反应转化率和选择性的影响。
1 实 验
1.1 主要原料与仪器
高哌啶,AR,江苏射阳化工厂;3-氯丙酸,CP,国药集团化学试剂;无水氯仿、二氯甲烷、无水乙醇、1,4-二溴丁烷、乙腈、丙酮,AR,国药集团化学试剂;对甲苯磺酸,AR,中国医药集团上海化学试剂公司。
Nicolet PROTEGE 460傅里叶变换红外光谱仪(KBr压片液膜法),美国Nicolet公司;AVANCE Ⅲ核磁共振波谱仪,瑞士Bruker公司;EA2400 II元素分析仪,美国PerkinElmer公司;SDT Q600热重示差扫描量热仪(氮气保护,升温速率为20 ℃/min),美国TA公司。
1.2 离子液体[HMILS]OTs的合成
[HMILS]OTs离子液体的合成:将一定量的3-氯丙酸溶解在无水氯仿中,在0 ℃冰水浴中缓慢滴加等量的高哌啶,70 ℃恒温水浴回流50 h;过滤产物得淡黄色固体,用无水乙醇洗涤3次后,在1.33 Pa、70 ℃条件下干燥5 h得白色片状晶体,称重并转移到250 mL三口烧瓶中;加入二氯甲烷将其溶解后缓慢加入等量的对甲苯磺酸,氮气保护下50 ℃水浴回流48 h,旋蒸除去二氯甲烷,用无水乙醚洗涤两次再次旋蒸,然后在1.33 Pa、70 ℃条件下干燥6 h得到淡黄色颗粒状固体,命名为[HMILS]OTs。
1.3 离子液体HMIBL[OTs]2的合成
将一定量的1,4-二溴丁烷溶于80 mL乙腈溶液,加入到带有机械搅拌装置的250 mL三口烧瓶中,在0 ℃冰水浴中缓慢滴加高哌啶,加入量与1,4-二溴丁烷物质的量比为2∶1,氮气保护下70 ℃水浴回流24 h;过滤所得固体用丙酮洗涤3次,在1.33 Pa、70 ℃条件下干燥5 h得乳白色针状晶体,称重并转移到250 mL三口烧瓶中,加入80 mL二氯甲烷使其充分溶解,然后按物质的量比1∶2缓慢加入对甲苯磺酸,氮气保护下40 ℃水浴回流48 h,旋蒸除去二氯甲烷,用无水乙醚洗涤两次再次旋蒸,在1.33 Pa、70 ℃条件下干燥6 h得到橙色黏稠状的物质,并命名为HMIBL[OTs]2。
1.4 酯化反应
将设定摩尔比的柠檬酸和正丁醇加入到带有分水器的三口烧瓶中,加热搅拌,待柠檬酸完全溶解时加入一定量的离子液体,迅速取样,参照国家标准GB/T 1668—2008,测定试样的初始酸值(NaOH,下同)为W1(单位:mg/g)。当体系开始蒸馏出共沸物时记录反应时间,控制温度并及时分水,待反应至预定时间后,停止加热,再次取样,测定试样的酸值为W2(单位:mg/g)。柠檬酸的转化率按X柠檬酸=(1-w2/w1)×100%计算[15]。柠檬酸三丁酯(TBC)的选择性则通过气相色谱分析,采用内标法计算,测试条件:色谱柱为30 m×0.25 mm×0.33 μm SE54毛细管柱;柱炉温度230 ℃,汽化温度250 ℃,检测温度250 ℃;柱前压 0.05 MPa,空气压0.06 MPa,氢气压0.12 MPa。
2 结果与讨论
2.1 离子液体的结构表征
[HMILS]OTs:1H NMR(500 MHz,D2O),δ:7.68(d,J=7.7 Hz,2H),7.36(d,J=7.3 Hz,2H),3.41(d,J=6.5 Hz,4H),3.25~3.04(m,2H),2.86(t,J=6.7 Hz,2H),2.38(s,3H),1.88(d,J=5.2 Hz,2H),1.81(d,J=5.0 Hz,2H),1.66(d,J=3.1 Hz,4H);13C NMR(500 MHz,D2O),δ:176.65(—COOH),145.13(SO3-ph),142.21(para-SO3-ph),132.14(ph),128.05(ph),57.58(—CH2CH2COOH),55.00(—CH2COOH),31.52(N—CH2-),28.58(N—CH2CH2—),25.78(N—CH2CH2CH2—),23.17(ph-CH3)。
HMIBL[OTs]2:1H NMR(500 MHz, D2O),δ:7.69(d,J=7.9 Hz, 2H),7.34(d,J=7.8 Hz, 2H), 3.37(m, 4H), 3.33~3.26(m, 4H),3.24~3.12(t, 4H),2.37(s, 6H),2.08(t, 4H), 1.79(d, 8H),1.63(d, 8H);13C NMR(500 MHz,D2O),δ:144.90(SO3-ph),142.36(para-SO3-ph),132.04(ph),127.97(ph),67.18,66.22(—CH2—N),48.80(—CH2CH2—N),29.18,28.56(N—CH2—),27.10(N—CH2CH2—),24.87,23.74(N—CH2CH2CH2—),23.11(ph-CH3)。

图1 离子液体的1H NMR谱

图2 离子液体13C NMR谱
元素分析结果。[HMILS]OTs(C16H25NSO5),实测值:C 52.76,H 7.86,N 3.61,S 10.86, O 24.79;分析计算值:C 55.97,H 7.29,N 4.10,S 9.33,O 23.32。 HMIBL[OTs]2(C30H48N2S2O6),实测值:C 56.89,H 7.79,N 5.36,S 11.98, O 17.52;分析计算值:C 60.40,H 8.05,N 4.69,S 10.74,O 16.11。
两种离子液体的红外光谱见图3。[HMILS]OTs曲线,σ/cm-1:3 413.77(—OH),3 058.89(N—H),2 933.53(C—H),2 858.13(C—H),1 458.08 (CH2),1 188.07(C—C),1 726.17(羧酸),798.47(CH2),1 598.88(苯环),1 458.08(苯环),1 423.37(苯环);813.90(苯环),1 168.78 ~1 188.07(νasSO2),1 031.85(νsSO2)。
HMIBL[OTs]2曲线,σ/cm-1:2 964.39(N—H),2 935.46(C—H),2 854.45(C—H),1 461.94(CH2),1 124.42(C—C),678.9(CH2),1 560(苯环),1 494.73(苯环),1 461.94(苯环),819.69(苯环),1 099.35 ~1 124.42(νasSO2),1 029.92 cm-1(νsSO2)。
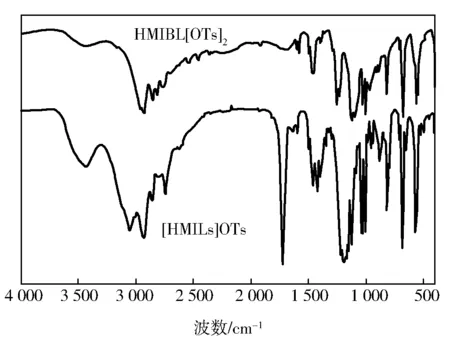
图3 两种离子液体的FT-IR谱
由上可知,产物分别为对甲苯磺酸叔铵盐离子液体1-(丙酸基)高哌啶对甲苯磺酸盐[HMILS]OTs和双-(1-高哌啶)亚丁基双对甲苯磺酸盐HMIBL[OTs]2两种新型离子液体,结构如图4所示。
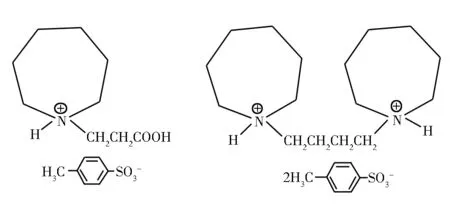
[HMILS]OTs HMIBL[OTs]2图4 离子液体的结构示意
2.2 离子液体的酸性与热稳定性
表1是两种离子液体水溶液的酸性。由表1可见:两种离子液体均显示出较强酸性,且pH值随浓度增加而降低,两种离子液体的酸性强度为:HMIBL[OTs]2>[HMILS]OTs。这是因为[HMILS]OTs靠羧基和叔铵盐阳离子上电离出的H体现酸性,HMIBL[OTs]2靠叔铵盐阳离子上电离出的两个H体现酸性,相对于[HMILS]OTs更容易电离,能相应的增加其酸性;二者比同等浓度的硫酸水溶液的酸性略低,表明合成的离子液体[HMILS]OTs 和HMIBL[OTs]2具有较强的酸性。

表1 不同浓度离子液体的酸性(pH值)
两种离子液体的热失重曲线见图5。由图5可知:[HMILS]OTs和HMIBL[OTs]2明显的分解温度分别为291.53和310.09 ℃,表明两种离子液体的热稳定性满足大多数酯化反应对温度的要求。

图5 两种离子液体的热重分析
2.3 离子液体在酯化反应中的催化活性
根据[HMILS]OTs和HMIBL[OTs]2的结构,它们均为Brønsted酸性离子液体,用它们作催化剂,在相同反应条件下催化柠檬酸与正丁醇反应制备柠檬酸三丁酯,反应条件为:n(醇)∶n(酸)∶n(催)=5∶1∶0.07,120 ℃,反应时间为3.5 h,反应结果见表2。

表2 不同离子液体的催化活性
由表2可见:新型离子液体HMIBL[OTs]2的催化活性高于 [HMILS]OTs,与表1中两种离子液体的pH值变化趋势一致;同时HMIBL[OTs]2的催化活性均高于两种常规的甲苯磺酸类离子液体1-甲基-3-(3-丙磺基)咪唑对甲苯磺酸盐([MIMPS]OTs)和1-甲基-3-咪唑对甲苯磺酸盐([MIM]OTs),与H2SO4为催化剂时的转化率相当,但对柠檬酸三丁酯的选择性更高。
2.4 影响酯化反应的因素
2.4.1醇酸比
图6为原料配比(n(正丁醇)∶n(柠檬酸),简称醇酸比)对反应的影响。由图6可以看出:醇酸摩尔比从理论配比3∶1开始增加,柠檬酸的转化率也随之增加,当醇酸摩尔比达到5∶1时转化率达到最高,这是因为过量的正丁醇起到带水的作用能够及时分离出反应产生的水促进平衡正向移动。继续增大醇酸摩尔比转化率开始降低,这可能与过量的醇使反应体系浓度降低有关,而酯的选择性随着醇酸摩尔比的增加一直呈上升趋势,但在醇酸最佳摩尔比之后上升幅度较小。

图6 醇酸比对反应的影响反应条件:120 ℃,3.5 h,催化剂用量0.07 mol。
2.4.2催化剂用量
HMIBL[OTs]2用量对反应的影响见图7。由图7可以看出:逐渐增加离子液体的用量,柠檬酸的转化率和TBC的选择性均随之增加,当HMIBL[OTs]2与柠檬酸的摩尔比为0.07时,柠檬酸的转化率达到最高为98.2%,继续增加催化剂的用量,柠檬酸转化率出现下降趋势。可能原因是离子液体黏度较大,用量过大会导致反应物之间的传质效果降低,酸与醇分子之间不能充分接触所致。
2.4.3反应温度
反应温度的影响见图8。由图8可见:温度较低时柠檬酸的转化率也较低,随着反应温度的不断升高,转化率呈现上升趋势,当温度达到120 ℃时达到最高;继续升高温度,转化率呈下降趋势,产物的颜色加深,产品的质量较差。可能原因是温度过高时正丁醇汽化量加大,液相中的正丁醇浓度相对降低,同时也不利于体系中TBC的稳定存在。因此,120 ℃为选最佳的反应温度,此时柠檬酸的转化率为98.2%,TBC的选择性为98.6%。
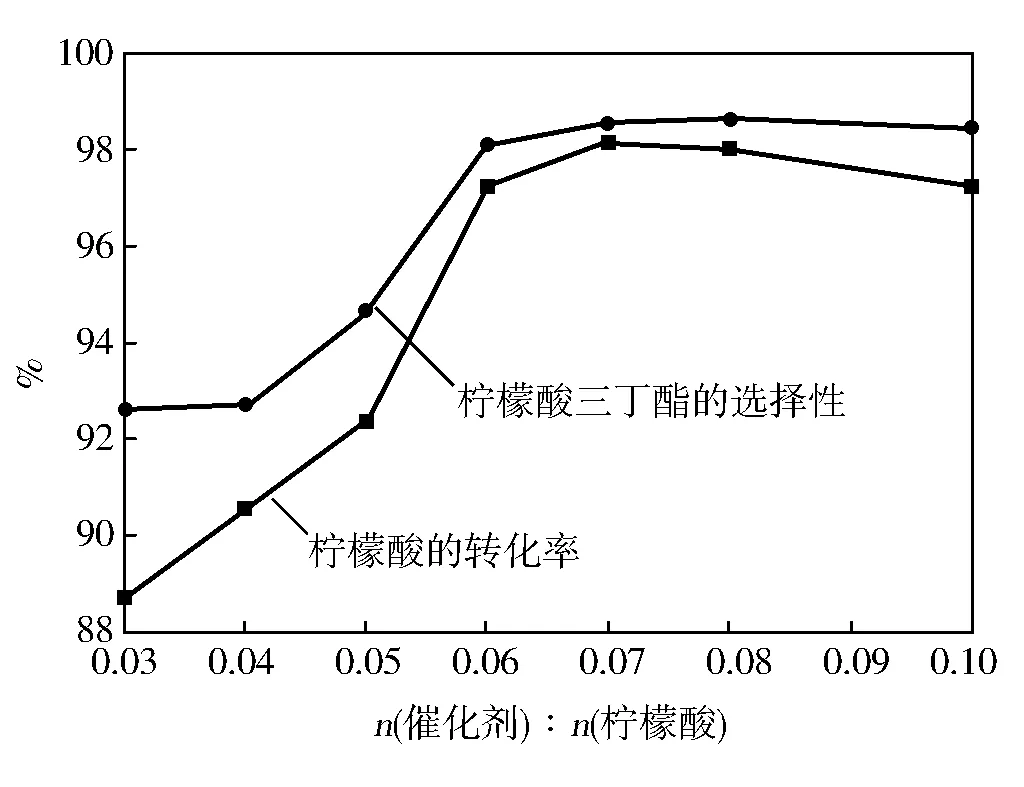
图7 HMIBL[OTs]2用量对反应的影响反应条件: 醇酸比=5∶1,120 ℃,3.5 h。
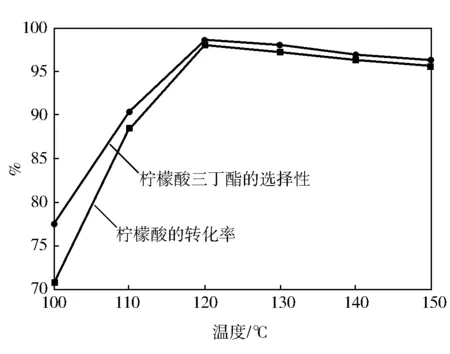
图8 反应温度对反应的影响反应条件: 醇酸比=5∶1,3.5 h,催化剂量0.07 mol。
2.4.4反应时间
图9为反应时间对反应的影响。由图9可知:柠檬酸的转化率随着反应时间的延长显著增高,在反应2 h时,柠檬酸转化率为88.9%,当反应时间为3.5 h时柠檬酸转化率达到98.2%,反应时间再延长转化率不再增加,反而有降低的趋势,这可能是反应达到平衡后,延长反应时间会导致TBC的水解以及副反应和逆反应的发生,都会不同程度的降低转化率,因此,认为最佳反应时间大约为3.5 h。
2.5 HMIBL[OTs]2的重复使用性能
反应结束后,HMIBL[OTs]2一部分沉淀于烧瓶底部,而大部分却能溶于反应混合物中,向反应混合物中加入少量水将HMIBL[OTs]2萃取出来,经真空干燥可得再生的HMIBL[OTs]2,可直接用于下一次酯化反应。图10是HMIBL[OTs]2的重复实验结果。
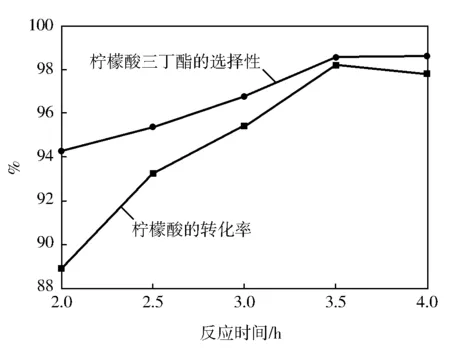
图9 反应时间对反应的影响反应条件: 醇酸比=5∶1,120 ℃,催化剂用量0.07 mol。

图10 HMIBL[OTs]2的重复使用性能反应条件: 醇酸比=5∶1,120 ℃,催化剂用量0.07 mol,3.5 h。
由图10可知:HMIBL[OTs]2循环使用8次后,柠檬酸的转化率降低不大,柠檬酸三丁酯的收率仍达96%以上,且降低的原因可能是在循环使用回收催化剂时损失造成的,表明新型离子液体HMIBL[OTs]2有着良好的循环使用效果。
3 结 论
a.采用两步法合成出两种新型对甲苯磺酸叔铵盐离子液体[HMILS]OTs和HMIBL[OTs]2,并对其进行了表征,它们的热分解温度均高于290 ℃。酸性测定表明HMIBL[OTs]2的酸性强于 [HMILS]OTs,但比同等浓度的硫酸水溶液的酸性略低。
b.在催化柠檬酸和正丁醇的酯化反应中,HMIBL[OTs]2的催化活性明显高于H2SO4和[HMILS]OTs,其对柠檬酸的转化率和对柠檬酸三丁酯的选择性分别为98.2%和98.6%。
c.离子液体催化剂HMIBL[OTs]2使用后易于回收,重复使用8次后催化活性降低不大。实验表明双核高哌啶为阳离子的离子液体明显比其单核离子液体的酸性和催化活性高,且原料易得,制备方法简单,可进一步拓宽在其他酸催化反应中的应用。
参 考 文 献
[1] 石万聪, 盛成祥. 增塑剂[M]. 北京: 化学工业出版社, 1987:248-252.
[3] 郭鑫, 张敏卿. 大孔强酸性阳离子交换树脂催化合成柠檬酸三丁酯[J]. 化工进展, 2010,29(4):673-676, 693.
[4] 邓斌,黄海英,刘国军.硫酸氢钠催化合成柠檬酸三丁酯[J]. 精细化工中间体, 2003,33(6):49-50.
[5] 陈平,汤涛.磷钨酸铝合成柠檬酸三丁酯[J]. 工业催化, 2007,15(11):46-49.
[6] 罗炜,朱银邦,王丹,等.柠檬酸三丁酯的合成研究[J]. 南京师大学报:自然科学版, 2010,33(1):59-62.
[7] Visser A E, Swatloski R P, Reichert W M, et al. Task-specific ionic liquids for the extraction of metal ions from aqueous solutions[J]. Chem Commun, 2001(1):135-136.
[8] Cole A C, Jensen J L, Ntai I, et al. Novel Brønsted acidic ionic liquids and their use as dual solvent-catalysts[J]. Journal of the American Chemical Society, 2002, 124(21): 5962-5963.
[9] Davis J H. Task-specific ionic liquids[J]. Chem Lett, 2004,33(9):1072-1077.
[10] 陈晓伟,包宗宏.室温离子液体的应用进展[J].精细石油化工,2006,23(2):60-64.
[11] Li D, Shi F, Peng J, et al. Application of functional ionic liquids possessing wwo adjacent acid sites for acetalization of aldehydes[J]. J Org Chem, 2004,69(10):3582-3585.
[12] Wu H, Sun J, Yang F, et al. Immobilization of HX:[Hmim]X as halogenating agent, recyclable catalyst and medium for conversion of alcohols to alkyl halides[J]. Chinese J Chem, 2004,22 (7):619-621.
[13] Liu D, Gui J, Zhu X, et al. Synthesis and characterization of task-specific ionic liquids possessing two Brønsted acid sites[J]. Synthetic communications, 2007, 37(5): 759-765.
[14] 梁金花,徐玥,任晓乾,等. 双核离子液体-杂多酸催化剂上高选择性合成单十二烷基磷酸酯[J].石油学报:石油加工, 2011,27(3):482-487.
[15] Xu J, Jiang J, Zuo Z, et al. Synthesis of tributyl citrate using acid ionic liquid as catalyst[J]. Process Saf Environ, 2010,88(1):28-30.

