154例患者664次万古霉素血药浓度监测分析
黄春燕,郭代红,朱 曼(解放军总医院药品保障中心,北京 100853)
154例患者664次万古霉素血药浓度监测分析
黄春燕,郭代红,朱 曼(解放军总医院药品保障中心,北京 100853)
目的:通过对万古霉素血清谷浓度监测数据的分析,探讨谷浓度有效范围对临床合理用药的指导作用。方法:回顾性调查我院2011年1月 – 2012年12月154例接受万古霉素药物治疗的患者,对664例次血清谷浓度分布情况进行分析。结果:平均血药浓度谷值(14.18 ± 9.28) mg·L-1,处于有效浓度范围内的为204例次(30.72%),超过有效浓度上限、处于美国感染病学会(IDSA)有效目标浓度的有124例次(18.68%)。肾功能不全患者的监测例次及调整用药比例均高于肾功能正常的患者。结论:依据万古霉素的有效目标浓度值调整给药剂量,更适合个体化用药需求,对于复杂感染的患者必要时可突破当前有效浓度范围的上限。
万古霉素;血药浓度监测;谷浓度;目标浓度
万古霉素是一种糖肽类抗生素,对革兰阳性菌有较强的杀菌作用,是临床治疗耐甲氧西林金黄色葡萄球菌、肠球菌重症感染的首选药物。因万古霉素具有潜在的肾毒性,其治疗窗窄、个体差异大,通过对其进行血药浓度监测有助于减少临床严重不良反应的发生,降低用药风险。本文回顾性调查分析解放军总医院2011 – 2012年154例患者664次万古霉素血药浓度谷值监测结果,探讨监测现状和血清谷浓度范围调整的问题,以期为临床合理用药提供参考。
1 材料与方法
1.1 仪器
万古霉素试剂盒、荧光偏振免疫分析仪及质控试剂(美国Abbott公司)。采用荧光偏振免疫分析法(FPIA)测定万古霉素血药浓度。
1.2 资料来源与评价标准
采用回顾性调查方法,利用医院信息系统提取2011年1月 – 2012年12月期间使用万古霉素治疗并进行血清谷浓度监测患者的一般资料、监测值、临床诊断等信息,以及院药品不良反应监测办公室收集报告等资料。万古霉素有效血药浓度谷值范围参照《中国药典·临床用药须知》(2010年版)[1]规定的10 ~ 15 mg·L-1;同时对照美国IDSA目标浓度的定义标准进行分析[2],将谷浓度范围分为4级:< 10mg·L-1、10 ~ 15 mg·L-1、15 ~ 20 mg·L-1、> 20 mg·L-1。治疗结果疗效评价参照《抗菌药物临床应用指导原则》分为痊愈、显效、进步、无效[3],用药少于或等于1次为无法评价,痊愈、显效、进步归为有效并计算有效率。
1.3 统计学方法
采用SPSS 19.0统计软件分析处理所得数据,定性资料以例数和百分数进行统计描述,以χ2检验分析差异性;定量资料以()进行统计描述,以t检验分析差异性,P < 0.05为差异有统计学意义。
2 结果
2.1 患者一般情况
154例接受万古霉素血药谷浓度监测的患者中,年龄最小2岁,最大94岁,平均年龄(61.33 ± 21.58)岁。其中,大于60岁者63人,占40.91%。疗效评价痊愈9.74%(15/154)、显效34.42%(53/154)、进步42.21%(65/154),总有效率86.36%(133/154)。原患疾病合计151种,其中呼吸系统76例、循环系统36例、泌尿系统18例、内分泌系统26例、神经系统44例、其他系统12例。相关的不良反应报告4例,分别为肝功能异常1例、皮疹3例。男性患者监测人次及例次均多于女性患者,采用样本均数的独立样本t检验,t = 1.733,P = 0.084(P > 0.05),显示其平均血药浓度差异无统计学意义。详见表1。

表1 患者性别分布Tab 1 Gender distribution of the patients
2.2 不同年龄段的谷浓度分布
对154例患者按照不同年龄段分组计算,各组的平均血药谷浓度监测值相近,未呈现随年龄段增大而递增的趋势。对3个年龄组4个血药浓度谷值范围的分布采用双向有序卡方检验,χ2= 4.391,v = 6,P = 0.624,显示各年龄组血药浓度分布差异无统计学意义(P > 0.05)。详见表2。

表2 不同年龄组患者万古霉素血药浓度谷值分布Tab 2 Distribution of the vancomycin trough concentrations in patients with different age groups
2.3 血药浓度谷值分布
将664次谷浓度监测数据参考相关资料[1-2],分为4级进行统计;鉴于有些患者为调整用药进行了多次监测,对所有患者的首次监测结果分布情况也进行了统计。各范围总体分布与首次分布对比采用单向有序卡方检验,χ2= 10.319,v = 3,P = 0.016(P < 0.05),结果显示差异有统计学意义。详见表3。

表3 万古霉素血药浓度谷值分布情况Tab 3 Distribution of trough concentration about vancomycin in plasma
2.4 肾功能不全患者的谷浓度监测数据
154例患者的谷浓度监测平均4.31次,最少1次,最多22次。其中,肾功能正常患者140例,谷浓度监测570例次,平均4.02次,用药调整93例(66.43%);肾功能不全患者14例,谷浓度监测94例次,平均6.64次,用药调整10例(71.43%)。肾功能不全患者的用药调整比例、平均监测例次均高于肾功能正常患者。将两组监测值分布数据采用单向有序卡方检验,χ2= 17.54,v = 3,P = 0.001 6(P < 0.05),结果显示差异有统计学意义。详见表4。
3 讨论
3.1 万古霉素血药浓度监测的必要性
近年来,围绕万古霉素血药浓度监测的探讨[4-5]以及对其峰浓度监测意义的质疑[6],使得目前临床更倾向于开展谷浓度监测。对于肾功能不全、老年、儿童、合并使用其他具有肾毒性药物的患者,因其具有加重万古霉素不良反应的风险因素[7-8],常列为需要实施血药浓度监测的特殊人群[9]。本调查中154例患者大多具备上述高风险因素,年龄在60岁以上者63例,12岁以下4例,肾功能不全者14例,联用肾毒性药物51例,合并糖尿病12例,合并高血压8例,合并心脑血管疾病18例;表明临床医师对特殊人群在治疗中需要开展个体化监测用药有正确认识。统计结果虽未发现性别及年龄在谷浓度范围分布的差异,但表3数据显示,首次监测值低于、高于有效浓度范围分别占44.16%(68/154)和19.48%(30/154),均显著高于总体分布的33.58%(223/664)和17.02%(113/664)。说明实施血药浓度监测,有助于及时调整万古霉素剂量,尽快达到有效浓度范围。
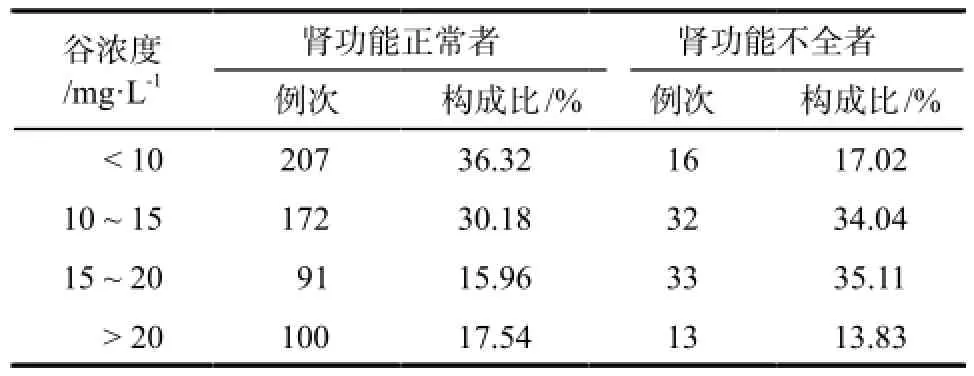
表4 肾功能正常与肾功能不全患者万古霉素谷浓度范围分布Tab 4 Distribution of the trough concentrations about vancomycin in patients with or without normal renal function
3.2 万古霉素血药浓度监测可规避不良反应的发生
154例患者中相关药品不良反应报告仅有4例,分别为肝功能异常1例、皮疹3例,不良反应发生率为2.60%(4/154),无肾功能不全的药品不良反应。调查显示,肾功能不全患者的监测例次及用药调整比例均高于肾功能正常患者,说明医师在万古霉素治疗中关注患者的肾功能,注意调整用药剂量,在达到有效治疗目的同时规避不良反应发生。表4中肾功能不全患者监测数据落在有效谷浓度范围内的比例明显高于肾功能正常患者,也说明了这一点。
3.3 万古霉素谷浓度监测的意义
指南[2]指出,万古霉素血药谷浓度< 10 mg·L-1可能产生对万古霉素中介的金黄色葡萄球菌(VISA)菌株,推荐血药浓度应 > 10 mg·L-1以避免耐药性产生。《中国药典·临床用药须知》(2010年版)的万古霉素血药浓度治疗窗也规定为 > 10 mg·L-1。表3中低于此参考范围达33.58%(223/664),可能与早期谷浓度范围标准5 ~ 10 mg·L-1[10]导致的较小剂量用药习惯有关;提示临床药师应在提供准确及时的治疗药物监测结果的同时,针对性宣传、深化药学服务。选用万古霉素时应根据患者实际体质量计算初始剂量,根据血药浓度调整剂量,在血药浓度达稳态后进行监测,同时规范标本留取与采血时间[11]。
3.4 万古霉素有效浓度监测可提高临床疗效
指南[2]提出,为增加达到最佳血药浓度的可能性,改善复杂感染的临床预后,推荐万古霉素有效目标浓度为15 ~ 20 mg·L-1。本研究中有18.68%(124/664)的患者血药浓度谷值在此范围。有效目标浓度是根据具体病情和药物治疗的目标效应,为具体患者设定的血药浓度目标值[12]。有证据表明,高浓度虽然不能缩短患者的住院时间,却可以提高万古霉素在组织间的渗透及减少细菌耐药的产生[13];因此,复杂感染的患者必要时可突破有效浓度范围的上限。由于国内目前关于万古霉素血药浓度谷值15 ~ 20 mg·L-1的安全资料有限,是否调整有效浓度范围上限还需大样本的深入研究[5,14]。而对于谷浓度范围 > 20 mg·L-1的患者,临床应用中应及时减量,避免血药浓度过高导致的不良反应[15]。
综上,具有应用万古霉素高风险因素的人群应借助血药浓度监测,实施临床药疗方案的个体化调整、维持有效血药浓度、减少用药风险与耐药菌产生。与有效浓度范围相比,根据患者病情和药疗目标制定的有效目标浓度更适合个体化用药需求。因此,对于复杂感染的患者,可在加强监测的同时突破目前有效浓度范围的上限。
[1]国家药典委员会.中华人民共和国药典·临床用药须知(化学药和生物制品卷)[M].2010年版.北京:中国医药科技出版社,2011:136.
[2]刘小丽,黄勋,译.美国感染病学会、美国药师学会、感染病药师学会共同推荐的万古霉素治疗指南[J].中国感染控制杂志,2009,8(5):373-374.
[3]中华人民共和国卫生部药政局.抗菌药物临床应用指导原则[S]. 1993.
[4]刘治军,胡欣.万古霉素治疗药物监测和临床应用相关指南解读[J].药品评价,2011,8(8):18-22.
[5]Karam CM, McKinnon PS, Neuhauser MM, et al. Outcome assessment of minimizing vancomycin monitoring and dosing adjustments[J]. Pharmacotherapy, 1999, 19(3): 257-266.
[6]Rybak MJ. The pharmacokinetic and pharmacodynamic properties of vancomycin[J]. Clin Infect Dis, 2006, 42(Suppl 1): S35-S39.
[7]陈佰义,管向东,何礼贤,等.万古霉素临床应用中国专家共识(2011版)[J].中国新药与临床杂志,2011,30(8):561-573.
[8]Rybak M, Lomaestro B, Rotschafer JC, et al. Therapeutic monitoring of vancomycin in adult patients: a consensus review of the American Society of Health-System Pharmacists, the Infectious Diseases Society of America, and the Society of Infectious Diseases Pharmacists[J]. Am J Health Syst Pharm, 2009, 66(1): 82-98.
[9]Lee P, DiPersio D, Jerome RN, et al. Approaching andanalyzing a large literature on vancomycin monitoring and pharmacokinetics[J]. J Med Libr Assoc, 2007, 95(4): 374-380.
[10]国家药典委员会.中华人民共和国药典·临床用药须知(化学药和生物制品卷)[M]. 2005年版.北京:人民卫生出版社,2005:547.
[11]张弨,翟所迪.万古霉素个体化用药的方法学评价[J].药学服务与研究,2008,8(5):381-384.
[12]朱曼,郭代红,石莉,等.2000~2004年我院4种抗癫痫药物血药浓度监测结果分析[J].药物流行病学杂志,2005,14(4): 223-225.
[13]Hermsen ED, Hanson M, Sankaranarayanan J, et al. Clinical outcomes and nephrotoxicity associated with vancomycin trough concentrations during treatment of deep-seated infections[J]. Expert Opin Drug Saf, 2010, 9(1): 9-14.
[14]陈超,郭代红,季晓英,等.重组人血小板的临床应用综合评价[J].中国药物应用与监测,2011,8(1):5-8.
[15]蒙龙,方芸,丁选胜.低谷浓度和高谷浓度万古霉素疗效与安全性比较[J].药学与临床研究,2013,21(1):74-77.
Therapy drug monitoring analysis on 664 cases of vancomycin in 154 patients
HUANG Chun-yan, GUO Dai-hong, ZHU Man(Department of Pharmaceutical Care, PLA General Hospital, Beijing 100853, China)
Objective:To guide clinical rational drug use by analyzing effective range of the trough concentration of vancomycin.Methods:A retrospective analysis was carried out to analyze the distribution of vancomycin trough concentrations of 154 patients (664 cases) in PLA General Hospital from January 2011 to December 2012.Results:The average trough concentration of vancomycin was (14.18 ± 9.28) mg·L-1. A total of 204 cases (30.72%, 204/664) were in the effective range of the blood concentration. The trough concentrations in 124 cases (18.68%, 124/664) exceeded the upper limit of the effective range but had the target blood concentration according to the recommended standard of the Infectious Diseases Society of America (IDSA). The monitoring cases and the ratio of dosage adjustment of the patients with renal insuf fi ciency were higher than that of the patients with normal renal function.Conclusion:Considering the needs of personalized medication, the dosage of vancomycin should be adjusted according to the target blood concentration. The concentrations of vancomycin in patients with complicated infection could exceed the upper limit of the current effective range if necessary.
Vancomycin; Therapy drug monitoring; Trough concentration; Target blood concentration
R978.1
A
1672 – 8157(2014)02 – 0068 – 04
2013-10-09
2014-01-03)
卫生部行业基金老年专项课题(201002011)
郭代红,女,主任药师,研究生导师,主要从事临床药学与药事管理工作。E-mail:guodh301@163.com
黄春燕,女,主管药师,在职硕士研究生,主要从事临床药学工作。E-mail:15010939441@163.com

