壳聚糖-纳米零价铁球去除水中二价镉的研究
颜小星 ,柳听义 ,王中良
(天津师范大学a.天津市水资源与水环境重点实验室,b.城市与环境科学学院,天津300387)
矿石开采、金属冶炼、制革厂和电镀厂会产生大量的工业废水,若这些含有大量重金属的工业废水未经处理直接排入水体,会造成严重污染[1-2].重金属具有较高的迁移性和毒性,在水体中不易被生物降解,具有生物富集和生物放大效应[2].镉相比其他重金属更容易被蔬菜和粮食作物吸收,并随着食物链进入人体内,主要积聚于肝和肾,对骨头、呼吸系统和心血管系统造成危害,具有致癌性[2-5].因此,国际癌症研究署把镉归类为第一类人类致癌物[6].水体重金属污染已成为关系到人类健康和生存的重大环境问题[2,7].
近年来,利用纳米零价铁(nanoscale zero-valent iron,NZVI)去除污染物作为一种新的污染控制技术已引起广泛关注.NZVI具有粒径小、比表面积大、反应活性高以及吸附性与还原性强等特性,对重金属离子有很强的净化能力[8-14].但NZVI颗粒容易团聚,造成比表面积减小、反应活性降低,且NZVI在空气中极易被氧化甚至自燃[15],这些问题限制了NZVI的应用.壳聚糖(chitosan,CS)是甲壳素脱去乙酰基后得到的一种直链大分子生物多糖,是一种低毒、可以降解、具有良好生物相容性的天然聚合物[16],其大分子链上分布着氨基和羟基,对重金属具有良好的吸附性,且CS具有网状结构,成球后能形成孔道结构,有利于物质的交换[16-18].利用壳聚糖表面改性纳米铁,可以有效防止NZVI颗粒团聚和氧化[19].目前,将NZVI负载在壳聚糖球内去除水相中的重金属Cd(II)还没有系统的研究.本研究以壳聚糖为载体,制备出壳聚糖-纳米零价铁(chitosan nanoscale zero-valent iron,CS-NZVI)球,用以去除水中的Cd(Ⅱ),考察Cd(Ⅱ)初始质量浓度、pH值、反应温度和NZVI投加量对去除效果的影响,探讨了CS-NZVI球去除Cd(Ⅱ)的规律和机理.
1 实验部分
1.1 CS-NZVI球的制备
在58℃条件下,将2.0g壳聚糖溶解于100mL体积分数为1%的醋酸中,持续搅拌4h后停止加热.缓慢冷却至27℃时加入NZVI(纳米零价铁购自南京埃普瑞纳米材料有限公司,纯度为95%),继续搅拌20min使NZVI颗粒均匀分散在CS和醋酸的混合液中.利用注射器将上述溶液逐滴滴加到浓度为2.0mol/L脱氧的NaOH溶液中,会立刻形成CS-NZVI球.将CS-NZVI球继续保存在NaOH中24h后,用脱氧去离子水冲洗3~4次,并将其保存在脱氧去离子水中备用.以上过程均在高纯氮气保护下完成.
1.2 Cd(Ⅱ)溶液的配制
将一定量的CdCl2·2.5H2O加入去离子水中,配制Cd(Ⅱ)质量浓度分别为20、50、100和200mg/L的溶液.
1.3 去除水中Cd(Ⅱ)的间歇实验
取一定初始质量浓度的Cd(Ⅱ)溶液100mL于聚乙烯瓶中,通过滴加稀HCl和稀NaOH调节pH值,投加CS-NZVI球后置于水浴恒温振荡器中,调节反应温度,转速为160r/min.每隔10min取样,经0.22μm针头滤膜过滤后进行仪器分析测试.根据实验设计,在保持其他反应条件不变的情况下,改变其中一个条件,进行批实验,具体实验参数如表1所示.

表1 批实验参数Tab.1 Parameters of batch test
1.4 表征
利用Nova Nano SEM 230型带能谱仪的扫描电镜(SEM/EDS)对CS-NZVI球的粒度和形貌进行观察,并对其内部Fe元素的分布进行分析.利用Tecnai G2F20型透射电镜(TEM)对NZVI的粒径和形貌进行观察.利用TAS-990型原子吸收分光光度计(AAS)测量Cd(II)的质量浓度.利用PHI1600型X线光电子能谱(XPS)对CS-NZVI球表面元素组成和各元素的化学结合能态进行分析.
2 结果与讨论
2.1 CS-NZVI球的表征
CS-NZVI球的表征结果如图1所示.

图1 表征照片Fig.1 Results of characterization
图 1(a)为制备所得的 CS-NZVI球,由图 1(a)可以看出,所有CS-NZVI球规则均一,均为直径约3.1mm的黑色球体.由CS-NZVI球的SEM照片(图1(b))可知,CS-NZVI球内部呈多孔结构,孔径大小不均,为9.5~102.8μm,平均孔径为40.6μm,与Guo等[20]的CS微球的孔径4.9~15.8μm相比,孔径较大,有利于NZVI与Cd(Ⅱ)的传质过程以及反应的进行.同时,利用SEM/EDS对其内部Fe元素的分布进行分析可知,Fe元素均匀分布,说明NZVI颗粒均匀地分布在 CS-NZVI球内,如图 1(c)所示.图 1(d)为 NZVI的TEM照片,由图1(d)可以看出,NZVI的平均粒径为21.6nm,由于具有磁性,NZVI呈链状.可见,本研究制备出的CS-NZVI球有效地解决了NZVI的团聚问题.
2.2 CS-NZVI球去除水中Cd(Ⅱ)的机理分析
图2为与Cd(II)溶液反应前以及反应后的CSNZVI球的 XPS 图谱.通过对比图 2(a)和图 2(b)可以发现,处理Cd(Ⅱ)溶液后图2(b)中出现了1个新的特征峰,即镉的特征峰,这说明污水中的Cd(Ⅱ)已经从水中分离出来吸附在CS-NZVI球上.
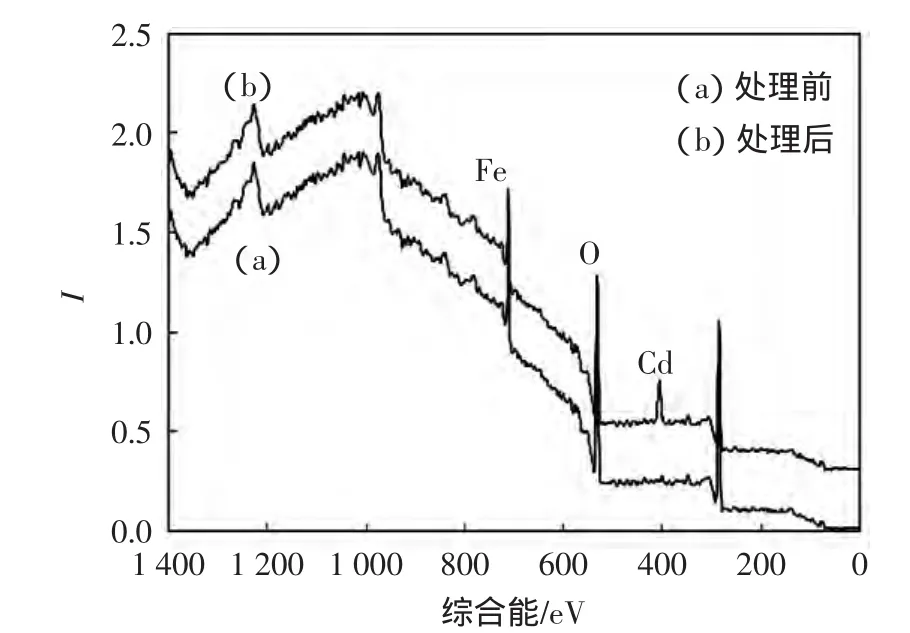
图2 CS-NZVI球处理Cd(Ⅱ)溶液前后的XPS图谱Fig.2 XPS survey for CS-NZVI beads before and after reacting with Cd(Ⅱ)
图3给出了CS-NZVI球处理Cd(Ⅱ)溶液后,Fe2p和 Cd3d5/2的 XPS详细图谱.在图 3(a)中,Fe2p3/2和Fe2p1/2的电子结合能谱峰分别出现在711.6eV和725.8eV处,这表明样品上主要是Fe(Ⅲ),几乎没有Fe(0)存在,说明NZVI几乎完全被氧化为Fe(Ⅲ)[21].图3(b)中Cd3d5/2出现了404.6eV和405.8eV2个谱峰,这表明样品上的镉为Cd(0)和Cd(Ⅱ).大量研究表明,CS表面暴露有大量的氨基和羟基,是重金属离子的主要吸附活性位点[21-25],对Cd(Ⅱ)有吸附能力.这说明Cd(Ⅱ)可以富集在CS-NZVI球表面和内部,而CS-NZVI的多孔隙大孔径结构有利于Cd(Ⅱ)与NZVI接触反应,使 Cd(Ⅱ)被还原为 Cd(0).但是 Li等[26]认为,利用纳米零价铁去除水中Cd(Ⅱ)的机理是水中的Cd(Ⅱ)由于静电相互作用和表面胶合作用等被富集在了铁的表面.本研究中,通过图3(b)可以看到Cd(0)的特征峰比Cd(Ⅱ)的特征峰强度大,说明CS-NZVI球去除水中Cd(Ⅱ)时,化学还原过程起了主要作用.
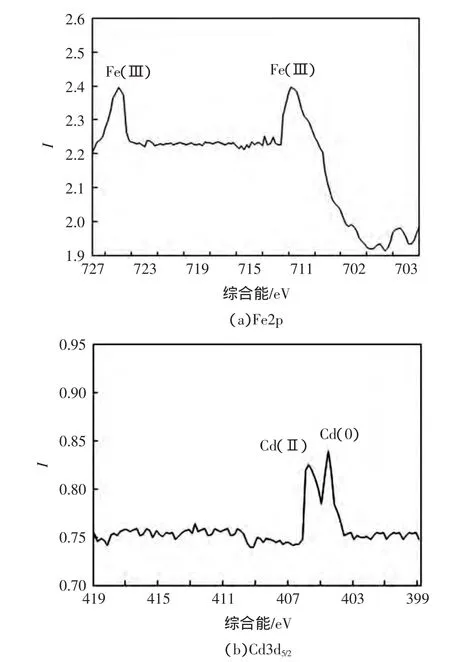
图3 CS-NZVI球的窄轨道XPS图谱Fig.3 High-resolution XPS survey of CS-NZVI bead
2.3 CS-NZVI球去除水中Cd(Ⅱ)的影响因素
随着Cd(Ⅱ)初始质量浓度的升高,CS-NZVI球对Cd(Ⅱ)的去除率逐渐降低,如图4所示.
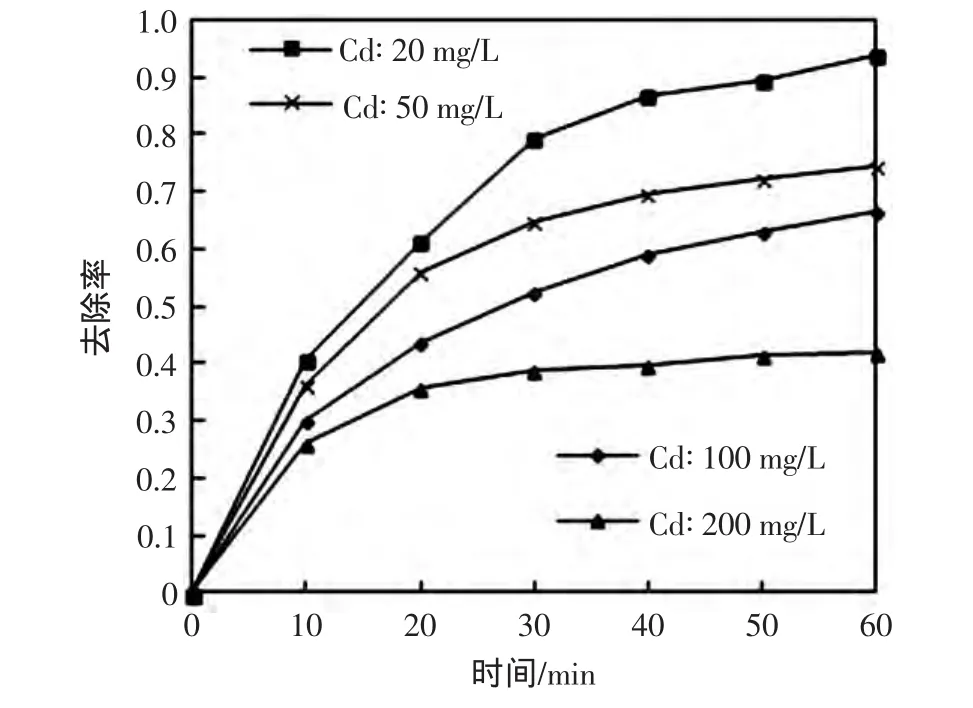
图4 Cd(II)初始质量浓度对 Cd(II)去除率的影响Fig.4 Effect of initial mass concentration on the removal rate of Cd(II)
NZVI的投加量是一定的,则其总的有效吸附面积和反应活性位点是一定的[27],随着Cd(Ⅱ)浓度的升高,部分吸附面积与反应位点被占用而使得有效的反应位点逐渐减少,Cd(Ⅱ)的去除率逐渐降低.
图5为反应体系pH值对Cd(Ⅱ)去除率的影响,从图5可以看出,pH值越高,CS-NZVI球对Cd(Ⅱ)的去除率越高,当pH=9,将CS-NZVI球加入Cd(Ⅱ)溶液1h时,去除率达到了100%.当pH值较低时,具有较强吸附位竞争力的H+浓度较高,且CS-NZVI球表面的氨基更易氨基化而带上正电荷[21],不利于Cd(Ⅱ)被吸附.当pH值较高时,有利于重金属离子的水解,其水解产物的亲和力比重金属离子的大,有利于镉离子的去除[28-29].
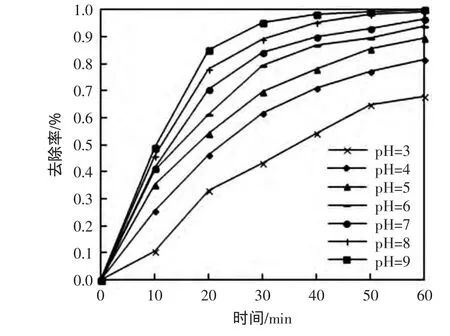
图5 pH值对Cd(Ⅱ)去除率的影响Fig.5 Effect of pH on the removal rate of Cd(Ⅱ)
图6为反应温度对Cd(Ⅱ)去除率的影响,由图6可知,随着反应温度的升高,CS-NZVI球对Cd(Ⅱ)的去除率逐渐升高.温度升高,镉离子的振动速率增加,提高了CS-NZVI球与Cd(Ⅱ)的冲撞频率[30],有利于更多的Cd(Ⅱ)进入CS-NZVI球的内部,且温度升高有利于增强电子的活动和转移[31],使得一部分Cd(Ⅱ)迅速转化为 Cd(0).
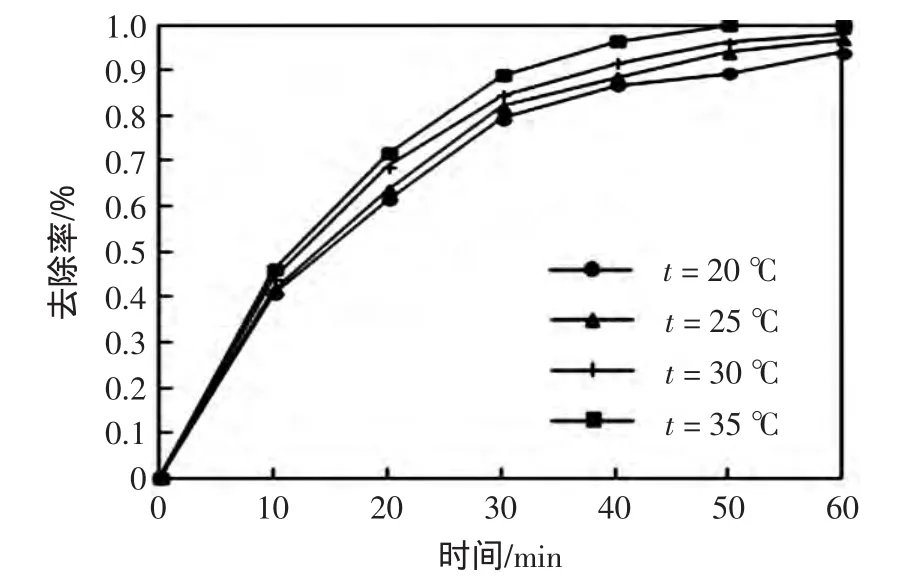
图6 反应温度对Cd(Ⅱ)去除率的影响Fig.6 Effect of reaction temperature on the removal rate of Cd(Ⅱ)
图7为NZVI投加量对Cd(Ⅱ)去除率的影响.随着NZVI投加量的增大,CS-NZVI对Cd(Ⅱ)的去除率逐渐升高.这是由于随着NZVI投加量的增加,有效吸附面积和反应活性位点增加[27],Cd(Ⅱ)的去除率也随之增大.
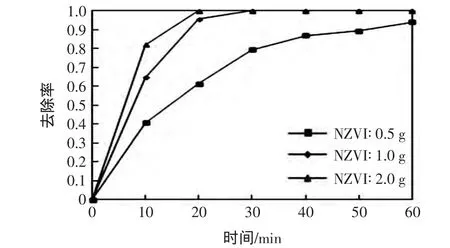
图7 NZVI投加量对Cd(Ⅱ)去除率的影响Fig.7 Effect of NZVI dosage on the removal rate of Cd(Ⅱ)
3 结论
利用壳聚糖负载纳米零价铁制备CS-NZVI球,所得CS-NZVI球为规则均一的黑色球体,具有多孔结构,平均孔径为40.6μm,这种多孔结构有利于NZVI与Cd(Ⅱ)的传质过程与反应的进行.NZVI均匀分散在CS-NZVI球内,说明CS载体可以有效防止NZVI颗粒的团聚.CS-NZVI球去除 Cd(Ⅱ)的机理为 Cd(II)被吸附在CS-NZVI球表面和内部,其中大部分Cd(Ⅱ)被NZVI还原为Cd(0),反应过程中化学还原过程起主要作用.
pH值对Cd(Ⅱ)的去除效果影响显著,pH较高时,CS-NZVI球对Cd(Ⅱ)的去除率较高;随着温度和NZVI投加量的增加,CS-NZVI球对Cd(Ⅱ)的去除率逐渐升高;但随着Cd(Ⅱ)初始质量浓度的提高,CSNZVI球对Cd(Ⅱ)的去除率逐渐降低.故在利用CSNZVI球处理被镉污染的水体时,可以通过适当提高污水pH值、温度以及增加NZVI投加量,提高对Cd(Ⅱ)的去除效率.
[1]许秀琴,朱勇,杨挺,等.水体重金属的污染危害及其修复技术[J].污染防治技术,2007,20(4):67-69.
[2] 朱映川,刘雯,周遗品,等.水体重金属污染现状及其治理方法研究进展[J].广东农业科学,2008,221(8):143-146.
[3]杨延军,刘建.浅谈水污染对人体健康的影响与危害[J].吉林水利,2003,255(11):37-40.
[4]任继平,李德发,张丽英.镉毒性研究进展[J].动物营养学报,2003,15(1):1-6.
[5]何孟常.水体沉积物重金属生物有效性及评价方法[J].环境科学进展,1998,6(5):9-19.
[6]陈永厚,蒙宽宏,刘际洲.水体中常见重金属污染物及其检测方法和排放标准[J].黑龙江生态工程职业学院学报,2008,104(4):5-6.
[7] 魏筱红,魏泽义.镉的毒性及其危害[J].公共卫生与预防医学,2007,18(4):44-46.
[8]PONDER S M,DARAB J G,MALLOUK T E.Remediation of Cr(VI)and Pb(II)aqueous solutions using supported,nanoscale zero-valentiron[J].Environmental Science and Technology,2000,34(12):2564-2569.
[9]LEWIS R D,CONDOOR S,BATEK J,et al.Removal of lead contaminated dusts from hard surfaces[J].Environmental Science and Technology,2006,40(2):590-594.
[10]KANEL S R,GRENECHE J M,CHOI H.Arsenic(V)removal from groundwater using nanoscale zero-valent iron as a colloidal reactive barrier material[J].Environmental Science and Technology,2006,40(6):2045-2050.
[11]LIU Q,BEI Y,ZHOU F.Removal of lead(II)from aqueous solution with amino-functionalized nanoscale zero-valent iron[J].Central European Journal of Chemistry,2009,7(1):79-82.
[12]CAO J,ZHANG W X.Stabilization of chromium ore processing residue(COPR)with nanoscale iron particles[J].Journal of Hazardous Materials,2006,132(2):213-219.
[13]张玉荣,吴杰,朱慧杰,等.纳米铁负载材料应用研究[J].河南城建学院学报,2012,21(1):35-39.
[14]柳听义,赵林,谭欣,等.纳米零价铁去除垃圾渗滤液中铬(Ⅵ)的性能及机理研究[J].环境化学,2010,29(03):429-433.
[15]KRAJANGPAN S,JARABEK L,JEPPERSON J,et al.Polymer modified iron nanoparticles for environmental remediation[J].Polymer Preprint,2008,49:921-922.
[16]高巍.甲壳质及壳聚糖在农业上的应用[J].农业与技术,2005,25(5):84-85.
[17]杨越冬.甲壳质/壳聚糖特性及其在农业中的应用[J].河北农业技术师范学院学报,1998,12(4):55-59.
[18]KRAJEWSKA B.Membrane-based processes performed with use of chitin/chitosan materials[J].Separation and Purification Technology,2005,41(3):305-312.
[19]GENG B,JIN Z H,LI T L,et al.Kinetics of hexavalent chromium removal from water by chitosan-Fe0nanoparticles[J].Chemosphere,2009,75:825-830.
[20]GUO T,XIA Y,HAO G,et al.Adsorptive separation of hemoglobin by molecularly imprinted chitosan beads[J].Biomaterials,2004,25(27):5905-5912.
[21]BODDU V M,ABBURI K,TALBOTT J L,et al.Removal of hexavalent chromium from wastewater using a new composite chitosan biosorbent[J].Environmental Science&Technology,2003,37(19):4449-4456.
[22]唐兰模,符迈群,张萍.用壳聚糖除去溶液中微量铬(VI)的研究[J].化学世界,2001,42(2):59-62.
[23]张廷安,豆志河.壳聚糖絮凝剂处理废水中的Ag+[J].东北大学学报:自然科学版,2006,27(1):53-56.
[24]张廷安,豆志河.用壳聚糖脱除废水中的铜离子[J].东北大学学报:自然科学版,2006,27(2):203-205.
[25]孙昌梅,曲荣君,王春华,等.基于壳聚糖及其衍生物的金属离子吸附剂的研究进展[J].离子交换与吸附,2004,20(2):184-192.
[26]LI X Q,ZHANG W X.Sequestration of metal cations with zerovalent iron nanoparticles:a study with high resolution X-ray photoelectron spectroscopy(HR-XPS)[J].American Chemical Society,2007,111:6939-6946.
[27]MORGADA M E,LEVY I K,SALOMONE V,et al.Arsenic(V)removal with nanoparticulate zerovalent iron:effect of UV light and humic acids[J].Catalysis Today,2009,143(3):261-268.
[28]张会民,徐明岗,吕家珑,等.pH对土壤及其组分吸附和解吸镉的影响研究进展[J].农业环境科学学报,2005,(S1):320-324.
[29]陈永贵,叶为民,张可能.温度和pH对填埋场防渗帷幕吸附重金属离子的影响[J].上海环境科学,2008,27(4):152-155.
[30]CHUANG F W,LARSON R A,WESSMAN M S.Zero-valent iron-promoted dechlorination of polychlorinated biphenyls[J].Environmental Science&Technology,1995,29(9):2460-2463.
[31]BREED A,DEMPERS C,SEARBY G,et al.The effect of temperature on the continuous ferrous-iron oxidation kinetics of a predominantly Leptospirillum ferrooxidans culture[J].Biotechnology and Bioengineering,1999,65(1):44-53.

