液态乳中氯丙二醇脂肪酸酯的检测与污染水平初步调查
崔 霞,丁 颢,邹建宏,李 珊,苗 虹,,傅武胜,赵云峰,吴永宁
(1.国家食品安全风险评估中心 卫生部食品安全风险评估重点实验室,北京 100021;2.第二炮兵总医院,北京 100088;3.福建省疾病预防控制中心 福建省人兽共患病研究重点实验室,福建 福州 350001)
氯丙醇脂肪酸酯(氯丙醇酯)是近年来发现的一类新型食品污染物,其在食用油和含油脂食品中的污染水平较高[1-4]。其中最典型、污染水平最高的是3-氯-1,2-丙二醇脂肪酸(3-monochloropropane-1,2-diol,3-MCPD)酯[5]。3-MCPD酯在生物体内脂肪酶的作用下分解成3-MCPD[6]。鉴于3-MCPD是氯丙醇类污染物中最重要的代表性物质,具有生殖、肾脏和神经毒性以及潜在的致癌作用和致突变作用[7-10],因此,由氯丙醇脂肪酸酯引发的健康风险也越来越受到人们的关注[8-9]。2007年,德国风险评估机构对氯丙醇酯的风险评估结果引起了欧盟食品安全局和联合国粮农组织/世界卫生组织食品添加剂联合专家委员会的重视。欧盟食品安全局食物链污染物专家组评估和确认了德国的3-MCPD酯数据,并进一步开展3-MCPD酯健康影响的风险评估。2008年联合国粮农组织/世界卫生组织食品添加剂联合专家委员会将3-MCPD酯列为优先评价的化合物。由于2-氯-1,3-丙二醇脂肪酸(2-monochloropropane-1,3-diol,2-MCPD)的结构与3-MCPD极其相似,其毒性以及其可能引起的健康风险不容忽视,2-MCPD酯在食品中的污染也应该引起关注,因此,有必要对食品中的3-MCPD酯和2-MCPD酯进行同时测定。
目前,食品中氯丙醇酯检测多采用气相色谱质谱-(gas chromatography-mass spectrometry,GCMS)法及液相色谱-质谱(liquid chromatography-mass spectrometry,LC-MS)法,其他检测技术几乎未见报道。检测的食品基质以食用油脂最常见。LC-MS法直接测定氯丙醇酯本身,样品前处理过程相对简单[11-12],因此,LC-MS法只能局限于测定某个或某些氯丙醇酯,而不能测定氯丙醇酯总量,因此不适合用于膳食暴露研究。GC-MS测定是将样品中的与各种脂肪酸酸结合的氯丙醇酯转化为氯丙醇进行测定,以氯丙醇的含量表征氯丙醇酯的含量。基本过程为脂肪水解、净化、衍生和GC-MS测定。在脂肪水解方面,现多采用碱水解法[13-16],以七氟丁酰化试剂[17]和苯基硼酸(phenyl boric acid,PBA)[13,16]或丁基硼酸[14,18]为最常用的衍生化试剂。本研究在前期食用油脂检测的基础上,以液态乳为研究对象,对样品前处理技术进行优化,建立了同时测定液态乳中3-MCPD酯和2-MCPD酯的检测方法,并对30 份牛乳样品进行检测,结合我国居民人均牛乳消费量对牛乳中氯丙醇酯引起的健康风险进行评估,以期为保障人体健康提供技术支持。
1 材料与方法
1.1 材料与试剂
牛乳样品购自北京市的大型超市,共30 份。
3-MCPD标准品(纯度98%) 德国Aldrich公司;D5-3-MCPD(纯度99%) 德国Dr Ehrenstorfer公司;2-MCPD、D5-2-MCPD、3-MCPD棕榈酸酯和D5-3-MCPD棕榈酸酯(纯度均≥98%) 加拿大TRC公司;正己烷、乙酸乙酯(色谱纯) 美国J.T.Baker公司;冰乙酸(色谱纯) 美国Tedia公司;甲基叔丁基醚(分析纯)天津市光复精细化工研究所;七氟丁酰咪唑(hepta fl uoro butyrylimidazole,HFBI)(分析纯) 美国Pierce公司;甲醇钠(分析纯) 天津市福晨化学试剂厂;氯化钠(分析纯) 北京化工厂;无水硫酸钠(优级纯,经200 ℃烘烤8 h后使用) 天津市津科精细化工研究所;超纯水,电阻率为18.2 MΩ•cm,由美国Millipore公司超纯水器制备。
标准溶液配制:精确称取各标准品10 mg(精确至0.01 mg)置于10 mL 棕色容量瓶中,以乙酸乙酯为溶剂定容至刻度,分别制备质量浓度为1 000 mg/L的标准储备液,于-20 ℃冰箱保存。将标准储备液用正己烷稀释并定容,配制成10.0 mg/L的标准使用液。
1.2 仪器与设备
5975C型气相色谱仪、7890型质谱联用仪、HP-5MS石英毛细管柱(30 m×0.25 mm,0.25 µm)、ChemElutTM硅藻土小柱(4 g,10 mL) 美国Agilent公司;Milli-Q超纯水器 美国Millipore公司;G-560E涡旋混合器 美国Scientific Industries公司;NDO-400型电热恒温鼓风干燥箱 杭州汇尔仪器设备有限公司;N-EVAPTM 111型吹氮浓缩仪 美国Organomation Associates公司。
1.3 方法
1.3.1 样品水解与净化
准确称取2.0 g液态乳样品,加入10 mg/L的D5-3-MCPD棕榈酸酯内标使用液60 μL(相当于0.2 μg D5-3-MCPD),加入2 mL正己烷,并充分混匀。超声萃取20 min,9 000 r/min 离心5min,收集正己烷相,重复提取3 次,合并提取液。加入质量浓度为10 mg/L 的D5-2-MCPD内标使用液20 µL,氮吹浓缩至约500 μL。加入500 µL甲基叔丁基醚-乙酸乙酯(8∶2,V/V)和1 mL甲醇钠-甲醇溶液(0.25 mol/L),充分振荡,反应4 min时加入100 μL 冰乙酸,混匀,再加入3 mL 20%的氯化钠溶液和3 mL正己烷,涡旋振荡1 min,弃去上层溶液。以3 mL 正己烷重复萃取一次,将下层水相溶液倒入ChemElutTM硅藻土小柱中,静置10 min,加入15 mL乙酸乙酯洗脱,洗脱液氮吹至近干,用2 mL正己烷溶解残渣。
1.3.2 样品衍生
用气密针加入HFBI 40 μL,立即密塞,涡旋混合30 s,于70 ℃恒温箱中衍生20 min后,取出冷却至室温,加入20%的氯化钠溶液2 mL,涡旋混合30 s,转移上层有机相并加入0.3 g无水硫酸钠除水分后,经0.22 μm有机滤膜过滤于进样小瓶中,供GC-MS测定。
1.3.3 气相色谱条件
色谱柱:H P-5 M S毛细管柱(3 0 m×0.25 mm, 0.25 μm);进样口温度:250 ℃;程序升温:50 ℃保持1 min,以2 ℃/min的速率升至90 ℃,以40 ℃/min的速率升至250 ℃,保持5 min;载气:高纯氦;流速1.0 mL/min;进样体积:1 μL;不分流进样。
1.3.4 质谱条件
离子化方式为电子电离,能量70 eV;电子倍增器电压1 000 V;选择反应离子监测;离子源温度230 ℃;传输线温度280 ℃;四极杆温度150 ℃;溶剂延迟时间8 min。主要质谱参数见表1。
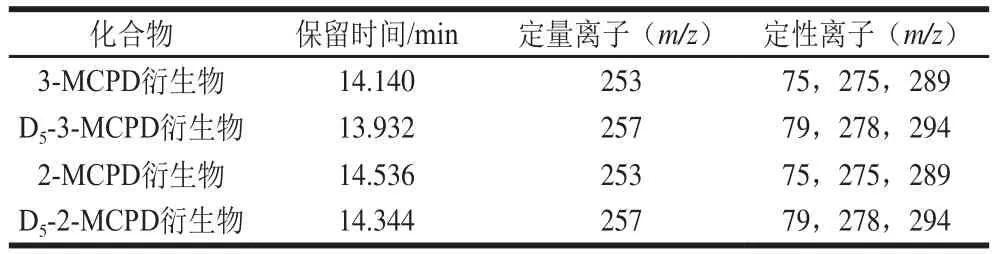
表1 目标化合物GC-MS保留时间及主要质谱参数Table 1 Main MS parameters and GC-MS retention time of target compounds
2 结果与分析
2.1 检测方法的确定
对于食品中氯丙醇酯的检测主要包括直接测定与间接测定两种方法。其中,直接测定法是直接测定一种或几种不同的氯丙醇酯[19-21],多以LC-MS法测定,作为进行暴露风险评估采用的方法,其缺陷为测定的是部分或大部分氯丙醇酯的含量,而不是总量,因此不能准确表征食品中氯丙醇酯的真实污染状况;间接测定法是通过酯键断裂反应使氯丙醇酯转化为氯丙醇进行测定,以氯丙醇的含量计氯丙醇酯的总量[2,20],其优点是可测定总氯丙醇酯的含量。本研究采用间接测定法,首先用正己烷将液态乳中的氯丙醇酯提取出来,以甲醇钠进行酯键断裂反应使氯丙醇从氯丙醇酯中游离出来,进行衍生化后以GC-MS测定,得到氯丙醇酯的总量。
2.2 提取方法的选择
氯丙醇酯是脂溶性物质,在植物油样品中可直接用甲醇钠进行酯键断裂反应使氯丙醇游离出来后衍生测定[14]。但液态乳样品由于水分以及蛋白质含量较高,基质更为复杂,需要先将氯丙醇酯提取出来,再进行后续处理。本研究分别采用加速溶剂萃取和以正己烷进行的液-液萃取两种方式进行了提取条件的摸索,空白加标回收实验表明,两种提取方法的差异不明显。鉴于加速溶剂萃取操作复杂繁琐,溶剂耗费量相对较大,最终确定采用以正己烷液-液萃取的方式进行提取。
2.3 酯键断裂反应参数的确定
已有文献[16-17]报道了植物油中氯丙醇酯检测过程中酯键断裂反应条件,但液态乳样品较植物油样品基质更为复杂,为避免由于样品差异对酯键断裂效果造成影响而导致检测结果出现偏差,本研究以牛乳样品为液态乳的代表性基质,对酯键断裂反应的参数进行了优化。目前测定氯丙醇酯多采用甲醇钠或硫酸甲醇溶液进行酯键断裂反应[16-17]。本实验中,使用甲醇钠进行酯键断裂反应,当配制浓度为0.5 mol/L甲醇钠的甲醇溶液时,有部分甲醇钠析出,并悬浮于溶液中,这样会导致每份样品提取液中的甲醇钠的量不一致,从而引起实验结果偏差。因此本研究将甲醇钠的浓度调整为0.25 mol/L,通过优化确定加入量为1.0 mL,保证了测定结果稳定可靠。
在酯键断裂时间方面,德国脂肪科学(deutsche gesellschaft für fettwissenschaft,DGF)方法的水解时间为10 min[14],有研究报道认为应控制在1 min左右,因酯键断裂时间延长会引起氯丙醇降解[16]。本研究分别设定水解时间为0.5、1.0、2.0、4.0、6.0、8.0 min,结果显示(图1),在4~6 min时,酯键断裂效果最佳。
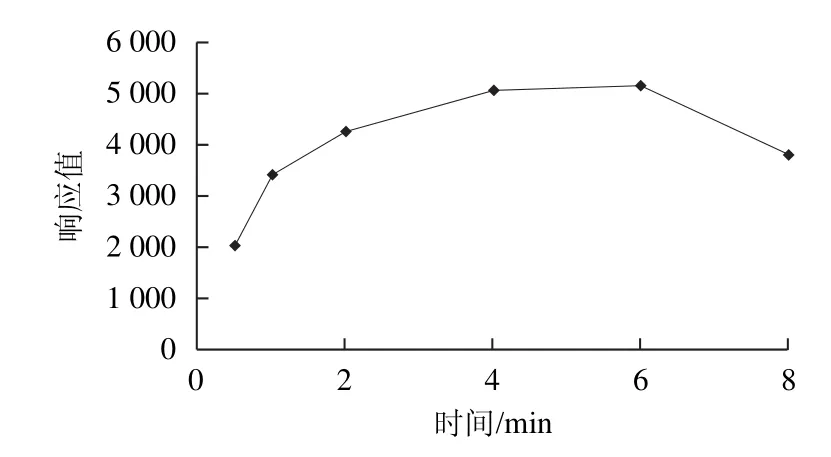
图1 酯键断裂时间对3-MCPD酯响应的影响Fig.1 Effect of transesterri fication time on response of 3-MCPD esters
2.4 方法学验证
由于在样品前处理过程中氯丙醇酯完全水解为氯丙醇进行后续测定,在计算氯丙醇酯的含量时分别以其对应的氯丙醇计。因此,系列标准工作溶液直接用3-MCPD和2-MCPD的混合标准溶液配制,用HFBI衍生后以GC-MS测定,记录化合物的色谱峰面积(A)(图2)和内标的色谱峰面积(Ai),以A和Ai的比值对相应的标准溶液中3-MCPD和2-MCPD的质量浓度进行线性回归计算,得出线性方程,线性范围和相关系数(r)。在5~500 μg/L范围内,3-MCPD和2-MCPD均呈良好线性相关,r大于0.999 5。
在空白样品中添加1、2、5、10 μg/kg四个水平的标准溶液,经样品前处理后上机测定的响应为基础,以信噪比为3的含量作为方法的检出限,以信噪比为10的含量作为方法的定量限。得到3-MPCD酯和2-MPCD酯检出限均为2.0 μg/kg,定量限均为5.0 μg/kg。
本实验选取3-MCPD棕榈酸酯作为代表物,进行3-MCPD酯的加标回收实验。由于暂未获得商品化的2-MCPD脂肪酸酯标准品,因此采用2-MCPD代替2-MCPD脂肪酸酯进行加标回收实验[17]。取空白牛乳样品分别做10、50、100 μg/kg和200 μg/kg水平的加标回收实验(表2),3-MCPD酯和2-MCPD酯的回收率分别为73.5%~102.6%和89.1%~106.6%,相对标准偏差分别为2.3%~6.0%和3.1%~7.7%。加标回收实验结果说明,方法的精密度和准确度良好。
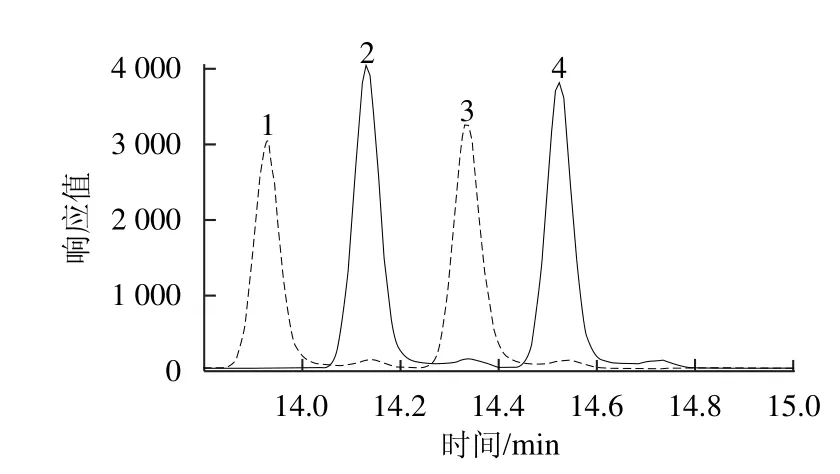
图2 3-MCPD和2-MCPD衍生物及其内标衍生物提取离子流图(50 μg/L)Fig.2 Extracted ion chromatograms (EIC) of derivatives of 3-MCPD,2-MCPD and internal standard (50 μg/L)
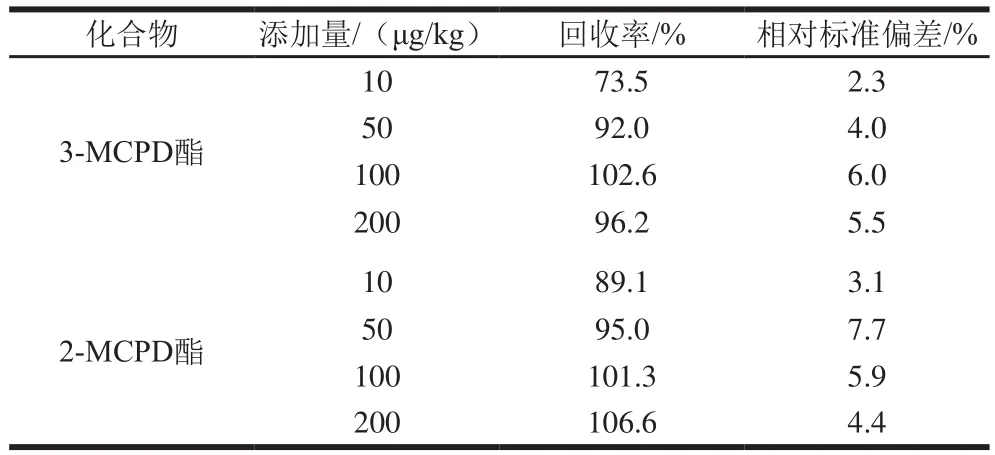
表2 牛乳样品氯丙醇酯的加标回收和精密度实验结果(n=6)Table 2 Recoveries and relative standard deviations (RSDs) of fatty acid esters of chloropropanediols in spiked milk (n=6)
通过前处理条件的优化,建立的方法准确可靠、灵敏度高,可同时测定两种在食品中污染最为广泛的单氯丙醇酯的总量,适用于液态乳中氯丙二醇脂肪酸酯总量的检测。与大部分报道的食品中氯丙醇酯的检测[3,22]相比,本方法的检测灵敏度更高,达到了2 μg/kg,这对于更准确地评估氯丙醇酯对人体的膳食暴露风险提供了强有力的技术支持。
2.5 牛乳中氯丙醇酯污染水平及其对人体的健康风险评估
在北京不同区域的超市和市场采集30 份牛乳样品,采用建立的检测方法进行测定。30 份牛乳样品中3-MCPD酯的检出率为95%,含量在未检出(not detected,ND)~13.8 μg/kg之间,平均值为4.3 μg/kg;2-MCPD酯的检出率为83.3%,含量在ND~10.3 μg/kg之间,平均值为3.6 μg/kg。由测定结果可见,牛乳中3-MCPD酯和2-MCPD酯的污染水平相对较低。
结合2002年中国居民营养与健康状况调查中我国标准人每日牛乳的平均消费量为21.09 g,以此估算北京地区人群3-MCPD酯的膳食暴露量,得到由于摄入牛乳而导致的3-MCPD酯的暴露量为0.001 4 μg/(kg•d),仅为3-MCPD最大耐受摄入量(provisional maximum tolerable daily intake,PMTDI)(2 μg/(kg•d))的0.07%。2-MCPD作为3-MCPD的同分异构体,虽目前暂无其毒性及健康指导值的文献报道,但作为3-MCPD的同分异构体,化学结构与3-MCPD相似,因此本研究将2-MCPD酯的含量与3-MCDP酯含量加和后进行了膳食暴露评估,结果显示,北京地区人群通过牛乳消费而摄入的3-MCPD酯与2-MCPD酯的总暴露量为0.002 6 μg/(kg•d),仅占PMTDI的0.13%。用于暴露评估的牛乳的消费量为2002年调查的数据,考虑到随着我国人民生活水平的提高,牛乳的消费量增大,若以10 倍于2012年消费量数据估算,北京地区人群对牛乳中的氯丙醇酯的膳食暴露量也只占3-MCPD的PMTDI的1.3%,健康风险仍较低。总体而言,由牛乳消费摄入3-MCPD酯和2-MCPD酯所带来的长期慢性暴露风险较低。由于牛乳只占人们每日膳食的很小一部分,且牛乳中氯丙醇酯含量较低,北京地区人群在每日膳食中还会摄入食用油等其他可能含有污染水平较高的氯丙醇酯的食品,因此氯丙醇酯的健康风险仍不容忽视。
3 结 论
本实验采用碱水解和固相支持液-液萃取净化等样品前处理技术,建立了气相色谱-质谱法测定牛乳中氯丙二醇脂肪酸酯含量的方法,此方法准确可靠、灵敏度高,可同时测定两种在食品中污染最为广泛的单氯丙醇酯的总量,适用于液态乳中氯丙二醇脂肪酸酯总量的检测。通过对北京市售牛乳样品进行氯丙醇酯的测定和膳食暴露评估,初步了解到牛乳中氯丙醇酯的污染水平较低,北京地区人群通过牛乳所摄入氯丙醇酯的健康风险较低。
[1]ZELINKOVA Z, DOLEZAL M, VELISEK J, et al.3-Chloropropane-1,2-diol fatty acid esters in potato products[J].Czech Journal of Food Sciences, 2009, 27: S421-S424.
[2]KUHLMANN J.Determination of bound 2,3-epoxy-1-propanol(glycidol) and bound monochloro-propanediol (MCPD) in refined oils[J].European Journal of Lipid Science and Technology, 2011,113(13): 335-344.
[3]SEEFELDER W, VARGA N, STUDER A, et al.al.Esters of 3-chloro-1,2-propanediol (3-MCPD) in vegetable oils: significance in the formation of 3-MCPD[J].Food Additives and Contaminants, 2008,25(4): 391-400.
[4]里南, 严小波, 方勤美, 等.我国市售食用植物油中氯丙醇酯的污染调查[J].中国粮油学报, 2013, 28(8): 28-35.
[5]Joint FAO/WHO Expert Committee on Food Additives (JECFA).Safety evaluation of certain food additives and contaminants prepared by the fifty-seventh meeting of the Joint FAO/WHO Expert Committee on Food Additives (JECFA)[R].Geneva: WHO Food Additives, 2002.
[6]HAMLET C G, SADD P A, GRAY D A.Generation of monochloropropanediols (MCPDs) in model dough systems.1.leavened doughs[J].Journal of Agricultural and Food Chemistry, 2004,52(7): 2059-2066.
[7]HWANG M, YOON E, kIM J, et al.Toxicity value for 3-monochloropropane-1,2-diol using a benchmark dose methodology[J].Regulatory Toxicology and Pharmacology, 2009,53(2): 102-106.
[8]Federal German Institute for Risk Assessment, Stellungnahme Nr.047/2007 des BfR vom 11, BfR, Berlin[R/OL].http://www.bfr.bund.de/cm/208/saeuglingsanfangs_und_folgenahrung_kann_gesundheitlich_bednkliche_3_mcpd_fettsaeureester_enthalten.pdf.
[9]Joint FAO/WHO Expert Committee on Food Additives (JECFA).Safety evaluation of certain food additives and contaminants/prepared by the sixty-seventh meeting of Joint FAO/WHO Expert Committee on Food Additives (JECFA)[R].Geneva: WHO Food Additives, 2007.
[10]kUSTERS M, BIMBER U, OSSENBRUGGEN A, et al.Rapid and simple micromethod for the simultaneous determination of 3-MCPD and 3-MCPD esters in different foodstuffs[J].Journal of Agricultural and Food Chemistry, 2010, 58(11): 6570-6577.
[11]HAINES T D, ADLAF K J, PIERCEALL R M, et al.Direct determination of MCPD fatty acid esters and glycidyl fatty acid esters in vegetable oils by LC-TOFMS[J].Journal of the American Oil Chemists’ Society, 2011, 88(1):1-4.
[12]YAMAZAKI K, OGISO M, ISAGAWA S, et al.A new, direct analytical method using LC-MSMS for fatty acid esters of 3-chloro-1,2-propanediol (3-MCPD esters) in edible oils[J].Food Additives and Contaminants, 2013, 30(1): 52-68.
[13]MARkUS k, UTE B.Rapid and simple micromethod for the simultaneous determination of 3-MCPD and 3-MCPD esters in different foodstuffs[J].Journal of Agricultural and Food Chemistry,2010, 58(11): 6570-6577.
[14]DGF Standard Method C-Ⅲ 18 (09) Tensiden und verwandten stoffen wissenschaftliche verlagsgesellschaft[S].
[15]NAOkI k, HIROFUMI S, HIROSHI Y.Bidirectional conversion between 3-monochloro-1,2-propanediol and glycidol in course of the procedure of DGF standard methods[J].Journal of the American Oil Chemists’ Society, 2011, 88(8): 1143-1151.
[16]傅武胜, 严小波, 吕华东, 等.气相色谱/质谱法测定植物油中脂肪酸氯丙醇酯[J].分析化学, 2012, 40(9): 1329-1335.
[17]LIU Q, HAN F, XIE k, et al.Simultaneous determination of total fatty acid esters of chloropropanols in edible oils by gas chromatographymass spectrometry with solid-supported liquid-liquid extraction[J].Journal of Chromatography, 2013, 1314(1): 208-215.
[18]VEJkOVSkA B, NOVOTNY O, DIVINOVA V, et al.Esters of 3-chloropropane-1,2-diol in foodstuffs[J].Czech Journal of Food Sciences, 2004, 22(5): 190-196.
[19]MASUkAWA Y, SHIRO H, NAkAMURA S, et al.A new analytical method for the quantification of glycidol fatty acid esters in edible oils[J].Journal of Oleo Science, 2010, 59(2): 81-88.
[20]HORI k, kORIYAMA N, OMORI H, et al.Simultaneous determination of 3-MCPD fatty acid esters and glycidol fatty acid esters in edible oils using liquid chromatography time-of- fl ight mass spectrometry[J].LWTFood Science and Technology, 2012, 48(2): 204-208.
[21]MORAVCOVA E, VACLAVIk L, LACINA O, et al.Novel approaches to analysis of 3-chloropropane-1,2-diol esters in vegetable oils[J].Analytical and Bioanalytical Chemistry, 2012, 402(9): 2871-2883.
[22]ZWLINkOVA Z, NOVOTNY O, SCHUREk J, et al.Occurrence of 3-MCPD fatty acid esters in human breast milk[J].Food Additives and Contaminants, 2008, 25(6): 669-676.

