慢性阻塞性肺疾病患者心脏复极离散度与肺功能的关系研究
李 峰,魏 龙,秦 勇
慢性阻塞性肺疾病(COPD)是由多种病因引起的以持续性、不完全可逆的气流受限为特征的肺部疾病,COPD患者呼吸系统功能和结构的改变会严重的影响心脏的结构和功能[1]。近来发现24%的COPD患者合并心血管疾病,患者的室性心律失常和心脏性猝死(SCD)发生率明显增加,这将直接增加患者的心血管死亡风险,因此早期识别和预防患者的心血管并发症具有十分重要的临床意义[2-3]。心脏复极离散如空间离散度(QTd)和短时程离散度(STVQT)是指心脏复极活动空间和时间的差异性,与心律失常的发生密切相关[4]。然而COPD是否影响心脏复极离散度,以及复极离散与肺功能的关系如何研究较少,因此本研究通过与健康人群比较,并进行相关性分析,试图探讨COPD患者心脏复极离散与肺功能之间的关系。
1 对象与方法
1.1 研究对象 纳入2012年1月—2013年6月在我院诊断为COPD的患者156例(COPD组),诊断符合中华医学会呼吸病学分会制定的《慢性阻塞性肺疾病诊治指南》[5],同时入选在我院行健康体检正常者64例(对照组),排除房颤、频发室性早搏和服用胺碘酮等影响心率和QT间期分析的病例,以及有低钠血症、低钾血症、急性呼吸衰竭和急性心力衰竭等病情不稳定的患者。

1.3 肺功能检测 在安静休息5 min后,由专科医生测定肺功能:通过用力肺活量(FVC)和第1秒末用力呼气量(FEV1)计算FEV1/FVC。FEV1/FVC<70%可确定为不能完全可逆的气道阻塞和气流受限;值越小,代表呼吸功能越差。
1.4 超声心动图检查 使用GE公司Vivid 7彩色多普勒超声显像仪,探头频率2.5 MHz。测量左室射血分数(LVEF)、左室内径(LVD)、左房内径(LAD)、右室内径(RVD)、右房内径(RAD)、肺动脉压(PAP),测量3个心动周期,取平均值。
1.5 呼吸困难指数评级 按照呼吸困难量表对入选病例进行呼吸困难指数评级。0级:除做剧烈活动外不会发生呼吸困难;1级:在平地上快步行走或者上坡时,感到呼吸困难;2:以比大多数人慢的速度行走于平地时呼吸困难,或者在停止行走15 min后依旧呼吸困难;3级:在平地上停止行走数分钟后依旧呼吸困难;4级:进行穿衣等非常轻微的活动时发生呼吸困难,并无法出门。

2 结果
2.1 一般资料比较 两组受检者年龄、性别等一般资料比较差异无统计学意义(P>0.05,见表1)。
2.2 心电图、心脏超声和肺功能比较 COPD组与对照组相比QTd和STVQT差异有统计学意义(P<0.01);LVD、LAD和RAD差异无统计学意义(P>0.05);LVEF、RVD、PAP相比差异均有统计学意义(P<0.01);FVC、FEV1、FEV1/FVC差异有统计学意义(P<0.01,见表1、2)。
2.3 复极离散度与肺功能相关性分析 在COPD患者中,心脏复极离散度与FEV1/FVC呈负相关:QTd(r=-0.52,P<0.01)和STVQT(r=-0.68,P<0.01),见图1。
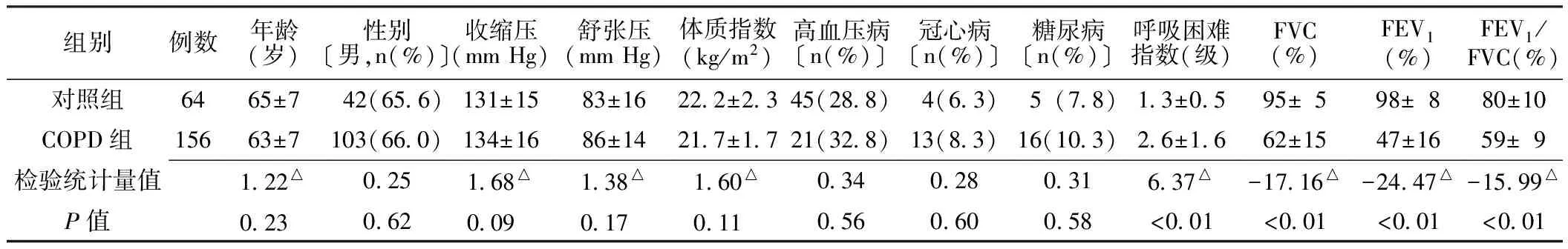
表1 两组一般资料和肺功能检测结果比较
注:△为t值,余检验统计量值为χ2值;FVC=用力肺活量;FEV1=第1秒末用力呼气量,COPD=慢性阻塞性肺疾病
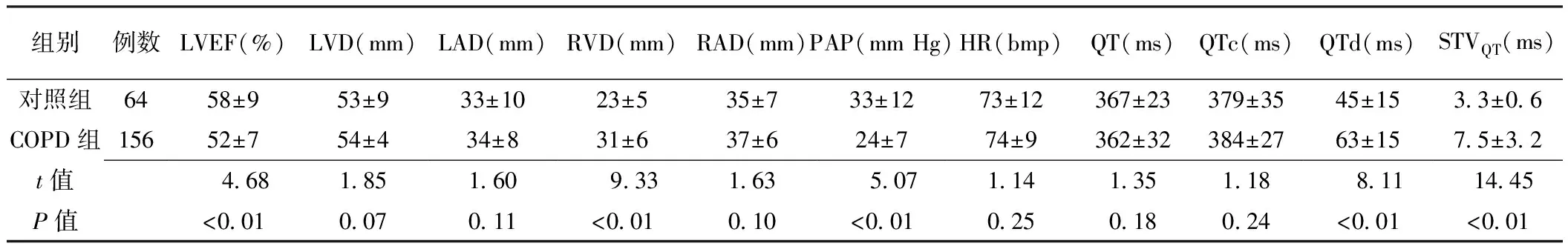
表2 两组心脏超声和心电图的结果比较
注:LVEF=左室射血分数,LVD=左室内径,LAD=左房内径,RVD=右室内径,RAD=右房内径,PAP=肺动脉压,HR=心率,QTc=校正QT间期,QTd=空间离散度,STVQT=短时程离散度

图1 COPD患者的心脏复极离散度与FEV1/FVC的散点图
Figure1 The correlation between the dispersion of cardiac repolarization and FEV1/FVC in COPD patients
3 讨论
心血管疾病是COPD患者的常见并发症,也是患者最主要的死亡原因,研究显示大约39%的COPD患者因心脏原因死亡,只有14%的死于呼吸衰竭[6]。其中心律失常在COPD患者中也十分常见,特别是室性心律失常引起的心脏性猝死,是患者心源性死亡的主要原因,因此研究COPD对患者心脏电生理的影响具有重要的临床意义[7]。本研究证实,COPD患者空间和时间复极离散度均大于对照组,并且复极离散度与FEV1/FVC呈负相关,提示COPD严重影响心脏电活动,并与病情程度相关。
心脏复极离散度指的是心脏各部位的心肌细胞复极空间和时间的变异程度,反映心脏电生理活动的差异性,QTd反映心脏的空间离散度,STVQT反映心脏的时间离散度[8]。因为正常心脏并不是一个合胞体,各部分的结构和功能、各种离子通道的分布和传导系统的路径均有一定的差异。一般心脏除极始于心内膜,而复极始于心外膜,有一定的时空顺序,也是正常心功能的重要保证。在心脏结构和功能改变时,心脏复极的正常顺序被打乱,为折返和触发活动提供了基质,是心律失常发生的重要原因[4]。
COPD导致心脏复极离散度增加可能与以下机制有关:(1)心脏结构改变:长期的肺部炎性反应使肺泡、毛细血管等发生重构,肺泡破坏,毛细血管床减少,引起继发性肺动脉高压,继而导致右心室前向压力增大,右心室心肌发生肥大[9]。本试验结果证实COPD患者的PAP和RVD均大于对照组,提示COPD患者的肺循环和右室已经发生了器质性改变。COPD患者长期处于低氧血症或高碳酸血症状态,由于全身炎性反应心血管系统也长期受累,在这种内环境异常和后向循环改变的影响下,左心室的功能也将受损[10],研究证实,COPD患者的左室的收缩和舒张功能均有显著下降,是患者发生心血管事件的重要原因,本试验结果显示COPD患者的LVD与对照组之间无差异,但是LVEF低于对照组,提示左室的收缩功能可能受损。(2)自主神经功能异常:COPD患者常常伴随着自主神经功能异常,交感神经兴奋性增加,使心率变异性下降和心率震荡增加,提示患者窦房结的适应能力下降[11];β受体激动剂是治疗COPD常规用药,然而在心脏结构和功能受损的情况下,β受体激动剂会加重心脏负担,增加心血管事件,研究也证实,长期使用β受体激动剂与COPD患者的心力衰竭、心律失常等发生密切相关[12]。因为COPD患者的左右心室和自主神经的上述改变,会使心脏电活动的顺序、时程发生改变,常常表现为复极活动异质性增大,复极时程和向量均会有所影响,本试验显示COPD的心脏空间复极离散度显著大于对照组,短时程的复极变异度也显著增加。
然而本试验也具有一定的局限性,首先本研究的样本量较小,未来研究需要扩大样本量,以进一步证实本试验的结果;其实,需要进行长期的前瞻性研究,随访室性心律失常、心脏性猝死和心源性死亡的情况,以研究引起心脏复极离散度和心血管事件增加的危险因素,以利于临床预防。最后,虽然本研究显示COPD的复极活动异常,但是具体的离子通道变化还未得到证实,这需要进一步的动物实验来验证。
1 van Gestel AJ,Kohler M,Clarenbach CF.Sympathetic overactivity and cardiovascular disease in patients with chronic obstructive pulmonary disease(COPD)[J].Discov Med,2012,14(79):359-368.
2 Vijayan VK.Chronic obstructive pulmonary disease[J].Indian J Med Res,2013,137(2):251-269.
3 Curkendall SM,DeLuise C,Jones JK,et al.Cardiovascular disease in patients with chronic obstructive pulmonary disease,Saskatchewan Canada cardiovascular disease in COPD patients[J].Ann Epidemiol,2006,16(1):63-70.
4 Antzelevitch C,Burashnikov A.Overview of basic mechanisms of cardiac arrhythmia[J].Card Electrophysiol Clin,2011,3(1):23-45.
5 中华医学会呼吸病学分会慢性阻塞性肺疾病学组.慢性阻塞性肺疾病诊治指南(2007年修订版)[J].中华内科杂志,2007,46(3):254-261.
6 文富强.重视慢性阻塞性肺疾病的合并症[J].中华肺部疾病杂志:电子版,2013,6(2):1-3.
7 Crisafulli E,Costi S,Luppi F,et al.Role of comorbidities in a cohort of patients with COPD undergoing pulmonary rehabilitation[J].Thorax,2008,63(6):487-492.
8 Varkevisser R,Wijers SC,van der Heyden MA,et al.Beat-to-beat variability of repolarization as a new biomarker for proarrhythmia in vivo[J].Heart Rhythm,2012,9(10):1718-1726.
9 Qaseem A,Wilt TJ,Weinberger SE,et al.Diagnosis and management of stable chronic obstructive pulmonary disease:A clinical practice guideline update from the American College of Physicians,American College of Chest Physicians,American Thoracic Society,and European Respiratory Society[J].Ann Intern Med,2011,155(3):179-191.
10 Hawkins NM,Virani S,Ceconi C.Heart failure and chronic obstructive pulmonary disease:The challenges facing physicians and health services[J].Eur Heart J,2013,34(36):2795-2807.
11 Dias DCT,Marcelo PC,Claudino RR,et al.Geometric index of heart rate variability in chronic obstructive pulmonary disease[J].Rev Port Pneumol,2011,17(6):260-265.
12 Matera MG,Martuscelli E,Cazzola M.Pharmacological modulation of beta-adrenoceptor function in patients with coexisting chronic obstructive pulmonary disease and chronic heart failure[J].Pulm Pharmacol Ther,2010,23(1):1-8.

