2型糖尿病患者中四种肾小球滤过率评估方法一致性的研究
程 莹,李宁娜,艾智华
肾小球滤过率(glomerular filtration rate,GFR)是评价肾脏功能的重要指标,目前临床上通常根据血肌酐(creatinine,Cr)、胱抑素C(cystain,Cys-C)或24 h内生肌酐清除率(endogenous creatinine clearance,CCr)估算GFR(estimated GFR,eGFR),由于24 h尿留取过程繁琐,常常计量不准确,影响结果的可信度。近年来,许多学者认为Cys-C是反映GFR理想的内源性标志物之一,根据Cys-C得到的eGFR应用逐渐广泛,其价值也得到了一些临床证据的支持[1]。本研究在2型糖尿病患者中对Cys-C计算的eGFR与其他几种传统方法检测结果的一致性进行了对比研究。
1 对象与方法
1.1 入选及排除标准 入选标准:符合2010年中华医学会糖尿病学分会《中国2型糖尿病防治指南》中的糖尿病诊断标准[2]:(1)糖尿病症状,且随机血糖≥11.1 mmol/L;(2)空腹血糖≥7.0 mmol/L;(3)75 g口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)葡萄糖负荷后2 h血糖≥11.1 mmol/L。排除标准:(1)糖尿病酮症酸中毒等糖尿病急性并发症;(2)妊娠、哺乳期妇女;(3)急性肾功能衰竭;(4)严重水肿;(5)使用利尿剂;(6)泌尿系梗阻;(7)膀胱不能排空;(8)严重感染;(9)心力衰竭;(10)恶性肿瘤。
1.2 研究对象 选取2013年2—11月在中国人民解放军成都军区总医院内分泌科住院的年龄≥18岁、符合入选及排除标准的2型糖尿病患者作为研究对象。
1.3 方法
1.3.1 检测指标及方法 记录患者的年龄、性别、身高、体质量(排空膀胱、粪便,去除外套、鞋帽)。禁食10 h后,清晨空腹安静状态下抽取肘静脉血检测血清清蛋白(Alb)、Cr、尿素氮(BUN)、Cys-C。留取24 h尿,记尿量,测定尿肌酐(UCr)水平。
1.3.2 eGFR计算方法 (1)eGFR1:通过测定Cys-C,根据如下公式计算:eGFR1=127.7×Cys-C-1.17×年龄-0.13×0.91(女)[3],公式中Cys-C(mg/L)、年龄(岁);(2)eGFR2:通过测定Cr、24 h尿量及UCr,根据如下公式计算:eGFR2=(UCr×24 h尿量)/(Cr×1 440)[4],公式中UCr(μmol/L)、24 h尿量(ml)、Cr(μmol/L);(3)eGFR3:应用Cockcroft-Gault方程[5]根据如下公式计算:eGFR3=〔(140-年龄)×体质量〕/(72×Cr)(女性则×0.85),公式中年龄(岁)、体质量(kg)、Cr(mg/dl);(4)eGFR4:应用MDRD方程[6]根据如下公式计算:eGFR4=170×Cr-0.999×年龄-0.176×(女×0.762)×BUN-0.170×Alb0.318,公式中Cr(mg/dl)、年龄(岁)、BUN(mg/dl)、Alb(g/dl)。Cr单位换算:1 μmol/L=88.4 mg/dl。
1.4 统计学方法 采用SPSS 18.0和MedCalc 12.3统计软件进行统计学分析,对eGFR1与其他3种方法获得的eGFR结果进行配对t检验、线性相关及回归分析,回归模型的统计学意义分析采用ANOVA方差分析。采用Bland-Altman作图法对3种eGFR测量方法与eGFR1结果的一致性进行评估,95%一致性界限宽度越大、差值均值回归线与0偏差线之间的距离越大代表一致性越差[7]。15%、30%和50%准确率分别表示其他3种方法计算获得的eGFR落在eGFR1±15%、eGFR1±30%和eGFR1±50%范围内的病例数。检验水准为α=0.05(双侧)。
2 结果
2.1 患者一般情况 根据入选及排除标准,共计81例患者入选,其中男49例(60.5%),女32例(39.5%);年龄18~87岁,中位数为61.0岁;体质指数为(24.79±4.18)kg/m2;糖化血红蛋白为(9.28±2.47)%;BUN为(5.93±2.62)mmol/L;Cr为(77.75±49.08)μmol/L;Cys-C为(0.99±0.44)mg/L;Alb为(40.97±4.77)g/L。
2.2 Cys-C估算法与24 h尿液测定法的比较 eGFR1和eGFR2的配对差均值为-13.45(P<0.05,见表1)。eGFR1和eGFR2的回归方程为Y=0.722X+40.915,Y轴截距不等于0,拟合优度数值低,见表2和图1。

表1 eGFR1与其他3种方法eGFR平均差值的配对t检验
注:eGFR=估算肾小球滤过率

表2 eGFR1与其他3种方法eGFR的线性回归分析

图1 eGFR1和eGFR2的趋势相关关系
Bland-Altman作图法示eGFR1和eGFR2的配对数据差值的均值为-14.7 ml·min-1·1.73 m-2,标准差(SD)=44.13 ml·min-1·1.73 m-2,95%一致性界限为(-101.2 ml·min-1·1.73 m-2,71.8 ml·min-1·1.73 m-2)。见图2。

图2 eGFR1和eGFR2的Bland-Altman分析图
2.3 Cys-C估算法与Cockcroft-Gault方程法的比较 eGFR1和eGFR3两种测量方法的配对差均值为0.86(P>0.05,见表1)。eGFR1和eGFR3的回归方程为Y=0.898X+8.596,Y轴截距接近0,拟合优度较高,见表2和图3。
Bland-Altman作图法示eGFR1和eGFR3的配对数据差值的均值为1.0 ml·min-1·1.73 m-2,标准差为 36.73 ml·min-1·1.73 m-2,95%一致性界限为(-71.0 ml·min-1·1.73 m-2,73.0 ml·min-1·1.73 m-2)。见图4。

图3 eGFR1和eGFR3的趋势相关关系
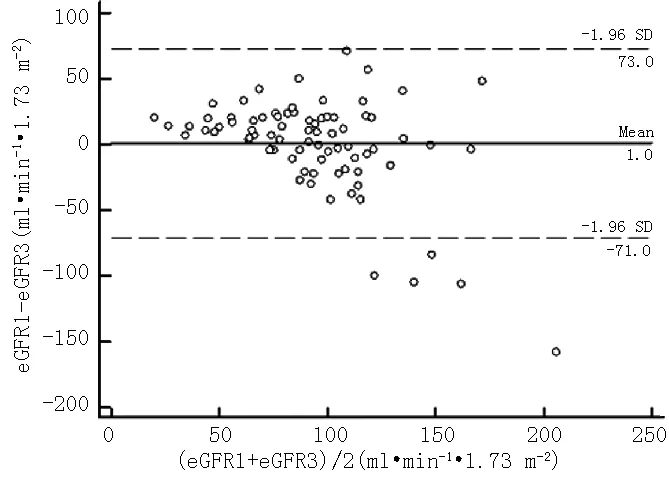
图4 eGFR1和eGFR3的Bland-Altman分析图
2.4 Cys-C估算法与MDRD方程法的比较 eGFR1和eGFR4两种测量方法的配对差均值为-6.79(P>0.05,见表1)。eGFR1和eGFR4的回归方程为Y=0.862X+21.929,Y轴截距与0较为接近,拟合优度尚可,见表2和图5。
Bland-Altman作图法示eGFR1和eGFR4的配对数据差值的均值为-8.9 ml·min-1·1.73 m-2,标准差为30.20 ml·min-1·1.73 m-2,95%一致性界限为(-68.1 ml·min-1·1.73 m-2,50.3 ml·min-1·1.73 m-2)。见图6。
2.5 其他3种方法eGFR与eGFR1估算值准确率的比较 3种方法中,通过24 h尿液测定法估算的值准确度最差,仅有不足30%的病例数落在了eGFR1±15%的范围之内。Cockcroft-Gault方程法和MDRD方程法的准确度相对较好,其中MDRD方程法的准确率更高,大多数的病例集中在了eGFR1±30%的范围之内,见表3。
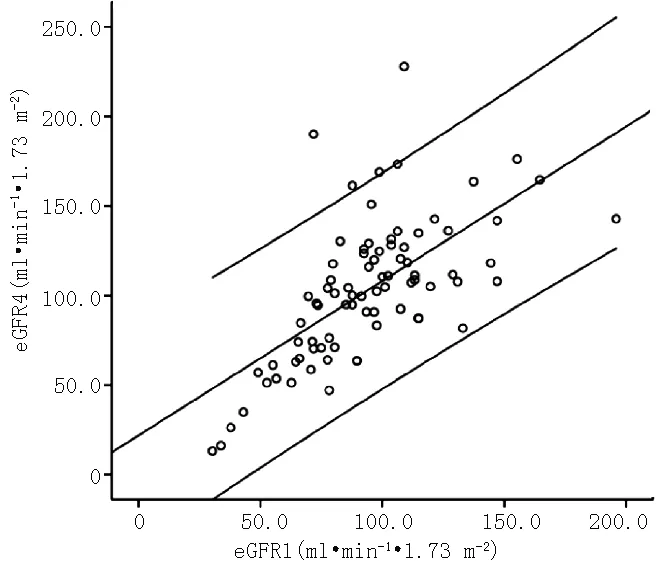
图5 eGFR1和eGFR4的趋势相关关系

图6 eGFR1和eGFR4的Bland-Altman分析图
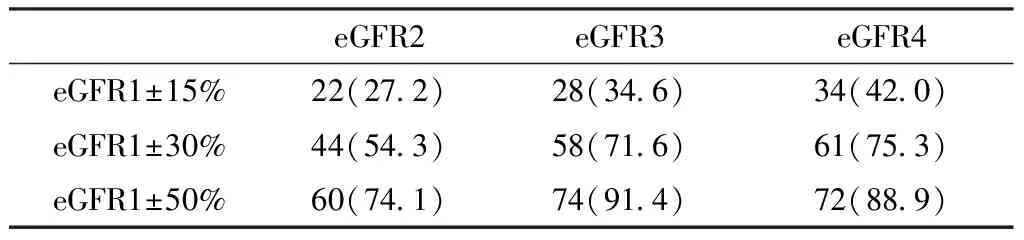
表3 3种方法eGFR与eGFR1估算值准确率的比较〔n(%)〕
3 讨论
GFR是目前评价肾脏功能的重要指标,菊粉清除率是评估GFR的金标准,但是这种方法繁琐,临床使用很少。现在大多数采用99Tcm-二乙烯三胺五醋酸(99Tcm-DTPA)法作为评估GFR的标准方法[8-9],然而这种方法因为要使用放射性注射药物,且依赖一定的检测设备,也难以作为临床普遍采用的方法。Cys-C是半胱氨酸蛋白酶抑制剂,体内产生稳定且不易受性别、炎症状态、肌肉量、免疫性和内分泌疾病等因素的影响[10],能够自由通过肾小球滤过膜,肾脏是清除Cys-C的惟一器官,血液中Cys-C水平主要由GFR决定[11]。因此在国际肾脏病改善预后协调委员会(KDIGO)慢性肾脏病指南中,推荐测定Cys-C评估eGFR[9,12]。大量的研究证实,Cys-C能够较早期地反映糖尿病患者的肾脏损害[13-14]。
多年以来临床通常将使用Cr和24 h UCr计算得到的CCr作为粗略评估GFR的指标,然而Cr水平容易受到年龄、饮食、肌肉容量等多种因素影响,24 h尿标本的留取又较为繁琐,计量常常不够准确,因此并不是评估GFR的理想方法。本研究结果显示,与其他两种方法相比,通过Cr和24 h UCr方法估算的eGFR与Cys-C法评估的eGFR差别最大,拟合度不理想。Bland-Altman图显示其数值离散度较大,因此这种方法对于糖尿病患者来讲并不是一种理想的eGFR评估方法。
Cockcroft-Gault方程不需要收集尿液,方程中除了Cr水平,还考虑到了年龄、体质量及性别因素对GFR的影响。Cockcroft-Gault方程的建立是基于肾功能正常的成年人,以24 h UCr计算的CCr作为参考值得到的回归方程,估算GFR。而MDRD方程的建立是以肾功能不全患者的资料为背景,除了年龄、性别、种族、Cr水平的差异外,还结合了BUN和Alb的水平。有研究表明,在新诊断的2型糖尿病患者中,Cockcroft-Gault方程和MDRD方程均有可能低估肾脏的高滤过状态[15]。在慢性肾功能不全的患者中,Cockcroft-Gault方程和MDRD方程可能对慢性肾脏病(CKD)1期患者的GFR造成低估,而对CKD5期患者的GFR造成高估[16]。
几种统计方法中,配对t检验比较两个均数的差值,主要分析两种测量方法之间的差异[17],这种检验方法受系统误差的影响比较大,但是对随机误差的估计不足。而Bland-Altman图能够通过简单直观的方式了解到两种测量方法的固定误差[18],同时还能够通过95%一致性的上下限观察到随机误差的分布。这两种统计方法均显示Cockcroft-Gault方程法估算的eGFR与Cys-C估算的eGFR最为一致。而MDRD虽然固定误差相对较大,但是离散度小,线性回归分析也显示其与Cys-C法的拟合优度相对最好,落在eGFR1±15%和eGFR1±30%范围内的病例数也最多,与Cys-C估算的eGFR一致性较好。而Cr和24 h UCr方法估算的eGFR无论是系统误差还是随机误差都比较大,准确度较差。
本研究选择的都是在内分泌科住院的2型糖尿病患者,eGFR1<60 ml·min-1·1.73 m-2的患者不足10%(9.88%)。研究显示,在早期肾功能损害的糖尿病患者中,Cys-C的评估价值的敏感性和特异性都比较高[19]。因此,在本研究这部分人群中,将Cys-C估算的eGFR作为参照是比较合理的。但是其在中重度肾功能不全的2型糖尿病患者中可能还不具备普遍适用性。以往的研究显示,在肾功能正常及轻度肾功能不全的患者中,MDRD方程常常出现低估GFR的倾向[16,20],与本研究结果一致。这应该与这个公式设计的背景人群有关,而且MDRD公式还加入了种族的因素,有研究考虑其并不适合亚裔人群[21],在中国人群中使用可能需要一定的改良[22]。
综上所述,通过Cys-C法估算的eGFR简便易行,结果准确,与传统的eGFR评估方法结果一致性较好,适合临床推广使用。但是其在中重度肾功能损害的2型糖尿病患者中的价值,还需要更进一步的研究来评估。
1 Waheed S,Matsushita K,Sang Y,et al.Combined association of albuminuria and cystatin C-based estimated GFR with mortality,coronary heart disease,and heart failure outcomes:The Atherosclerosis Risk in Communities(ARIC) study[J].Am J Kidney Dis,2012,60(2):207-216.
2 中华医学会糖尿病学分会.中国2型糖尿病防治指南[M].2010年版.北京:北京大学医学出版社,2011:5-8.
3 Stevens LA,Coresh J,Schmid CH,et al.Estimating GFR using serum cystatin c alone and in combination with serum creatinine:A pooled analysis of 3 418 individuals with CKD[J].Am J Kidney Dis,2008,51(3):395-406.
4 吴灵萍,罗群.三种常用肾小球滤过率测定方法的比较[J].现代实用医学,2010,22(12):1345-1346,1351.
5 Cockcroft DW,Gault MH.Prediction of creatinine clearance from serum creatinine[J].Nephron,1976,16(1):31-41.
6 Levey AS,Bosch JP,Levis JB,et al.A more accurate method to estimate glomerular filtration rate from serum creatinine:A new prediction equation[J].Ann Intern Med,1999,130(6):461-470.
7 陈卉.Bland-Altman分析在临床测量方法一致性评价中的应用[J].中国卫生统计,2007,24(3):308-309,315.
9 Stevens PE,Levin A,Kidney Disease:Improving Global Outcomes Chronic Kidney Disease Guideline Development Work Group Members.Evaluation and management of chronic kidney disease:Synopsis of the kidney disease:improving global outcomes 2012 clinical practice guideline[J].Ann Intern Med,2013,158(11):825-830.
10 Pucci L,Triscornia S,Lucchesi D,et al.Cystatin C and estimates of renal function:Searching for a better measure of kidney functionin diabetic patients[J].ClinChem,2007,53(3):480-488.
11 柯萧韵,余育才.尿单核细胞趋化蛋白1和血清胱抑素C在糖尿病肾病早期诊断中的临床意义[J].中国全科医学,2011,14(11):3781-3783.
12 Levin A,Stevens PE.Summary of KDIGO 2012 CKD Guideline:Behind the scenes,need for guidance,and a frameworkfor moving forward[J].Kidney Int,2014,85(1):49-61.
13 傅美华,陈军,陈秋.胱抑素C与糖尿病肾病的相关研究进展[J].中国全科医学,2013,16(1):229-231.
14 Rigalleau V,Beauvieux MC,Gonzalez C,et al.Estimation of renal function in patients with diabetes[J].Diabetes Metab,2011,37(5):359-366.
15 Chudleigh RA,Dunseath G,Evans W,et al.How reliable is estimation of glomerular filtration rate at diagnosis of type 2 diabetes?[J].Diabetes Care,2007,30(2):300-305.
16 Zuo L,Ma YC,Zhou YH,et al.Application of GFR-estimating equations in Chinese patients with chronic kidney disease[J].Am J Kidney Dis,2005,45(3):463-472.
17 BeAdard M,Martin NJ,Krueger P,et al.Assessing repro-ducibility of data obtained with instruments based on continuous measurements[J].Exp Aging Res,2000,26(4):353-365.
18 黄茜,梁酩珩,覃海燕.给予Bland-Altman差异分析图法系统误差的检出[J].中国当代医药,2013,20(14):110-111.
19 Perlemoine C,Beauvieux MC,Rigalleau V,et al.Interest of cystatin C in screening diabetic patients for early impairment of renal function[J].Metabolism,2003,52(10):1258-1264.
20 Rule AD,Larson TS,Bergstralh EJ,et al.Using serum creatinine to estimate glomerular filtration rate:Accuracy in good health and in chronic kidney disease[J].Ann Intern Med,2004,141(12):929-937.
21 Jafar TH,Schmid CH,Levey AS.Serum creatinine as marker of kidney function in South Asians:A study of reduced GFR in adults in Pakistan[J].J Am Soc Nephrol,2005,16(5):1413-1419.
22 全国eGFR课题协作组.MDRD方程在我国慢性肾脏病患者中的改良和评估[J].中华肾脏病杂志,2006,22(10):589.

