葛根螺旋藻复合片配方和生产工艺优化
杨生辉,罗光宏*,祖廷勋,王丹霞,陈天仁
(河西学院凯源生物技术开发中心,甘肃省微藻工程技术研究中心,甘肃 张掖 734000)
螺旋藻是一种药食两用植物蛋白新资源,是目前地球上发现的营养最均衡、最丰富的天然食品[1]。世界卫生组织和联合国粮食和农业组织推荐螺旋藻为二十一世纪人类的理想食品和健康食品[2],已引起国际生物学、营养学和医学界的高度关注。螺旋藻营养成分的特点是高蛋白质、低脂肪、低胆固醇,纤维素含量也很低,并且还含有多种维生素、矿物质和微量元素,对人体非常有益[3-7]。它是可吸收性铁、VB12和β-胡萝卜素含量最高的食品,还含有具有防癌、治癌作用的藻类蛋白,含有的藻多糖、γ-亚麻酸等生物活性物质,具有提高机体免疫力等保健作用[8-12]。
葛根(Pueraria lobata)是药食两用植物,既可入药,又是一种很好的营养保健品。《本草纲目》中记载:气味甘、辛、平、无毒。主治消渴、身大热、呕吐、诸痹、起阴气、解诸毒[13]。中医认为,葛根味甘辛,性平无毒,具有生津止渴、清热解毒、解酒等功效。葛根含丰富的淀粉、矿物质、维生素和18种氨基酸,具有较高的营养价值[14]。现代医学研究表明,葛根中含有大量的葛根素和黄酮类物质,是一种较为常见的心肌保护物质;能解痉止痛,防治高血压、冠心病、心绞痛等;能清热凉血、抗菌消炎、抗过敏、抗病毒、抗糖尿病并发症等药理作用;具有抗自由基、抗氧化、抗癌和增强肌体的免疫力等功效,且无毒无害,对人类的肿瘤、衰老、心血管疾病的治疗和预防具有重要意义[15-17]。
目前,国内外对葛根提取物、螺旋藻有效成分的提取的研究较多,将葛根提取物和螺旋藻粉制成复合片的研究未见报道。本研究拟以螺旋藻粉为基础营养原料,葛根提取物、二氧化硅等赋形剂为配料,对葛根螺旋藻复合片配方和生产工艺进行了研究,生产出了一种具有解酒、醒酒的新型营养食品,为螺旋藻、葛根的利用开发及其产品的生产提供科学依据。
1 材料与方法
1.1 材料与试剂
葛根提取物(葛根黄酮质量分数42.5%) 河北宝恩生物科技有限公司;螺旋藻粉 甘肃凯源生物技术开发中心。
二氧化硅(食品添加剂)、微晶纤维素、硬脂酸镁(药品级) 湖州展望药业有限公司。
1.2 仪器与设备
混合机 上海申港机械厂;振动筛 上海申港机械厂;ZP37压片机 上海雪马制药机械有限公司;电子天平 北京赛多斯仪器系统有限公司。
1.3 方法
1.3.1 葛根螺旋藻复合片工艺流程及操作要点
25%螺旋藻粉、葛根提取物、赋形剂→预混合→过筛→混合(加入剩余螺旋藻粉)→过筛→压片→定量包装→成品
原辅料混合:由于物料颗粒细,葛根提取物用量少,所以采取二次混合法来提高混合的均匀度。先将葛根提取物、25%螺旋藻粉、二氧化硅、微晶纤维素、硬脂酸镁投入混合机进行预混合,时间5 min,然后过筛、再混合5 min,最后将剩余螺旋藻粉投入混合机进行二次混合,时间5 min,然后过筛,再混合5 min。
压片:将混合均匀的物料放入压片机进行压片(0.2 g/片)。
1.3.2 赋形剂配方优化工艺设计
赋形剂是在药物制剂中除主药以外的附加物,也可称为辅料。片剂的辅料种类较多,一般有稀释剂、吸收剂、润湿剂、黏合剂、崩解剂、润滑剂等,可根据片剂原料的不同特点,选择不同的辅料[18]。研究中主要选用黏合剂、崩解剂、润滑剂,以增加物料的流动性、可压性及复合片的崩解度。以复合片的硬度、外观、物料的流动性为评价指标进行对比试验。先选择二氧化硅(0.5%、1%、1.5%、2%、2.5%)、微晶纤维素(0.25%、0.5%、1%、1.5%、2.0%)、硬脂酸镁(0.125%、0.25%、0.5%、0.75%、1.0%)做单因素试验,根据结果设计三因素三水平正交试验,得到赋形剂的最佳配方。
1.3.3 葛根螺旋藻复合片配方优化工艺设计
本研究所用葛根提取物的黄酮含量达45%,综合考虑葛根黄酮在临床医学上的使用量、物料的流动性、可压性、醒酒效果、成本,选择葛根提取物的添加量分别为2.5%、5%、7.5%、10%、15%,以物料的流动性、复合片的硬度、外观、醒酒效果、成本为评价指标进行对比试验,醒酒效果是小白鼠先灌胃定量的饮用酒,使其醉酒(翻正反射消失),30 min后再灌胃定量复合片悬浊液,记录小白鼠的醒酒(翻正反射恢复)时间。
螺旋藻粉的含水量的多少直接影响压片的质量及成品的保存。水分过高,物料流动性差,而且容易滋生微生物、发霉变质不易保存;水分太少,压片易疏松、不完整、制片困难。
以螺旋藻粉含水量(5%、6%、7.5%、10%、15%)做压片单因素试验,物料的流动性、复合片的硬度、外观等为考察指标,螺旋藻粉的含水量通过调整喷雾干燥设备原料的进出口温度来控制。通过试验,喷雾干燥设备原料进口温度180℃,出口温度在80、75、70、65、60℃条件下分别取样,以GB/T 5009.3—2003《食品中水分的测定》中的测定方法测定螺旋藻粉含水量为5%、6%、7.5%、10%、15% 。
在确定葛根提取物、赋形剂用量,选定复合片的最佳填充量、厚度时,通过逐渐加大制片的压力(20、25、30、35、40 kN),对复合片的硬度和外观进行了对比实验。
2 结果与分析
2.1 赋形剂配方单因素试验
2.1.1 二氧化硅用量对制片的影响
选择二氧化硅用量0.5%、1%、1.5%、2%、2.5%压片,物料的流动性、复合片的硬度、外观和边缘整齐度等为考察指标,结果见表1。

表1 二氧化硅用量对制片的影响Table1 Influence of silicon dioxide content on tablet properties
由表1可知,二氧化硅主要控制复合片的硬度,对复合片的外观、边缘整齐度、物料流动性没有影响。二氧化硅用量1.5%以上时复合片硬度符合质量要求,所以确定二氧化硅用量为1.5%。郭文等[19]的研究中二氧化硅用量为3.5%,黄金宝等[20]的研究中二氧化硅用量为5%,都高于本研究。
2.1.2 微晶纤维素用量对制片的影响
选择微晶纤维素用量0.25%、0.5%、1%、1.5%、2.0%压片,物料的流动性、复合片的硬度、外观和边缘整齐度等为考察指标,结果见表2。

表2 微晶纤维素用量对制片的影响Table2 Influence of microcrystalline cellulose content on tablet properties
由表2可知,微晶纤维素主要控制复合片的外观、边缘整齐度,对硬度、物料流动性没有影响,说明微晶纤维素是物料的黏合性的决定因素。使用量1%以上时复合片外观、边缘整齐度符合质量要求,所以确定微晶纤维素用量为1%。郭文等[19]的研究中微晶纤维素用量为6%,黄金宝等[20]的研究中微晶纤维素用量为20%,都远高于本研究。
2.1.3 硬脂酸镁用量对制片的影响
选择硬脂酸镁用量0.125%、0.25%、0.5%、0.75%、1.0%压片,物料的流动性、复合片的硬度、外观和边缘整齐度等为考察指标,结果见表3。

表3 硬脂酸镁用量对制片的影响Table3 Influence of magnesium stearate content on tablet properties
由表3可知,硬脂酸镁主要控制物料流动性,对复合片的硬度、外观、边缘整齐度没有影响,说明硬脂酸镁是物料的流动性的决定因素,与潘建国等[21]的研究结果一致。用量0.25%以上时物料的流动性符合要求,所以确定硬脂酸镁用量为0.25% 。
2.2 赋形剂配方正交试验结果与分析
根据以上单因素试验结果,以复合片的硬度、外观、物料的流动性为评价指标进行对比试验。先选择二氧化硅用量1%、1.5%、2%,晶纤维素用量0.5%、1%、1.5%,硬脂酸镁用量0.125%、0.25%、0.5%,设计三因素三水平正交试验,得到赋形剂的最佳配方。
因素水平见表4,多指标综合评分见表5,正交设计安排及评分结果见表6。由表6中R值大小可知,赋形剂配方中各因素的作用主次为A>C>B,即二氧化硅>微晶纤维素>硬脂酸镁。结果表明,赋形剂配方中二氧化硅为主要影响因素,微晶纤维素和硬脂酸镁为次要因素,结合极差结果,综合分析各因素、水平、处理间的显著性差异,得出赋形剂种类和用量最佳配比为A2B2C2。
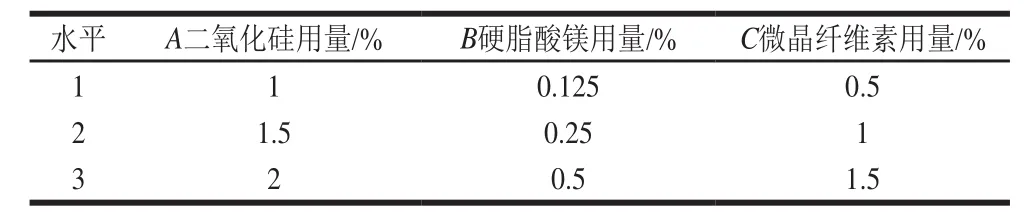
表4 赋形剂混合配方因素水平表Table4 Factors and levels used in orthogonal array design for optimization of excipient formulation

表5 复合片多指标综合评分表Table5 Multi-indicator evaluation of composite tablets
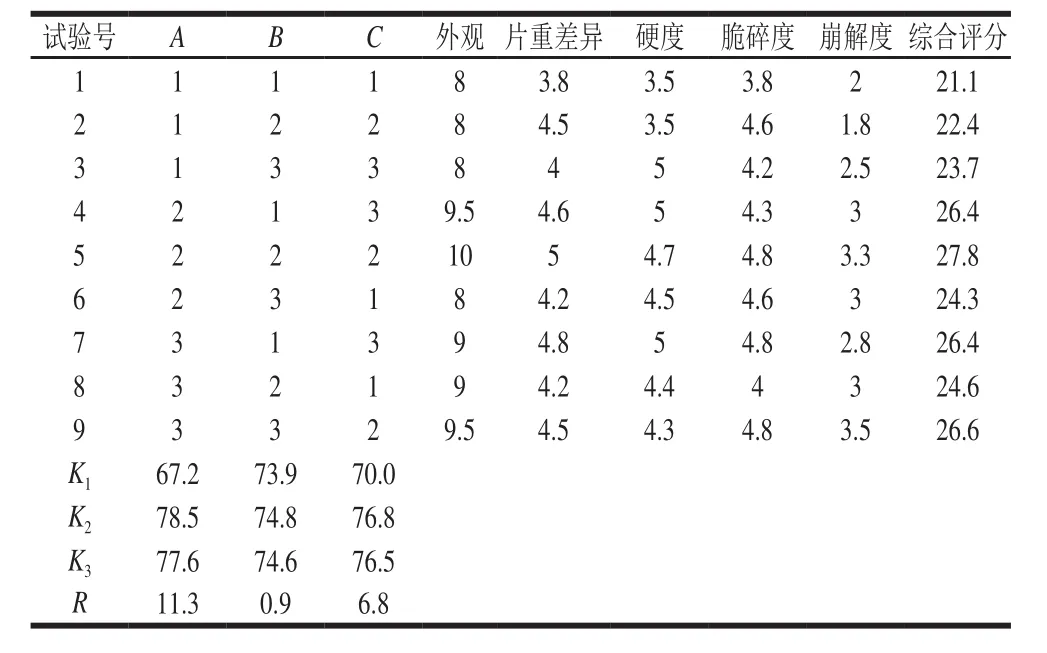
表6 赋形剂混合配方正交试验结果Table6 Results of orthogonal array design for optimization of excipient formulation
2.3 葛根螺旋藻复合片配方单因素试验
2.3.1 葛根提取物用量对制片影响

表7 葛根提取物添加量对复合片制片效果、醒酒效果和成本的影响Table7 Influence of Puerariae Radix extract content on properties,anti-alcoholic effect and cost of composite tablets
根据表7对比试验结果,随着葛根提取物的用量的增加,复合片制片效果和物料流动性越来越差,小白鼠醒酒的时间逐渐缩短,当葛根提取物用量为10%以上时,复合片出现硬度不够,易出现裂片、分层等现象,物料流动性不够,综合考虑产品制作成本及醒酒效果,确定葛根提取物添加量为10%。
葛根螺旋藻复合片主要是以螺旋藻为基础营养源,添加具有针对性的有效功能成分葛根提取物,以达到在满足生理营养的条件下,醒酒、解酒的作用。因而葛根提取物的用量是葛根螺旋藻复合片解酒功效的决定因素。这与章文炽等[22]对葛根提取物解酒实验和张恩户等[23]对葛根醇提取物的进行解酒功效研究结果相符。
2.3.2 螺旋藻粉含水量对制片影响

表8 螺旋藻粉含水量对制片的影响Table8 Influence of water content of Spirulina powder on tablet properties
根据表8对比试验结果,螺旋藻粉含水量低于6%时,物料流动性虽然好,但制片困难、复合片外观差;含水量接近10%时,复合片硬度特别高、表面光滑,但物料流动性差,填充困难,不利于制片;含水量接近15%时,物料流动性极差,不能填入模具中,无法压制成型;含水量在7%~8%时,复合片硬度适中、表面光滑、物料流动性好、边缘整齐。所以选择含水量7.5%的螺旋藻粉(喷雾干燥进口温度180℃、出口温度70℃)制片最佳。这与冯燕堂[24]对螺旋藻片剂制作技术的研究结果含水量10%~12%不同。
2.3.3 压片机压力对制片影响
根据表9对比试验结果,随着制片压力的增加,复合片硬度越来越高,外观也越来越好。当压力达到30 kN时,复合片硬度和外观符合质量要求,而压力升到40 kN时,复合片硬度增加不明显。而从维护设备和节约能源的角度出发,只要选择使产品获得适宜的硬度和外观质量时的压力即可,所以将制片的最适压力确定为30 kN。

表9 制片压力对复合片的硬度和外观的影响Table9 Influences of tableting pressure on hardness and appearance of tablets
2.4 葛根螺旋藻复合片配方正交试验
根据单因素试验结果,为进一步考察各因素影响的显著性以及复合片的最佳配方和工艺条件,以赋形剂用量(1.5%、2.5%、3.5%)、螺旋藻粉含水量(6%、7.5%、10%)、葛根提取物用量(7.5%、10%、15%)为考察目标,根据L9(33)进行三因素三水平正交试验。因素水平见表10,正交设计安排及评分结果见表11。

表10 复合片配方正交试验因素与水平Table10 Factors and levels used in orthogonal array design for optimization of tablet formulation
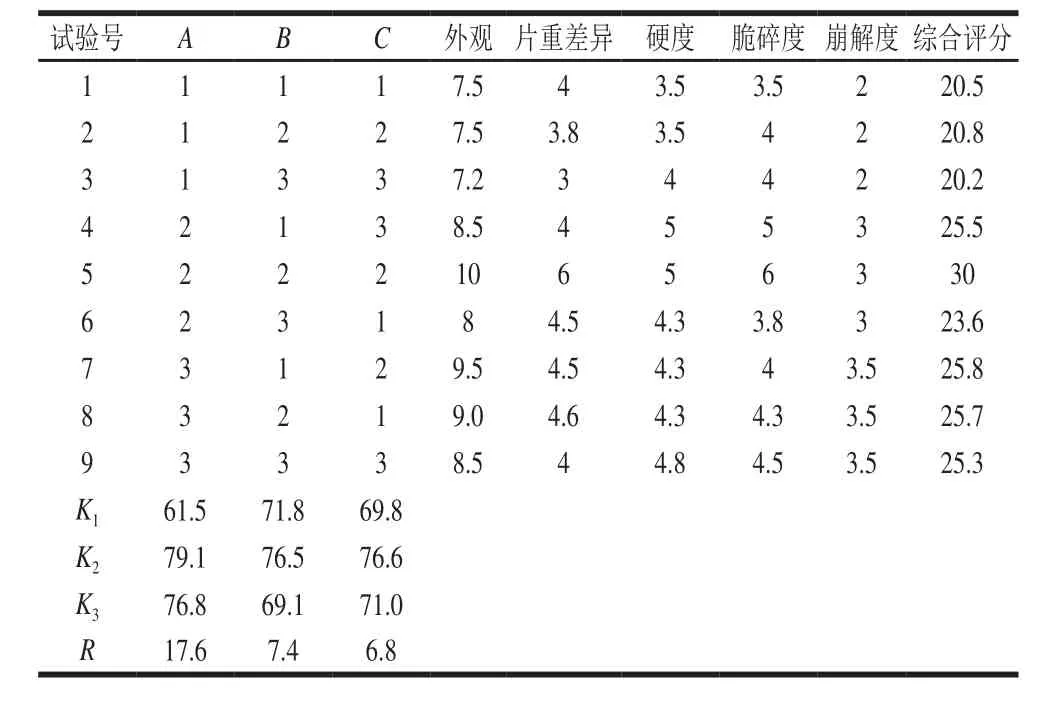
表11 复合片配方正交试验设计及结果Table11 Results of orthogonal array design for optimization of tablet formulation
由表11中R值大小可知,葛根螺旋藻复合片配方中各因素的作用主次为A>B>C,即赋形剂用量>葛根提取物用量>螺旋藻含水量。结果表明,赋形剂用量为复合片成型质量主要影响因素,而螺旋藻含水量和葛根提取物用量为次要因素,结合极差结果,并考虑生产成本因素,综合分析因素、水平、处理间的显著性差异,得出葛根螺旋藻复合片配方最佳配比为A2B2C2。
李琴等[25]的研究中赋形剂种类为4种,用量为14%;宋伟国等[26]的研究中赋形剂种类为3种,用量为10%;郭文等[19]的研究中赋形剂种类为6种,用量为40%;黄金宝等[20]的研究中赋形剂种类为3种,用量为35%。与上述研究相比,本研究使用赋形剂种类少,用量减小,保证了复合片的纯度和营养价值。与潘建国等[21]研究相比,少制粒干燥工艺,制作工艺简单,更具有实用推广价值。
3 结 论
3.1 赋形剂配方
各物质用量分别为二氧化硅1.5%、微晶纤维素1%、硬脂酸镁0.25%。二氧化硅主要控制复合片的硬度,微晶纤维素控制物料的黏合性,影响复合片的外观、边缘整齐度,硬脂酸镁主要控制物料流动性,影响物料制片过程中的填充量;3种物料中二氧化硅为主要影响因素,而微晶纤维素用量和硬脂酸镁为次要因素,3种物料按比例配合,极小的用量就能使复合片外观达到规定的要求。
3.2 葛根螺旋藻复合片生产配方
葛根螺旋藻复合片配方为葛根提取物用量10%、螺旋藻粉用量87.5%、赋形剂用量2.5%、螺旋藻粉含水量约7.5%、制片压力30 kN。在葛根螺旋藻复合片配方中,赋形剂用量为复合片成型质量主要影响因素,而螺旋藻含水量和葛根提取物用量为次要因素,制片压力对复合片成型的影响极不显著,葛根提取物用量是影响复合片醒酒效果的主要因素。
葛根螺旋藻复合片主要是以螺旋藻为基础营养源,添加具有针对性的有效功能成分葛根提取物,集螺旋藻和葛根营养和功能于一体,增强协同性,以达到在满足生理营养的条件下,具有一定的醒酒、解酒作用。复合片工艺简单,采用干粉直接压片而成,易于控制片剂质量;不经过制粒干燥,避免高温烘干过程,从而能够很好地保留住螺旋藻的生物活性物质。
[1]王文博, 高俊莲, 孙建光, 等.螺旋藻的营养保健价值及其在预防医学中的应用[J].中国食物与营养, 2009(1): 48-51.
[2]吴海军, 郭勇.螺旋藻的营养价值及在生物资源回收中的应用[J].广州食品工业科技, 2003, 19(2): 71-72.
[3]陈必链, 施巧琴.螺旋藻藻种选育研究进展[J].食品与发酵工业,2000, 26(3): 78-81.
[4]周淑荣, 李沐森.螺旋藻的营养保健功能与其开发利用[J].特产研究, 2001(2): 63-65.
[5]DEARMAN R J, KIMBER I.Food allergy: what are the issues[J].Toxicology Letters, 2001, 120(1): 165-170.
[6]罗光宏.高纬度高海拔地区螺旋藻生产工艺及免疫调节功能的测定[J].食品科学, 2003, 24(6): 135-138.
[7]朱王飞, 钱胜峰.螺旋藻的营养价值及开发利用前景[J].饲料博览,2005(11): 36-38.
[8]HAYASHI K, HAYASHI T, MORITA N, et al.An extract from spirulina platensisis a selective inhibitor of herpes simplex virus type 1 penetration into HeLa cells[J].Phytotherapy Research, 1993, 7(1): 76-80.
[9]IM H M, LEE E H, CHO H H, et al.Inhibitory effect of mast cellmediatedimmediate-type all ergicreaction sinrats by Spirulina[J].Biochem Pharmacol, 1998, 55(7): 1071-1076.
[10]张洪义, 王淑田, 李进贤, 等.螺旋藻营养液增强机体免疫调节功能的研究[J].食品科学, 1998, 19(7): 44-46.
[11]杨世诚.螺旋藻及其营养保健功能[J].中国食物与营养, 2003(3):47-50.
[12]吴文龙, 杨志娟.螺旋藻保健食品的功能因子与研究开发进展[J].食品研究与开发, 2006, 27(2): 129-131.
[13]苏中医学院.中药大辞典: 下册[M].上海: 上海科学技术出版社,1985: 2307-2308.
[14]郑皓.葛根的研究与开发现状[J].氨基酸和生物资源, 2006, 28(2):24-26.
[15]龚志刚, 胡红霞, 朱笃, 等.葛根素对糖尿病大鼠血糖和抗氧化能力的影响[J].食品科学, 2006, 27(11): 498-501.
[16]LU Y R, FOO Y L.Antioxidant activities of polyphenols from sage(Salvia officinalis)[J].Food Chemistry, 2001, 75: 197-202.
[17]DU Xianfeng, JIA Jianhua, XU Shiying, et al.Molecular structure ofstarch from Pueraria lobata (Willd.) Ohwi relative to kuzu starch[J].Starch, 2007, 59(12): 609-613.
[18]谢华, 夏敏丽, 宋建平.利咽灵片生产工艺考查[J].黑龙江医药,2011, 24(3): 401-403.
[19]郭文, 李俊, 罗姗, 等.一种螺旋藻片及其制备方法: 中国,CN101999713A[P].2011-04-06.
[20]黄金宝, 贾福怀, 邢晓伟.灵芝螺旋藻片及其制备工艺: 中国,CN101731622A[P].2010-06-16.
[21]潘建国, 王开发, 刘远红.花粉螺旋藻片生产工艺研究[J].养蜂科技,2001(3): 2-4.
[22]章文炽, 夏培源.枳葛饮解酒作用的实验观察[J].中国医院药学杂志, 1994, 14(3): 137.
[23]张恩户, 赵勤, 梁作峰, 等.葛根总黄酮解酒作用的实验观察[J].陕西中医学院学报, 1995, 18(3): 38.
[24]冯燕堂.螺旋藻片的制作技术[J].广东农机, 1999(4): 26-27.
[25]李琴, 李战.益多螺旋藻片的制备及质量控制[J].中国药业, 2005,14(8): 54-55.
[26]宋伟国, 宋成刚, 高东圣, 等.一种螺旋藻粉直接压片法: 中国,CN103169108A[P].2013-06-26.

