PEITC通过抑制结肠癌细胞PI3K/NF-κB活性而抑制MMP-9表达
魏付桥,申清香,刘昌化,罗康宁,谢文彪,胡 军
(1.南华大学附属第二医院胃肠外科;湖南 衡阳 421001;2.南华大学附属第二医院妇产科;3.南华大学附属第二医院心胸外科)
结肠癌是消化系统最常见的恶性肿瘤,全世界每年新发病例可达120万人以上,在我国,由于饮食结构的改变,其发病率也有逐年递增的趋势。结肠癌起病隐匿,90%以上患者死于癌细胞的侵袭和转移[1]。肿瘤细胞从原发灶脱落,并降解细胞外基质(extracellular matrix,ECM)是肿瘤发生转移的最重要病理生理改变,而此过程与基质金属蛋白酶(matrix metalloproteinases,MMPs)的活性密切相关[2]。因此,以MMPs为研究靶点,探索抑制MMPs活性的治疗药物,对结肠癌的治疗具有重要意义。
异硫氰酸苯乙酯(phenethyl isothiocyanate,PEITC)异硫氰酸脂的一种,广泛存在于橄榄,花椰菜等十字花科植物当中。研究显示,PEITC可通过多种机制肿瘤细胞的生长与增殖,如PEITC可与β-微管蛋白结合,促进微管蛋白的稳定而影响细胞有丝分裂[3]。也能抑制去乙酰化酶的活性而影响染色质功能[4]。本文旨在观察PEITC对结肠癌SW480细胞的迁移与侵袭有何影响,并探讨其可能的调控机制。
1 材料与方法
1.1 实验试剂
PEITC购自LKT Laboratories(纯度≥95%),并用二甲基亚砜溶解。细胞培养基为Invitrogen产品,培养板和Transwell小室购自Corning。Trizol试剂购自Invitrogen公司。RT-PCR试剂盒购自大连宝生物。抗MMP-9和β-actin抗体购自Santa Cruz。磷酸化Akt,总Akt抗体购自Cell Signaling。ECL化学发光试剂盒购自Amersham Pharmacia。NF-κB荧光素酶报告基因购自SABioscicence,双重荧光素酶实验系统购自Promega。pGL3-basic载体和DNA转染试剂购自Invitrogen。
1.2 细胞培养
SW480细胞株购自中南大学肿瘤研究所,用含10%胎牛血清的RPMI-1640培养基于37 ℃,5% CO2条件下培养。分别设立对照组(加入等体积的二甲基亚砜)及不同浓度PEITC处理组(加入终浓度为10、30、50 μmol/L的PEITC作用24 h)。采用MTT观察PEITC对SW480细胞的增殖情况,即,SW480孵育结束后,每孔加入30 μL MTT溶液(1 mg/mL)孵育2 h。弃上清,并加入200 μL二甲基亚砜,充分混匀,用酶标仪测定各孔的吸光度值(OD570),并计算抑制率。抑制率=(对照组OD值-实验组OD值)/对照组OD值×100%。
1.3 RT-PCR检测MMP-9 mRNA表达
采用Trizol提取RNA,并根据试剂盒提供的步骤进行逆转录PCR(reverse transcription-PCR,RT-PCR)。PCR反应条件如下:94 ℃变性30 s,65 ℃(MMP-9)或59 ℃(GAPDH) 30 s,72 ℃延伸30 s。随后进入40(MMP-9)或35(GAPHD)个扩增循环。其中MMP-9引物分别为5′-CGCTACCACCTCGAACTTTG-3′和5′-GCCATTCACGTCGTCCTTAT-3′,产物196 bp。GAPDH:5′-TCACCATCTTCCAGGAGCGA-3′,5′-CACAATGCCGAAGTGGTCGT-3′,产物700 bp。扩增产物随后经2%琼脂糖凝胶电泳,并采用Image J软件进行灰度分析并计算两者比值。
1.4 划痕愈合实验
通过划痕愈合实验测定细胞的迁移能力。即,5×106细胞接种于6孔板中37 ℃培养6 h。待细胞呈单层贴壁生长后,用200 μL的移液管尖端在板上划痕。PBS洗涤后加入含有PEITC的完全培养基孵育24 h。在显微镜下拍照并计算迁移率:(1-处理后划痕距离/对照组划痕距离)×100%。
1.5 侵袭性实验
将基质胶均匀铺至Transwell小室上室,并加入100 μL细胞悬液(106/mL),下室加入500 μL完全培养基,37 ℃孵育24 h。取出Transwell,多聚甲醛固定,风干后加入0.1%结晶紫染色20 min。擦除上室细胞,显微镜下随机选择视野拍照,计算迁移到下腔表面的细胞数。其中侵袭抑制率=(1-样本穿膜细胞数/对照组穿膜细胞数)×100%。
1.6 Western blot
根据试剂盒提供的步骤提细胞总蛋白并测定其浓度。获取100 μg蛋白用于SDS-PAGE。分离的总蛋白或核蛋白随后转印至PVDF膜上(Millipore),并利用含5%脱脂牛奶的TBST封闭1 h,随后加入一抗抗体4 ℃孵育过夜。多次洗涤之后,加入HRP标记的二抗孵育膜1 h。ECL法(Amersham)发光、显影。
1.7 瞬时转染和荧光素酶报告基因分析
获取MMP-9基因(基因ID:D10051)上游-720 bp~-11 bp启动子区域序列,用PCR克隆至pGL3-basic载体中,构建pGL3-MMP-9-luc报告基因质粒。SW480细胞接种于6孔板中,当其密度达视野的70%~80%时,共转入0.2 μg pGL3-MMP-9-luc(或NF-κB-luc)报告基因质粒以及0.2 μg pSV-β-半乳糖苷酶并培养18 h。随后细胞加入不同浓度PEITC作用24 h,根据试剂盒(Promega)提供的操作步骤,采用光测定仪(Turner BioSystems,Luminometer 20/20n)获取萤光素酶和β-半乳糖苷酶活性。以β-半乳糖苷酶活性为内参,计算萤光素酶活性的相对值。
1.8 统计学分析
2 结 果
2.1 PEITC抑制SW480细胞的迁移和侵袭
MTT结果显示,10~50 μmol/L PEITC处理对细胞的活性无明显影响(结果未显示)。而划痕愈合实验显示,10、30和50 μmol/L PEITC处理SW480细胞后,细胞迁移率分别为(64.27±5.14)%,(51.57±4.39)%和(43.81±3.61)%,与对照组相比,差异均有显著性。Transwell结果显示,不同浓度的PEITC也能呈剂量依赖性方式抑制SW480细胞侵袭(图1,表1)。

图1 PEITC抑制SW480细胞迁移和侵袭(×10)

表1 PEITC对SW480细胞的迁移率和侵袭率(%)
2.2 PEITC抑制SW480细胞MMP-9蛋白及mRNA表达
RT-PCR结果显示,SW480细胞未处理前,MMP-9 mRNA表达水平较高,经不同浓度PEITC处理后,其mRNA水平随着浓度的增高而降低(图2A)。Western blot结果也显示,10~50 μmol/L PEITC处理后,MMP-9蛋白含量逐渐降低(图2B)。
2.3 PEITC抑制PI3K/NF-κB通路的活性
Western blot结果显示,PEITC处理后,SW480细胞中磷酸化Akt水平明显降低,而总Akt无明显影响(图3A)。此外,报告基因结果显示,PEITC也能影响NF-κB-luc的转录活性,同时,采用20 μmol/L PI3K抑制剂LY294002处理后,NF-κB-luc活性显著降低(图3B)。
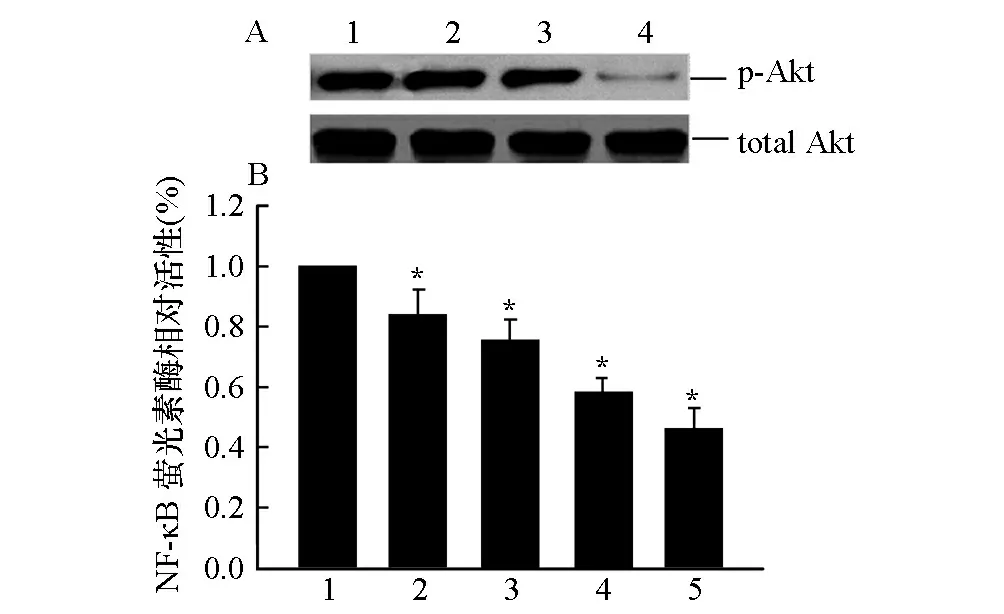
图3 PEITC对PI3K/NF-κB活性的影响
2.4 PEITC经PI3K/NF-κB抑制MMP-9的表达与转录
Western blot显示,PI3K抑制剂LY294002和NF-κB抑制剂PDTC处理SW480细胞后,MMP-9表达显著降低。此外,报告基因显示,不同浓度PEITC处理能显著抑制MMP-9的启动子活性,从而抑制MMP-9的转录(图4A)。

图4 PEITC对MMP-9表达及转录活性的影响
3 讨 论
对于结肠癌而言,癌细胞的局部浸润以及远处转移是患者治疗失败和死亡的首要原因。癌细胞在浸润性生长过程中,细胞基质的降解是癌细胞从原发部位脱落,并经淋巴结或血液转移的关键。而MMP-9在其中发挥至关重要作用。因此,预防或抑制癌细胞浸润和转移在很大程度上可提高癌症患者的生存率。有研究显示PEITC能抑制前列腺癌、乳腺癌以及肺癌细胞肺转移[5],然而,PEITC对结肠癌的抑制作用尚未完全清楚,本研究证实PEITC在无细胞毒性的浓度范围内能明显抑制SW480细胞的浸润和转移,并能明显抑制明胶酶活性和MMP-9的表达,这表明PEITC在结肠癌中通过抑制MMP-9的表达和活性而具有抗侵袭的潜能。
PI3K是一种脂质激酶,通过激活Akt(即蛋白激酶B)控制多种生理过程,它通过诱导P21WAF1定位于细胞质,并通过灭活前凋亡因子BAD和caspase-9发挥抗凋亡作用,此外,活化的Akt可通过诱导MMPs的表达而促进癌细胞侵袭和转移[6]。研究显示,MMP-9 mRNA含量与PI3K的活性成正相关[7]。本研究也证实,PEITC能抑制PI3K产物Akt磷酸化,从而抑制MMP-9的表达。NF-κB是Akt下游通路的重要靶分子。并参与调控MMP-9的表达,并与炎症、肿瘤细胞增殖、浸润和转移密切相关[8]。此外,NF-κB在多种肿瘤细胞中持续激活,并诱导多种抗凋亡蛋白表达而导致化疗/放疗耐受[9]。因此抑制NF-κB的活性可能有利于提高药物的疗效。本研究结果显示,PEITC可有效抑制NF-κB转录活性。由于MMP-9的启动子区域存在NF-κB的结合位点[10],因此本研究构建了MMP-9启动子序列的报告基因,结果也证实,PEITC可通过影响PI3K/NF-κB的活性,从而抑制MMP-9的转录激活作用。
总之,本研究证明PEITC具有抑制SW480细胞浸润的能力。其机制可能通过抑制PI3K/ NF-κB信号通路的活性而抑制MMP-9表达。由于PEITC来源于可食用天然植物[11],这无疑为肿瘤的预防和治疗提供了重要参考,长期食用PEITC含量丰富的蔬菜可降低肿瘤发生的风险,此外,PEITC有望成为结肠癌的重要辅助治疗药物。
[1]沈默,曲宸绪,游伟程,等.北京市城区结肠癌发病率分布滞后预测模型研究[J].首都医科大学学报,2008,29(4):501-504.
[2]Nakayama Y,Okazaki K,Shibao K,et al.Alterative expression of the collagenase and adhesion molecules in the highly metastatic clones of human colonic cancer cell lines[J].Clin Exp Metastasis,1998,16(5):461-469.
[3]Di PAJ,Hong C,Wu MY,et al.Sensitization of non-small cell lung cancer cells to cisplatin by naturally occurring isothiocyanates[J].Chem Res Toxicol,2010,23(8):1307-1309.
[4]Tang NY,Huang YT,Yu CS,et al.Phenethyl isothiocyanate (PEITC) promotes G2/M phase arrest via p53 expression and induces apoptosis through caspase- and mitochondria-dependent signaling pathways in human prostate cancer DU 145 cells[J].Anticancer Res,2011,31(5):1691-1702.
[5]Sarkars R,Mukherjee S,Roy M.Targeting heat shock proteins by phenethyl isothiocyanate results in cell-cycle arrest and apoptosis of human breast cancer cells[J].Nutr Cancer,2013,65(3):480-493.
[6]Chen JS,Wang Q,Fu XH,et al.Involvement of PI3K/PTEN/AKT/mTOR pathway in invasion and metastasis in hepatocellular carcinoma:Association with MMP-9[J].Hepatol Res,2009,39(2):177-186.
[7]Hildebrandt MA,Yang H,Hung MC,et al.Genetic variations in the PI3K/PTEN/AKT/mTOR pathway are associated with clinical outcomes in esophageal cancer patients treated with chemoradiotherapy[J].J Clin Oncol,2009,27(6):857-871.
[8]Kim Y,Kang H,Jang SW,et al.Celastrol inhibits breast cancer cell invasion via suppression of NF-kB-mediated matrix metalloproteinase-9 expression[J].Cell Physiol Biochem,2011,28(2):175-184.
[9]Lee CH,Jeon YT,Kim SH,et al.NF-kappaB as a potential molecular target for cancer therapy[J].Biofactors,2007,29(1):19-35.
[10]Wu HT,Sie SS,Kuan TC,et al.Identifying the regulative role of NF-kappaB binding sites within promoter region of human matrix metalloproteinase 9 (mmp-9) by TNF-alpha induction[J].Appl Biochem Biotechnol,2013,169(2):438-449.
[11]Tang L,Zhang Y.Mitochondria are the primary target in isothiocyanate-induced apoptosis in human bladder cancer cells[J].Mol Cancer Ther,2005,4(8):1250-1259.

