甲烷水合物降压分解控制机理实验研究
梁海峰, 宋永臣, 赵阳升, 赵建忠
(1.太原理工大学采煤工艺研究所,山西太原030024;2.大连理工大学海洋能源利用与节能教育部重点实验室,辽宁大连116024;3.太原理工大学化学化工学院,山西太原030024)
甲烷水合物作为一种新型能源,由于具有储量大、能量密度高、燃烧清洁等优点,已经吸引了越来越多国家的关注。自然界中甲烷水合物主要储藏在海底沉积层和永久冻土地区,复杂的地质条件大大限制了其开采利用。目前认为,甲烷水合物的开采方式主要有3种:降压开采、注热开采以及注入化学抑制剂开采,而降压开采被认为是最具前景的开采方式。许多学者对多孔介质中甲烷水合物的降压分解特性及影响因素进行了研究[1-4],但这些研究缺乏对水合物降压分解过程中边界传热的影响进行关注。本文搭建了水合物生成与分解实验系统,对大孔高渗多孔介质中甲烷水合物的相平衡曲线进行了测定,研究了不同边界传热条件下水合物降压分解特性,结果表明,在渗透率较大的多孔介质中,热量传递是影响水合物分解的主要控制因素。
1 甲烷水合物实验系统
到目前为止,关于水合物生成和分解研究的实验系统,在李淑霞[1]的博士论文中已经有了详细的介绍,本文就不再赘述。需要指出的是,无论何种实验系统,都需满足以下几种功能:多孔介质和水合物生成所需反应容器、低温控制系统、压力控制系统、温度、压力数据采集系统、生成水合物所需的甲烷、水等供气供水系统以及其他实验辅助系统。
图1为水合物生成和分解实验系统图,该实验台可以对多孔介质中甲烷水合物生成、分解实验中的温度、压力、流量等参数进行连续测量,并且通过传感器、工控机进行自动记录、控制。实验反应釜内填充石英玻璃砂模拟多孔介质,使用高纯度CH4气体作为甲烷气来源。整个系统的压力由电动计量泵控制,压力精度可以达到±0.1 MPa。反应釜进、出口压力分别由高精度的压力传感器测定,其压差由精度为±0.01kPa的差压传感器测定。在反应釜的腔体上等间距(35mm)安装了5个精度为±0.05℃的热电偶测量甲烷水合物生成、分解时的温度以及温度梯度。

图1 甲烷水合物实验系统实物图Fig.1 Schematic showing the real experimental equipment
图2所示为填充多孔介质的反应容器。整个实验系统放置在一个较大的冷冻室中,可以保证进入反应容器的气、水的温度不至于太高。
2 相平衡实验研究及结果分析
为了测试实验系统能否满足模拟多孔介质中水合物生成分解实验要求,进行了一系列相平衡曲线测定实验,与文献[2,5-7]研究结果进行对比。实验中采用日本AS-ONE 公司生产的BZ-01、BZ-02玻璃砂(平均粒径分别为110、213.5μm),大连光明特种气体有限公司生产的纯度99.9%的甲烷来进行水合物生成相平衡实验,本实验采用定容温度搜索法,得到相平衡点数据。

图2 填充多孔介质的反应容器Fig.2 The diagram of reaction vessel with porous media
在 图3 中,樊 栓 狮[2]、J L Thakore[5]、S Adisasmito[6]实 验 数 据 是 在 纯 水 中 测 得,T Uchida[7]、李淑霞[1]以及本实验数据都是在多孔介质中测得,由此可以看出本文实验数据和李淑霞数据都跟纯水中测量结果一致,而Uchida的相平衡出现偏移。分析可知,Uchida采用的多孔介质孔径为30nm 和100nm,远远小于本实验采用的多孔介质孔径,因此可以认为该条件下毛细压力较大,导致了水合物相平衡的改变。正如文献[8-13]的研究结果表明的,多孔介质在一定程度上改变了水合物的相平衡曲线,随着孔径的减小,毛细压力增大,水合物相平衡曲线改变增大。对于本实验,所用玻璃砂属于高孔高渗多孔介质,毛细管力对水合物相平衡的影响可以忽略,所以测得的相平衡曲线与纯水中的一致。
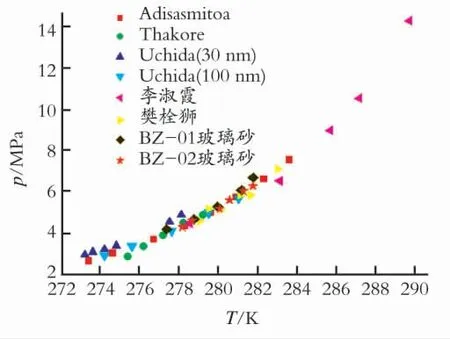
图3 甲烷水合物相平衡图Fig.3 Phase equilibrium of methane hydrate
3 甲烷水合物降压分解实验研究
3.1 实验步骤
为了模拟自然界中甲烷水合物的降压开采过程,首先需要在多孔介质(本文采用玻璃砂)中进行水合物的合成,确定水合物生成后各相(水、气和水合物)饱和度,然后设定出口压力进行降压分解,通过气体流量计来测量反应生成的气体量,分解产生的水的质量通过反应前后测量气体分离装置的质量来确定。
3.2 水合物分解动态特性分析
图4为水合物分解过程中压力变化曲线。从图4中可以看出,封闭端和出口端压力变化曲线重合且同时在短时间内达到出口阀设定压力,这是因为在本实验条件下反应釜内多孔介质的渗透率比较大,导致了压力快速下降。同时可以看到,在开始时刻,甚至出现压力低于背压阀设定压力的现象,这是由背压阀的精度以及灵敏度特性所决定的。
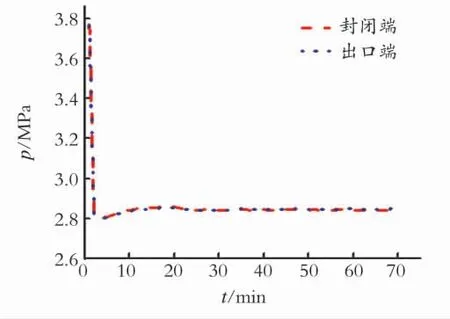
图4 水合物分解过程中压力变化曲线Fig.4 Time evolution of pressure during the hydrate dissociation
图5为水合物分解过程中测点温度变化。从图5中可以看出,随着出口端阀门的开启,测点温度迅速下降,而后缓慢上升并基本保持不变,50 min后开始快速升高。显然在阀门刚开启时,压力迅速下降产生气体节流效应同时水合物分解速度也较快导致了温度的大幅降低。温度稳定阶段可以认为是水合物分解吸热导致,1kg甲烷水合物分解吸收的热量可使108kg水或者543kg玻璃砂的温度下降1 K。随着水合物量的减少,边界传热量高于水合物分解吸热量,造成了温度出现缓慢上升,而在50 min后系统温度出现快速的升高,表明此时水合物已基本完全分解。
图6为水合物在分解过程中产气速率与累积产气体积随时间变化。从图6中可以看出,产气速率曲线存在一定的波动,这是因为气液两相渗流本身具有一定的不稳定性,同时受出口背压阀灵敏性的影响。产气速率变化经历如下几个阶段:(1)产气速率瞬间增大阶段。随着出口阀的开启,产气速率瞬间升高。(2)产气速率出现暂时下降。系统的渗透率较大导致压力下降较快,而水合物分解产气速率与之相比较低,系统温度压力在一段时间内出现在平衡线以上,这导致了水合物驱动力下降从而水合物分解速率减慢。(3)产气速率再次上升阶段。这一阶段出现主要因为反应的进行更多的体现了热量对水合物分解速率的影响加大了。(4)产气速率缓慢下降为0。
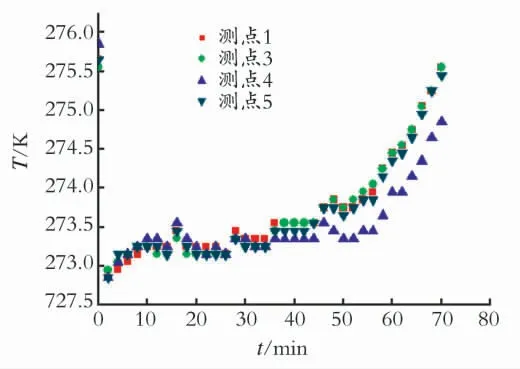
图5 水合物分解过程中各测点温度变化Fig.5 Time evolution of the temperatures during the hydrate dissociation
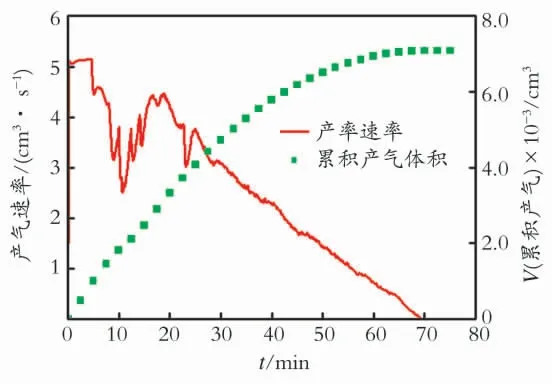
图6 水合物分解过程中产气速率以及累积产气体积变化曲线Fig.6 Gas generation rate and cumulative gas production time evolution curve
通过分析可知,阀门开启时产气速率瞬间增大,这是因为在较大的渗透率条件下,反应釜中的自由气迅速流向出口造成的。而后产气速率变化是由于水合物分解造成的,则水合物分解速率经历了一个逐渐增大到最大值而后下降为零的过程。这种变化过程可以通过水合物分解动力学反应理论予以解释[14-18]。水合物分解速率跟动力学反应速度、水合物反应表面积以及气体三相平衡逸度与固体表面气体逸度差成正比。在分解初期,水合物分解推动力(即逸度差)较小;随着分解的进行,相应的逸度差增大,同时动力学反应速度是温度的函数,也是逐渐增大的,但是水合物粒子总表面积是先增大再减小的[4],基于上述因素导致水合物分解速率表现出先增大到最大值而后下降为零的变化特征。
图6中也描述了水合物降压分解过程中累计产气量变化。从图6中可以看出,在本实验条件下,累积产气体积的变化规律同普通油气藏相似,初始时刻产量上升较快,然后逐渐平缓,到末期产量增加幅度已经很小了。在60 min时累积产气体积达到最大值为7 082cm3。
3.3 边界传热对分解速率的影响
在降压法开采甲烷水合物过程中,边界传热的影响是非常重要的,文献[3]模拟了水合物藏降压开采情形,发现在开采过程中会出现冰的生成,导致孔隙堵塞阻碍了气液流动,造成了水合物的分解速率下降。鉴于李淑霞已对降压幅度以及降压速度的影响进行了实验研究,因此本论文主要对边界传热对降压开采效果的影响进行研究。
通过采用不同的恒温槽升温速率,共进行了3个周期的甲烷水合物等容合成与分解实验,基本数据见表1。
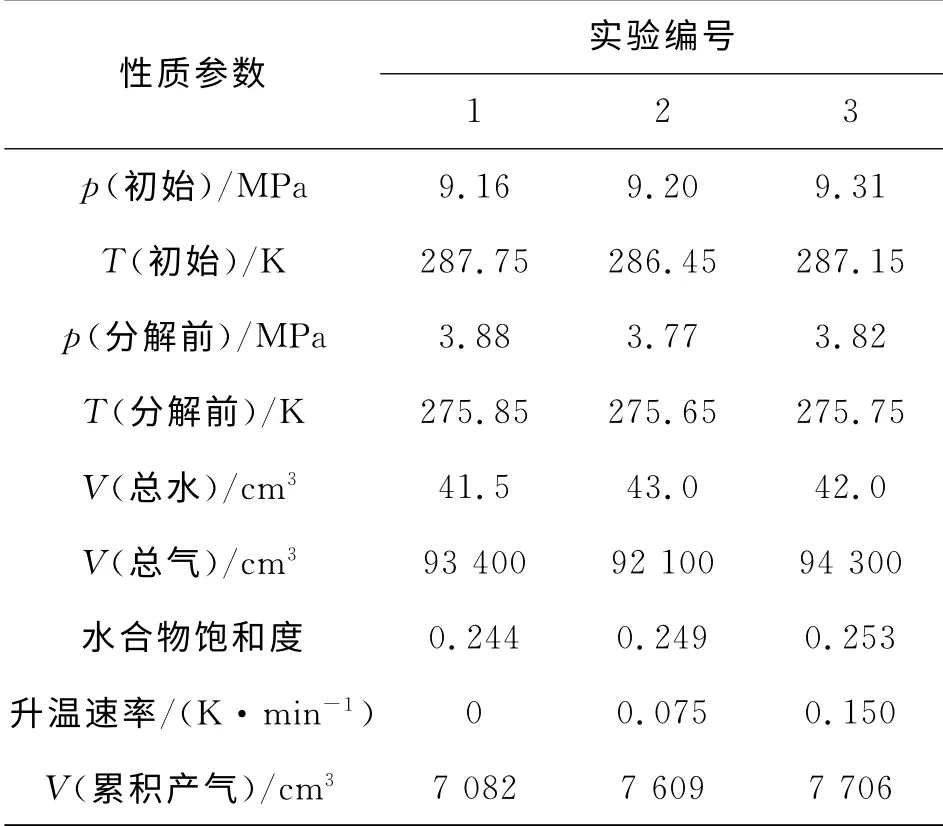
表1 甲烷水合物不同升温速率分解实验基本数据Table 1 The experiment data for hydrate dissociation with different heating rate
图7为不同边界传热条件下产气速率随时间变化曲线。从图7中可以看出,当边界温度以一定速率增加时,产气速率曲线发生了改变,分析实验设备可知采用的流量计最大量程为5cm3/s,反应釜中自由气还未排出时,较快的边界传热导致了水合物分解速度的加快,这也导致了水合物完全分解所需时间减少。
图8为不同边界传热条件下累积产气体积随时间变化曲线,随着升温速率的增加,累积产气体积增加,同时达到最终值所需时间大大减少。
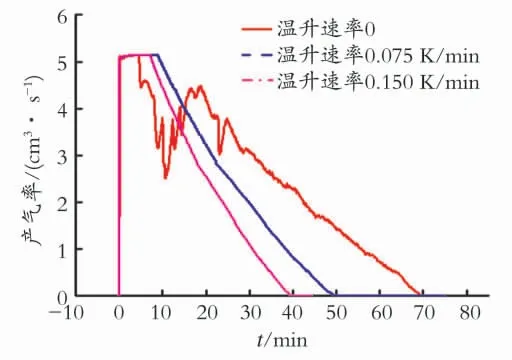
图7 不同升温速率条件下产气速率随时间变化曲线Fig.7 Time evolution of the gas generation rate for different heating rate

图8 不同升温速率条件下累积产气体积变化曲线Fig.8 Time evolution of the cumulative gas production for different heating rate
4 结论
(1)搭建了甲烷水合物生成和分解实验系统,能够进行多孔介质中甲烷水合物的生成、分解、相平衡测试等实验。
(2)进行了玻璃砂中甲烷水合物的相平衡测定实验,对比相关文献发现非常吻合。同时发现在大孔径条件下,甲烷水合物相平衡曲线与纯水中基本一致。
(3)进行了甲烷水合物降压分解实验,表明水合物分解过程是一个受压力驱动、分解速度以及传热影响的复杂过程,单纯靠降压而边界绝热时会导致分解减慢直至水合物分解停止。
(4)研究了边界传热对甲烷水合物降压分解的影响,发现随着恒温槽升温速率的提高,水合物分解速度加快,累积产气体积也迅速达到最大值。在多孔介质渗透率较大条件下,水合物分解主要取决于温度变化,也即传热为水合物分解控制机理。
[1] 李淑霞.天然气水合物开采物理模拟与数值模拟研究[D].东营:中国石油大学,2006.
[2] 樊栓狮,石磊,郭彦坤,等.甲烷气体水合物相平衡测试新装置及新方法[J].天然气工业,2001,21(3):71-73.
[3] Sun X,Mohanty K K.Kinetic simulation of methane hydrate formation and dissociation in porous media[J].Chemical Engineering Science,2006,61(11):3476-3495.
[4] 冯自平,沈志远,唐良广,等.水合物降压分解的实验与数值模拟[J].化工学报,2007,58(6):1548-1553.
[5] Thakore J L,Holder G D.Solid vapor azeotropes in hydrate-forming systems[J].Industrial &Engineering Chemistry Research,1987,26(3):462-469.
[6] Adisasmito S,Frank R J,Dendy E,et al.Hydrates of carbon dioxide and methane mixtures[J].Journal of Chemical &Engineering Data,1991,36(1):68-71.
[7] Uchida T,Ebinuma T,Takeya S,et al.Effects of pore sizes on dissociation temperatures and pressures of methane,carbon dioxide,and propane hydrates in porous media[J].Journal of Physical Chemistry B,2002,106(4):820-826.
[8] Smith D H,Joseph W W,Kal S,et al.Equilibrium pressure and temperatures for equilibria involving SI and SII Hydrate,liquid water,and free gas in porous media[C].Proceedings of the Fourth International Conference on Gas Hydrates,Yokohama,Japan:Heat Transfer Society of Japan,2002,295-300.
[9] Zhang W,Wilder J W,Smith D H.Interpretation of ethane hydrate equilibrium data for porous media involving hydrate-ice equlibria[J].AIchE Journal,2002,48(10):2324-2331.
[10] Zhang W,Wilder W,Smith D H.Methane hydrate-ice equilibria in porous media[J].Journal of Physical Chemistry B,2003,107(47):13084-13089.
[11] Zhang W,Wilder W,Smith D H.Equilibrium pressure and temperatures for equilibria involving hydrate,ice,and free gas in porous media[C].Proceedings of the Fourth International Conference on Gas Hydrates,Yokohama,Japan:Heat Transfer Society of Japan,2002,321-326.
[12] Anderson R,Llamedo M,Tohidi B,et al.Experimental measurement of methane and carbon dioxide clathrate hydrate equilibria in mesoporous silica[J].Journal of Physical Chemistry B,2003,107(15):3507-3514.
[13] Anderson R,Llamedo M,Tohidi B,et al.Characteristics of clathrate hydrate equilibria in mesopores and interpretation of experimental data[J].Journal of Physical Chemistry B,2003,107(15):3500-3506.
[14] Kim H C,Bishnoi P R,Heidemann R A,et al.Kinetics of methane hydrate decomposition[J].Chemical Engineering Science,1987,42(7):1645-1653.
[15] Englezos P,Kalogerakis N,Dhalabhai P D,et al.Kinetics of formation of methane and ethane gas hydrate[J].Chemical Engineering Science,1987,42(11):2647-2658.
[16] Englezos P,Kalogerakis N,Dhalabhai P D,et al.Kinetics of formation of from mixtures og methane and ethane[J].Chemical Engineering Science,1987,42(11):2659-2666.
[17] Clarke M,Bishnoi P R.Determination of the intrinsic rate of ethane gas hydrate decomposition[J].Chemical Engineering Science,2000,55(21):4869-4883.
[18] Clarke M,Bishnoi P R.Determination of the active energy and intrinsic rate constant of methane gas hydrate decomposition[J].Canada Journal of Chemical Engineering,2001,79(2):143-147.

