原位水热合成La1-xCexCoO3/SBA-15钙钛矿型催化剂和CO催化氧化反应性能的研究
李金林,杨 武,张煜华,赵福真
(中南民族大学 催化材料科学湖北省暨国家民委-教育部共建重点实验室,武汉 430074)
汽车尾气的主要污染成分为CO,在大气中分布最广、数量最多,也是燃料燃烧过程中生成的主要污染物之一,尾气所造成的污染日益受到全球关注和重视[1],其中采用催化剂净化处理汽车尾气,是减少汽车排放污染的主要措施之一.汽车尾气净化催化剂多为负载型催化剂,活性组分主要是以贵金属Pt、Rh、Pd为活性组分的“三效”催化剂[2],但此类催化剂价格昂贵,资源有限.故减少贵金属的用量或利用非贵金属替代贵金属,已成为汽车尾气净化催化剂的发展趋势.近年来,ABO3型稀土钙钛矿型氧化物因其独特的物理化学性质获得广泛研究.一般而言,B阳离子的氧化态和结构缺陷(阴离子和阳离子空缺)可通过以不同氧化态的金属(对应用A+,B+表示)部分取代A或B加以改变,因此通过仔细选择A+和B+可改变钙钛矿的催化性能[3,4],达到特定反应要求.
本文采用原位水热合成法制备了一系列La1-xCexCoO3/SBA-15催化剂,采用X-射线粉末衍射(XRD),氮气物理系脱附测试,透射电子显微镜(TEM),氢气程序升温还原(H2-TPR)等表征手段对催化剂进行表征,并对催化剂的CO催化氧化性能进行评价,以考察Ce掺杂对催化剂结构和CO催化氧化性能的影响.
1 实验部分
1.1 样品、试剂和仪器
聚氧乙烯醚-聚氧丙烯醚-聚氧乙烯醚三嵌段共聚表面活性剂(P123,Aldrich),正硅酸四乙酯(TEOS,上海国药集团化学试剂有限公司),浓盐酸(HCl,河南开封化学试剂厂),硝酸镧(La(NO3)3·6H2O上海国药集团化学试剂有限公司),硝酸铈(Ce(NO3)3·6H2O上海国药集团化学试剂有限公司),硝酸钴(Co(NO3)2·6H2O上海国药集团化学试剂有限公司),柠檬酸(上海国药集团化学试剂有限公司),所有试剂均为分析纯.
X-射线粉末衍射仪(Bruker Advanced D8,德国布鲁克公司,Cu靶,38 kV,2θ:小角度为0.4°~5°;大角度为10°~80°),物理吸附仪(Autosorb-1-C-TCD-MS,美国康塔公司),气相色谱仪(Agilent Micro-GC 3000A型),催化剂多功能表征仪(AMI-200型,美国ZETON ALTAMIRA公司).
1.2 催化剂的制备
采用原位水热合成法制备La1-xCexCoO3/SBA-15钙钛矿型催化剂.将4 g的P123、按化学计量的硝酸镧、硝酸铈、硝酸钴和柠檬酸(n(总金属)︰n(柠檬酸)=1︰3)溶于pH=1.5的150 mL HCl中,40 ℃持续搅拌,将8.66 g (9.2 mL)的正硅酸四乙酯逐滴加入上述溶液中,充分搅拌24 h.再将所得的混合溶液转移至不锈钢反应釜中,100 ℃水热条件下处理24 h,并将所得混合溶液干燥后研磨.在空气气氛下以1℃/min的升温速率先后在550 ℃焙烧6 h,650 ℃焙烧6 h,得催化剂La1-xCexCoO3/SBA-15(x=0.05~0.25).
1.3 催化剂的表征
测试样品的孔结构先在200 ℃下脱气除尽空气和水分等杂质,再在-196 ℃测得其等温吸附-脱附曲线.由BJH脱附曲线计算求得孔体积和平均孔径,由N2吸附等温线结合BET方程求得比表面积.
在催化剂多功能表征仪测试氢气程序升温还原(H2-TPR),以热导池检测器(TCD)记录氢气信号,TCD电流为55 mA,信号放大倍数为5,数据采集速率为10.0 s/point.
1.4 CO催化氧化反应活性测试
催化剂的CO催化氧化反应是在内径12mm的固定床反应器上进行,将1g催化剂装入反应器内,在常压下,通入反应气(3%CO和空气,空速GHSV=52000h-1)升温进行反应,由气相色谱仪在线分析尾气成分后得到气相的组成,检测器为TCD检测器.CO 的转化率计算公式如下:
CO转化率(%)=
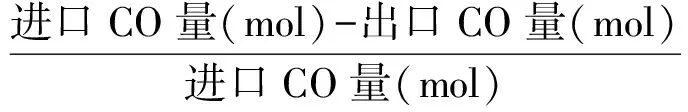
2 结果与讨论
2.1 X-射线粉末衍射
催化剂的小角XRD 衍射图见图1.由图1可见,在0.9°,1.6°和1.9°处有3个明显的衍射峰,分别对应于二维六方有序结构的(100),(110)和(200)晶面.这说明用原位水热法制备的钙钛矿型催化剂具有类似于SBA-15介孔有序分子筛的二维六方介孔结构[5].随着Ce 掺杂量的增加,(100)晶面的衍射峰逐渐减弱,归因于钙钛矿颗粒占据和堵塞了部分孔道致其结构有序性降低.

2θ/(°)
催化剂的大角XRD 衍射图谱见图2.由图2可见,所有催化剂均保持LaCoO3(23.2°,32.7°,40.7°,47.3°,53.5°,58.7°,69.2°,78.8°)钙钛矿型结构.随着Ce掺杂量的增加,LaCoO3的衍射峰先增强后减弱,当x(Ce)≥0.20时,CeO2(27.3°)和Co3O4(2θ=36.8°)物相的衍射峰增强,说明LaCoO3钙钛矿的颗粒尺寸先增大后减小.说明随着Ce 的掺杂的增加,钙钛矿结构的结晶度降低,进一步产生La1-xCexCoO3晶格缺陷,在A 位离子上形成了具有晶格缺陷的3种不同(La1-xCexCoO3-δ,CeO2和Co3O4)物相的混合体系.
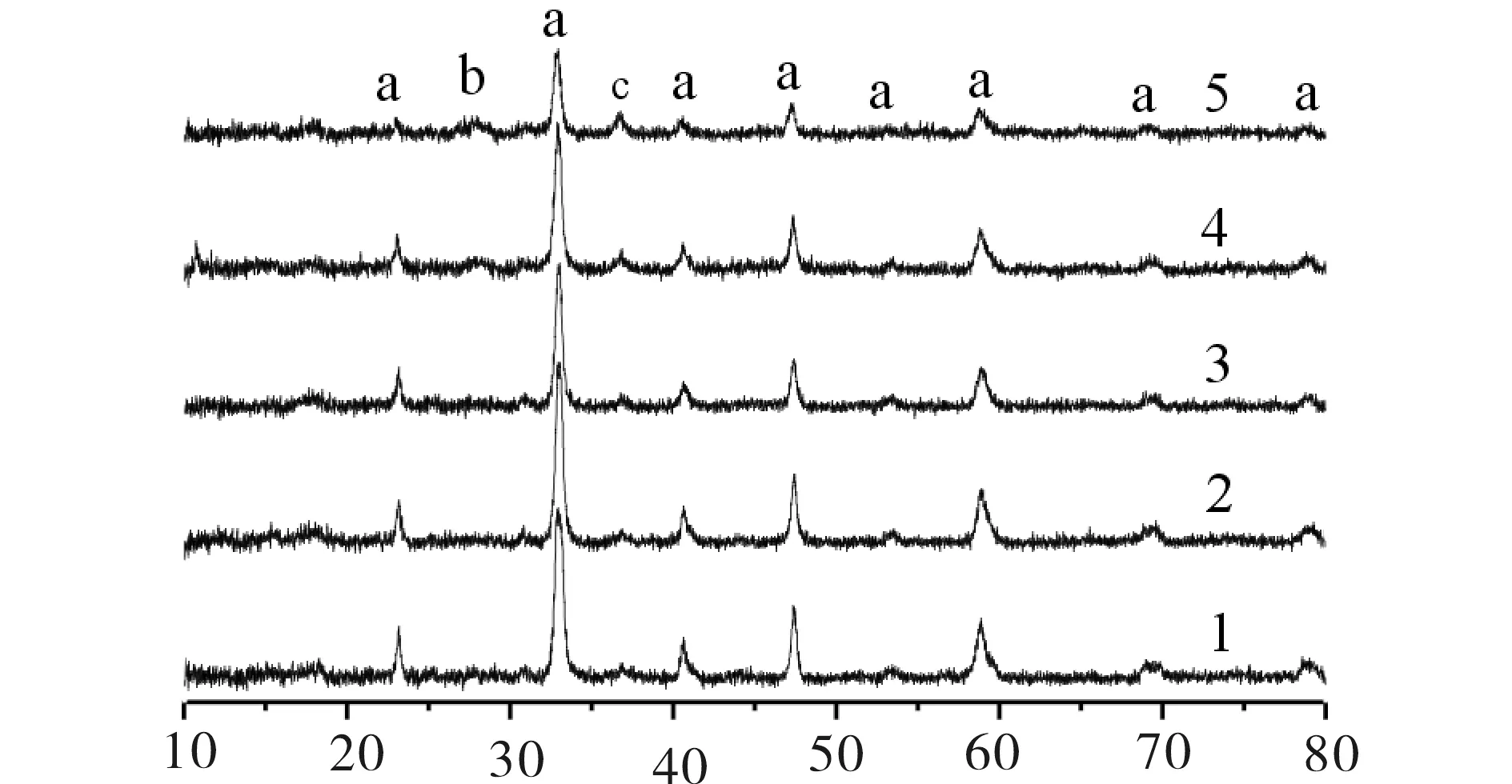
2θ/(°)
2.2 氮气物理吸附-脱附
催化剂的氮气物理吸附-脱附曲线见图3.由图3可见,所有催化剂都具有IV 型吸附等温线,且伴有H1 型滞后环.在相对压力p/p0=0.6~0.8 处,出现了闭合环,说明催化剂具有二维六方结构的中孔特征.随着Ce 含量的增加,闭合环有所缩小,是由于部分钙钛矿颗粒进入了载体孔道内导致孔容减小.

2θ/(°)
不同Ce 掺杂量的催化剂结构参数如表1 所示.由表1可见,随着Ce掺杂量的增加,催化剂的比表面积依次减小,但平均孔径基本未改变,因为随着Ce掺杂量的增加,钙钛矿结构有不同程度的破坏,使其比表面积下降.

表1 催化剂的孔结构参数
a粒径结果由XRD算得
2.3 氢气程序升温还原
不同Ce 掺杂量的钙钛矿型催化剂的H2-TPR 图谱见图4.由图4可见,此催化剂主要有2个还原峰.第1个还原峰位于300 ~500 ℃ 内,属于钙钛矿型催化剂表面吸附氧的还原和Co3+还原为Co2+过程,低温还原峰的高低反映了催化剂与氧的结合能力.第2个还原峰在500~600 ℃ 内,最高的还原温度为600 ℃,对应于Co2+还原为Co0[6],此时钙钛矿型结构完全被破坏,高温的还原峰的高低反映了催化剂结构的稳定性,这2步还原过程是根据LaCoO3[7]来推断的.由图4可见,随着Ce 含量的增加,第1个还原峰的还原温度逐渐向低温区移动,说明表面吸附氧和氧空穴处的化学吸附氧更易迁移[8].低温区和高温区的还原峰面积均随着Ce 含量的增加而增加,说明催化剂的表面吸附氧和晶格氧均有所增加.
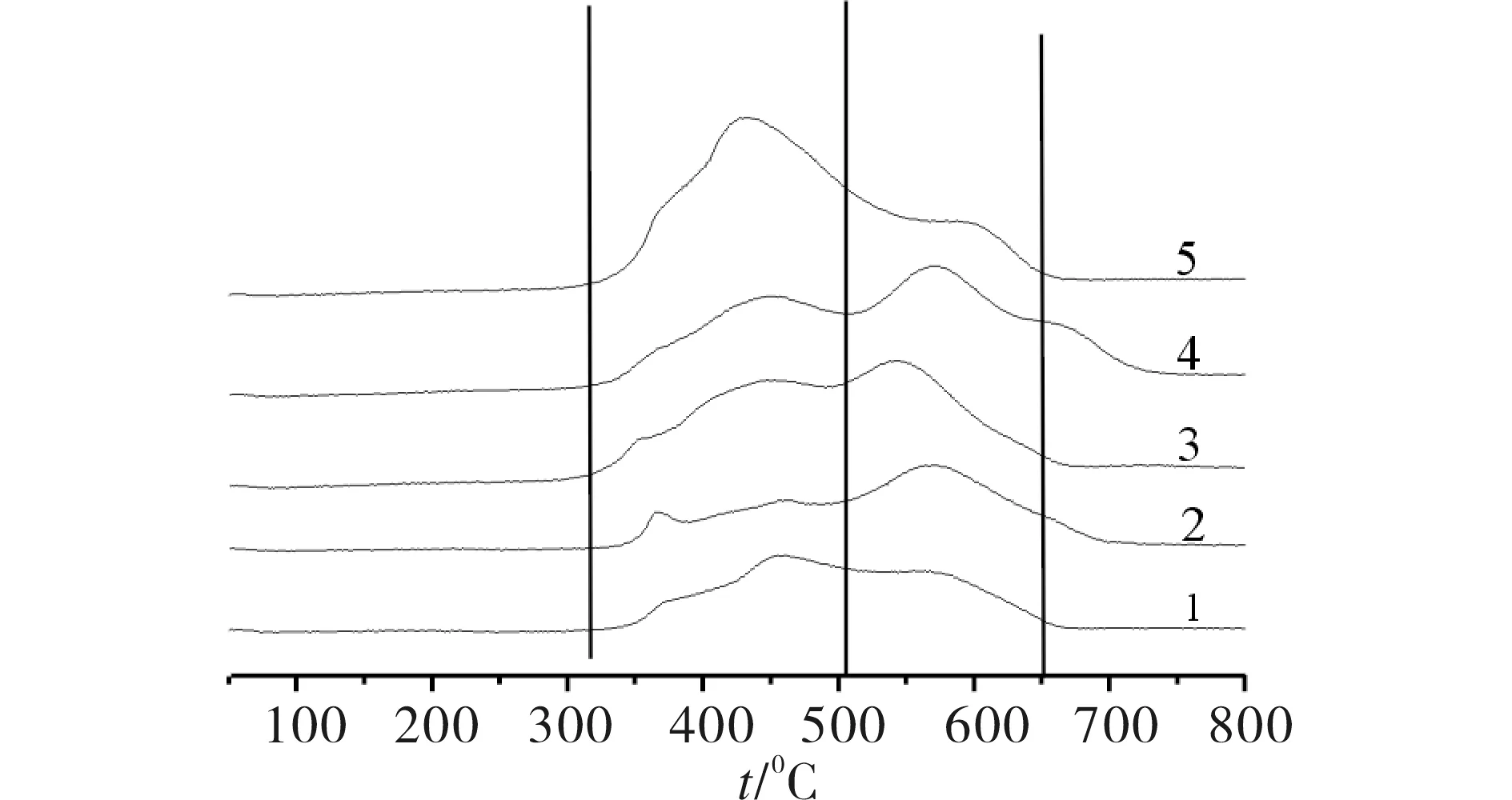
Ce掺杂量:1)0.05;2)0.10;3)0.15;4)0.20;5)0.25
2.4催化剂的活性测试
催化剂的CO 氧化活性测试结果如图5 所示.由图5可见,随着Ce 掺杂量增加,CO 的催化活性先增加后降低.当Ce 的掺杂量为0.2 时,催化剂的CO 催化氧化活性最高,起活温度点是245 ℃,当温度达到380 ℃ 时,CO的转化率达到100%(完全转化).而x=0.05时,催化剂的起活温度点虽然比x=0.2时低了20 ℃,当温度升高至430 ℃时,CO的转化率仅为92.09 %(未完全转化).当x=0.1 时,催化剂的起活点在240 ℃以下,但是当温度升至430 ℃时其转化率为97.45%(未完全转化),这说明催化剂的活性主要与掺杂后所形成的钙钛矿晶格缺陷有关.
当Ce 的掺杂量为20%时,形成了更多的钙钛矿晶格缺陷.Voorhoeve R J H[9]认为,CO催化氧化反应在低温区是一种表面上的反应,参加反应的氧化物种是表面的吸附氧.由于Ce 掺杂量的增加,催化剂多以La1-xCexCoO3-δ钙钛矿、CeO2相和Co3O4相的混合体系存在,导致了较多的A 位离子的空缺和更多的氧空位的产生,提高了催化活性.Kirchnerova J等[10]报道,当Ce 掺杂部分取代La 之后,由于Ce 不能完全取代A 位上的La,导致形成了A 位有缺陷的钙钛矿型结构,使晶格氧的浓度增加,即催化剂的活性受钙钛矿型结构缺陷的影响.
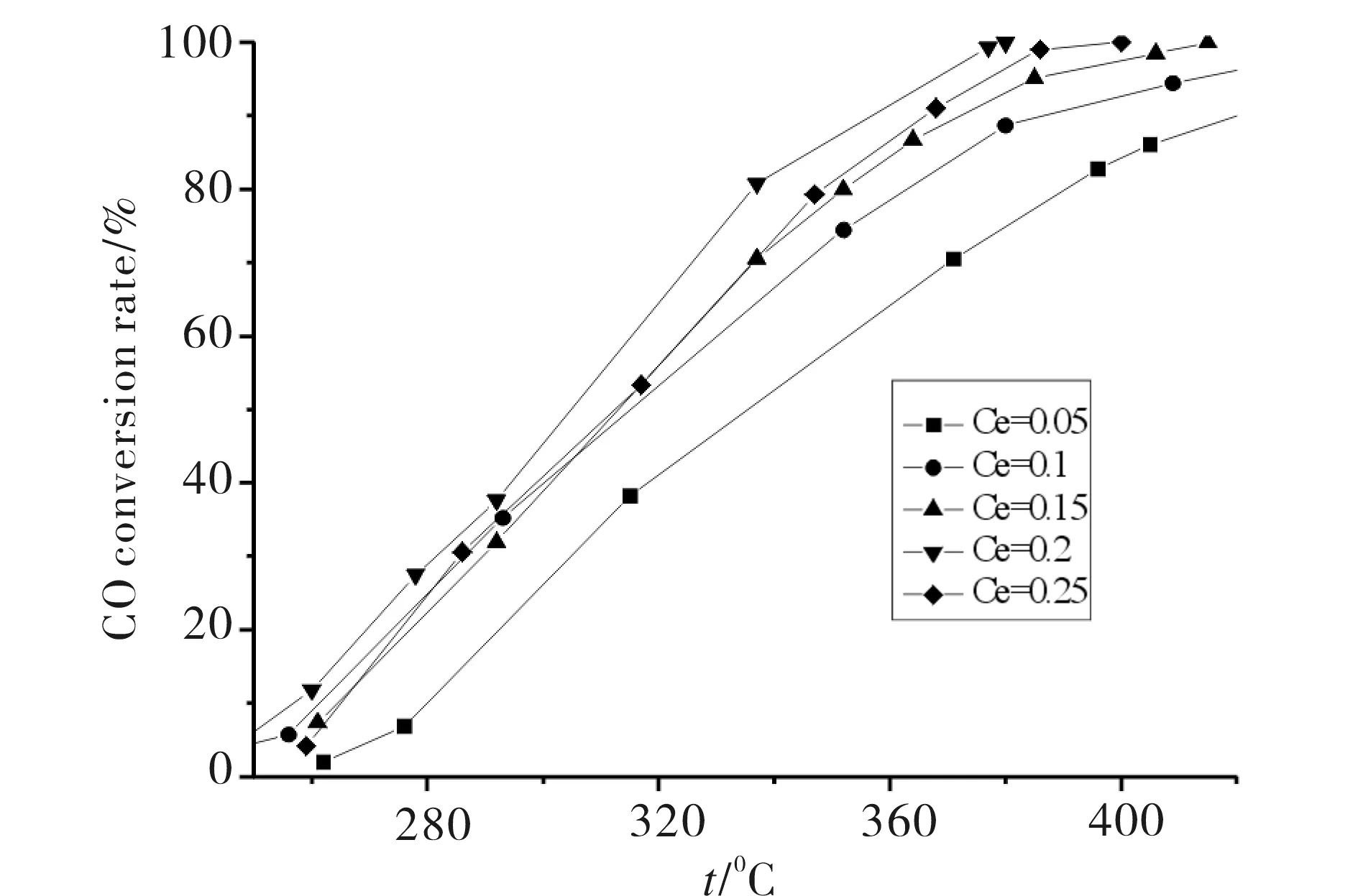
图5 Ce掺杂对催化剂的CO催化氧化活性的影响
3 结语
本文采用原位水热合成法,以硝酸镧、硝酸铈、硝酸钴和柠檬酸为原料,一步合成了钙钛矿型复合氧化物催化剂30%La1-xCexCoO3/SBA-15(x=0.05~0.25),研究了Ce 的不同掺杂量对催化剂结构及对CO 催化氧化反应的性能.结果表明:原位合成的钙钛矿型复合氧化物催化剂30%La1-xCexCoO3/SBA-15(x=0.05~0.25)具有类似SBA-15 的二维六方有序中孔结构,随着Ce 掺杂量增加,钙钛矿型催化剂颗粒尺寸先增加后降低,CO 催化氧化反应的活性先增加后降低.当Ce 的掺杂量为0.2 时,催化剂在380 ℃ 时,CO 的转化率达到100%(完全转化).这是由于Ce 的掺杂导致钙钛矿结构缺陷的变化,使晶格氧浓度增加,吸附氧更易移动,有利于提高CO 催化氧化活性.
[1]Shinjoh H. Noble metal sintering suppression technology in three-way catalyst: automotive three-way catalysts with the noble metal sintering suppression technology based on the support anchoring effect[J]. Catal Surv Asia,2009,13(3): 184-190.
[2]Heck R M,Farrauto R J. Automobile exhaust catalysts[J]. Appl Catal A-Gen,2001,221(1): 443-457.
[3]王东辉,程代云,郝郑平,等.纳米金催化剂上CO低(常)温氧化的研究[J].化学进展,2002,14(5):360-367.
[4]郝郑平,安立敦,王弘立.负载型金催化剂的制备、催化性能及应用前景[J].分子催化,1996,10(3):235-240.
[5]Han Y J,Kim J M,Stucky G D. Preparation of noble metal nanowires using hexagonal mesoporous silica SBA-15[J]. Chem Mate,2000,12(8): 2068-2069.
[6]Tien-Thao N,Alamdari H,Zahedi-Niaki M H,et al. LaCo1-xCu+O3-δperovskite catalysts for higher alcohol synthesis[J]. Appl Catal A-Gen,2006,311: 204-212.
[7]Navarro R M,Alvarez-Galvan M C,Villoria J A,et al. Effect of Ru on LaCoO3perovskite-derived catalyst properties tested in oxidative reforming of diesel[J]. Appl Catal B:Environ,2007,73(3): 247-258.
[8]Kharas K C C,Lunsford J H. Catalytic partial oxidation of methane over barium metaplumbate BaPbO3:possible involvement of peroxide ion[J]. J Am Chem Soc,1989,111(6): 2336-2337.
[9]Voorhoeve R J H,Johnson D W,Remeika J P,et al. Perovskite oxides: Materials science in catalysis[J]. Science,1977,195(4281): 827-833.
[10]Alifanti M,Kirchnerova J,Delmon B. Effect of substitution by cerium on the activity of LaMnO3perovskite in methane combustion[J]. Appl CatalA-Gen,2003,245(2): 231-244.

