马钱子碱对人宫颈癌细胞HeLa及未成年小鼠子宫增质量的影响
孔建明
(袁浦社区卫生服务中心中医科,浙江 杭州 310024)
传统中药马钱子,为马钱子科植物马钱子的干燥成熟种子,具有通络止痛、散结消肿的功效。马钱子碱 (Brucine)是从马钱子中提取的吲哚型结构的生物碱,是一种白色晶体,是马钱子组成和发挥药效的主要成分之一[1]。研究显示马钱子碱的药理活性主要集中在镇痛作用[2-4]、抗炎及免疫系统作用[5-8]、心血管作用[9-11]和抗肿瘤作用[12-14]等几个方面。
妇科肿瘤已成为全球妇女的头号恶性肿瘤疾病。近年来关于妇科肿瘤与雌激素分泌表达异常之间的分子调控机制已成为国内外研究的重点。临床及实验研究均认为雌激素可通过雌激素受体调节机体的多种信号途径,引起内皮细胞增殖、凋亡、运动、芽生、黏附等特性改变,导致肿瘤血管生成的异常,从而最终影响到肿瘤发生、发展、转移过程。宫颈癌是女性生殖系统常见的恶性肿瘤,其病死率在所有妇女癌症病死率中位居第二,且近年来宫颈癌发病率存在逐年增加和发病年龄日趋年轻化的问题[15],因此研究药物的抗宫颈癌活性具有重要意义。
本研究通过检测雌二醇、马钱子碱以及两者联合作用分别对HeLa细胞生长的增殖和抑制作用,探讨可能的作用机制,并通过马钱子碱对未成年小鼠子宫发育的影响,为其用于临床治疗肿瘤提供实验依据。
1 材料与方法
1.1 材料 马钱子碱 (购自中国药品生物制品检定所),人宫颈癌细胞系HeLa(购自中国医学科学院细胞库),雌二醇 (Sigma公司),DMEM培养基和胰酶 (美国Gibco),新生小牛血清 (杭州四季青生物材料研究所),3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐 [MTT,3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide](Sigama 公司),乙二胺四乙酸 (EDTA)(华美公司)。SPF级昆明种(ICR)断乳雌性小鼠60只,20日龄,由浙江中医药大学实验动物中心提供,饲养环境温度为 (22±2)℃,相对湿度60% ±20%,昼夜周期为12 h/12 h,自由饮水进食。
1.2 药物处理 分别配制0.1 mol/L雌二醇和800 mg/L马钱子碱的DMSO贮存液,4℃冰箱中保存备用。实验时雌二醇用培养液稀释依次梯度稀释成 10-5、10-6、10-7、10-8、10-9、10-10、10-11mol/L 浓度,马钱子碱依次梯度稀释成终质量浓度50、100、200、400、800 mg/L。称取0.05 g MTT溶于10 mL PBS中,终质量浓度为5 mg/mL,过滤除菌,避光保存于4℃冰箱,两周内有效。
1.3 HeLa细胞系培养 将HeLa细胞培养于含10%小牛血清的DMEM(1 L含NaHCO32 g;HEPES 3.57 g)中,置于37℃ 5%CO2的培养箱中。细胞均贴壁生长,每3 d传代。传代时移去旧培养液,以D-Hanks液洗涤2次,加入0.03%EDTA和0.125%胰酶消化2~5 min至细胞分散,离心 (1000 r/min,5 min),培养液重新悬浮,接种于培养瓶,传代率为1∶2或1∶3。
1.4 MTT比色实验 培养HeLa细胞至对数期,胰酶消化用含5%小牛血清的DMEM将细胞制成5×104/mL的细胞悬液,以每孔200 μL接种于96孔板,37℃,5%CO2条件培养。24 h后取不同质量浓度的马钱子碱加至细胞培养液中,实验设阴性对照组和各种药物浓度实验组。每孔加入含5%小牛血清的DMEM配制的药液10 μL,每种药物浓度10个孔,12 h后采用倒置显微镜观察细胞形态变化,并拍照记录。加药48 h后每孔加入20 μL MTT(5 mg/mL),37℃继续孵育4 h后小心吸去上清液,然后每孔加入DMSO 200 μL,振荡器振荡10 min,充分混匀后于490 nm处测定各吸光度值,按公式计算细胞增殖抑制率。

1.5 子宫增质量实验 将50只离乳ICR小鼠 (20日龄)按体质量()随机分为5组,每组10只,分别为阴性对照组 (生理盐水),马钱子碱质量浓度组共3组,在体浓度分别为2、4、8 mg/(kg·d),分别以0.1、0.2、0.4 mg/mL的马钱子碱溶液进行灌胃。阳性对照组雌二醇4 mg/(kg·d)。对上述5组小鼠同一时间称量体质量后,进行灌胃。每天定时灌胃1次,连续3 d,给药期间每天称量体质量,根据体质量调整药量。末次灌胃24 h后候颈椎脱臼法处死小鼠,迅速解剖并分离子宫周围的脂肪和系膜组织,剪取子宫,用生理盐水润洗,滤纸同等时间 (30 s)吸干子宫表面血渍和子宫内液,于万分之一天平上称量子宫湿质量 (采用双盲法)并记录有效数字,计算脏器系数(子宫湿体质量),剪取分组标本制作病理切片。
1.6 统计学处理 采用spss18.0软件统计包对各组数据进行统计分析,各项数据均以平均数±标准差()表示,采用双样本t检验进行组间分析,以P<0.05为差异有显著性。
2 结果
2.1 雌激素促进HeLa细胞增殖 采用MTT法测定光密度(OD)(490 nm)值,与正常对照组比较,雌二醇 (10-8~10-5mol/L)呈剂量依赖性地促进HeLa细胞的增值,低于10-9mol/L的雌二醇对HeLa细胞的吸光度值无显著影响(见图1)。
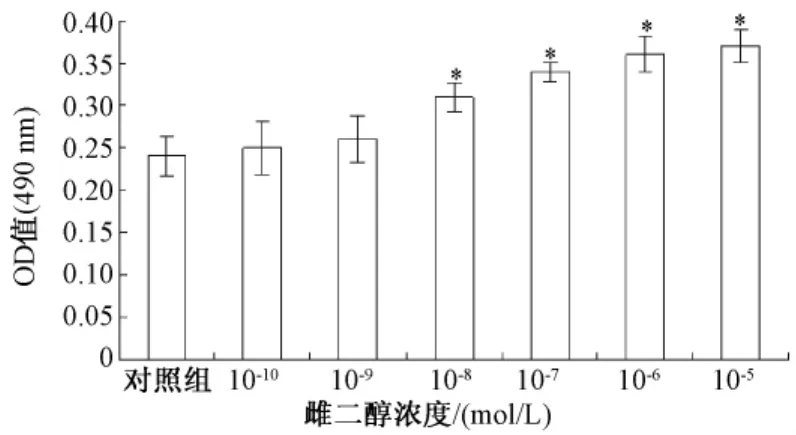
图1 雌二醇剂量依赖性的促进HeLa细胞增殖
2.2 不同质量浓度马钱子碱处理后的HeLa细胞形态 从图1中可以看到,与对照组相比,马钱子碱作用HeLa细胞后,出现可能的细胞凋亡现象,细胞皱缩变小、细胞间隙增加、悬浮细胞增多,随质量浓度的增大此形态变化更加明显。且在相同的视野下,细胞数也随质量浓度的增大而减少 (见图2)。

图2 不同质量浓度的马钱子碱处理HeLa细胞的形态变化结果 (×40)
2.3 不同质量浓度的马钱子碱对HeLa细胞增殖的影响对照组及50、100、200、400、800 mg/L的马钱子碱组对HeLa细胞作用48 h的增殖抑制率随着作用质量浓度的增加而增加,呈明显的剂量—效应关系 (P<0.05),OD值随质量浓度和时间的增加而降低 (P<0.05)。雌二醇显著的促进HeLa细胞的增殖作用,而马钱子碱对HeLa细胞有抑制作用,结果显示不同质量浓度的马钱子碱和10-8mol/L的雌二醇联合作用于HeLa细胞48 h后,相比单独的马钱子碱组增殖抑制率均有所下降 (见表1)。
2.4 马钱子碱对小鼠子宫增质量及子宫脏器系数的影响 将马钱子碱作用之后幼雌ICR小鼠子宫湿质量及子宫脏器系数的变化做了统计,具体结果见表2。由表2可见,与对照组相比较,以4 mg/(kg·d)的雌二醇对幼雌ICR进行灌胃3 d可显著促进小鼠的子宫增质量,与对照组相比具有显著性差异 (P<0.05);马钱子碱处理组,2、4、8 mg/(kg·d)剂量时均抑制未成年ICR小鼠的子宫增质量,与对照组相比具有统计学意义 (P<0.05),而且随着马钱子碱质量浓度的增加,子宫增质量抑制效应明显。
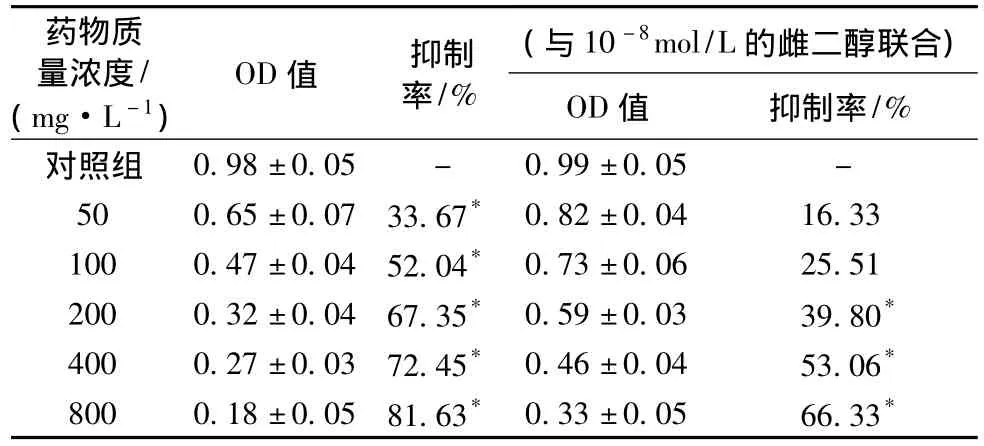
表1 不同质量浓度的马钱子碱及联合作用对HeLa细胞作用于48 h后的抑制率 (n=10)
表2 马钱子碱作用后幼雌ICR子宫湿质量及子宫脏器系数的变化 ()

表2 马钱子碱作用后幼雌ICR子宫湿质量及子宫脏器系数的变化 ()
注:与对照组比较,*P<0.05。
实验组 剂量/(mg·kg-1)平均子宫质量/g 脏器系数生理盐水组 对照 0.04432±0.00478 0.0031±0.0004雌二醇组 4 0.07617±0.01384*0.0050±0.0008*马钱子碱处理组 2 0.03454±0.00476*0.0025±0.0009*马钱子碱处理组 4 0.02947±0.00398*0.0020±0.0004*马钱子碱处理组 8 0.01962±0.00223*0.0014±0.0005*
3 讨论
马钱子作为散血热、消肿、止痛的药物,具有显著的镇痛、抗炎、抗肿瘤、兴奋中枢等作用,用于风湿顽痹、麻木瘫痪、痈疽肿痛、小儿麻痹后遗症和类风湿性关节痛等症[16-17]。马钱子碱是中药马钱子的主要有效成分且具有吲哚型的化学结构,这一类结构物质被认为具有潜在的抗肿瘤活性,如长春碱,粗榧生物碱等大多对肿瘤有生长抑制作用,并可诱导肿瘤细胞的凋亡[18-19],因此从植物中寻找抗肿瘤药物也成为极为重要的研究方向。体外研究发现,马钱子碱可显著抑制多种细胞的增殖[20],而且对小鼠的实体瘤均表现出明显的抑瘤作用,能有效抑制移植性肝癌模型荷瘤小鼠体内肿瘤生长,宋爱英等[21]发现一定质量浓度的马钱子水煎液的抑瘤率达到37.8%。马钱子碱能引起HepG-2细胞的萎缩,阻碍细胞的形成,使DNA片段断裂,最终导致HepG-2细胞凋亡[22]。余志艳等[23]发现马钱子碱对乳腺癌细胞MDA-MB-231细胞具有增殖抑制作用,曲雷鸣等[24]研究表明,马钱子碱对胃癌细胞株SGC7901的增殖有明显的抑制作用。张蕻等[25]研究发现马钱子碱高剂量组对小鼠移植性肿瘤H22的抑瘤率达到38.9%,证明了马钱子碱对小鼠移植性肿瘤H22的生长有明显的抑制作用。以上结果证明马钱子碱是很有前途的抗肿瘤药物,但目前关于马钱子碱抗宫颈癌作用的研究很少,有待进一步深入探索。HeLa细胞作为常用的生物材料被广泛应用于药物抗肿瘤的药理活性研究,本实验通过体外细胞增殖实验来研究马钱子碱的抗肿瘤活性。本研究发现不同质量浓度的马钱子碱溶液作用于HeLa细胞后会出现细胞凋亡现象,而且随着药物质量浓度的上升,细胞增殖抑制率逐渐升高。
之前的研究[26]发现宫颈癌细胞HeLa的发生发展与雌激素水平的变化具有很大关系,雌二醇通过促进细胞周期的转化和细胞内Ca2+的释放,显著的促进宫颈癌细胞的增殖作用,提示雌二醇在宫颈癌的发生发展过程中可能起着重要的调节作用,本研究也发现雌激素可以明显促进HeLa细胞的增殖并具有质量浓度梯度依赖效应,并且不同质量浓度的马钱子碱和的雌二醇联合作用于HeLa细胞48 h后,相比单独的马钱子碱组增殖抑制率均有所下降,可以推测马钱子碱对天然雌激素可能具有拮抗作用。另外,出生20 d左右的未成年雌性小鼠处于雌激素分泌最为旺盛的阶段,主要表现为这个阶段的子宫快速发育,本实验通过研究这段时间马钱子碱对未成年雌性小鼠子宫生长的影响可以判断马钱子碱的抗雌激素样活性,实验结果发现马钱子碱抑制小鼠子宫发育,同样可以推测马钱子碱对天然雌激素可能具有拮抗作用,这也可能是马钱子碱抑制HeLa细胞增殖的作用机制,相关的分子机制有待后续研究。
[1]魏 宁,张松伟.马钱子的研究进展[J].航空军医,2004,32(3):131.
[2]殷 武.马钱子生物碱的镇痛研究[D].南京:南京中医药大学,2000.
[3]朱建伟,武继彪,李成韶,等.马钱子碱镇痛作用及其药效动力学研究[J].中国中医药科技,2005,12(3):166-167.
[4]朱建伟,武继彪,李成韶,等.复方马钱子碱的镇痛作用及其药效动力学初步观察[J].中国中医药信息杂志,2005,12(9):36-37.
[5]赵红卫,翁世艾,朱燕娜,等.马钱子碱对小鼠淋巴细胞功能的影响[J].中国药理学通报,1999,15(4):354-356.
[6]徐丽君,魏世超,陆付耳,等.马钱子若干组分治疗实验性关节炎的比较研究[J].同济医科大学学报,2001,30(6):564-565.
[7]Yin W,Wang TS,Yin FZ,et al.Analgesic and anti-inflammatory properties of brucine and brucine N-oxide extracted from seeds of Strychnos nux-vomica[J].J Ethnopharmacol,2003,88(2-3):205-214.
[8]张 梅,李 平,陈朝晖,等.马钱子碱对一氧化氮诱导软骨细胞凋亡的影响[J].中国临床康复,2003,7(26):3554-3555.
[9]李明华,万光瑞,朱 明,等.马钱子碱对实验性心律失常的影响[J].新乡医学院学报,1997,14(2):101-103.
[10]李明华,张贵卿,赵德华.马钱子碱对豚鼠心脏乳头肌慢反应动作电位的影响[J].中药药理与临床,1997,13(4):19-21.
[11]周建英,卞慧敏,马 骋,等.马钱子碱和马钱子碱氮氧化物抗血小板聚集及抗血栓形成作用的研究[J].江苏中医,1998,19(4):41-43.
[12]邓旭坤,蔡宝昌,殷 武.等.马钱子碱对小鼠肿瘤的抑制作用[J].中国天然药物,2005,3(6):392-396.
[13]Deng X K,Yin F Z,Cai B C,et al.The apoptotic effect of brucine from the seed of Strychnos nux-vomica on human hepatoma cells is mediated via Bcl-2 and Ca2+involved mitochondrial pathway[J].Toxicol Sci,2006,91(1):59-69.
[14]邓旭坤,蔡宝昌,吕晓宇,等.马钱子碱及其脂质体对移植性荷瘤小鼠抗肿瘤作用的对比研究[J].中草药,2006,37(3):389-393.
[15]朱晓武.17β雌二醇对宫颈癌细胞株生物学的影响和上皮性卵巢肿瘤微淋巴管内皮细胞的体外培养[D].武汉:华中科技大学,2010.
[16]邓旭坤,蔡宝昌.马钱子抗肿瘤药理研究及临床应用进展[C]//21世纪中医药-2004江苏省博士研究生学术论坛文集,南京:南京中医药大学,2004:168-173.
[17]罗 刚,吴世成.马钱子药理学及毒理学研究进展[J].科技信息,2007(31):351-352.
[18]迟德彪.钩吻素子体外抑制人结肠腺癌细胞生长并诱导其凋亡及其机制的探讨[D].广州:第一军医大学,2000,25-261.
[19]程 磊,周秀佳.植物生物碱抗肿瘤机制[J].中草药,2004,35(2):216-221.
[20]Lazareno S,Gharagozloo P,Kuonen D,et al.Subtype-selective positive cooperative interactions between brucine analogues and acetylcholine at muscarinic receptors:radioligand binding studies[J].Mol Pharmacol,1998,53(3):573-589.
[21]宋爱英,张国烈,刘松江,等.马钱子抗肿瘤作用的实验研究[J].中国中医药科技,2004,11(6):363.
[22]邓旭坤,蔡宝昌,殷 武,等.Brucine对Heps荷瘤小鼠的抗肿瘤作用和毒性的研究[J].中国药理学通报,2006,22(1):35-39.
[23]余志艳,李 平.马钱子碱对乳腺癌细胞MDA.MB.231作用的实验研究[J].安徽医药,2008,12(9),779-783.
[24]曲雷鸣,龚 伟.复方郁金片抗肿瘤的实验研究[J].辽宁中医药大学学报,2007,9(3):96-97.
[25]张 蕻,李燕玲,任连生,等.马钱子天南星对小鼠移植性肿瘤的抑瘤作用[J].中国药物与临床,2005,5(4):272-273.
[26]邹自英,袁成良,何亚平,等.雌激素对宫颈癌HeLa细胞增殖的影响及ERB的表达[J].四川医学,2003,12(24):1288-1291.

