水热法钛酸钠的制备与结构研究
刘义章,何 杰
(1.滁州职业技术学院,安徽滁州 239001;2.安徽理工大学化工学院,安徽淮南 232001)
近年来,钛酸盐的水热反应备受关注,用以制备纳米管、纳米线、钛酸盐晶须等纳米材料[1-4]。水热反应法制备的粉体因其结晶度高、晶粒完整、反应温度不高且烧结活性高成为钛酸盐物质制备主要方法之一。但水热反应法中前驱物和制备条件不同,制备出的钛酸盐的理化性能有所不同[5-9]。由于合成过程的反应机理尚不明确,导致控制目标产物的合成过程难度较大,造成实验的重现性较差,成为制约水热反应的关键;同时也为水热反应形成极大的研究空间。本次工作采用水热法制备出不同Ti/Na(摩尔比)的钛酸钠,研究探索水热反应中的钛源、反应温度和时间、碱溶液浓度(或用水量)等对钛酸盐结构的影响。
1 实验部分
1.1 钛酸钠的制备
TiO2、NaOH(AR,华东试剂工业公司经销)按Ti/Na=0.5,1.5,3(摩尔比)制取 Na2TinO2n+1(n=1,3,6)样品;用P25(AR,国药集团化学试剂有限公司)替代TiO2制备Na2TiO3一份;再以不同浓度的NaOH对同一系列样品做两份。
将NaOH、TiO2按计量关系称量后移入聚四氟乙烯高压反应釜内,然后进行超声(KQ-200KDB,昆山市超声仪器有限公司)混合,混合后将其在230℃下于程序控制箱式电炉(KS6-63-160,上海意丰电炉有限公司)中焙烧96 h;待冷却至室温后取出,洗涤、抽滤、烘干、研磨后进行表征。
将TiO2分别换成 Ti(OH)4、Ti(OC4H9)4再与NaOH反应制取Na2Ti3O7。反应温度仍为230℃,焙烧改为48 h,与上述样品进行对比实验。
1.2 钛酸钠的结构表征
X-射线粉末衍射(XRD):实验在D/max-3BX射线衍射仪(日本理学制造)上进行。Cu靶,管压36kV,管电流30 mA。
紫外—可见漫反射光谱(UV-vis-DRS):采用北京普析通用仪器有限公司生产的TU-1901型双光束紫外—可见分光光度计(带IS19-l积分球,BaSO4为参比标准白板)对样品进行紫外可见漫反射光谱(DRS)分析。
2 结果与分析
2.1 X-射线粉末衍射(XRD)谱图分析
首先通过XRD测试了解合成的样品的结构。结果见图1。
XRD 图谱[10]图 11 中 2θ =10.3°,11.06°,25.11°,25.29°,28.67°,32.43°,34.43°,39.7°,43.95°,48.56°都是钛酸钠所对应的特征峰,表明水热反应中有钛酸盐生成。但是图1中曲线1和2都存在2θ =25.3°,37.78°,48.03°,53.78°,55.1°的 TiO2锐钛矿(101),(004),(200),(105),(211)晶面衍射(PDF 84-1286)特征峰,表明反应没有完全进行,曲线3和4的TiO2特征峰基本消失,反应进行的很完全。
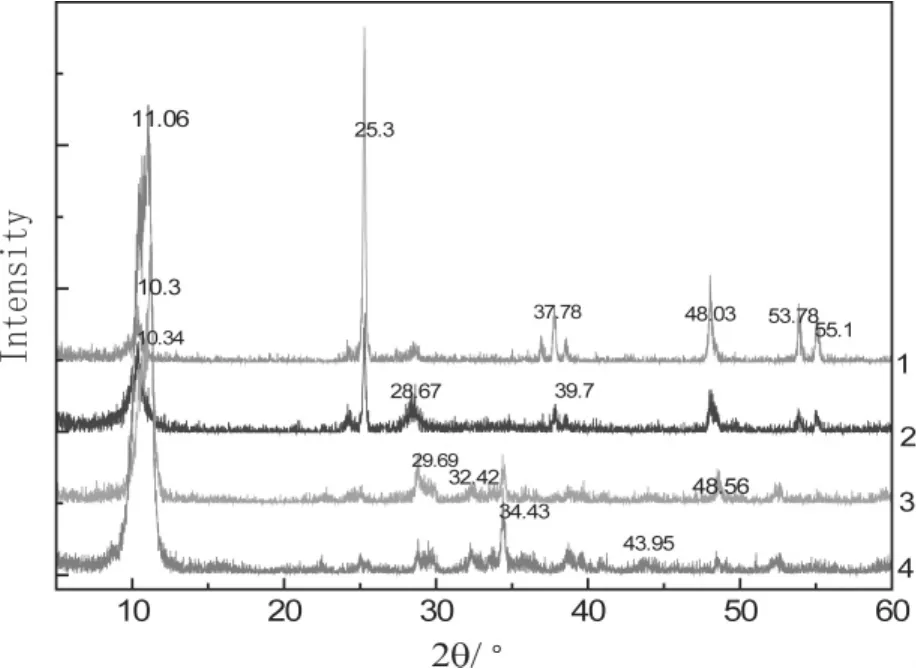
图1 不同Ti/Na比钛酸钠的XRD谱图
由于实验的反应温度和反应时间对于水热合成的进行是足够的,一般而言100℃以下得不到一维纳米结构;纳米管的反应温度在110—160℃之间;温度高于170℃时,得到纳米线。王竹梅选择在120℃水热处理12 h或24 h;许元妹在160℃水热处理24 h制备纳米管;李伊荇在190℃水热处理12 h;张月[11]在175—240℃下恒温加热72 h制备纳米线。究其原因初步判定:Na2Ti3O7和Na2Ti6O13样品含有锐钛矿晶相是因为NaOH浓度(10 mol·L-1)较大,且又按照计量比,使得参与水热循环的水量很少,从而高压反应釜产生的压力过小,不能促进反应的完全进行,而Na2TiO3样品因其Ti/Na小,参与水热循环的水量有保障,所以反应得以进行完全。
根据XRD图库包PDF72-0148查得:图1中2θ =10.3°,25.1°,28.36°,43.86°对应的是Na2Ti3O7的(100),(110),(111)和(104) 晶面所对应的特征峰值;由文献[12]图4中 Na2Ti6O13的图谱分析:2θ =11.06°,28.67°,32.42°,34.43°,39.7°分别是 Na2Ti6O13的(200),(402),(311),(312),(204)晶面特征峰。同时根据PDF73—1398图谱:图中 2θ =11.8°,29.8°,33.4°分别是 Na2Ti6O13的(200),(310),(402)晶面所对应的特征峰值。但在寻找Na2TiO3样品的特征峰时出现了困难。
图1中曲线3和4对应的物质应该是Na2TiO3样品的 XRD 谱线。图中的 10.38°和 11.06°在Na2TiO3标准图谱中并不存在,且这两个强峰使得Na2TiO3特征谱线不明显。仔细分析该样品具备Na4(TiO4)的一些结构特征峰,对照PDF 80—1785可看出:2θ =10.7°,17.5°,22.7°,38.6°,39.6°分别是 Na4(TiO4)的(100),(001),(201),(312),(302)晶面所对应的特征峰,但是最强峰37.6°(120)和33.5°(102)看不出,而 Na2TiO3图谱(PDF 47 -0130)中,34.4°(101)和 58.6°(104)晶面所对应的特征峰是存在的。图 1中 11°处曲线 3(10.29°,10.38°)和曲线 4(10.26°,11.06°)的肩峰表明该样品是两种物质的混合物。出现这种情况的原因可能是因为水热合成的反应中,钛酸钠的结晶物存在着Na4TiO4·nH2O,或在洗涤的过程中发生离子交换而生成了部分的钛酸;但是XRD图谱库中没能找到与之对应的钛酸特征谱线。张月在制备纳米线时也出现了这种情况,推断的结果认为在10°附近的衍射峰对应的晶面间距是层状化合物的层间距,并且做了选区电子衍射(SAED)和高分辨透射电镜(HRTEM)分析。
上述分析初步推断:随着样品Ti原子数目的增加,体系循环的水量越来越少,反应不能进行完全;使1(Na2Ti3O7),2(Na2Ti6O13)号样品中都存在还没反应的TiO2。而3,4号样(Na2TiO3)中循环水量相对较多,所以产物中基本上没有出现TiO2锐钛矿晶相的特征峰,反应很完全。
为验证上述循环水量对反应深度的影响,以及NaOH浓度的影响,以低浓度NaOH制备出以下几个样品。其结构如图2所示。
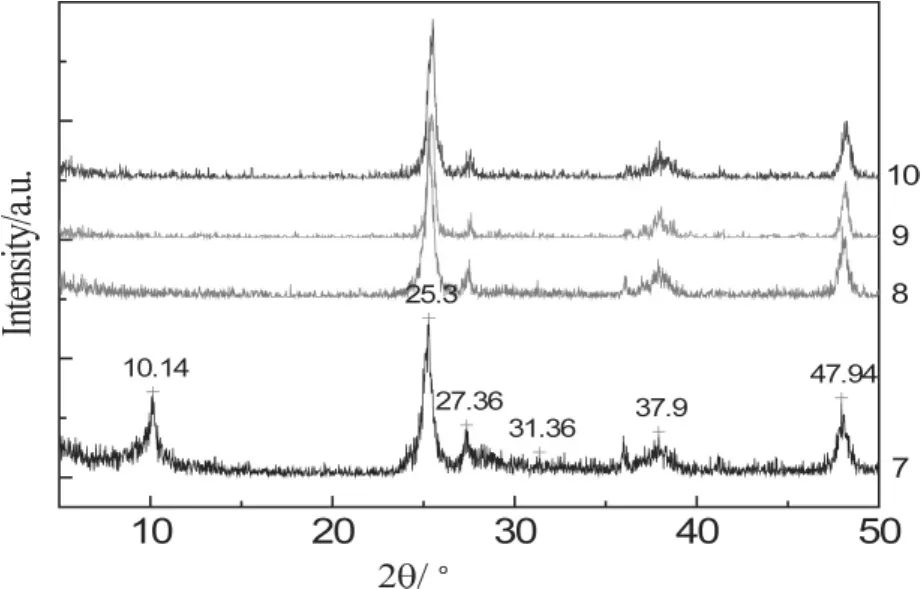
图2 不同NaOH浓度下钛酸盐样品的XRD谱图
图 2 中,2θ =25.3°,37.9°,47.94°为 TiO2锐钛矿的(101),(004),(200)晶面衍射。
由前面分析可知,由于参与水热循环的水量太少,高压反应釜产生的压力很小,无法促进反应的进行,使得产物中含有明显的TiO2锐钛矿晶相。所以本次实验便减少NaOH浓度,使得参与循环反应的水量相对而言增多,进而水热反应中产生的压力增大,应该能够促进反应的进行。但从图2来看,可以说NaOH和TiO2基本上没有反应。只有7号样品有些反应。说明NaOH的浓度是反应能否进行的关键;它既影响到反应所需的压力,同时又保证反应能够进行的最低浓度。若浓度太小,反应不能进行。
结合上述两次实验,本次实验改变NaOH的浓度,研究浓度对反应的影响;同时变换钛源(用Ti(OH)4和Ti(OC4H9)4替代TiO2反应),观察样品的结构。对比实验所得产品XRD图如图3所示。
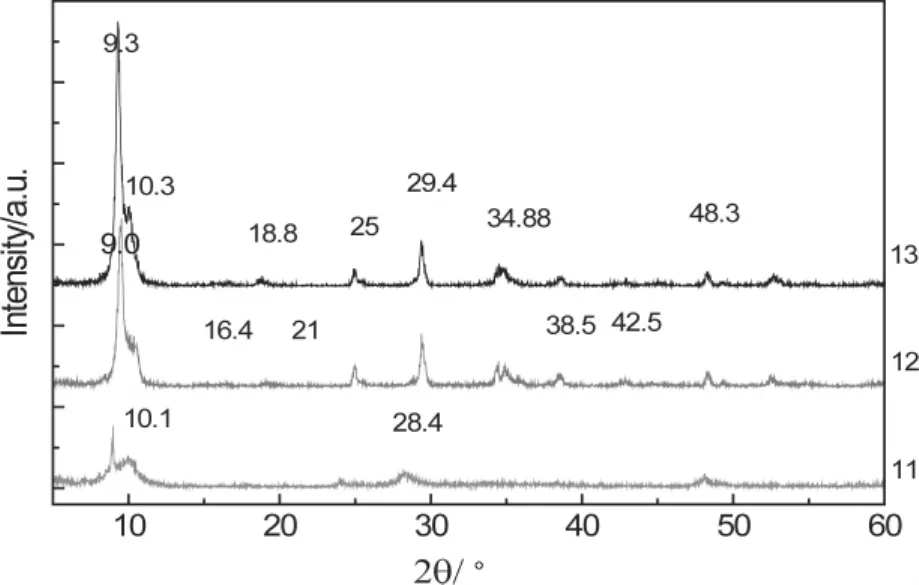
图3 对比实验所得产品XRD图
图3中曲线12,13中10°处附近的两个肩峰(9.3°,10.3°)说明该样品是两种物质的混合物。同时从 PDF73—1398 知:2θ =10.3°,25°,29.4°,48.3°分别对应 Na2Ti6O13的(001),(110),(310),(020)晶面的特征峰。文献[12]中的图3中 Na2Ti3O7的XRD 图谱比对:2θ =9.3°,16.4°,25°,29.4°,48.3°分别为 Na2Ti3O7的(001),(101),(011),(300),(020)晶面特征峰。之所以在合成Na2Ti3O7过程中会出现Na2Ti6O13的特征峰,通过文献知:王竹梅等在合成的Na2Ti3O7进行热处理时也出现了新晶相Na2Ti6O13晶体的特征衍射峰;同时,董正洪等人研究时也有“合成条件的变化很容易导致产物结构与组成的改变”的结论得出。
纵上分析:曲线11中10°处的肩峰是钛酸钠的混合物,造成衍射峰有一定偏移的原因可能是合成时形成了水合阳离子。阳离子与水形成的水合阳离子使它的离子半径变大,导致层板间距增大,导致衍射峰向小角度偏移,出现了与标准PDF图谱上的特征峰值有些偏差。
从图3中11和12号样可以看出,NaOH的浓度的增大能促使反应进行的完全些。
在变换钛源的样品分析知:用NaOH(10 mol·L-1)和Ti(OC4H9)4按计量比反应得到的Na2Ti3O7样品,其峰形与12号样品峰形大体一致,说明不同的原料可以合成出一样的目标产物。
2.2 紫外漫反射光谱图分析
通过紫外漫反射光谱分析,验证不同的钛源对合成的同一目标产物结构的影响,同时确定Na2Ti3O7的特征吸收波长。其谱图如图4所示。
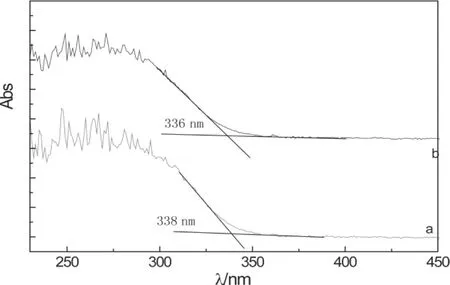
图4 紫外-可见光漫反射光谱图
图a的最大吸收波长是338 nm,图b的最大吸收波长是336 nm,非常接近。进一步验证了不同的原料可以合成出一样的目标产物。
3 结论
采用水热反应法合成钛酸钠,NaOH的浓度和反应的量是反应能否进行的关键;能合成出产品的NaOH浓度最好不低于5 mol·L-1,同时 NaOH过量更有利于产物的合成,但过量多少有待于实验进一步确定。
水热合成制取钛酸钠的实验中,反应过程中参与水热循环的水可能会形成水合阳离子影响晶体的纯度、分散性和晶型。
通过紫外漫反射对其光吸收特性进行了检测,得出合成的原料不同,一样可以合成目标产物,且Na2Ti3O7的吸收带位置在337 nm左右。但合成条件的变化很容易导致产物结构与组成的变化。
[1]王竹梅,李月明,杨小静,等.钛酸盐纳米管的水热合成及晶型研究[J].无机化学学报,2007,23(2):225 -230.
[2]李伊荇,李明辉,杜方,等.钛酸钠纳米线的制备及其性能[J].吉林大学学报(理学版),2010,48(1):121 -123.
[3]景晓明,卢佳美,马晨,等.钛酸钾晶须研究现状及发展前景[J].西南民族大学学报(自然科学版),2010,34(3):539 -544.
[4]蔡领峰,黄 垒,彭峰,等.水热法制备钛酸盐纳米管的稳定性研究[J].无机盐工业,2007,39(2):21-23.
[5]李云飞,韦志仁,罗小平.钛酸盐纳米管的研究及应用进展[J].材料导报,2008,22(4):50-52.
[6]张麟熹,罗明标,刘淑娟,等.钛纳米管的水热合成研究及应用进展[J].化工新型材料,2010,38(7):23 -26.
[7]方晓明,周美玲,许元妹,等.温度对钛酸盐纳米管水热转化的TiO2纳米晶形貌演变的影响机制[J].人工晶体学报,2010,39(6):64 -72.
[8]许元妹,方晓明,张正国.钛酸盐中钠离子含量对其水热转化制备TiO2纳米材料的影响[J].功能材料,2010,41(2):314 -317.
[9]董正洪,赵永男,苏皓,等.钛酸盐纳米结构的水热合成[J].过程工程学报,2009,(9):27-30.
[10]Dong-Seok Seo,Hwan Kim,Jong - Kook Lee.Hydrothermal synthesis of Na2Ti6O13 and TiO2 whiskers[J].Crystal Growth,2005(275):2371-2376.
[11]张月,陈清,龚巍巍,等.钛酸钠纳米线的合成和结构[J].北京大学学报(自然科学版),2007,43(1):125 -131.
[12]Inés Becker,Ingo Hofmann,Frank A.Mǘller.Preparation of bioactive sodium titanate ceramics[J].European Ceramic Society,2007(27):4547-4553.

