青霉素钠与普鲁卡因青霉素的临床实践比较
李翠霞
青霉素G在20世纪40年代初的时候开始被用来作为抗菌药物被应用于临床[1]。因青霉素抗菌活性强,毒性相对较低,青霉素G的临床疗效显著,青霉素G的应用越来越广泛[2]。但是问题也随着应用的广泛而开始被发现,近些年来,因为细菌的耐药性越来越强,青霉素G被滥用情况严重,细菌开始对青霉素G耐药,因此青霉素G在临床的应用不能取得满意的疗效,这让青霉素G在临床应用上受到了很大的限制[3]。但是尽管如此,青霉素仍然有其不可替代性,青霉素G仍然是治疗敏感葡萄球菌感染,A组、B组溶血性链球菌等细菌感染的首选药物;除此以外,青霉素G还可以来用于肺炎链球菌、草绿色链球菌、肺炎双球菌、不产青霉素酶的金黄色葡萄球菌、厌氧的阳性球菌、脑膜炎奈瑟球菌、白喉棒状杆菌、炭疽芽孢杆菌、破伤风杆菌以及螺旋体中的梅毒螺旋体、钩端螺旋体、鼠咬热螺旋体。青霉素G仍然是扁桃体炎、化脓性关节炎、蜂窝组织炎、败血症、心内膜炎、脑膜炎、猩红热、咽炎等疾病的最有效的治疗药物[4]。
1 青霉素钠和普鲁卡因青霉素血药浓度比较
青霉素钠在临床上主要用于敏感菌造成的急性感染,青霉素钠在使用的时候既可以静脉滴注和肌肉注射,青霉素钠均能够被机体均匀迅速吸收[5]。当青霉素钠进行肌肉注射的时候,注射量为100万U,半个小内峰值浓度为20U/mL,并且注射后排泄迅速,大部分通过尿排出体外,在4~6h内都会完全从体内排出,体内无残留;相对于青霉素钠,普鲁卡因青霉素的吸收比较慢,当肌体注射80万U之后,血药浓度半个小时后达到峰值浓度4U/mL,24h后,体内仍可检测到普鲁卡因青霉素的存在[6]。
2 青霉素钠和普鲁卡因青霉素的药效比较
青霉素一类的药物为细菌繁殖期的杀菌药,细菌静止期无杀菌作用,只有在细菌繁殖期青霉素G才能有效的发挥杀菌作用充分发挥药效[7]。低浓度长时间给药,可使细菌由繁殖状态转变成静止期,静止期使用青霉素G,就会降低青霉素G的药效,所以在临床治疗的时候,一般没有必要长时间一直维持一定的血药浓度[8]。在使用青霉素类药物时,短时间内产生体内比较高的血药浓度对患者的临床治疗会更加有效。
下面通过表1和表2对临床患者应用青霉素钠和普鲁卡因青霉素后的效果进行比较。其中表1为急性扁桃体炎引起的255例病例运用青霉素钠以及普鲁卡因青霉素的退烧消肿时间;表2为急性尿路感染65例运用青霉素钠和普鲁卡因青霉素后的脓球消失的时间,比较结果如下。

表1 急性扁桃体炎用青霉素钠哈普鲁卡因青霉素后退烧以及消肿之间比较
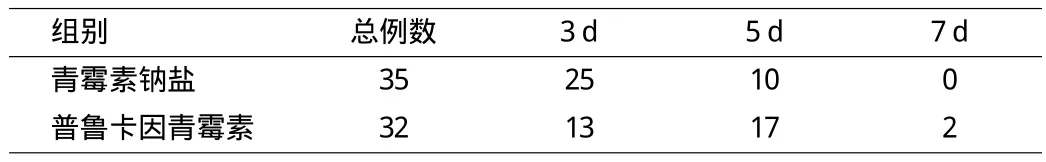
表2 急性尿路感染患者运用青霉素钠和普鲁卡因青霉素后脓球消失时间比较
通过分析表1可得出:急性扁桃体炎应用青霉素钠3d消肿和退烧的有效率分别为53.85%和57.69%,应用普鲁卡因青霉素3d的有效率分别为44%和48%。通过分析表2可得出:急性尿路感染应用青霉素3d脓球小事有效率为71.42%,应用普鲁卡因青霉素有效率为40.63%。综合表1和表2的分析结果可得出结论:青霉素钠和普鲁卡因青霉素均能有效的杀灭细菌控制感染,但是青霉素钠的短期疗效优于普鲁卡因青霉素。在应用于急性感染时青霉素钠的临床疗效更为显著。
3 青霉素钠及普鲁卡因青霉素局部吸收的比较
青霉素钠盐是一种白色结晶形状的粉末,易溶于水,加水后溶解成为澄清溶液;普鲁卡因青霉素是一种白色微晶状粉末,微溶于水,加水后振摇成混悬液,因此普鲁卡因青霉素在肌肉注射时吸收速度比青霉素钠更为缓慢。两种药物均取80万U加0.9%的氯化钠溶液4mL溶解之后进行臀部肌注3d,5d,7d观察肌肉硬结的情况,肌肉注射普鲁卡因青霉素发生硬结的情况明显要比青霉素钠盐肌注硬结严重。结果见表3。
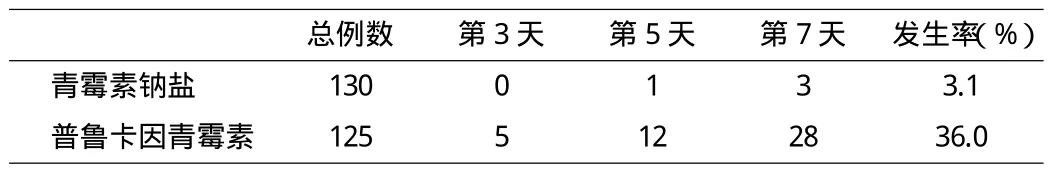
表3 青霉素钠盐和普鲁卡因青霉素肌注硬结情况比较表
4 青霉素钠盐和普鲁卡因青霉素因针头阻塞而导致的重注比较
试验方法与步骤:青霉素钠盐以及普鲁卡因青霉素同样用7号针头,用同样物质的量的氯化钠溶液稀释,同样采用肌肉注射的方法在身体的同一个部位进行注射,最终青霉素钠盐和普鲁卡因青霉素两两相比较的针头阻塞情况结果表明,青霉素钠盐的实验组130例临床注射案例中没有一例有针头阻塞的情况,相比之下,普鲁卡因青霉素对照组125例临床试验案例中发生40例针头阻塞情况导致重注,重注的发生既增加了病人的痛苦,又会导致药物的浪费,严重的时候还会有生命危险,所以要严加防范,确保每一环节都万无一失[11-16]。
在给药途径方面青霉素钠既可肌肉注射也可静脉点滴,而普鲁卡因青霉素只能肌注,青霉素G优于普鲁卡因青霉素。
5 结论
青霉素G因为半衰期短代谢排泄快,所以青霉素G药效时间短,临床治疗时为达到治疗效果需多次给药。普鲁卡因青霉素是长效青霉素,很好的弥补青霉素G的这一缺点。但是普鲁卡因青霉素并没有完全取代青霉素在临床中的应用。青霉素G起效迅速、对急性感染作用强、给药途径多种等优点是普鲁卡因青霉素没有的。在临床实践中应该根据疾病特点和患者的实际情况合理使用,取得最好的临床治疗效果。
[1]马春宏,尹彦苏,王仁章,等.离子液体双水相萃取分离四环素的研究[J].吉林师范大学学报(自然科学版),2009(1):154.
[2]林棋,马梦林,蒋维东,等.离子液体介质中Knoevenagel缩合反应研究[J].四川大学学报(自然科学版),2007(2):29.
[3]王平,徐群.离子液体的研究和应用[J].牡丹江师范学院学报(自然科学版),2007(1):116.
[4]桑潇.离子液体的合成法研究[J].中国科技信息,2008(5):23.
[5]宋红光,马宁.离子液体应用研究进展[J].科技资讯,2009(11):89.
[6]杨志远,蔡源,黄德英,等.咪唑类离子液体[PMIm]BF4的合成及表征[J].科技信息,2010(35):107.
[7]肖友军,周磊,王灵峰,等.离子液体EMBF4中对硝基甲苯电还原的研究[J].江西师范大学学报(自然科学版),2010(2):64.
[8]尹万香,李润生,龙俞霖,等.离子液体[Hmim]BF4催化合成β-烯胺酮类化合物[J].暨南大学学报(自然科学与医学版),2010(5):149.
[9]雷达,范芳,严建芳.甲苯/TX-100/1-丁基-3-甲基咪唑六氟磷酸盐微乳液的相结构研究[J].华中师范大学学报(自然科学版),2007(3):153.
[10]魏颖,张庆国.离子液体BMIBF4水溶液粘度性质的研究[J].渤海大学学报(自然科学版),2008(2):52.
[11]王军,张艳,时召俊,等.N-乙基-N-丁基吗啉离子液体双水相体系萃取分离蛋白质[J].应用化工,2009(1):127.
[12]马春宏,尹彦苏,王仁章,等.离子液体双水相萃取分离四环素的研究[J].吉林师范大学学报(自然科学版),2009(1):18.
[13]张冬梅,阿颖利,宋静.青霉素的抗菌作用机制及合理使用分析[J].求医问药:下半月刊,2012(8):143.
[14]康小瑜,郭英.改良苄星青霉素抽吸方法降低药液残余量[J].吉林医学,2012(29):79.
[15]刘耀川.细菌对大环内酯类药物耐药机制简介[J].现代畜牧兽医,2012(10):133.
[16]张芝莲,梁丽珍.青霉素过敏反应的急诊救治[J].基层医学论坛,2012(30):87.

