Pt含 量对Co@Pt/C 核壳结构催化剂性能的影响
赵天天 林 瑞,* 张 路 曹春晖 马建新,*
(1同济大学新能源汽车工程中心,上海201804;2同济大学汽车学院,上海201804)
1 引言
质子交换膜燃料电池(PEMFC)可直接将化学能转化为电能,具有能量转化效率高、无(低)污染、噪音低、启动快等优点,被视为用于电动汽车、便携式电源的理想电源.目前质子交换膜燃料电池严重依赖贵金属催化剂铂(Pt)的使用,但Pt价格昂贵,储量有限,导致PEMFC的制造成本居高不下,限制了其商业化发展.研制新型高性能、低成本催化剂对推动燃料电池的发展具有重要意义.1
Pt基合金催化剂一直是PEMFC领域的研究重点之一.2,3有研究表明,4Pt基合金催化剂具有合适的Pt-Pt原子间距以及更多的d带空穴,两者的共同作用促进了其对于氧还原反应(ORR)的催化活性.Pt基合金催化剂的研究重点之一就是从几何形状上构筑催化剂,在纳米尺度上对金属催化剂颗粒的结构进行理性设计和化学裁剪有可能显著改变金属催化剂的物理化学性质,获得性能更好的催化剂,如多面体形状、核壳结构、纳米线结构的Pt基合金催化剂等.5-11其中以Pt为壳层的M@Pt(M为Co,Ni,Cu等过渡金属)核壳结构电催化剂在降低Pt载量、提高催化剂活性等方面表现出的良好性能,已经成为燃料电池领域的研究热点.12-15由于电催化反应为表面过程,因此,只有分布在纳米颗粒表面的活性组分才有可能被利用,而体相中的活性组分无法参与反应过程.将Pt分散在非铂纳米粒子表面,形成核壳结构催化剂,可有效提高贵金属铂的利用效率.同时由于具有特殊的表面电子结构以及核壳之间特殊的相互作用,Pt基核壳结构催化剂表现出更高的催化活性和稳定性.16,17
Kristian等18第一次在水溶液中用还原法合成了高活性的Co@Pt/C催化剂,其对ORR的催化活性(specific activity)是Pt/C催化剂的2-4倍.Kristian认为催化活性提高的原因是Pt原子之间具有合适的间距,同时其表面缺陷很少,抑制了Pt-OH的形成.Wu等19用两步还原法制备Co@Pt/C催化剂,Co@Pt纳米粒子的直径约为3-4 nm.其催化活性相较于Pt/C有较大提高,但电化学活性比表面积(ECSA)并没有增加.Wu认为催化活性提高的原因是在核壳结构中,Pt-Pt之间发生压缩变形,影响了表面的Pt原子与吸附物如H、CO、OH之间的相互作用.经过5000次循环伏安扫描后,Co@Pt/C电催化剂的活性表面积损失与Pt/C相当,稳定性佳.Brushett等20对Pt3Co合金电催化剂进行表面酸处理,Pt3Co表面Co元素溶解,形成富Pt表面,即核壳结构.将制得的Co@Pt催化剂用于一个微流体氢氧燃料电池测试,发现其催化性能与纯Pt相当,耐久性好于纯Pt.
已有研究表明Co@Pt/C核壳结构催化剂表现出良好的催化性能.18-21然而目前对于Co@Pt/C核壳结构催化剂的研究大多针对其制备方法与表征,有关Pt含量对Co@Pt/C核壳结构催化剂性能影响的研究则较为少见.为同时达到降低Pt载量与提高性能的目标,突破燃料电池商业化的瓶颈,研究不同Pt含量的Co@Pt/C核壳结构催化剂的性能十分必要.本研究采用两步还原法制备了系列20%Co@Pt/C催化剂,并采用透射电镜(TEM)、循环伏安(CV)、光电子射线能谱(XPS)分析、线性扫描伏安(LSV)等方法考察其结构形貌与电化学性能.研究不同Co:Pt原子比对20%Co@Pt/C催化剂性能的影响.同时将20%Co@Pt/C催化剂与实验室早先制备的40%Co@Pt/C催化剂的性能进行比较.
2 实验
2.1 电催化剂的制备
实验所用的碳载体为XC-72碳黑(美国Cabot公司,比表面积为235 m2·g-1).CoCl2、H2PtCl6、NaOH、乙醇、乙二醇和聚乙烯吡咯烷酮(PVP)购自国药集团化学试剂有限公司,均为分析纯;质量分数为5%的Nafion溶液购自美国Dupont公司.
碳黑的预处理:XC-72碳黑用2.0 mol·L-1盐酸在120°C回流处理4 h,以去除硫等无机杂质;用5.0 mol·L-1硝酸在120°C回流进行表面氧化处理4 h,以增加表面的官能团;过滤,用去离子水洗涤,100°C真空干燥12 h.
本研究的20%Co@Pt/C核壳结构电催化剂采用两步还原法制备.22两步还原法是目前制备核壳结构电催化剂最常采用也是最成熟的方法,两步还原法实验装置简单,制备的纳米粒子粒径小,颗粒分散性较好,制备条件温和.先以NaBH4还原CoCl2得到Co核的纳米颗粒,然后以乙二醇为还原剂还原氯铂酸(H2PtCl6)形成Co@Pt核壳结构纳米颗粒,并以碳为载体,制得了Co@Pt/C电催化剂,其中Co与Pt的总含量为20%.通过改变金属前驱体CoCl2与H2PtCl6的用量,制备了不同比例的Co@Pt/C电催化剂(CoCl2与H2PtCl6的用量摩尔比分别为1:1和1:3).具体制备方法如下.
(1)Co核制备:在0.01 mol·L-1CoCl2乙醇溶液中加入PVP作为稳定剂,搅拌30 min,逐滴加入新制的0.05 mol·L-1NaBH4乙醇溶液,以NaBH4还原CoCl2,离心分离后得到Co的纳米颗粒.
(2)将步骤(1)中得到的Co核分散到乙二醇溶液中,加入PVP作为稳定剂,搅拌30 min后,在N2气氛保护下逐滴加入0.03862 mol·L-1H2PtCl6乙二醇溶液,调节溶液pH至12,升温至120°C,不断搅拌并加热2 h,以乙二醇还原H2PtCl6形成Co@Pt核壳结构纳米颗粒.
(3)向上述混合液中加入经过预处理的XC-72碳(分散于乙二醇中),继续于120°C加热1 h,冷却后调节pH至3,过滤后用丙酮、乙醇和水多次洗涤,并于80°C真空干燥,得到以碳为载体的Co@Pt/C电催化剂,其中Co与Pt的总含量为20%(质量分数).通过改变金属前驱体CoCl2与H2PtCl6的用量,制备了不同摩尔比的Co:Pt电催化剂,分别以20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C(CoCl2与H2PtCl6的用量摩尔比分别为1:1和1:3)表示.同时采用E-tek公司生产的20%Pt/C电催化剂作为性能参考,实验室早先制备的40%Co@Pt(1:1)/C和40%Co@Pt(1:3)/C电催化剂也被用作性能比较.
2.2 电催化剂的表征
2.2.1 结构表征
采用透射电镜对电催化剂进行结构表征.在测试纳米粒子的形貌、粒度以及结构的方法中,TEM是最常用也是最直观的手段,可以考察催化剂金属颗粒的颗粒大小和颗粒分布.所用仪器为日本电子光学公司的JEM-2010透射电子显微镜.加速电压为200 kV,采用铜网微栅样品架,样品在无水乙醇中超声分散,然后负载到样品架上制成电镜样品.
采用光电子射线能谱对电催化剂的元素组成及化学价态进行分析.催化剂表面元素通过PHI Model 5700型X光电子能谱仪(美国PHI公司)进行分析.辐射源为Mg Kα(hv=1253.6 eV),电子结合能用碳(C 1s,结合能为284.6 eV)校正.
2.2.2 电化学表征
采用循环伏安、线性扫描伏安等电化学方法对电催化剂进行催化活性表征.使用上海辰华公司的CHI104P电化学工作站与美国PINE公司的AFE5T050PTHT型旋转圆盘电极进行催化剂电化学性能表征.以0.1 mol·L-1HClO4溶液为电解质,测试温度25°C,可逆氢电极(RHE)为参比电极,铂丝作为对电极,涂有催化剂层的旋转圆盘电极为测试电极.
(1)测试电极催化层的制备:称取0.0020 g催化剂,加入1 mL的5%Nafion与甲醇(质量比为1:30)混合溶液,超声2 h使催化剂分散均匀,用微量进样器抽取混合液10 μL,滴加到旋转圆盘电极表面,干燥后进行测试.
(2)CV测试:CV是一种常用的电化学研究方法,可以用于判断电极反应的可逆程度、计算电催化剂的电化学活性比表面积等.本研究中CV测试的扫描范围为0.05-1.15 V(vs RHE),扫描速率为50 mV·s-1.测试前,在HClO4溶液中通N230 min排出溶液中的O2.
(3)LSV测试:为研究电催化剂的对氧还原反应(ORR)的催化性能,对其进行LSV测试.本研究中LSV的扫描范围为0.05-1.2 V(vs RHE),扫描速率为5 mV·s-1,转速为1600 r·min-1.测试前,在HClO4溶液中通O230 min使溶液中的O2饱和.为了计算ORR的动力学参数,分别在转速300、400、600、800、1200、2000和2400 r·min-1下进行LSV扫描,扫描范围同上.
3 结果与讨论
3.1 TEM测试
图1(a,c)分别为20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C电催化剂的TEM图.从图中可以看出活性组分(Co@Pt)高度分散在碳载体上,分布非常均匀,颗粒粒径较小.图1(b,d)分别为20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C电催化剂的金属颗粒粒径分布图,从图中可以看出Co@Pt(1:1)和Co@Pt(1:3)的粒径分布范围都很窄,颗粒大小均匀.Co@Pt(1:3)的平均粒径为2.3 nm,相较于Co@Pt(1:1)(2.2 nm)没有明显改变,可能是因为Pt原子层很薄,因此难以观察到Pt含量对Pt壳层厚度的影响.23Co与Pt的比例为1:3和1:1的两种情况对粒径和分散性没有明显的影响.
3.2 XPS测试

图1 20%Co@Pt(1:1)/C(a,b)和20%Co@Pt(1:3)/C(c,d)电催化剂的TEM图像(a,c)及粒径分布(b,d)Fig.1 TEM images(a,c)and particle size distributions(b,d)of 20%Co@Pt(1:1)/C(a,b)and 20%Co@Pt(1:3)/C(c,d)electrocatalysts
图2 (a,b)为20%Co@Pt(1:3)/C电催化剂的XPS图谱.从全谱图2(a)中可以观察到对应于Pt 4f、C 1s、O 1s和Co 2p的四个峰,出现Co 2p的峰说明在催化剂的金属颗粒表面可能存在少量Co和Co的氧化物,未被Pt原子层完全覆盖.图2(b)是20%Co@Pt(1:3)/C电催化剂的Pt 4f的XPS谱图,根据标准XPS谱,Pt(0)的结合能为71.0和74.4 eV.自制催化剂样品中Pt(0)所对应的结合能的值有所偏移,说明其中部分Pt以Pt的氧化物的形态存在,可能是催化剂中部分金属颗粒表面的Pt被氧化所致.对Pt 4f峰进行拟合,拟合结果如图2(b)所示,自制催化剂样品中零价Pt与Pt的氧化物的含量分别为71.5%和29.5%,Pt主要仍以还原态存在.

图220 %Co@Pt(1:3)/C电催化剂的XPS图谱Fig.2 XPS spectra for the as-prepared 20%Co@Pt(1:3)/C electrocatalyst
3.3 CV测试

图320 %Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和20%Pt/C(E-tek)电催化剂的CV曲线Fig.3 CV curves of 20%Co@Pt(1:1)/C,20%Co@Pt(1:3)/C,and 20%Pt/C(E-tek)electrocatalysts
由图3中氢的吸脱附峰可以计算出20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和 商 业 20%Pt/C(E-tek)电催化剂的活性比表面积(ECSA)分别为56、60和54 m2·g-1.自制20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C电催化剂的ECSA较商业电催化剂20%Pt/C(E-tek)都有所提高,Co@Pt核壳结构提高了Pt的利用率.结合图1自制电催化剂的TEM图像与粒径分布情况,20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C电催化剂中的金属颗粒直径约为2-3 nm.Yang等23曾采用类似的种子生长法制备了Co0.32@Pt0.68/C电催化剂,其金属颗粒的平均直径为3.0 nm,其中Pt层厚度约为0.5 nm.Lee和Do24曾采用热分解与化学还原相结合的方法,制备了Co@Pt/C电催化剂,其中金属颗粒的平均直径为4.12 nm.本次实验中的金属颗粒纳米较小,从几何学的角度来看,较小的颗粒直径将获得较大的比表面积,提高Pt的利用率.
3.4 LSV测试
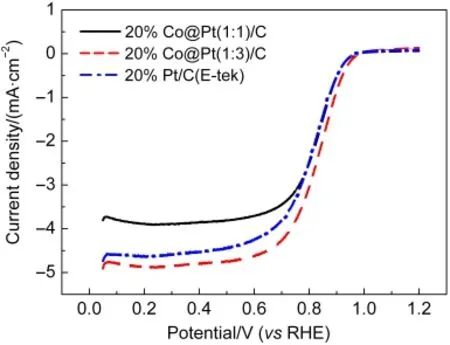
图420 %Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和20%Pt/C(E-tek)电催化剂的LSV曲线Fig.4 LSV curves of 20%Co@Pt(1:1)/C,20%Co@Pt(1:3)/C,and 20%Pt/C(E-tek)electrocatalysts
自制20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和商业20%Pt/C(E-tek)电催化剂的LSV测试结果如图4所示.20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和20%Pt/C(E-tek)的ORR起始电位都出现在约1.0 V,三者的半波电位相近,分别为0.831、0.840和0.833 V.Co@Pt/C电催化剂的ORR性能受Co和Pt比例的影响,20%Co@Pt(1:3)/C电催化剂表现出良好的ORR性能,与20%Pt/C(E-tek)电催化剂相比有小幅提升,但20%Co@Pt(1:3)/C电催化剂在降低Pt载量方面具有优势.电压0.9 V下20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C和商业20%Pt/C(E-tek)电催化剂的电流密度分别为692、857和507 μA·cm-2,自制20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C的比活性(specific activity)都超过了商业20%Pt/C(E-tek)电催化剂.其中20%Co@Pt(1:3)/C在0.9 V下的比活性超过了美国能源部(DOE)要求(720 μA·cm-2).计算三种催化剂在0.9 V下对应的质量比活性(mass activity),分别为0.064、0.067、0.036 A·mg-1,与DOE要求的0.44 A·mg-1仍有差距,但是可以看出自制催化剂的质量比活性已经超过了商业催化剂.ORR极限电流密度约为4-5 mA·cm-2,小于理论值(6 mA·cm-2),25该值与催化剂的活性关系不大,可能与电极催化层的制作过程有关,催化层在干燥过程中可能出现了部分团聚,未能铺满铂碳电极表面;另一个可能的原因是LSV测试前需要先进行50圈CV扫描使催化剂性能稳定,这个过程中可能有少量催化剂脱落.研究报道核壳结构电催化剂具有良好的催化性能,但是核壳结构改善电催化剂催化性能的原因尚无统一定论,目前有以下几种解释:18,19(1)原子结构理论认为合金作用造成了表层Pt原子中d空穴的增加,必然导致金属与氧之间相互强烈的作用,这种作用使氧的吸附和O―O键减弱,加快氧分子间键的断裂和电解质中O与H+之间的形成;(2)最小原子间距理论认为合金元素的引入使Pt与Pt的原子间距缩短,有利于O2的解离吸附,但催化剂表面的电子结构并未发生变化;(3)表面粗糙效应(雷尼效应)认为合金催化剂中第二元素的溶解使催化剂表面变得更加粗糙,增加Pt的有效比表面,从而提高了催化活性.
20%Co@Pt(1:3)/C电催化剂的ORR动力学性质测试结果如图5所示.用20%Co@Pt(1:3)/C制备旋转圆盘电极催化层,在O2饱和的0.1 mol·L-1HClO4溶液中对其进行不同转速下的LSV测试.氧还原的动力学性质用Koutecký-Levich关系式分析,分别以图中0.3、0.5和0.7 V下得到的电流倒数和转速平方根的倒数为对应关系作图,结果如图6所示,得到一组斜率相近的平行直线.

图5 不同转速下20%Co@Pt(1:3)/C电催化剂的LSV曲线Fig.5 LSV curves of 20%Co@Pt(1:3)/C electrocatalysts at different speeds

图620 %Co@Pt(1:3)/C电催化剂ORR的Koutecký-Levich图Fig.6 Koutecký-Levich plots for ORR on 20%Co@Pt(1:3)/C electrocatalyst
方程(1)中,斜率1/B直接与氧还原反应的总电子数相关联:24

表1 不同电位下0.1 mol·L-1HClO4溶液中20%Co@Pt(1:3)/C电催化剂的平均电子转移数(n)Table 1 Average number of electrons transferred for ORR(n)on 20%Co@Pt(1:3)/C electrocatalyst at different potentials in 0.1 mol·L-1HClO4solution

式中,id是实验观察到的电流,n是每摩尔O2被还原时所转移的电子数目,A是电极面积(0.283 cm2),F是法拉第常数(96485 C·mol-1),CO是氧气的溶解度(0.969×10-6mol·cm-3),DO是氧气的扩散系数(1.9×10-5cm2·s-1),v是溶液的动力学粘度(0.893×10-2cm2·s-1),ω是旋转圆盘电极的转速,B是Koutecký-Levich图中直线斜率的倒数.在0.3、0.5和0.7 V电压下,计算得到n值分别为4.12、4.16和4.30(如表1所示),表明Co@Pt/C催化剂表面发生的ORR反应是以四电子进程进行的.
3.5 20%Co@Pt/C与40%Co@Pt/C的性能比较
将本研究中自制的20%Co@Pt(1:1)/C和20%Co@Pt(1:3)/C与实验室早先制备的40%Co@Pt(1:1)/C和40%Co@Pt(1:3)/C进行TEM图比较,在图7中可以明显看出20%Co@Pt/C电催化剂的金属颗粒数量较少,在碳载体上的分散更加均匀,极少出现团聚现象,这有助于提高电催化剂的比表面积,提高Pt利用率,改善催化活性.
将20%Co@Pt/C电催化剂的ECSA与40%Co@Pt/C电催化剂比较,20%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C、40%Co@Pt(1:1)/C、40%Co@Pt(1:3)/C的ECSA分别为56、60、30和45 m2·g-1,20%Co@Pt/C电催化剂的ECSA为相同Co:Pt比例的40%Co@Pt/C电催化剂的1.9与1.3倍(表2),可能是因为金属含量少的电催化剂中的活性组分更易于分散,因此具有更大的活性比表面积,Pt的利用率更高,这与TEM结果的推测一致.

图7 20%Co@Pt(1:1)/C(a)、20%Co@Pt(1:3)/C(b)、40%Co@Pt(1:1)/C(c)和40%Co@Pt(1:3)/C(d)电催化剂的TEM图像Fig.7 TEM images of 20%Co@Pt(1:1)/C(a),20%Co@Pt(1:3)/C(b),40%Co@Pt(1:1)/C(c)and 40%Co@Pt(1:3)/C(d)electrocatalysts

表2 Pt/C和Co@Pt/C电催化剂的电化学活性面积Table 2 ECSAs of Pt/C and Co@Pt/C electrocatalysts

图820 %Co@Pt(1:1)/C与40%Co@Pt(1:1)/C、20%Co@Pt(1:3)/C与40%Co@Pt(1:3)/C电催化剂的LSV曲线比较Fig.8 LSV curves of 20%Co@Pt(1:1)/C and 40%Co@Pt(1:1)/C,20%Co@Pt(1:3)/C and 40%Co@Pt(1:3)/C electrocatalysts
将20%Co@Pt/C电催化剂的LSV曲线与40%Co@Pt/C电催化剂比较(图8),2620%Co@Pt(1:1)/C的半波电位(0.831 V)相较于40%Co@Pt(1:1)/C(0.794 V)向正向移动了37 mV;20%Co@Pt(1:3)/C的半波电位(0.840 V)相较于40%Co@Pt(1:3)/C(0.804 V)向正向移动了36 mV.半波电位是描述电催化剂对于ORR催化活性的重要指标.虽然20%Co@Pt/C电催化剂极限电流密度小于40%Co@Pt/C电催化剂,但是半波电位向正向移动,仍然表现出更好的催化性能,这可能是由于20%Co@Pt/C电催化剂的载量较低,更加有利于分散.当金属颗粒数量较多时,容易发生团聚,团聚后中心的Pt则难以被利用.由于20%Co@Pt/C电催化剂的Pt载量较低,可以有效降低电催化剂成本,因此比40%Co@Pt/C电催化剂表现出更大的优势.
4 结论
本研究采用两步还原法制得核壳结构Co@Pt/C电催化剂.以NaBH4还原CoCl2得到Co核的纳米颗粒,然后以乙二醇为还原剂还原氯铂酸(H2PtCl6)形成Co@Pt核壳结构纳米颗粒,并以碳为载体,制得了Co@Pt/C电催化剂,其中Co与Pt的总质量分数为20%.通过改变金属前驱体CoCl2与H2PtCl6的用量,制备了不同比例的Co@Pt/C电催化剂(CoCl2与H2PtCl6的用量比例分别为1:1和1:3).采用TEM、CV、LSV等方法考察了其结构与性能.自制20%Co@Pt(1:3)/C与20%Co@Pt(1:1)/C的ECSA分别达到56和60 m2·g-1,都超过了商用催化剂20%Pt/C(E-tek).与40%Co@Pt/C电催化剂比较,20%Co@Pt(1:1)/C与20%Co@Pt(1:3)/C的ECSA分别是40%Co@Pt(1:1)/C与40%Co@Pt(1:3)/C的1.9和1.3倍.20%Co@Pt/C电催化剂的半波电位相较于40%Co@Pt/C向正向移动,比40%Co@Pt/C电催化剂表现出更好的ORR催化性能,有望降低催化剂的成本,在PEMFC领域表现出很好的应用前景.
(1)Mazumder,V.;Lee,Y.M.;Sun,S.H.Adv.Funct.Mater.2010,20,1224.doi:10.1002/adfm.v20:8
(2) Yang,H.Angew.Chem.Int.Edit.2011,50,2674.doi:10.1002/anie.201005868
(3) Fu,R.;Zheng,J.S.;Wang,X.Z.;Ma,J.X.Acta Phys.-Chim.Sin.2011,27(9),2141.[符 蓉,郑俊生,王喜照,马建新.物理化学学报,2011,27(9),2141.]doi:10.3866/PKU.WHXB20110809
(4) Mukerjee,S.;Srinivasan,S.;Soriaga,M.P.J.Phys.Chem.1995,99,4577.doi:10.1021/j100013a032
(5)Zong,J.;Huang,C.D.;Wang,Y.X.Battery Bimonthly 2011,41(2),104. [宗 军,黄成德,王宇新.电池,2011,41(2),104.]
(6) Lim,B.;Jiang,M.J.;Camargo,H.C.P.;Cho,E.C.;Tao,J.;Lu,X.M.;Zhu,Y.M.;Xia,Y.M.Science 2009,324,1302.doi:10.1126/science.1170377
(7)Stamenkovic,V.R.;Fowler,B.;Mun,B.S.;Wang,G.F.;Ross,N.P.;Christopher,A.L.;Nenad,M.M.Science 2007,315,493.doi:10.1126/science.1135941
(8)Wang,C.;Chi,M.F.;Li,D.G.;Strmcnik,D.;Vliet,D.;Wang,G.F.;Komanicky,V.;Chang,K.C.;Paulikas,A.P.;Tripkovic,D.;Pearson,J.;More,K.L.;Markovic,N.M.;Sramenkovic,V.R.J.Am.Chem.Soc.2011,133,14396.doi:10.1021/ja2047655
(9)Chen,Y.M.;Liang,Z.X.;Yang,F.;Liu,Y.W.;Chen,S.L.J.Phys.Chem.C 2011,115,24073.doi:10.1021/jp207828n
(10) Zhang,J.;Yang,H.Z.;Fang,J.Y.;Zou,S.Z.Nano Lett.2010,10,638.doi:10.1021/nl903717z
(11) Lin,R.;Zhang,H.Y.;Zhao,T.T.;Cao,C.H.;Yang,D.J.;Ma,J.X.Electrochimica Acta 2012,62,263.doi:10.1016/j.electacta.2011.12.018
(12)Zhang,H.Y.;Cao,C.H.;Zhao,J.;Lin,R.;Ma,J.X.Chinese Journal of Catalysis 2012,33(2),222. [张海艳,曹春晖,赵 健,林 瑞,马建新.催化学报,2012,33(2),222.]
(13) Zhu,H.;Li,X.W.;Wang,F.H.International Journal of Hydrogen Energy 2011,36,9151.doi:10.1016/j.ijhydene.2011.04.224
(14) Mani,P.;Srivastava,R.;Strasser,P.J.Phys.Chem.C 2008,112,2770.doi:10.1021/jp0776412
(15) Dang,D.;Gao,H.L.;Peng,L.J.;Su,Y.L.;Liao,S.J.;Wang,Y.Acta Phys.-Chim.Sin.2011,27(10),2379.[党 岱,高海丽,彭良进,苏允兰,廖世军,王 晔.物理化学学报,2011,27(10),2379.]doi:10.3866/PKU.WHXB20110922
(16) Liu,B.;Liao,S.J.;Liang,Z.X.Progress in Chenmistry 2011,23(5),852.[刘 宾,廖世军,梁振兴.化学进展,2011,23(5),852.]
(17)Adzic,R.R.;Zhang,J.;Sasaki,K.;Vukmirovic,M.B.;Shao,M.;Wang,J.X.;Nilekar,A.U.;Marvrikakis,M.;Valerio,J.A.;Uribe,F.Top Catal.2007,46,249.doi:10.1007/s11244-007-9003-x
(18)Kristian,N.;Yu,Y.L.;Lee,J.M.;Liu,X.W.;Wang,X.Electrochimica Acta 2010,56,1000.doi:10.1016/j.electacta.2010.09.073
(19)Wu,H.M.;Wexler,D.;Wang,G.X.;Lin,H.K.J.Solid State Electrochem.2012,16,1105.
(20) Brushett,F.R.;Duong,H.T.;Ng,J.W.;Behrens,R.L.;Wieckowski,A.;Kenis,P.J.A.Journal of the Electrochemical Society 2010,157(6),B837.
(21)Wang,R.F.;Wang,H.;Wei,B.X.;Wang,W.;Lei,Z.Q.International Journal of Hydrogen Energy 2010,35,10081.doi:10.1016/j.ijhydene.2010.07.008
(22)Lin,R.;Cao,C.H.;Zhao,T.T.;Huang,Z.;Li,B.;Wieckowski,A.;Ma,J.X.Journal of Power Sources 2013,223,190.doi:10.1016/j.jpowsour.2012.09.073
(23) Yang,X.J.;Cheng,F.Y.;Tao,Z.L.;Chen,J.Journal of Power Sources 2011,196,2785.doi:10.1016/j.jpowsour.2010.09.079
(24) Lee,M.H.;Do,J.S.Journal of Power Sources 2009,188,353.doi:10.1016/j.jpowsour.2008.12.051
(25) Gasteiger,H.A.;Kocha,S.S.;Sompalli,B.;Wagner,F.T.Applied Catalysis B:Environmental 2005,56,9.doi:10.1016/j.apcatb.2004.06.021
(26) Cao,C.H.;Lin,R.;Zhao,T.T.;Huang,Z.;Ma,J.X.Acta Phys.-Chim.Sin.2013,29(1),95.[曹春晖,林 瑞,赵天天,黄 真,马建新.物理化学学报,2013,29(1),95.]doi:10.3866/PKU.WHXB201209272