纤维素在乙醇介质中直接生成乙酰丙酸乙酯的研究
常 春,朱伟娜,候胜利,乔建援,朱 峰
(1.郑州大学 化工与能源学院,河南 郑州450001;2.中国石油吉林石化公司 炼油厂,吉林 吉林132022;3.车用燃料技术国家重点实验室,河南南阳473000)
0 引言
乙酰丙酸乙酯(Ethyl levulinate,EL)作为一种潜在的绿色生物质基平台化合物,其分子中含有一个羰基和一个酯基,具有良好的反应性,能够进行水解、还原、缩合、亲和加成多种反应.利用以上特性,乙酰丙酸乙酯不仅应用于溶剂、香料、油品添加剂和增塑剂等行业,还作为重要的医药和化工原料.另外,乙酰丙酸乙酯还是一种新型的液体燃料添加剂,被广泛应用于石油替代能源领域[1].
近年来,人们开始关注利用生物质直接转化制备乙酰丙酸乙酯的研究.许多研究者报道了利用葡萄糖原料制备乙酰丙酸乙酯的研究[2-5],但对纤维素生物质原料转化生成乙酰丙酸乙酯的研究却少有报道.Graves曾研究了纤维素在醇中经强酸催化酯化工艺的可行性,在高温及酸催化剂的作用下,纤维素生成乙酰丙酸乙酯的产率为44%[6].但研究者未对纤维素的降解规律进行系统研究,而且未对纤维素形态特征的变化进行研究.
据此,笔者主要对纤维素在乙醇体系中直接转化生成乙酰丙酸乙酯的规律进行了研究,分别考察了固液比、反应温度、反应时间和硫酸浓度以及体系中含水量对乙酰丙酸乙酯摩尔产率的影响,并考察了乙酰丙酸乙酯在高温高酸下的稳定性,以及纤维素反应前后结构特征的变化.研究结果可以为纤维素生物质转化制备乙酰丙酸乙酯提供重要的参考和借鉴.
1 实验部分
1.1 实验试剂与实验装置
纤维素粉(粒径:90 μm)、乙酰丙酸乙酯,分析纯,上海阿拉丁有限公司;无水乙醇,正辛醇,硫酸,均为分析纯,天津风船试剂.实验采用容积为200 mL的间歇式高压反应釜,材质为316 L不锈钢.该装置的最高工作温度为300℃,设计压力20 MPa,釜内温度通过与之相连的热电偶温度计测得.
1.2 实验步骤
将纤维素放置在105℃的烘箱中干燥24 h,并根据实验要求配制一定浓度的硫酸乙醇溶液,硫酸质量与溶液质量之比即为体系中硫酸质量浓度.称取一定量的纤维素,使其与80 mL硫酸乙醇溶液混合均匀后置于200 mL反应釜中,密封反应釜.待反应釜升到设定温度后开始计时.反应完成后,将反应釜取出迅速放入冰浴中进行快速冷却.过滤分离得到液体产物和固体残渣.液体产物用气相色谱进行分析.固相残渣利用扫描电镜、红外吸收光谱仪和X射线衍射仪进行分析.
1.3 分析方法
1.3.1 液相产物的分析方法
利用气相色谱仪(GC1690)对液相产物中的乙酰丙酸乙酯进行了定性和定量分析,气相色谱分析条件为:FFAP毛细管柱(30 m×0.32 mm×0.33 μm,大连中汇达科学仪器有限公司),氢火焰离子化检测器(FID);程序升温:柱温90℃,保持3 min,然后以10℃/min速度升至210℃,再保持10 min;汽化室温度240℃;检测器温度250℃;进样量1 μL,分流进样;载气为氮气.乙酰丙酸乙酯摩尔产率的计算如式(1)所示,m1为反应后乙酰丙酸乙酯的质量,m0为纤维素原料的质量,M1为乙酰丙酸乙酯的摩尔质量(144 g/mol),M0为纤维素的摩尔质量(162 g/mol):
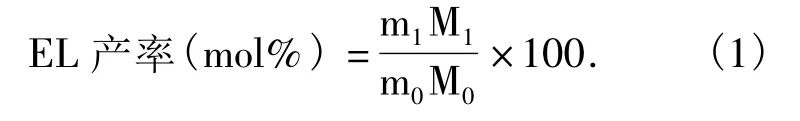
1.3.2 固相残渣的分析方法
利用扫描电镜(JSM-7500F)对固体残渣的形貌进行了表征.技术参数为:分辨率为1.0 nm(15 kV)/1.4 nm(1 kV);加速电压为0.1~30 kV;放大倍数为25~100万倍;束流强度:10-13~2×10-9.
利用红外吸收光谱仪分析了固体残渣官能团的变化.光谱扫描范围为4 000~400 cm-1,测定分辨率为2 cm-1,扫描次数为32.
利用X射线衍射仪(X'Pert PRO)对固体产物的晶态结构进行了分析.工作条件为:Cu Kα射线,波长λ=0.154 18 nm,镍滤波,管压40 kV,管电流40 mA,扫描范围(2θ)为 5°~80°,扫描速度为4.0°/min.
2 结果与讨论
2.1 纤维素降解产物分析
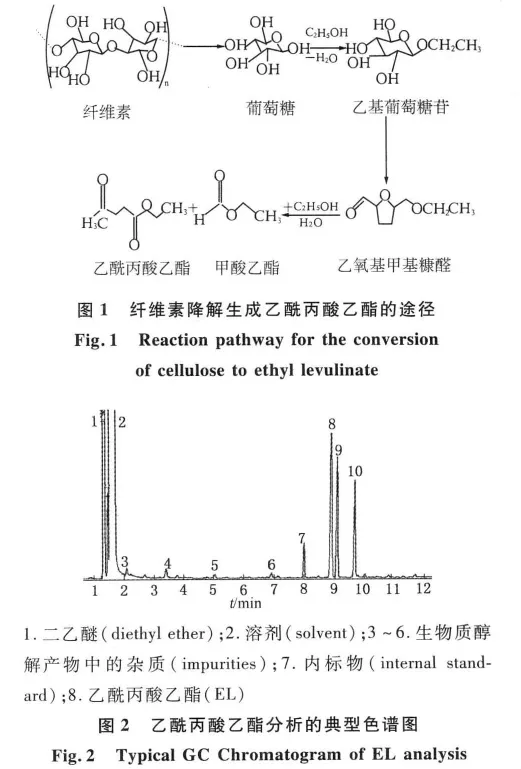
在酸催化作用下,纤维素首先会降解生成葡萄糖.葡萄糖与乙醇在无机酸的高温催化下脱水形成乙基葡萄糖苷,进一步转化为乙氧基甲基糠醛,乙氧基甲基糠醛醇解为乙酰丙酸乙酯和甲酸乙酯[2].其反应途径如图1所示.对反应后液相产物进行GC-MS分析发现,EL是液相中的主要产物.液相中还含有小分子的有机酸酯类,如:甲酸乙酯、乙酸乙酯、丙酸乙酯、丙酮酸乙酯等和糠醛类物质,如:糠醛、5-甲基糠醛、2-甲基呋喃及呋喃酮类等.这些副产物主要来自于纤维素分子的C—C、C—H、C—O 键,经过断键、脱水、重整、酯化等反应而成.图2显示了在设定条件下内标物和反应产物的典型图谱.在此基础上,进一步考察了不同反应条件对EL产率的影响.
2.2 反应温度对乙酰丙酸乙酯产率的影响
在反应过程中,温度对纤维素的醇解起着重要作用.图3显示了当硫酸浓度为1 wt%,固液比(m固/V液)为1∶15时,反应温度对乙酰丙酸乙酯产率的影响.从图中可以看到,当反应温度为170℃时,EL产率随反应时间的延长逐渐升高,反应60 min后仍未达到平衡.当反应温度为190℃,反应时间为30 min时,EL产率达到最高,为42.68%.温度达到210℃,反应15 min即达到平衡,延长反应时间,EL产率反而下降,可能是由于EL在较高温度下稳定性不佳导致的.因此温度越高,醇解反应速率越快,达到平衡所需时间越短,但较高的温度并不利于乙酰丙酸乙酯产率提高.
2.3 硫酸浓度对乙酰丙酸乙酯产率的影响
当反应温度为190℃,固液比为1∶15,考察了硫酸浓度对EL产率的影响.如图4所示,硫酸浓度越高,反应达到平衡所需的时间越短,即硫酸浓度的提高可以加快反应速率.但是当硫酸浓度为2.0 wt%,反应时间为30~60 min,EL的产率逐渐下降,说明酸度过高可能导致体系发生一些副反应,从而降低EL的稳定性.此外,从工业生产的角度出发,酸度越高,对反应器的防腐蚀性要求越高,进而增加生产成本.在后续实验中,选用1.0 wt%的硫酸作为催化剂.

2.4 固液比对乙酰丙酸乙酯产率的影响
固液比能显著地影响反应体系中纤维素向EL的转化,这主要是因为较低的固相浓度能够增大硫酸产生的氢离子与体系中纤维素的接触机率,从而能更好地催化纤维素进行醇解.当固液比过大时,整个反应体系的流动性降低,造成固相和液相之间的混合性及传热性下降,不利于纤维素的醇解[7].因此有必要对体系中的固液比进行选择.反应温度为190℃,硫酸浓度为1.0 wt%,反应时间为30 min,研究了不同固液质量体积比(g/mL)对EL产率和反应液中EL浓度的影响,如图5所示.随着固液比的减少,EL的产率逐渐增加,最高可达47.10 mol%.然而随着固液比的减小,反应体系中EL的浓度逐渐下降,当EL的产率达到最高时,反应液中EL的浓度则只有11.16 g·L-1.综合考虑纤维素的利用率、设备的效率、EL的产率以及体系中EL的浓度,选定固液质量体积比(g/mL)为1∶15,进行后续试验研究.

图5 固液比对EL产率和浓度的影响Fig.5 Effect of liquid solid ratio on the yield and the concentration of EL
2.5 含水量对乙酰丙酸乙酯产率的影响
纤维素降解过程中需要水的参与,因此有必要对体系中含水量对EL产率的影响进行研究,以体系中水占总溶液的体积分数作为考察指标.图6所示为硫酸浓度为1.0 wt%,反应温度为190℃,固液比为1∶15,含水量分别为0%、10%、30%和50%对EL产率的影响.从图中可以看出,EL的产率随着反应时间的延长逐渐增大,当反应时间相同时,含水量越高,EL的产率越低.这主要是由于在乙醇—水体系中存在着水解和醇解两条降解路径,当体系含水量增加时,主反应更倾向于水解反应,生成更多的水解产物乙酰丙酸,而不是醇解产物乙酰丙酸乙酯[8].

图6 含水量对EL产率的影响Fig.6 Effect of water addition on the yield of EL
2.6 反应前后纤维素的SEM分析
反应前后纤维素的SEM分析如图7所示,其中图7(a)为新鲜纤维素的SEM图像,7(b)为温度190℃,反应时间为30 min,硫酸浓度为1.0 wt%时的固体残渣的SEM图像.从图7(a)中可以看到新鲜的纤维素表面光滑平整,缺陷少,而且显微结构明显.图7(b)中纤维素表面出现不规则结构,而且纤维结构也发生了扭曲,这可能是由于反应温度的升高使得纤维素发生一定程度的降解所致.

图7 反应前后纤维素SEM图Fig.7 SEM images of original cellulose and the residue of cellulose
2.7 反应前后纤维素的XRD分析
通过对固体残渣进行XRD分析,可以对纤维素在反应过程中结晶结构的变化有更清晰的认识.图8中(1)表示新鲜纤维素,(2)~(4)表示反应温度为190℃,硫酸浓度为1.0 wt%,反应时间分别为0 min、30 min、60 min时固体残渣的XRD图.如图8所示,随着反应时间的延长,与新鲜纤维素相比,特征衍射峰强度逐渐减小.反应时间为30 min时,2θ =14.8°和16.5°处的衍射峰消失.当反应时间为60 min时,固体残渣的晶体结构遭到了氢离子的严重破坏,使得XRD图中的衍射峰没有规律,这也说明在此过程中纤维素发生大量降解和转化.
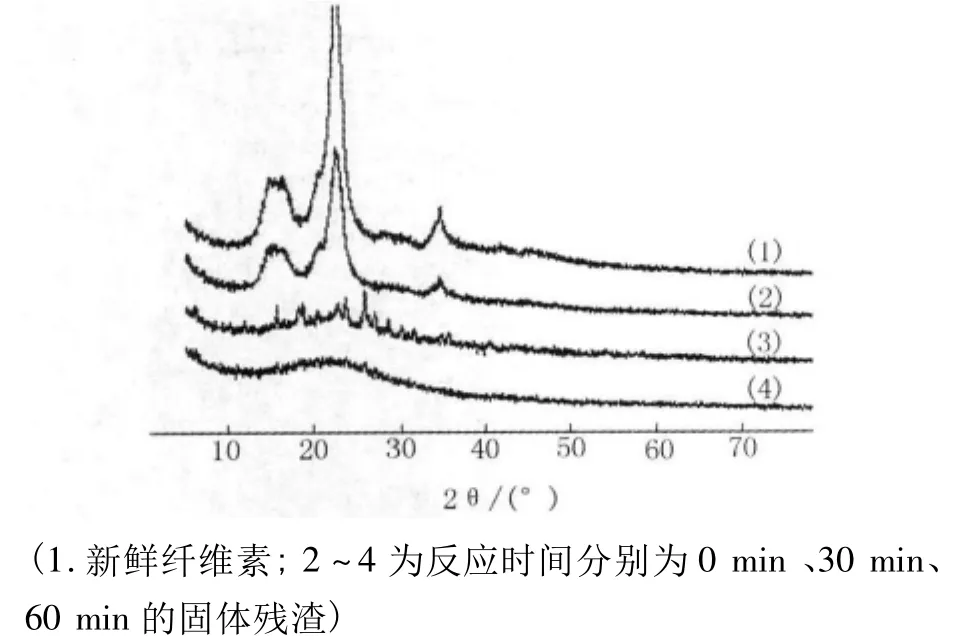
图8 应前后的纤维素的XRD图谱Fig.8 XRD patterns of original cellulose and residues
2.8 反应前后纤维素的FT-IR分析
纤维素经过醇解后固体残渣的红外光谱图如图9所示.其中图谱(1)代表新鲜的纤维素,图谱(2)和(3)代表反应温度为190℃,硫酸浓度为1.0 wt%,反应时间分别为0、30 min的固体残渣.从图中可以看出,(1)与(2)中各主要峰出现的波数基本相同并未引入新的基团.在(3)中,3 430 cm-1处的纤维素羟基振动伸缩峰、2 900 cm-1处的纤维素中的甲基、亚甲基中的C—H伸缩振动峰以及1 059 cm-1处的纤维素糖苷键C—O—C的不对称伸缩振动峰均有所减弱[9],说明在反应过程中纤维素的晶体结构被破坏并发生降解,部分官能团也发生了变化.
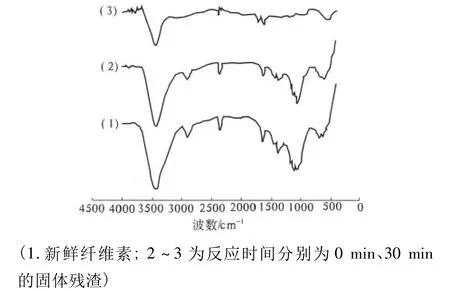
图9 反应前后纤维素的红外图谱Fig.9 T-IR spectra of original cellulose and after reaction
3 结论
对纤维素在乙醇体系中直接转化生成EL的研究表明:当纤维素粒径为 90 μm,固液比为1∶15,硫酸浓度为1.0 wt%,反应温度为190℃,反应时间为 30 min时,EL产率达到最高,为42.68 mol%.反应温度的升高和硫酸浓度的增大都能够促进纤维素的转化,但高温高酸条件下不利于纤维素生成EL,此外,体系中含水量越高,EL的产率越低.反应时间的延长会使得EL的稳定性下降.通过扫描电镜、X-射线衍射和红外吸收光谱对反应前后纤维素进行了表征.结果表明,在乙醇体系中,纤维素明显发生降解,外部形貌和结晶结构发生很大改变.
[1]BOZELL J J.Technology development for the production of biobased products from biorefinerty carbohydrates-the US Department of Energy’s“Top 10”revisited[J].Green Chemistry,2010,12(4):539-554.
[2]PENG Lin-cai,LIN Lu,ZHANG Jun-hua,et al.Solid acid catalyzed glucose conversion to ethyl levulinate[J].Applied Catalysis A,2011,397(1/2):259-265.
[3]Saravanamurugan S,Riisager A.Solid acid catalysed formation of ethyl levulinate and ethyl glucopyranoside from mono or disaccharides[J].Catalysis Communica-tions,2012(17):71-75.
[4]吴晓宇,吕秀阳,陈天,等.近临界甲醇中稀硫酸催化葡萄糖醇解反应动力学[J].化工学报,2010,61(10):2587-2589.
[5]PENG Lin-cai,LIN Lu,LI Hui.Extremely low sulfuric acid catalyst system for synthesis of methyl levulinate from glucose[J].Industrial Crops and Products,2012(40):136-144.
[6]GARVES K.Acid catalyzed degradation of cellulose in alcohols[J].Wood Chem Technol,1988,8(1):121-134.
[7]GIRISUTA B,JANSSEN L P.Kinetic study on the acid-catalyzed hydrolysis of cellulose to levulinic acid[J].Ind Eng Chem Re,2007(46):1696-1679.
[8]HU Xun,LIEVENS C,LARCHER A,et al.Reaction pathways of glucose during esterification:Effect of reaction parameters on the formation of humin type polymers[J].Bioresource Technology,2011(102):10104-10113.
[9]晏群山,黄富邦,武书彬.高温液态水预处理蔗渣的研究[J].食品工业科技,2012,33(7):260-263.

