8-甲氧基补骨脂素柔性纳米脂质体不同研制方法的比较*
广东省第二人民医院皮肤科(广州510317) 郑荣昌 马 静 周贵滨 秦 思 温 炬
柔性纳米脂质体(flexible nano-liposomes,FNL)又称传递体或变形脂质体,是将表面活性剂(如胆酸钠、去氧胆酸钠等)加入到制备脂质体的类脂材料中制成的具有高度自身形变、可高效地穿过比其自身小数倍的皮肤孔道的类脂质体,具有高效渗透性、高度柔韧性和高亲水性[1]。柔性纳米脂质体的结构类似生物膜,是一种多功能的定向药物载体,能使更多的药物保留在皮肤中,减少药物进入血循环,在表皮和真皮内形成药物贮库,使药物持久地作用于病变部位。8-甲氧基补骨脂素(MOP)是治疗白癜风的重要药物[2]。本实验通过不同方法研制8-甲氧基补骨脂素柔性纳米脂质体,筛选合适的制作方法。
材料与方法
1 材 料 ①试 剂:注射用大豆磷脂(上海浦江磷脂有限公司),胆固醇(中国医药(集团)上海化学试剂公司),胆酸钠(中国医药(集团)上海化学试剂公司),8-甲氧基补骨脂素(重庆友邦制药),所有试剂均为分析纯。②仪器:日立H-00透射电镜(日本Hitachi公司),高效液相色谱仪(日本岛津公司),旋转蒸发器(上海亚荣生化仪器厂),超声波粉碎机(美国Auto Science),分析天平(中国湖南湘仪厂),酸度计(上海精密科学仪器有限公司雷磁仪器厂),改良的Franz扩散池(自制),UV-2201紫外可见分光光度计(日本岛津),电子恒温水浴锅(天津市泰斯特仪器有限公司)。
2 方 法 基本配方:根据正交实验设计及预试验,确定基本配方:大豆磷脂∶胆固醇∶MOP∶胆酸钠=20∶10∶3∶10,分别采用逆相蒸发法、乙醚注入法、薄膜法、薄膜-超声法等方法制备MOP柔性纳米脂质体。①逆相蒸发法制备大单层脂质体:按处方量将药物溶于60ml氯仿-甲醇((2∶1)液,加入PBS 15ml,水浴式超声仪超声30min,倒入500ml烧瓶中,置于40℃水浴,减压除去有机溶剂,达胶态后滴加PBS(10mmol/L)5ml,旋转使壁上的凝胶脱落,继续减压蒸发即可制得透明的均匀乳白色液体。②乙醚注入法:水相:磷酸盐缓冲液((0.05mol/L,pH7.3)4ml放入试管中,置于55℃至60℃水浴中;有机相:乙醚2ml溶解总脂及 MOP;用带5号针头的注射器以0.25ml/min速度将有机相注入水相中,不断搅拌至有机溶剂除尽,直至得到透明的均匀乳白色液体。③薄膜法制备多室脂质体:按处方量将药物溶于60ml氯仿-甲醇(2∶1)液,置于500ml圆底烧瓶中,用旋转蒸发器减压旋转去除有机溶剂,形成均匀薄膜。取5ml PBS(10mmol/L)加热至55℃,倾入薄膜中,浸入55℃水浴中搅拌30min,直至得到透明的均匀乳白色液体。④薄膜-超声法制备小单层脂质体:将③制得的脂质体再经超声即得。用水浴式超声处理机处理30min,再在探头式超声仪上超声粉碎5次,每次3min,直至形成均匀的上清液。4000g离心10min,收集上清液得到透明的均匀乳白色液体。
3 纳米脂质体质量评价 ①高效液相色谱(HPLC)测定MOP柔性纳米脂质体含量:取1ml脂质体以PBS稀释至100ml,取5ml置于25ml量瓶中,加甲醇定容,超声5min,0.45μm 微孔滤膜过滤后,精密进样2μl。另取 MOP对照品溶液(10ug/ml)20μl进样,外标法计算含量。②凝胶柱法测定包封率:取MOP柔性纳米脂质体1g,用PBS 20ml混悬均匀,上葡Sephadex G-25柱,用PBS洗脱,接取流分100ml,流速3ml/min,取含药脂质体流分5ml置于25ml量瓶中,加甲醇定容,超声处理5min,0.45mm微孔滤膜过滤,取20μl进样,计算包封于脂质体中的药物W1。同时,取柔性纳米脂质体1g,用PBS 100ml混悬均匀,然后取5ml用甲醇稀释至25ml,超声处理5min,0.45μm微孔滤膜过滤,进样20μl。计算得总药物量W2,按下式计算包封率:EE=W1/W2×100%。③负染-电镜法测定粒径:取柔性纳米脂质体样品适量,用PBS稀释200倍,滴于铜网上,2%磷钨酸负染,自然晾干,5000-20000倍电镜下观察并拍照。随机测定5个视区,每个视区测定50个柔性纳米脂质体的粒径,以照片粒径除以放大倍数即得柔性纳米脂质体的粒径大小。④Zeta电位测定:取MOP柔性纳米脂质体1ml,PBS 1ml稀释,检测。测定条件:电流0.43mv、电场16.24V/cm、波长660nm。
4 统计学分析 采用SPSS13.0进行统计学分析。试验结果以±s表示。各组均数间差异使用方差分析;P<0.05为差异具有统计学意义。
结 果
1 不同制备方法MOP脂质体含量、包封率、平均粒径、Zeta电位 见表1。逆相蒸发法制备的脂质体包封率低,粒径大;乙醚注入法包封率低且平均粒径小;薄膜法包封率高,粒径大;薄膜-超声法包封率高,平均粒径适中。
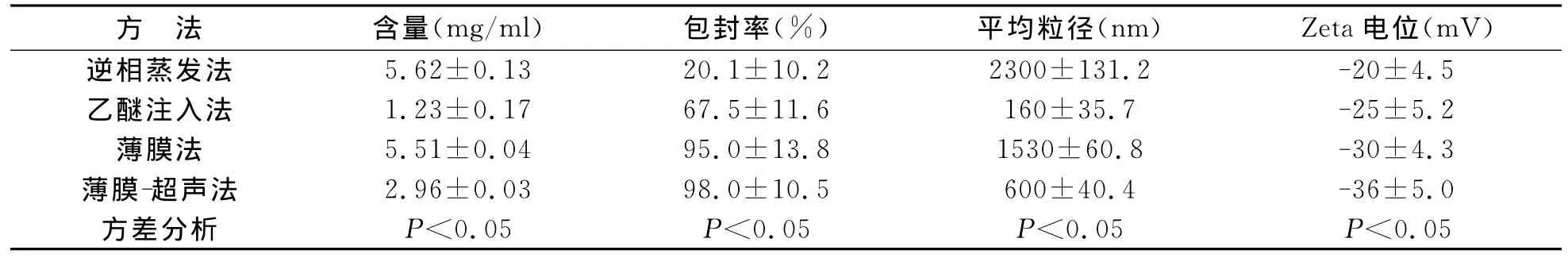
表1 不同制备方法MOP脂质体含量、包封率、平均粒径、Zeta电位的测定
2 时间对薄膜-超声法制备脂质体质量的影响见表2。随着超声时间的延长,薄膜-超声法制备的MOP柔性纳米脂质体粒径越小,同时包封率也明显下降。
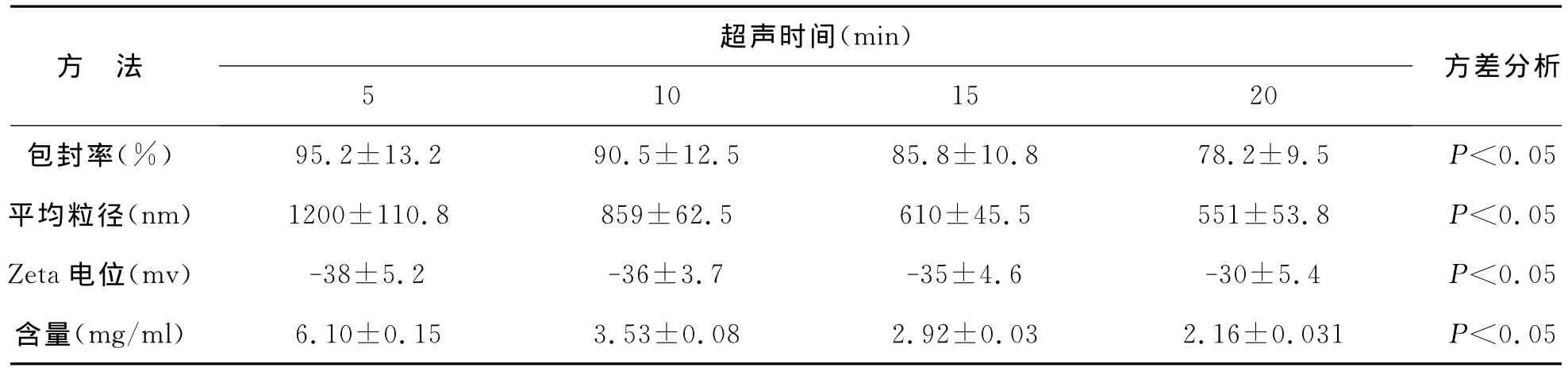
表2 时间对薄膜-超声法制备脂质体质量的影响
讨 论
FNL是将表面活性剂(如胆酸钠、去氧胆酸钠等)加入到制备脂质体的类脂材料中制成的具有高度自身形变、可高效地穿过比其自身小数倍的皮肤孔道的类脂质体,具有高效渗透性、高度柔韧性和高亲水性。普通脂质体的制备配方中不含胆酸钠。
不同工艺制备的脂质体的成层性、均匀性、粒径、荷电等均不一样,影响脂质体的包封率、稳定性以及脂质体与皮肤的的相互作用如脂质体渗透皮肤的量及程度。目前常用的方法有逆相蒸发法、乙醚注入法、薄膜法、薄膜-超声法。逆相蒸发法通常制备大单层脂质体,特点是可包裹较大的水容积,适合于包裹水溶性药物、大分子生物活性物质如胰岛素、干扰素等,薄膜法常用于制备多室脂质体,超声法制备的脂质体以小单层为多,因此应根据实验目的选择制备工艺。脂质体的大小影响其透皮吸收。直径600nm以下的脂质体非常容易穿透皮肤,而直径1000nm以上的脂质体则易停留在角质层内[3]。脂质体的荷电荷能够减少相互间的聚集和融合,增加稳定性。通过调整组分的荷电性质和荷电量及介质的离子强度,可以使Zeta电位保持在足够高的水平,阻止粒子间相互集聚。Zeta电位是衡量电荷多少的一个重要指标,当Zeta电位大于60mV时,荷电粒子相当稳定;Zeta电位在30~60mV时,荷电粒子比较稳定;Zeta电位小于30mv时,荷电粒子不稳定,容易聚集[4]。
本试验中逆相蒸发法和薄膜法制备的MOP脂质体的包封率很高,但粒径较大,且粒径分布不均匀;乙醚注入法则包封率较低,仅为45.3%,且平均粒径太小。薄膜-超声法置备的MOP脂质体包封率高,平均粒径适中,基本满足皮肤局部用脂质体的粒径要求,且Zeta电位负值较高,预示稳定性较好。薄膜-超声法中超声时间的长短也影响了脂质体的质量。超声时间越长粒径越小,同时包封率也有所下降较明显。超声15min获得的脂质体包封率较高,平均粒径大小合适,Zeta电位的负值也比较高。综上所述,采用薄膜-超声法,超声时间15min是制备补骨脂素柔性纳米脂质体是比较适宜的方法。
补骨脂素是白癜风治疗最常用且疗效肯定的药物。目前局部外用补骨脂素有酊剂、凝胶,存在药物渗透性差;易出现红斑、水疱、大疱等副作用。补骨脂素柔性纳米脂质体作为新型药物载体,可减少相关副作用。在后续研究中将进一步探讨补骨脂素柔性纳米脂质体的药代和药效学特点。
[1] Cevc G,Gebauer D,Stieber J,et al.Ultraflexible vessicles,Transfrsomes,have an extremely low pore penetration resistance and transport the rapeutic amountsof insulin across the intact mammalian skin [J].Biochem Biophy Acta,2008,1368(2):201.
[2] Jam WD,Berger T,Elston D.Andrews’Disease of the Skin[M].The tenth edition.USA:Elsvier,2006:160.
[3] Schramloval J,Blazek K,Bartackova M,et al.Electron microscopic demonstration of the penetration of liposomes through skin[M].Folia Biol Praha,1997,43(4):165.
[4] 刘 辉,汤 韧,何晓霞,等.脂质体处方和制备方法对阿昔洛韦棕榈酸酯脂质体稳定性的影响[J].药学学报,2002,37(7):563-566.

