星点设计-效应面法优化脂溶性丹参提取物速释滴丸处方工艺
符少莲, 冯翠娟, 李 沙
(暨南大学药学院药剂学教研室,广东广州510632)
丹参为唇形科多年生草本植物丹参Salvia miltiorrhiza Bge.的干燥根及根茎。性微寒,味苦,具有活血调经,凉血消痈,清心安神的功效[1]。丹参酮是丹参中具有橙黄色和橙红色特征的脂溶性有效成分,大量研究表明丹参酮在抗肿瘤、心脑血管疾病、抗菌消炎等方面均有良好的治疗作用[2-4],但丹参酮在水中的溶解度极小,口服给药生物利用度低,从而影响了其药效作用的发挥[5-6]。为改善其溶出,已有研究报道将其制成固体分散体、环糊精包合物等[7-8],均能有效提高其溶出度。但这些研究均以纯度很高的丹参酮ⅡA为研究对象,而工业生产中目前主要使用的原料是丹参提取物。为此本研究采用丹参提取物作为研究对象制备滴丸,以提高丹参脂溶性成分的溶出性能。
采用适宜的水溶性基质将难溶性药物制成滴丸,可有效地提高其溶出性能,且滴丸因具有操作简便,生产周期短,剂量准确,便于贮存和服用的优点而得到广泛研究[9]。丹参酮ⅡA是丹参中脂溶性成分的代表[10],本实验在前期单因素试验的基础上,以丹参酮ⅡA作为代表性成分,测定其累积溶出百分率作为评价指标,采用星点设计-效应面法进一步优化处方,研制速释型脂溶性丹参提取物滴丸,更适合于工业化生产与临床用药需求。
1 仪器与材料
DF-101S集热式恒温加热磁力搅拌器 (巩义市英峪予华仪器厂);RCZ-8A智能药物溶出仪 (天津大学精密仪器厂);高效液相色谱仪 (岛津公司LC-10A);滴丸机 (广东正洪公司)。
脂溶性丹参提取物 (丹参酮ⅡA纯度40%,广州美晨药业有限公司,丹参酮ⅡA纯度47%,批号080906);丹参酮ⅡA对照品 (中国药品生物制品检定所,批号2006019);聚乙二醇 (PEG)2000(广东光华化学厂有限公司,20100918);聚乙二醇4000(广东光华化学厂有限公司,20100413);十二烷基硫酸钠 (SDS,上海晶纯实业有限公司,1098983);甲醇 (色谱纯)。
其他试剂和试药均为分析纯,实验用水为双蒸水。
2 方法与结果
2.1 滴丸的制备 称取适量PEG 2000与PEG4000于60℃水浴中熔融,加入脂溶性丹参提取物,搅拌一定时间,使其均匀分散,最后将药液滴入液体石蜡冷却液中冷凝成丸,待滴丸完全冷却后,取出滴丸,去除表面附着的液体石蜡,放入真空干燥箱中干燥12 h即得。
2.2 体外溶出试验 参照《中国药典》2010年版二部溶出度测定法第一法进行溶出实验,以1%SDS(十二烷基磺酸钠)水溶液为溶出介质,温度(37±0.5)℃,转速100 r/min进行试验,于5、10、20、30、45、60 min分别取样2 mL,用0.45 μm微孔滤膜滤过,同时补加等量同温溶出介质。取续滤液采用HPLC方法测定其中丹参酮ⅡA的量,并计算累积溶出百分率,作为处方优化的评价指标。
2.3 丹参酮ⅡA测定方法的建立 采用HPLC法建立丹参酮ⅡA的测定方法。
2.3.1 色谱条件 汉邦Hedera C18色谱柱(4.6 mm×150 mm,5 μm);流动相为甲醇-水 (85∶15);检测波长为270 nm;体积流量为1.0 mL/min;进样量为 20 μL。
2.3.2 溶液的制备 (1)对照品溶液:取丹参酮ⅡA对照品约10 mg,精密称定,置25 mL棕色量瓶中,用甲醇溶解并稀释至刻度,作为对照品贮备液,再根据需要用甲醇稀释成相应浓度。 (2)脂溶性丹参提取物溶液:精密称取脂溶性丹参提取物适量,置于10 mL棕色量瓶中,用甲醇溶解,并稀释至刻度,摇匀即得。(3)供试品溶液:取制得的滴丸,研细,取约0.02 g,精密称定,置于25 mL棕色量瓶中,加甲醇15 mL超声20 min,再加甲醇至刻度,摇匀,用微孔滤膜 (0.45 μm)滤过,取续滤液,即得。(4)阴性对照液:取对应量的空白载体材料,精密称定,按供试品溶液项下操作,制成阴性对照品溶液。(5)脂溶性丹参提取物溶出液:精密称取脂溶性丹参提取物适量,进行溶出试验,于60 min取样2 mL,滤过,取续滤液,即得。(6)滴丸溶出液:取某一代表性处方制备的滴丸,进行溶出试验,于60 min取样2 mL,滤过,取续滤液,即得。(7)溶出试验阴性对照液:取对应量的空白载体材料,精密称定,进行溶出试验,于60 min取样2 mL,滤过,取续滤液,即得。
2.3.3 专属性考察 按2.3.1项色谱条件,分别取丹参酮ⅡA对照品溶液 (40 mg/L)、脂溶性丹参提取物溶液 (含丹参酮ⅡA40 mg/L)、供试品溶液 (含丹参酮ⅡA 40 mg/L)、阴性对照液、脂溶性丹参提取物溶出液、滴丸溶出液、溶出试验阴性对照液各 20 μL进样,记录 HPLC图谱 (图 1、2)。提取物中丹参酮ⅡA在所用色谱条件下,分离度好,峰形对称稳定,保留时间约为9.7 min。载体材料与溶出介质在丹参酮ⅡA色谱峰处无干扰。
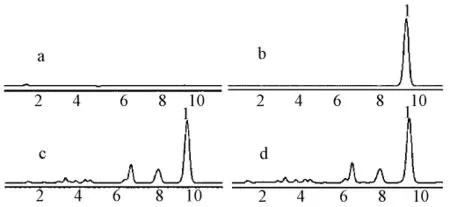
图1 高效液相色谱图Fig.1 HPLC chromatograms
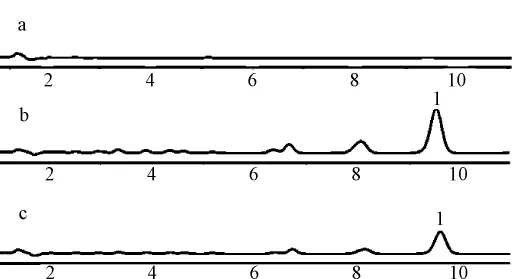
图2 溶出样品高效液相色谱图Fig.2 Typical HPLC chromatograms of drug dissolution samples
2.3.4 标准曲线的建立 精密量取适量2.3.2项下的对照品贮备液,用甲醇稀释成0.2、0.5、1、5、10、20、40、80 mg/L的标准溶液,进样测定,结果在0.2~80 mg/L内,峰面积 (A)与药物浓度 (C)有良好的线性关系,回归方程为A=126831C+4968.1,r=0.9999。
2.3.5 日内与日间精密度试验 精密吸取丹参酮ⅡA对照品溶液 (40 mg/L)20 μL,连续进样6次,记录峰面积,计算RSD为日内精密度;精密吸取丹参酮ⅡA对照品溶液 (40 mg/L)20 μL,连续进样3次,连续5 d,记录峰面积,计算RSD为日间精密度。测得日内精密度为1.11%,日间精密度为0.53%,表明方法精密度良好。
2.3.6 稳定性考察 配制3份供试品溶液和3份具代表性的滴丸溶出样品,置于室温,分别于0、4、8、12、24 h进样,记录峰面积及计算RSD。供试品溶液RSD分别为1.42%、1.92%、1.89%,滴丸溶出样品 RSD分别为0.75%、1.56%、1.42%,说明待测样品在24 h内稳定。
2.3.7 重复性试验 按2.3.2项下方法平行制备六份供试品溶液,分别取20 μL进样测定,连续进三针,按外标一点法用峰面积计算样品中丹参酮ⅡA的含量,计算平均值与RSD。测得丹参滴丸中丹参酮ⅡA的质量分数为 (47±0.6)mg/g,RSD为1.31%,说明方法的重复性好。
2.3.8 加样回收率试验 取制得的滴丸,研细,取约8.5 mg,精密称定,置于10 mL棕色量瓶中,共9份,3份一组,分别精密加入相当于样品处方中丹参酮ⅡA量的80%、100%、120%的对照品溶液,按2.3.2项下方法制成供试品溶液,进样20 μL测定峰面积,按外标一点法计算丹参酮ⅡA的量,求得高、中、低3个加样量下的平均回收率分别为100.68%、101.46%、101.67%,表明样品回收率符合要求。
2.4 单因素考察与结果 按2.1项法制备滴丸,选取两种载体比例、药物与载体比例、搅拌时间作为考察因素,以累积溶出百分率为评价指标,通过单因素试验评价各处方工艺因素对滴丸溶出性能的影响。具体因素水平分别为:PEG 2000∶PEG4000(1∶9、3∶7、5∶5、7∶3)、药物∶载体 (1∶11、1∶9、1∶7、1∶5)、搅拌时间 (1、2、3 h)。结果见图3。
由图3结果可知,以PEG 2000与PEG 4000作为载体材料制备滴丸能有效提高脂溶性丹参提取物的溶出效果,利用SPSS软件对各取样时间点的溶出数据分别进行单因素方差分析,结果显示,两种载体比例、药物与载体比例这两个因素对各时间点溶出结果的影响有显著差异 (P<0.05),搅拌时间对各时间点溶出结果则没有显著影响 (P>0.05)。单因素考察结果显示PEG 2000∶PEG 4000为3∶7、药载比为1∶9时,丹参酮ⅡA释放最快最完全。
2.5 星点设计与处方优化
2.5.1 星点设计实验与结果 在单因素试验的基础上,确定PEG 2000与PEG 4000的比例、药物与载体比例作为考察因素,以累积溶出百分率为评价指标进行2因素、5水平的星点设计。根据2.4项的单因素考察结果选取两因素的极大值和极小值水平,各因素水平代码值和实际操作物理量值见表1。按照星点设计原理安排13次试验,各试验的溶出结果见表2。
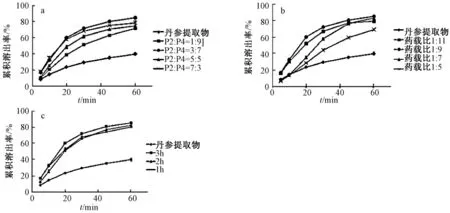
图3 处方工艺因素对滴丸溶出效果的影响 (n=3)Fig.3 Effect of the formulation and process factors on the dissolution behaviour of dropping pills(n=3)
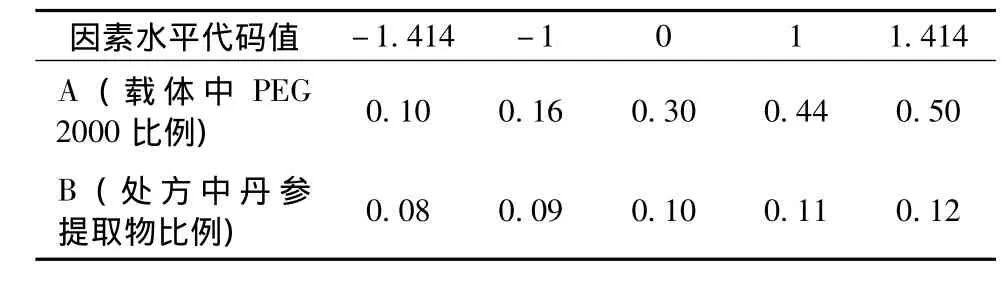
表1 各因素各水平的代码值及实际数值Tab.1 Factors and levels in code and actual values
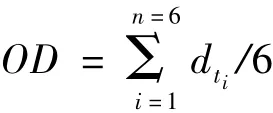
2.5.2 数据分析 以载体比例和药载比为自变量,累积溶出百分率的“总评归一值”为因变量,采用Design Expert 7.0软件进行多元线性回归和二次多项式回归,并以拟合优度 (r)和置信度 (P)作为模型判定标准。

表2 实验设计及溶出试验结果Tab.2 Experimental design and results of dissolution test
多元线性模型公式为R=X0+X1A+X2B,二次多项式模型公式为R=X0+X1A+X2B+X3AB+X4A2+X5B2。实验结果拟合得到的多元线性方程为R=1.509+1.412A– 13.044B(P=0.029,r=0.713),二次多项式模型方程为:R=-5.189+3.668A+118.581B+42.5AB-10.844A2-721.875B2(P=0.003,r=0.946),两种模型均P<0.05,但线性模型方程的复相关系数r太低,预测性相对较差,因此选择二次多项式模型进行处方优化,其拟合参数值见表3。
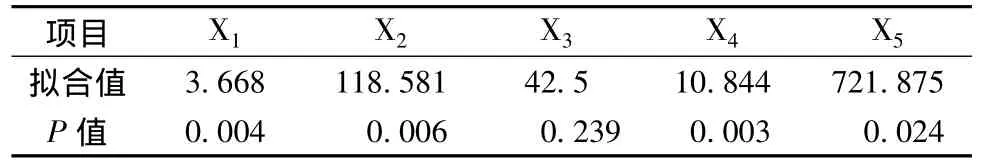
表3 二次多项式模型方程中各项的拟合参数值及统计学检验结果Tab.3 Values of fitting parameters in quadratic polynomial model equation and statistical test
2.5.3 效应面优化 根据拟合方程,通过Design Expert 7.0软件绘制评价指标OD值随因素变化的效应面图和等高线图 (图4、图5)。
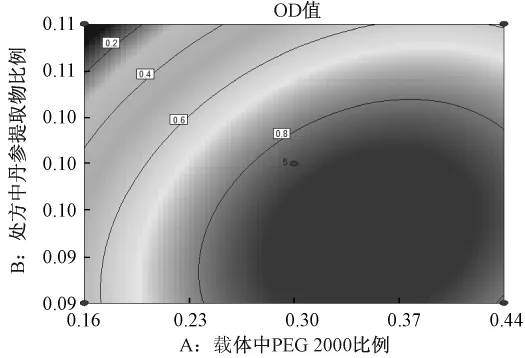
图4 等高线图Fig.4 Contour map

图5 效应面图Fig.5 The response surface graph
图4、图5显示,随着PEG 2000量的不断升高,溶出呈增加趋势,但过高会使溶出减少;随着丹参提取物量的减少,溶出效应升高。从效应面图和等高线图可知,当A的取值范围在0.26~0.40,B的取值范围在0.09~0.10之间时,OD值落在最高效应值区间,即溶出效果最佳,因此确定两个因素的最佳取值范围在此区间。进一步通过Design Expert 7.0软件预测分析,获得一组OD响应值最大的优化条件:A为0.35,B为0.09,在此优化条件下,因变量OD值的预测值为0.93。
2.5.4 优化处方验证 按上述预测的优化处方制备3批样品,进行验证试验,结果见表4。3批样品的OD实测值与预测值间的偏差均小于5%,表明本实验设计方法预测性良好。按照单因素实验获得的最佳条件 (A=0.3,B=0.1)所制备的滴丸,测得OD值均值为0.85(n=3)。经t检验得到,效应面法获得的优化实验条件显著优于单因素实验法 (P<0.01)。
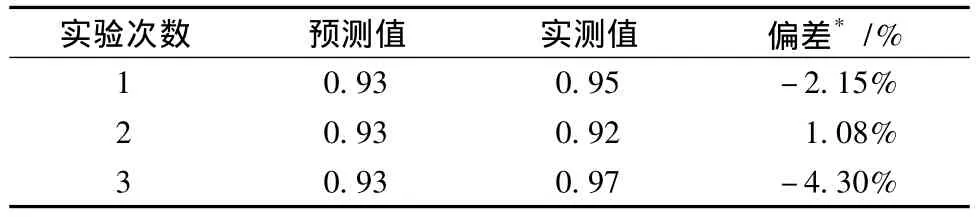
表4 星点设计-效应面法优化处方验证实验结果Tab.4 Validation of the optimized formulation obtained by central composite design-response surface methodology
3 讨论
丹参酮是丹参中含有的脂溶性活性成分,在水中的溶解度小,口服给药生物利用度低。为改善其溶出,本研究采用固体分散技术,将脂溶性丹参提取物制成滴丸。结合药典,选取其中最主要的脂溶性成分丹参酮ⅡA(其量约为药材的0.11% ~0.19%)[11]作为代表性测定成分,评价滴丸对丹参脂溶性成分溶出性能的改善作用。图2溶出液的色谱图显示,制成滴丸后,不但丹参酮ⅡA的溶出明显增加,在相同的时间点下,提取物中其它各成分的峰面积在滴丸组中也均有不同程度的增高,说明本研究所制备的滴丸可提高丹参提取物中各种脂溶性成分的整体溶出性能,达到了预期目的。
以PEG 2000和PEG 4000作为载体材料制备的脂溶性丹参提取物滴丸中,丹参酮ⅡA的溶出得到极显著的提高 (P<0.01),在20 min中时已达到53%,约为提取物原料的2倍。目前上市的丹参速释制剂有复方丹参滴丸,但其所含的有效成分主要为丹参的水溶性成分,如丹参素,尚无丹参脂溶性成分的速释制剂上市。本研究使用工业化生产常用的脂溶性丹参提取物作为原料药制备滴丸,较单体成分的同类研究成本低,更适合临床用药需求,其后期进一步的研发具有较高的可操作性和实际应用价值。
在采用单因素试验进行初步处方工艺优化时,溶出度随着PEG 2000用量的增大有增高的趋势,在PEG 2000与PEG 4000比例为3∶7时溶出度最高,加入过多的PEG 2000不易滴制成丸,因此两者比例选在3∶7附近较为合适。固定载体比例,丹参酮ⅡA的溶出度随着药载比的降低而增加,但当药载比降低到1∶11时,溶出却比1∶9时有所减少。这可能是因为载体量越来越高时,载体在溶出过程中易形成集中层,围绕于药物颗粒周围,因而影响了药物在溶出介质中的溶出[12],因此药载比选在1∶9周围较为合适。
星点设计是国内外近年来常用于优化药材提取工艺与制剂处方工艺筛选的方法,简便、直观,且在模型建立上采用非线性数学模型拟合,复合相关系数较高,预测值更接近真实值[13-15]。与正交设计和均匀设计相比,星点设计试验所得的信息量更大,采用效应面法分析更直观,精密度更高,预测性更好。本实验在单因素考察的基础上,采用2因素5水平星点设计-效应面法优化了脂溶性丹参提取物滴丸的处方,与正交试验常用的3水平相比,增加了考察水平,可使优化结果更具可预测性、准确性。星点设计实验的结果表明,两种载体的比例、药物与载体比例对丹参提取物滴丸的溶出性能有显著影响,通过效应面法预测的优化处方的实验结果与其函数预测值之间的偏差小于5%,表明此法拟合的数学模型方程对因素水平的优化预测性高。
[1]黄兆胜.中药学[M].北京:人民卫生出版社,2006:309-310.
[2]梁 勇,羊裔明,袁淑兰.丹参酮药理作用及临床应用研究进展[J].中草药,2000,31(4):304-306.
[3]吴 杲,何招兵,吴汉斌.丹参酮的药理作用研究进展[J].现代中西医结合杂志,2005,14(10):1382-1385.
[4]李 博,朱平先,吴清华.丹参酮心血管药理作用及临床应用研究[J].江西医学院学报,2009,49(6):126-128.
[5]钱名望,杨保津,顾文华等.丹参有效成分的研究[J].化学学报,1978,36(3):199-205.
[6]Yu Xiyong,Lin Shuguang.Role of P-glycoprotein in the intestinal absorption of tanshinoneⅡA,a major active ingredient in the root of Salvia miltiorrhiza Bunge[J].Current Drug Metab,2007,8(4):325-340.
[7]袁菊勇,毛声俊,沈千万,等.载体联用固体分散技术对丹参酮ⅡA体外溶出的影响[J].中国中药杂志,2009,34(6):685-688.
[8]闫金红,张翠萍,杨 频.羟丙基-β-环糊精与丹参酮IIA包合作用的研究[J].化学学报,2006,64(7):652-656.
[9]张兆旺.中药药剂学[M].北京:中国中医药出版社,2003:382-383.
[10]蔡丽萍,习志刚,杨 红.丹参酮的药理作用和临床研究进展[J].广东药学院学报,2006,24(3):321-324.
[11]赵 娜,郭治昕,赵 雪,等.丹参的化学成分与药理作用[J].国外医药·植物药分册,2007,22(4):155-160.
[12]Li Jin,Liu Pan,Liu Jianping.Novel TanshinoneⅡ A ternary solid dispersion pellets prepared by a single-step technique:In vitro and in vivo evaluation[J].Eur J Pharm Biopharm,2012,80(2):426-432.
[13]吴 伟,崔兴华.星点设计-效应面优化法及其在药学中的应用[J].国外医学药学分册,2000,27(5):292-297.
[14]刘艳杰,项荣武.星点设计效应面法在药学试验设计中的应用[J].中国现代应用药学杂志,2007,24(6):455-457.
[15]刘 芳,傅超美.星点设计-效应面法筛选丹参面膜的主要辅料[J].华西药学杂志,2011,26(4):319-321.

