牛黄消炎片中非法成分土大黄苷的检测
朱南霖, 许 菊
(1.内蒙古大学,内蒙古呼和浩特010021;2.绍兴市食品药品检验所,浙江绍兴 312071)
牛黄消炎片中非法成分土大黄苷的检测
朱南霖1, 许 菊2*
(1.内蒙古大学,内蒙古呼和浩特010021;2.绍兴市食品药品检验所,浙江绍兴 312071)
目的 建立牛黄消炎片中非法成分土大黄苷的检测方法。方法 采用薄层色谱法对牛黄消炎片中有可能投入的伪品大黄中的土大黄苷成分进行薄层鉴别;采用高效液相色谱-二极管阵列检测法对土大黄苷成分作进一步定性鉴别。结果 对牛黄消炎片中存在的非法成分土大黄苷能有效检测。结论 该方法操作简便,灵敏可靠,可用于牛黄消炎片中非法成分土大黄苷的检查。
牛黄消炎片;土大黄苷;TLC;HPLC
牛黄消炎片为收载于《中国药典》的中成药[1],其处方由人工牛黄、珍珠母、蟾酥、青黛、大黄、天花粉、雄黄组成,其中的大黄目前市场中存在多个《中国药典》收载品种以外的混伪品,并存在充正品投料的现象,这些混伪品大多含有土大黄苷成分,而有3个植物来源 (掌叶大黄、唐古特大黄和药用大黄)的正品大黄不含有此成分[2-4]。近年国家食品药品监督管理局尚有对含大黄成分的中成药 (如牛黄解毒片、炎可宁片等)检查土大黄苷的药品检验补充检验方法颁布[5],但尚无牛黄消炎片中检测非法成分土大黄苷的补充检验方法,也未见有关报道。为此,通过查阅相关文献[6-12],采用薄层色谱法和高效液相色谱法,建立了牛黄消炎片中土大黄苷成分的检测方法,可方便的检查出投料大黄的真伪情况。现将检测方法介绍如下,以供质量控制参考。
1 仪器与试药
1.1 仪器 高效液相色谱仪:Agilent 1200高效液相色谱仪,检测器为二极管阵列 (DAD)检测器。
1.2 试药 土大黄苷对照品 (批号110794-201105,购自中国药品生物制品检定所);大黄对照药材 (唐古特大黄,批号120902-200609,购自中国药品生物制品检定所);牛黄消炎片由哈尔滨某制药有限公司生产 (批号:20100101);甲醇、乙腈为色谱纯,水为高纯水;硅胶G预制板;聚酰胺薄膜;其它试剂均为分析纯。
2 方法与结果
2.1 土大黄苷的薄层检查
2.1.1 供试样品溶液制备 样品去糖衣,研细,取0.5 g,置锥形瓶中,加甲醇10 mL,超声处理20min,滤过,滤液作为供试样品溶液。
2.1.2 阴性样品溶液制备 按牛黄消炎片的处方组成制得阴性样品,取0.5 g,同2.1.1项供试品溶液制备法,制得阴性样品溶液。
2.1.3 大黄对照溶液制备 取大黄对照药材0.1 g,同2.1.1项供试品溶液制备法,制得大黄对照溶液。
2.1.4 土大黄苷对照品溶液制备 取土大黄苷对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。
2.1.5 薄层色谱条件与检出 采用3个不同的展开系统进行实验。展开系统①:硅胶G薄层板,以丁酮-乙酸乙酯-甲酸-水 (7∶10∶1∶1)为展开剂。展开系统②:硅胶G薄层板,以三氯甲烷-甲醇-水 -甲酸 (20∶6∶0.6∶0.4)为展开剂。展开系统③:聚酰胺薄膜,以甲苯-甲酸乙酯-丙酮-甲醇-甲酸 (15∶2.5∶2.5∶10∶0.05)为展开剂。点样量:供试品溶液、对照品溶液、大黄对照溶液和阴性样品溶液各5μL。检出方法:展开,取出,晾干后,置紫外光灯(365 nm)下检视。结果供试品色谱中,在与对照品色谱相应的位置上,均显相同持久蓝紫色的荧光斑点;阴性样品溶液、大黄对照溶液对土大黄苷检出无干扰。薄层的色谱图见图1。
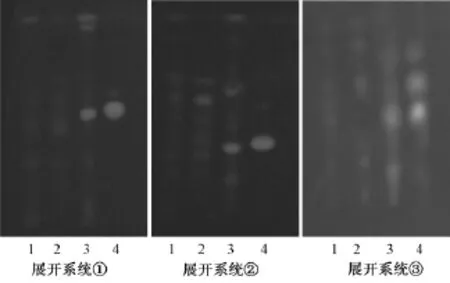
图1 薄层色谱图
2.2 高效液相色谱法 (HPLC法)
2.2.1 色谱条件 色谱柱Atlantis d-C18(4.6 mm×150 mm,5 μm),柱温35℃,流动相为甲醇-乙腈-水 (25∶7∶68),检测波长324 nm;进样量10 μL。
2.2.2 供试样品溶液的制备 样品去糖衣,研细,取1 g,置烧瓶中,加乙酸乙酯30 mL,加热回流30 min,滤过,滤液蒸干,残渣加甲醇25 mL溶解,溶液高速离心,取上清液作为供试样品溶液。
2.2.3 阴性样品溶液的制备 取按牛黄消炎片处方组成制得的阴性样品1 g,同2.2.2项供试品溶液制备法,制得阴性样品溶液。
2.2.4 土大黄苷对照品溶液的制备 取土大黄苷对照品适量,加甲醇制成每mL含50 μg的溶液,即得。
2.2.5 大黄对照溶液制备 取大黄对照药材0.2 g,同2.2.2项供试品溶液制备法,制得大黄对照溶液。
2.2.6 样品测试 取供试品溶液、阴性样品溶液、大黄对照溶液及对照品溶液各10 μL,分别注入高效液相色谱仪中,记录色谱图。液相色谱图见图2。
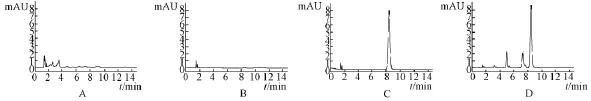
图2 HPLC图
为进一步确认供试品溶液中出现的与土大黄苷对照品保留时间一致的色谱峰,利用DAD检测器在200~400 nm对色谱峰进行了光谱扫描,结果二峰的光谱扫描图相一致,相似度为99.9%。紫外光谱图见图3。
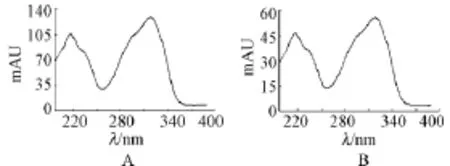
图3 紫外光谱图
3 讨论
3.1 在薄层色谱检查中,采用了3种不同的展开系统,其中使用聚酰胺薄膜时,土大黄苷的检出灵敏度非常高,分离度也好,同一土大黄苷对照品在硅胶板上为一个斑点,而在聚酰胺薄膜上除主斑点外尚可见另2个斑点,久贮的对照品溶液不稳定,主斑点会分解,出现主次颠倒现象,故对照品以新制为宜。
3.2 在高效液相色谱检查中,供试品溶液制备时,对用甲醇和用乙酸乙酯为溶剂提取作了比较,用甲醇时土大黄苷色谱峰也能较好分离,但色谱中会有较多杂峰,用乙酸乙酯作溶剂提取相对较好。本实验还考察了不同厂牌的液相仪 (Waters e2695高效液相色谱仪和Agilent 1100高效液相色谱仪)、不同品牌和型号的多根色谱柱 (Agilent SB-C18、Agilent XDB-C18、Diamonsil(TM)钻石C18、Ultimate XB-C18等)的情况,尚对不同的流动相系统也进行了考察,有乙腈-甲醇-水 (7∶30∶63)和乙腈-水 (20∶80)等系统,均能获得好的分离。
3.3 用上述建立的方法对从流通领域抽取的11批牛黄消炎片样品 (分别由4家企业生产)进行了土大黄苷的检测,结果其中有4批检测出了土大黄苷,对于由同一企业生产的不同批次样品,有的检出有的未检出,说明其投料的大黄部分存在伪品现象。通过对牛黄消炎片市场中同品种中土大黄苷的检测,说明本检测方法应该是可靠和有效的。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社2010:457-459.
[2]郑俊华,西泽新,山岸乔,等.三种非正品大黄中34种化学成分的高效液相色谱法定量分析[J].北京医科大学学报,1989,20(4):315-316.
[3]蒋海强,容 蓉,吕青涛.大黄化学成分的液相色谱-质谱联用鉴别[J].时珍国医国药,2011,22(7):1705-1706.
[4]秦 晨,段玉萍,薛海晨,等.大黄主要化学成分的高效液相色谱法指纹图谱研究[J].现代仪器,2000(3):8-11.
[5]国家食品药品监督管理局药品检验补充检验方法和检验项目批准件:2008013,2008015[S].
[6]杨 萍.一清颗粒中土大黄苷检查方法研究[J].中国药事,2011,25(3):279-281.
[7]蒋永海.妇乐冲剂中非法成分土大黄苷的检测[J].中国现代应用药学杂志,2011,28(9):863-866.
[8]蒋永海,朱 辉.妇炎消胶囊中非法成分土大黄苷的检测[J].中国现代应用药学杂志,2011,28(10):959-961.
[9]徐 颖,郭增军,谭 林.土大黄苷研究进展[J].中国现代应用药学杂志,2009,26(7):549-552.
[10]冯有龙,余伯阳.HPLC法鉴别大黄及部分含大黄中成药的真伪[J].中国药品标准,2009,10(4):296-298.
[11]武裕文,杨国亮,刘艳新.大黄中土大黄苷薄层鉴别方法的改进[J].中国实用医药,2009,4(30):196.
[12]鲁 静,王臣芳,何 轶,等.三黄片质量情况分析及标准修订的建议[J].中国药事,2007,21(11):927-929.
R927.1
B
1001-1528(2013)04-0870-02
10.3969/j.issn.1001-1528.2013.04.060
2012-06-18
朱南霖 (1991—),女,本科,主要从事化学分析与研究工作。E-mail:5157421@163.com
*通信作者:许 菊 (1962—),女,主任中药师,主要从事中药质量研究工作。Tel:(0575)88338271,E-mail:sxxuju@126.com

