抗柯萨奇B病毒性心肌炎胶囊有效部位正交设计
韩淑英, 张博男, 包巨太, 储金秀, 余 红, 马会霞, 李 洁
(河北联合大学,河北唐山 063000)
抗柯萨奇B病毒性心肌炎胶囊有效部位正交设计
韩淑英, 张博男, 包巨太*, 储金秀, 余 红, 马会霞, 李 洁
(河北联合大学,河北唐山 063000)
目的 优化抗柯萨奇B病毒性心肌炎胶囊提取分离有效部位的最佳配伍。方法 提取分离抗柯萨奇B病毒性心肌炎胶囊的有效部位 (乙酸乙酯部位、正丁醇部位、水提部位)为三因素,拟定1、2、3三个剂量水平,通过三因素三水平的正交试验表L9(34)安排试验,以感染抗柯萨奇B3亲心肌病毒 (CVB3)小鼠死亡率为观察指标,考察三个组分的配伍关系,并优选配伍剂量。用优选的新复方治疗CVB3性心肌炎小鼠,进行多指标的药效学验证实验。结果正交试验结果表明正丁醇部位为影响药效的主要因素;优选的最佳配伍是正丁醇部位高剂量、水提部位中剂量和乙酸乙酯部位低剂量组合 (即A1B3C2),三者的配伍比例是A∶B∶C=1∶15.17∶14.83,给药量是原方的1/7~1/6。进一步药效学多指标验证实验表明,新组方对CVB3心肌炎小鼠死亡率、心重指数和血清酶活性均有降低作用,并能减轻心肌组织病理损伤程度;新组方中、高剂量组效果更好,但二者之间无差异,二者均好于原方水煎组。结论 正交试验优选的有效部位组方是正丁醇部位、乙酸乙酯部位和水提部位,三者的配伍质量比是1∶15.17∶14.83,新组方优于原方水煎。
正交试验;抗柯萨奇B病毒性心肌炎胶囊;有效部位;配伍;柯萨奇B3亲心肌病毒;心肌炎
抗柯萨奇B病毒性心肌炎胶囊是治疗病毒性心肌炎的临床验方,由黄芪、西洋参、莱菔子、五味子、麦冬、王不留行、丹皮七味药材组成,有益气养阴、补益心气、保护心肌等作用,临床证明该方不仅可以改善症状,稳定病情,而且可以缩短病程,减少复发[1]。但抗柯萨奇B病毒性心肌炎胶囊临床用量较大,给患者带来了不利。为改进上述缺点,进一步从组分层次探讨抗柯萨奇B病毒性心肌炎胶囊方的药效物质基础,本研究制备了抗柯萨奇B病毒性心肌炎胶囊的不同提取部位,用正交试验筛选出有效组分及最佳组分配伍方案,为制备疗效好、应用方便的新型组分复方制剂提供实验依据和理论支持。
1 材料
1.1 药物与试剂 西洋参、黄芪、丹皮、麦冬、五味子、莱菔子、王不留行 (抗柯萨奇B病毒性心肌炎原药材)均购自石家庄市柏林药材公司,经河北联合大学药学院韩刚教授鉴定;D101大孔树脂 (天津海光化工有限公司);谷草转氨酶 (AST)试剂盒 (批号:20100111)和乳酸脱氢酶 (LDH)测定试剂盒 (批号:20100111)均购自南京建成生物工程研究所;病毒唑 (广州市市桥药业有限公司,批号:20091006)。
1.2 病毒和细胞株 柯萨奇B3亲心肌病毒(CVB3)由中国中医科学院中药所惠赠,本实验室-70℃低温冰箱保存备用;Hep-2细胞由中国中医科学院中药所惠赠。CVB3病毒在Hep-2细胞中传代,反复冻融3次,测定得其半数组织培养感染剂量 (TCID50)为10-3.66/mL,分装后于-70℃冻存。
1.3 实验动物 6~8周雄性近交系Balb/c小鼠,清洁级,体质量 (20±2)g,由北京华阜康生物科技股份有限公司提供,合格证号为SCKX(京)2009-0004。
1.4 主要仪器 电子调温电热套 (天津市泰斯特仪器有限公司,型号:98-1-B);旋转蒸发仪 (上海亚荣生化仪器厂,型号:RE-5205);电热鼓风干燥箱 (上海博讯实业有限公司医疗设备厂,型号:GZX-9070 MBE);数显恒温水浴锅(国华电器有限公司,型号:HH-6);MP200A型电子天平(上海第二天平仪器厂)。酶标仪 (BIO-RAD),2123TC CO2培养箱 (美国),XDS-1B型倒置式生物显微镜 (china),YXQ.DY-250高速蒸汽灭菌器 (上海核医疗仪器厂),THZ-82B型汽浴恒温振荡器 (江苏省金坛市医疗仪器厂)。
2 方法
2.1 抗柯萨奇B病毒性心肌炎胶囊方有效部位的提取与制备 按处方比例 (西洋参100 g,黄芪100 g,麦冬50 g,莱菔子20 g,王不留行13 g,五味子50 g,丹皮66 g)称取各药材,加10倍量80%乙醇,回流提取3次,每次2.0 h,合并提取液,滤过,减压回收乙醇。药液浓缩后用D101大孔吸附树脂进行分离富集,经过乙酸乙酯洗脱3次,旋转蒸发乙酸乙酯洗脱液,干燥后得到乙酸乙酯部位(A);树脂再用正丁醇洗脱3次,旋转蒸发正丁醇洗脱液,干燥后得到正丁醇部位 (B);醇提后的药渣,水煎煮3次,加水量分别10、8、8倍,每次1.5 h,合并水煎液减压浓缩,加乙醇至含醇量60%,放置过夜,离心,取沉淀,用等体积95%乙醇清洗2次,减压干燥,得到水提部位(C)。
2.2 正交实验分析法[2-3]按正交试验设计各部位配伍,同时考虑与总方、阳性药物对比,筛选各成分的较好组合(配伍)。确定影响作用较大的成分,筛选较优配伍。
2.2.1 因素水平的确定 3个提取组分 (部位)构成3种因素 (A、B、C),计算每一组分按每付药提取量,将该每付药提取量视为相当人临床用量,小鼠有效量为人临床用量(g/kg)的8倍,以此为中剂量,其0.5倍为低剂量,2倍为高剂量。拟定1、2、3(低、中、高)三个剂量水平,通过三因素三水平的正交试验表L9(34)安排试验,以死亡率为考察指标,考察三个组分的配伍关系,并优选配伍剂量。见表1。

表1 因素水平
2.2.2 动物分组及给药 按三因素三水平的正交试验设计L9(34)小鼠应分9组,每组20只。根据人与小鼠的标准kg体质量剂量折算方法[2-3],换算得小鼠的各组分每日用量 (表1)。实验当日各组小鼠腹腔接种 CVB3病毒液0.2 mL,其CVB3病毒接种量为两倍半数致死量 (LD50)(预先测得小鼠LD50为1.6×10-6滴度)。小鼠在隔离实验室饲养,于接种病毒当日按表2分组,各组灌胃相应药物配伍给药,每天1次,连续21 d。
2.3 优选新组方验证实验[2-3]对正交优选的有效部位组方,观察其对病毒性心肌炎小鼠的治疗作用,进一步验证其抗柯萨奇B病毒性心肌炎的效应。BALB/c小鼠,随机分为正常对照组、模型对照组、病毒唑组、原方水煎组和新组方高、中、低治疗组,每组20只。实验当日正常对照组腹腔接种细胞培养液0.2 mL,其他组小鼠腹腔接种CVB3病毒液0.2 mL,小鼠 CVB3病毒接种量为 0.8LD50(1.3×10-6滴度)。小鼠在隔离实验室饲养,于接种病毒当日安各组灌胃相应药物给药,每天1次,连续10 d(正常和病毒模型对照组灌胃同体积的生理盐水)。给药第10天小鼠经眼球采血,用全自动生化分析仪测定血清心肌酶AST和LDH。小鼠取血后迅速开胸取出心脏 (除去大血管、结缔组织,用滤纸吸干表面血液),称定质量并计算质量指数,之后取心脏置10%甲醛固定,常规石蜡包埋,HE染色,光镜下观察心肌病理变化,并计算心肌病理积分:即每张切片取上、下、左、右、中5个高倍视野,计算每个视野中炎性细胞浸润及坏死区域面积与整个视野面积之比[4],无病变计 0分,病变面积﹤ 25%计 1分,25%~50%计2分,50% ~75%计3分,﹥75%计4分。结果见表2。
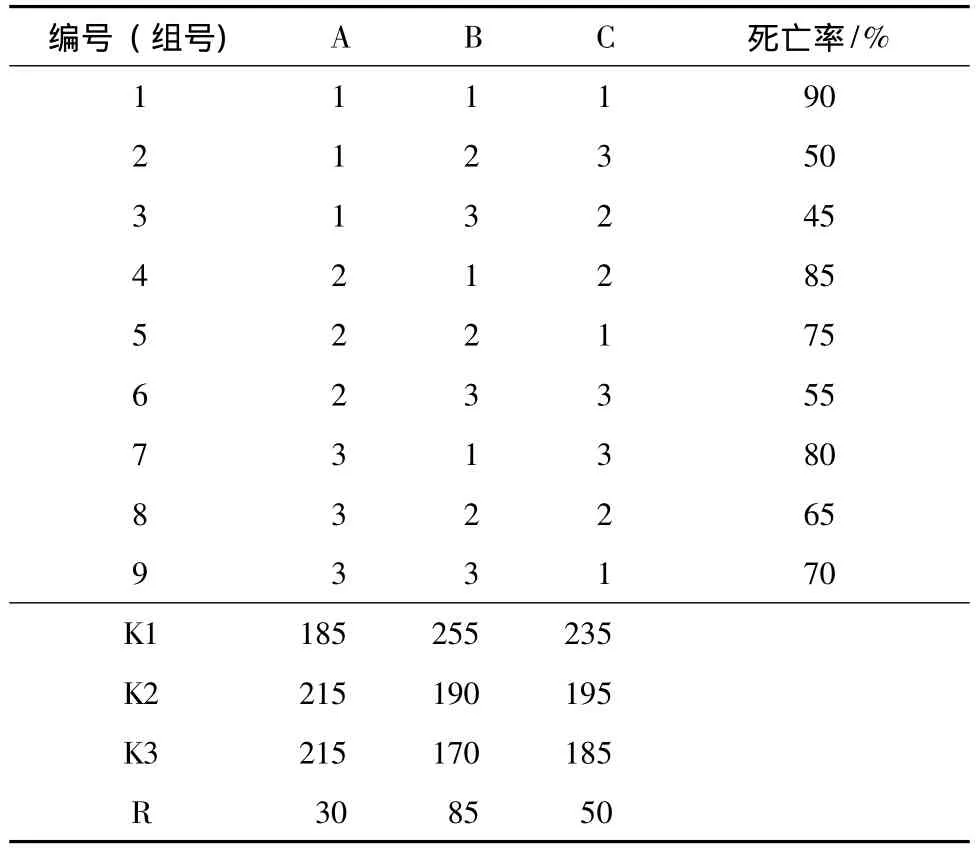
表2 正交试验设计及结果
2.4 统计学方法 实验数据经Excel表建库整理后,用SPSS 13.0统计软件包进行分析。用因素方差分析,P<0.05为差异有统计学意义。
3 结果
3.1 正交试验结果分析 正交试验中R为各因素的极差,由表2可见B因素R值最大,其次是C,再次是A因素。表3结果显示,B因素的F值最大为主要因素对结果有显著影响 (P<0.05),C因素的F值次之,综合分析认为最佳配伍是正丁醇部位高剂量、水提部位中剂量和乙酸乙酯部位低剂量组合,既A1B3C2。

表3 方差分析
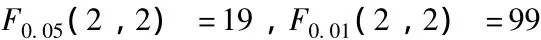
3.2 优选新组方对CVB3心肌炎小鼠治疗作用的验证实验
3.2.1 新组方对小鼠一般状况的影响 以上述正交试验的最佳配伍为基础,既A1B3C2组合 (既三者的配伍比例是A∶B∶C=1∶15.17∶14.83)为给药中剂量(0.029+0.44+0.43=0.899 g/kg),中剂量 ×0.5为低剂量 (0.4495 g/kg),中剂量 ×2为高剂量 (1.798 g/kg)。结果显示正常组小鼠活动、毛色正常、体质量增加;各实验组自第3天起出现活动减少,摄食下降,耸毛,蜷缩,皮毛稀疏无光泽,消瘦等症状;新组方组、病毒唑组和原方水煎组小鼠生存状态较模型组有明显改善,各组死亡情况见表4。
3.2.2 新组方对CVB3小鼠心质量指数 (体质量/心质量)的影响 表5显示,与正常对照组比较,模型组小鼠体质量明显降低,心质量及心质量指数明显增高 (P<0.01)。各药物治疗组小鼠心质量指数明显低于模型组,其中新组方中、高剂量组与病毒唑组相近,新组方低剂量组与原方水煎组相近。新组方有明显量效关系,但高、中剂量组间无明显差异 (P>0.05)。

表4 小鼠死亡统计
表5 小鼠体质量 (BW)、心质量 (HW)、心质量指数(±s)

表5 小鼠体质量 (BW)、心质量 (HW)、心质量指数(±s)
注:与正常对照组比较,*P<0.05,**P<0.01;与模型组比较,▲P<0.05,▲▲P<0.01;与病毒唑组比较,■P<0.05;与原方水煎组比较,★P<0.05;与新组方低剂量组比较,P<0.05,P<0.01。
组 别 剂量/(g·kg-1) 例数/只 体质量/g 心质量 /mg 心质量指数/(mg·g-1)正常对照组20 21.86±2.03 89.65±14.82 4.17±0.36模型对照组 15 18.44±2.16* 113.48±21.27* 6.27±0.61**病毒唑组 0.03 17 19.73±2.05 98.28±21.33 5.15±0.48**▲原方水煎组 6.00 17 20.01±2.12 109.67±20.37* 5.42±0.45**▲新组方低剂量组 0.449 5 17 19.23±1.94 107.33±20.82 5.59±0.45**▲新组方中剂量组 0.899 18 20.57±1.88 97.74±19.28 4.83±0.47**▲■★新组方高剂量组 1.798 19 21.18±1.97 92.48±21.16▲ 4.42±0.49▲*★
3.2.3 新组方对CVB3小鼠血清AST、LDH的影响 表6结果显示,模型组小鼠AST和LDH明显高于正常对照组(P<0.01);与模型组比较,各药物治疗组血清AST和LDH有不同程度的降低,其中新组方中、高剂量组AST和LDH活性最低,二者之间无差异,且均好于原方水煎组。
表6 各组小鼠血清LDH、AST水平变化(±s)

表6 各组小鼠血清LDH、AST水平变化(±s)
注:与正常对照组比较,**P<0.01;与模型组比较,▲P<0.05,▲▲P<0.01;与新组方低剂量组比较,#P<0.05。
组 别 剂量/(g·kg-1) 例数/只 AST/(U·mL-1) LDH/(U·L-1)正常对照组20 74.6±11.3 1 083±128模型组 15 138.4±31.5** 1 930±216**病毒唑组 0.03 17 113.8±22.8** 1 540±174**原方水煎组 6.00 17 118.6±19.5** 1 655±236**▲▲新组方低剂量组 0.449 5 17 121.1±20.9** 1 758±207**新组方中剂量组 0.899 18 108.5±26.4**▲▲ 1 474±220**▲▲#新组方高剂量组 1.798 19 114.3±21.6**▲ 1 573±185**▲▲
3.2.4 新组方对CVB3心肌炎小鼠心肌病理组织积分的影响 光镜下见模型组小鼠心肌内出现小血管炎,大量心肌变性、坏死,炎性细胞浸润,呈现典型的病毒性心肌炎改变;各药物治疗组小鼠心肌病变较模型对照组明显减轻,各组病理积分 (炎性浸润及坏死)见表7和图1。
表7 各组小鼠心肌组织病理积分(±s)

表7 各组小鼠心肌组织病理积分(±s)
注:与模型组比较,▲P<0.05,▲▲P<0.01。
组 别 剂量/(g·kg-1) 例数/只 炎性浸润/分 坏死/分正常对照组20 0 0模型组 15 2.33±0.44 1.55±0.46病毒唑组 0.03 17 2.05±0.38 1.01±0.24▲▲原方水煎组 6.00 17 2.16±0.35 1.25±0.36▲新组方低剂量组 0.449 5 17 2.27±0.29 1.17±0.30▲▲新组方中剂量组 0.899 18 2.05±0.24▲ 1.04±0.25▲▲新组方高剂量组 1.798 19 1.91±0.35▲▲ 0.98±0.27▲▲

图1 心肌组织HE染色光镜照片(×200)Fig.1 Myocardial HE staining Light micrograph(×200)
4 讨论
病毒性心肌炎 (Viral myocarditis)已成为临床的常见病和多发病,其中柯萨奇B3病毒是导致人类心肌炎的最主要的因素,病毒的感染和复制可迅速引起严重的心功能紊乱,严重地危害人类健康[5]。前期临床应用和大量实验研究证明抗柯萨奇B3病毒性心肌炎胶囊对病毒性心肌炎具有良好的治疗效果[6]。实验研究显示抗柯萨奇B3病毒性心肌炎胶囊提取物及其提取组分有抗氧化、抗应激、免疫增强和对心肌损伤具有保护作用[7-8]。本研究在前期研究的基础上,用抗柯萨奇B3病毒性心肌炎胶囊复方中提取分离的活性部位为研究对象,按正交试验方法,以CVB3心肌炎小鼠死亡率为指标,对各提取组分组合进行优化筛选。正交实验结果表明,以正丁醇部位高剂量和水提部位中剂量和乙酸乙酯部位低剂量配伍组小鼠死亡率最低,同时显示正丁醇部位是主要因素,其次是水提部位。进一步将优选的新组分处方进行药效多指标验证实验,结果显示新组方 (乙酸乙酯部位 ∶正丁醇部位 ∶水提部位组合比例为1∶15.17∶14.83)对小鼠死亡率、心质量指数和血清酶活性均能降低,并能减轻心肌组织病理损伤程度,降低坏死面积,其中新组方中、高剂量组效果最好,但二者之间无差异,且均好于低剂量组和原方水煎组。
病毒性心肌炎至今尚无特效治疗药物。西药虽有干扰素、肿瘤坏死因子等用于治疗病毒性心肌炎,但效果均不理想,常有不同程度的不良反应,且价格昂贵[9-10]。中医药治疗该病有一定优势,抗柯萨奇B病毒性心肌炎胶囊治疗病毒性心肌炎具有良效,但该药的有效成分或有效部位群等都不明确,且临床应用剂量较大。为解决这些缺点和不足,本研究从该全方药材中提取分离了有效组分,通过试验对有效组分进行优化组合,得到由活性成分组成的新型中药复方。与原复方相比,富集了有效组份,不仅服用量小 (约为原方用量的1/7~1/6),而且提高了疗效,符合中医用药特色的现代复方新药,为明确药效的物质基础提供了实验依据。中医用药的特色之一是复方用药,将来源于不同原料药材的有效成分组成复方即“有效组分群”[11-13]用于临床,不仅体现了中医药特色,而且提高了技术含量,使中药质量标准具有可控性,也是中药现代化和国际化的需要。研究中药有效部位特别是以有效组分群为原料、开发各种剂型的新药,已成为国内外关注的热点。
[1]邢纪萍,包巨太,李志田,等.抗柯萨B中药胶囊治疗病毒性心肌炎的临床疗效评价[J].中国临床药理学与治疗学,2003,8(6):701-702.
[2]金丕焕.医用数理统计方法[M].上海:上海医科大学出版社,1993:450.
[3]徐叔云,卞如濂,陈 修.药理实验方法学[M].2版,北京:人民卫生出版社,1994:719.
[4]古 乎,何 民.黄芪总苷治疗小鼠柯萨奇B3病毒性心肌炎的实验研究[J].西南国防医药,2007,17(3):281-284.
[5]Peng Tiangqing,Sadusky T,Li Yangwen,et al.Altered expression of Bag-1 in Coxsackievirus B3infected mouse heart[J].Cardiovasc Res,2011,50(1):46-55.
[6]闫莉婷,冯会红,牛云锋,等.抗柯萨奇B病毒性心肌炎胶囊对柯萨奇B3病毒性心肌炎小鼠LDH、CK的影响[J].华北煤炭医学院学报,2011,13(1):3-4.
[7]张博男,韩淑英,李 洁,等.抗柯萨奇B病毒性心肌炎胶囊复方水提物的镇痛和抗应激作用[J].中国实验方剂学杂志,2011,17(6):133-135.
[8]姚荣妹,包巨太,郑彩慧,等.抗柯萨奇病毒性心肌炎胶囊复方提取物对心肌保护作用的实验研究[J].时珍国医国药,2011,22(6).2223-2225.
[9]Swain S M,Whaley F S,Ewer M S.Congestive heart failure in patients treated with doxorubicin:a retrospective analysis of three trials[J].Cancer,2003,97(11):2869-2879.
[10]Singal P K,Iliskovic N.Doxorubicin-induced cardiomyopathy[J].N Engl J Med,1998,339(13):900-905.
[11]刘小玲,张 勇,刘小雷.广枣总黄酮体外抗CVB3病毒活性[J].中国医院药学杂志,2007,27(12):1-5
[12]郑兰兵,魏 青,刘小玲,等.黄芪多糖体外抗CVB3病毒活性[J].中国医药指南,2011,9(13):45-47.
[13]蔡 飞,陈金和,吴基良.大蒜多糖对小鼠病毒性心肌炎的治疗作用[J].武汉大学学报:医学报,2003,24(2):109-112,120.
R285.5
B
1001-1528(2013)04-0823-04
10.3969/j.issn.1001-1528.2013.04.045
2012-09-04
国家“十一五”规划科技重大专项课题 (重大新药创制)(2009ZX09103-442)
韩淑英 (1959—),女,硕士,教授,硕士生导师。研究方向:中药防治心血管疾病。Tel:(0315)3725870,E-mail:shuyinghan59@126.com
*通信作者:包巨太 (1957—),男,教授,硕士生导师,研究方向:中医药治疗病毒性心肌炎。Tel:(0315)3725030,E-mail:baojutai@sohu.com

