HPLC 法测定不同厂家三七伤药片中乌头碱、新乌头碱和次乌头碱
汪剑飞
(芜湖市食品药品检验所,安徽芜湖 241001)
HPLC 法测定不同厂家三七伤药片中乌头碱、新乌头碱和次乌头碱
汪剑飞
(芜湖市食品药品检验所,安徽芜湖 241001)
目的 建立HPLC法测定不同厂家三七伤药片 (三七、草乌、雪上一枝蒿、红花等)中乌头碱、新乌头碱和次乌头碱。方法 采用Intersil C18色谱柱 (250 mm×4.6 mm,5 μm),以甲醇-0.1%三乙胺为流动相进行梯度洗脱;检测波长235 nm;柱温为35℃;体积流量1.0 mL/min。结果 不同厂家三七伤药片中乌头碱、新乌头碱和次乌头碱的含有量差异悬殊。结论 该法灵敏度高,重复性好,能准确测定三七伤药片中乌头碱、新乌头碱和次乌头碱,为乌头碱限量检查提供参考依据。
HPLC;三七伤药片;乌头碱;新乌头碱;次乌头碱
三七伤药片收载于《中国药典》2010年版一部,由三七、草乌 (蒸)、雪上一枝蒿、红花等八味中药组成,具有舒筋活血、散瘀止痛的功能,用于治疗跌打损伤、风湿瘀阻、关节痹痛、扭挫伤、神经痛[1]451。其中草乌及雪上一枝蒿中的双酯型二萜类生物碱乌头碱、次乌头碱即是镇痛、抗炎的有效成分,又是毒性成分[2]。《中国药典》对乌头碱做了限量检查,采用薄层色谱法[1]451,该方法既不能有效控制乌头碱的限量,又不能保证药品的内在质量及有效性。为此笔者收集市场上在售的同一厂家不同批号及不同厂家的三七伤药片,同时测定其中的乌头碱、新乌头碱和次乌头碱。
1 仪器与试药
1.1 仪器 Waters2695高效液相色谱仪,2489紫外检测器 (沃特世公司);AB304-S电子天平和XP-205电子天平[梅特勒-托利多仪器 (上海)有限公司];超声波清洗仪 (上海杰理科技有限公司)。
1.2 试药 乌头碱 (110789-200404),新乌头碱(110799-200404)、次乌头碱 (110720-200410),均为定量测定用,均购自中国药品生物制品检定所;甲醇 (色谱纯),水为双蒸水,其余试剂均为分析纯;三七伤药片 (市售品),阴性三七伤药片按处方缺草乌 (蒸)、雪上一枝蒿配制。
2 方法与结果
2.1 色谱条件 Intersil C18色谱柱 (250 mm×4.6 mm,5 μm),检测波长235 nm;柱温35℃;体积流量为1.0 mL/min;流动相为甲醇-0.1%三乙胺,按表1进行梯度洗脱。

表1 梯度洗脱程序Tab.1 Procedure of gradient elution
2.2 溶液的制备
2.2.1 混合对照品溶液的配制 精密称取乌头碱对照品9.66 mg,新乌头碱对照品10.38 mg,次乌头碱对照品9.64 mg,分别置入同一10 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,作为对照品贮备液。
2.2.2 供试品溶液的配制 取三七伤药片40片,除去糖衣,精密称定,研细,精密称取7.5 g(相当于30片),加入浓氨试液4 mL,浸润10 min,加入乙醚150 mL,振摇10 min后超声提取10 min,过滤,再以50 mL乙醚分次洗涤滤渣及滤纸,合并滤液及洗液,40℃以下回收溶剂至干,残渣加甲醇溶解并转移至2 mL量瓶中,加甲醇稀释至刻度,摇匀,用0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.2.3 阴性对照溶液的制备 取阴性样品7.5 g,按2.2.2项供试品溶液的制备方法制成阴性对照溶液。
2.3 方法学考察
2.3.1 专属性考察 按照2.1项色谱条件,吸取对照品溶液10 μL,供试品溶液、阴性对照溶液各20 μL,分别注入高效液相色谱仪,结果见图1。表明其他药味不干扰供试品溶液中乌头碱、新乌头碱和次乌头碱的测定。
2.3.2 线性关系考察 分别精密量取对照品贮备液 62.5、125、250、500、1 000 μL,分别置 10 mL量瓶中,用甲醇稀释至刻度,摇匀,滤过,分别精密吸取上述溶液10 μL进样,按照2.1项下条件测定峰面积,以对照品进样量(X)为横坐标,峰面积 (Y)为纵坐标,分别绘制标准曲线,求得乌头碱、新乌头碱和次乌头碱的回归方程分别为:Y=2 251 717.52X-52 666.44(r=0.999 5,n=5),Y=2 371 218.18X+22 261.58(r=0.999 0,n=5),Y=2 408 303.27X-42 079.31(r=0.999 8,n=5),结果表明三者进样量分别在0.060 4~0.966 μg,0.064 9 ~ 1.038 μg,0.060 2 ~ 0.964 μg范围内与峰面积线性关系良好。
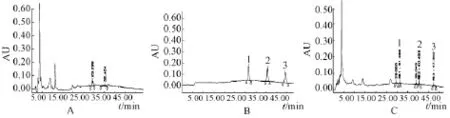
图1 三七伤药片中乌头碱、新乌头碱和次乌头碱HPLC色谱图Fig.1 HPLC chromatograms of mesaconitine aconitine and hypaconitine in Sanqi Shangyao Tablets
2.3.3 精密度试验 精密量取同一对照品溶液10 μL,按2.1项色谱条件连续进样5次,乌头碱、新乌头碱和次乌头碱峰面积的RSD分别为1.88%、0.84%、1.04%,表明精密度良好,满足定量测定要求。
2.3.4 稳定性试验 取同一供试品溶液,按2.1项色谱条件分别于0、2、4、8、12、24 h后进样20 μL,测定峰面积,乌头碱、新乌头碱和次乌头碱峰面积的RSD分别为1.81%,1.96%,2.26%。表明3种生物碱在甲醇溶液中24 h内稳定。
2.3.5 重复性试验 取同一批样品,共5份,按2.2.2项下的方法制成供试品溶液,各进样20 μL,按2.1项色谱条件测定,乌头碱、新乌头碱和次乌头碱的含量分别为 0.92 μg/片、4.23 μg/片和2.01 μg/片,RSD 分 别 为 1.97%、2.74% 和1.64%。结果表明该方法具有较好的重复性。
2.3.6 检测限 取混合对照品贮备液,进行定量倍比稀释,进样并记录色谱图,直到信噪比为3∶1,计算乌头碱、新乌头碱和次乌头碱的检测限分别为1.9 ng、2.1 ng、1.9 ng。
2.3.7 回收率试验 精密称取已知乌头碱、次乌头碱和新乌头碱量的样品9份,置具塞锥形瓶中,分别精密加入混合对照品贮备液0.25、0.5、1.0 mL各3份,按2.2.2项供试品溶液制备方法处理,定容至10 mL量瓶中,制成供试品溶液,按2.1项色谱条件测定并计算回收率,结果乌头碱、新乌头碱和次乌头碱的平均回收率分别为97.6%、98.8%、95.5%,RSD分别为 2.07%、2.33%、1.26%,表明该方法的回收率良好。见表2。
2.4 样品测定 精密称取不同批号的样品细粉各7.5 g(每批平行取3份),分别按2.2.2项下方法处理制成供试品溶液。按2.1项色谱条件测定并计算乌头碱、新乌头碱和次乌头碱及三者的总量,结果见表3。
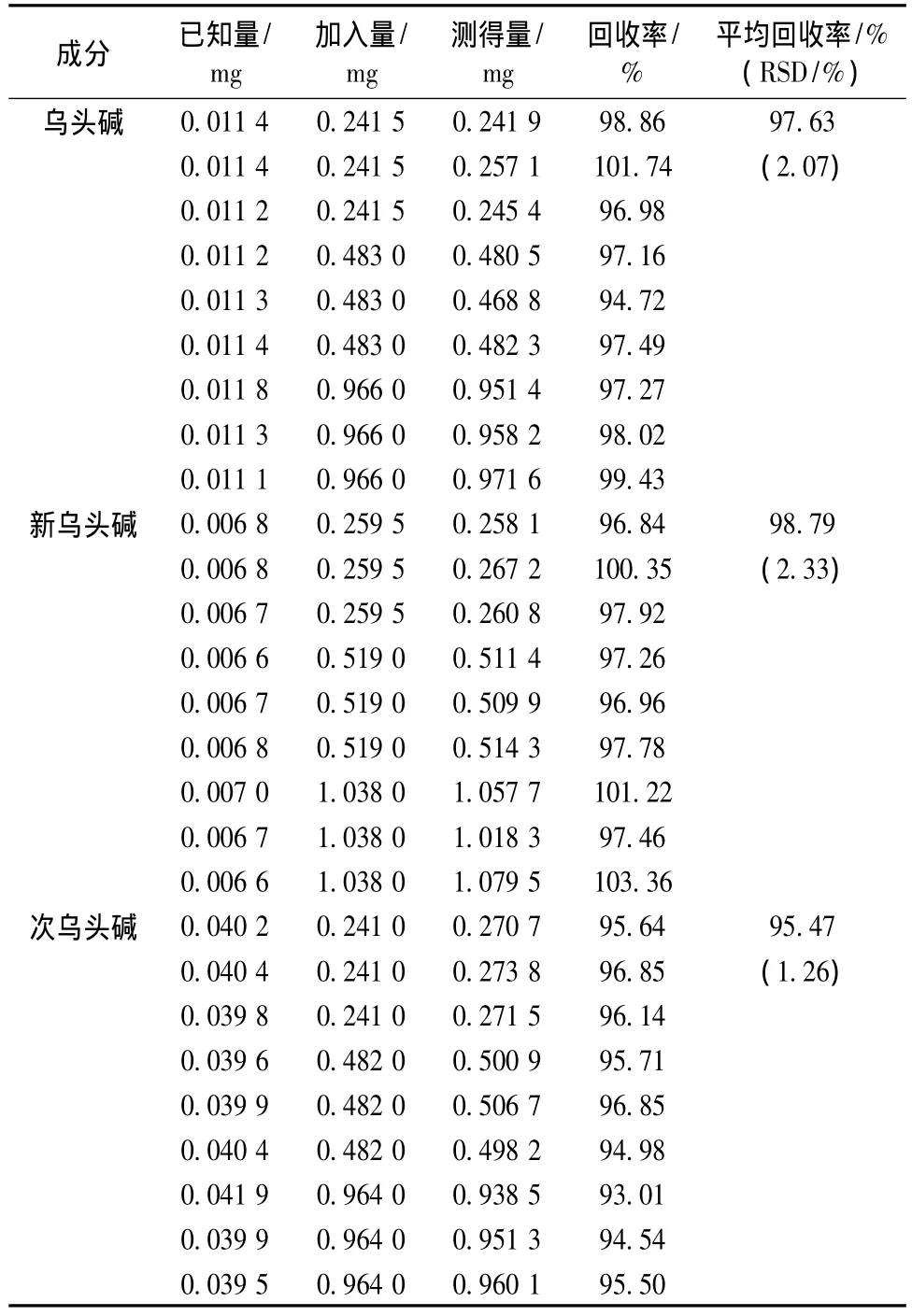
表2 回收率试验结果 (n=9)Tab.2 Results of recovery tests(n=9)
3 讨论
3.1 检测波长及色谱条件的选择 参考《中国药典》2010年版一部草乌与制草乌的【含量测定】项[1]220-221及参考文献[3-4],检测波长考察了 230 nm、235 nm及240 nm 3个检测波长,3个组分在此波长下都有良好的吸收,最终选择检测波长为235 nm;流动相考察了甲醇-0.1%三乙胺、乙腈-乙酸铵缓冲液 (pH=10.5)、乙腈-四氢呋喃-乙酸铵等,进行不同比例的等度洗脱及梯度洗脱,发现本实验的色谱条件分离效果最好。
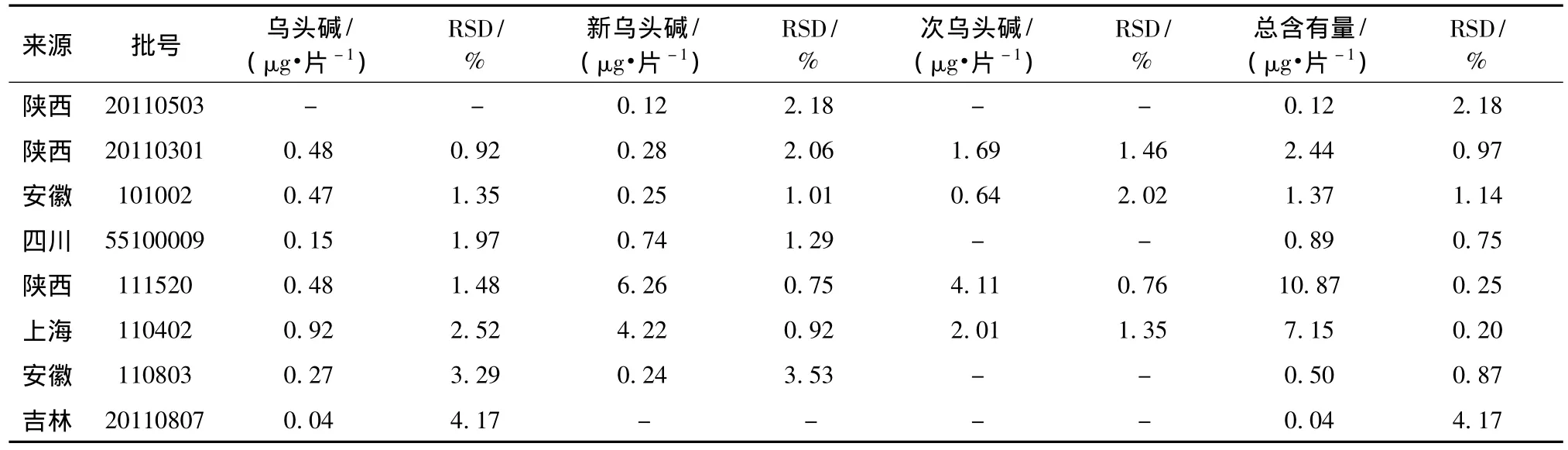
表3 样品测定结果 (n=3)Tab.3 Determination results of samples(n=3)
3.2 样品处理方法的考察 乌头碱类为脂溶性生物碱,在提取溶媒上主要考察了乙醚、三氯甲烷以及异丙醇-乙酸乙酯 (1∶1),在加同样浓氨试液的条件下,三者提取效率无明显差别,考虑到三氯甲烷的毒性远大于乙醚,所以选择乙醚为提取溶媒;还考察了浓氨试液用量 (2、4、6 mL)和提取时间 (5 min、10 min、15 min),加浓氨试液4 mL超声提取10 min的效果最优;乌头碱受热易水解为乌头原碱,乙醚液蒸干的温度以不超过40℃为宜[3]。
3.3 8批样品中乌头碱限量按照国家标准[1]检测均符合规定,而使用本法测定的乌头碱、新乌头碱、次乌头碱的量及三者总量相差悬殊,因此笔者认为,在制定乌头碱限量的标准时,既要控制上限保证安全性,也要制定下限保证有效性。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2]龚千峰,丁安伟,孙秀梅,等.中药炮制学[M].北京:中国中医药出版社,2003:310-314.
[3]张兴德,郁红礼,崔小兵.HPLC测定癌痛宁凝胶剂中乌头碱含量[J].中成药,2007,29(12):1862-1863.
[4]丘振文,罗丹冬,王佩坚.HPLC法测定舒痹宁颗粒中次乌头碱、新乌头碱的含量[J].中国新药与临床药理,2008,19(4):304-306.
[5]张启云,朱战杰,余日跃,等.RP-HPLC法测定白附片中乌头碱、新乌头碱和次乌头碱[J].中国试验方剂学杂志,2007,13(12):1-3.
[6]王 瑞,刘 芳,孙毅坤,等.不同附子炮制品中乌头碱、新乌头碱、次乌头碱含量的HPLC测定[J].药物分析杂志,2006,26(10):1361-1363.
[7]邓雅琼,刘荣华,邵 峰,等.反相高效液相色谱法测定附子中乌头碱等3种成分的含量[J].时珍国医国药,2009,20(5):1038-1039.
[8]刘玉兰,刘世坤,裴 奇,等.高效液相色谱法测定附子中3组分的含量[J].中国药房,2006,17(16):1255-1266.
[9]赵英永,崔秀明,戴 云,等.高效液相色谱法测定草乌类药用植物活性成分含量[J].中国药学杂志,2007,42(11):815-818.
Determination of aconitine,mesaconitine and hypaconitine in Sanqi Shangyao Tablets from different factories by HPLC
WANG Jian-fei
(Wuhu Municipal Institute for Food&Drug Control,Wuhu 241001,China)
HPLC;Sanqi Shangyao Tablets;aconitine;mesaconitine;hypaconitine
R927.2
A
1001-1528(2013)04-0717-04
10.3969/j.issn.1001-1528.2013.04.018
2012-04-27
汪剑飞 (1982—),男,主管中药师,研究方向:药品检验。Tel:18019533956

