溶液的搅拌与空气搅拌(一)
袁诗璞
(成都市武侯区晋阳巷2 号会所花园A3-02-202,四川 成都 610045)
对电镀液及一些工艺溶液进行搅拌,是常用的工艺手段。对绝大部分光亮性电镀液而言,搅拌是必要的工艺条件之一。搅拌到底有哪些作用、是如何起作用、应注意哪些问题,既很基本,又很实际。
强制搅拌通常采用工件移动(或旋转)与空气搅拌两类方式。工件往复移动时,若工件作为阴极,称为阴极移动;铝件电抛光时,工件的移动则为阳极移动。空气搅拌时,工件相对静止,通过在溶液中不断鼓入空气,形成上流的空气泡来使溶液翻动。空气搅拌具有搅拌强度连续可调、搅拌效果均匀、适用性广等优点而获得越来越多的应用。
本文试图较深入全面地分析搅拌的作用原理,重点讨论空气搅拌的一些问题,供电镀工作者参考。
1 搅拌对传质的影响
镀液中的金属离子从在可溶性阳极上形成后向镀液深处转移,以及从溶液深处再移动到阴极界面的过程,称为传质。不溶性阳极电镀及直接向镀液中加入的各种物质,则少一个传质过程。搅拌的根本作用,在于影响传质速度。
1.1 3 种传质方式
溶液中各种离子、分子的移动均需消耗能量。这些能量来源可以是对带电离子的电场力,带电与电中性物质浓度差造成的浓度场力,以及液体流动的速度场力。它们分别产生电迁移、扩散与对流3 种传质方式。研究者们已经推导出各种场力产生的传质速度方程式[1]。
1.1.1 电迁移
电迁移是带电离子在电场力作用下,由于静电吸引而使正负离子分别向阴阳两极的定向运动。
设在y方向与平面垂直的电场强度为Ey,离子的带电数为n,带电离子的扩散系数为Di,其浓度为Ci(严格地讲应为活度ia),法拉第常数为F,气体常数为R,溶液的绝对温度为T,则指定i种离子向y方向电迁移的速度yv为:
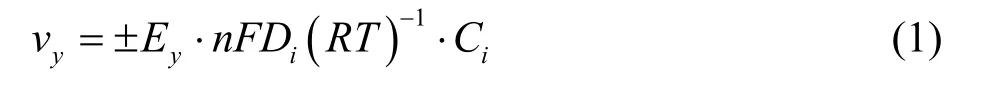
式中,对正离子取正号,对负离子取负号。电迁移表现出以下特征:
(1) 非离子型的中性分子,不存在电迁移传质。
(2) 溶液不外加直流电场时,不存在电迁移传质。
(3) 带电离子的实际电迁移速度很慢。例如,对于含硫酸铜1 mol/L 的溶液,在25 °C、槽电压3 V、阴阳极间距为10 cm 时,可计算出Cu2+的电迁移速度仅为1.8 × 10-4cm/s。只靠电迁移传质,Cu2+从阳极表面到达阴极表面的时间约需15 h。
(4) 当镀液中加有大量惰性电解质导电盐时,传导电流主要靠导电盐来承担。在这种情况下,主盐金属离子的电迁移传质可以忽略不计。
(5) 式(1)中没有与搅拌相关的因子,因此搅拌不影响电迁移传质速度。
可见,电迁移不是镀液中的主要传质方式,搅拌也无益于提高电迁移的传质速度。
1.1.2 扩散
扩散是在浓度场力作用下,溶液(流体)中物质从高浓度处向低浓度处自然运动的现象。
1.1.2.1 扩散方程式
理想的稳态状况下的扩散速度可用菲克(Fick)第一定律表示,其方程式为一次偏微分方程;非稳态的扩散速度可用菲克第二定律表示,其方程式为二次偏微分方程。方程式的计算复杂,在此不再赘述,有兴趣的读者可参看文献[1]。
从菲克定律可知,扩散传质速度正比于浸入液中的阴极表面积A(cm2)、离子的扩散系数Di(cm2/s)、单位距离的浓度差,即与阴极表面垂直方向的浓度梯度及离子的浓度Ci(在同样距离差下,Ci越大,浓度梯度越大)。
1.1.2.2 扩散层厚度
由于阴极表面附近主盐金属离子的放电还原消耗等,阴极表面液层中总有一层浓度较低的层,这一低浓度层称为“扩散层”。代入相应的边界条件,解菲克第二定律的二次偏微分方程可知,任一瞬间扩散层的有效厚度而当达到“极限电流密度”jd时,以上二式中t为时间(s)。
1.1.2.3 极限电流密度
当把离子向阴极的迁移完全归之于扩散时,稳态扩散电流密度j为:

式(2)中,n、F、Di、Ct的含义同式(1);为阴极表面金属离子i的浓度,当不通电而无电沉积发生时,Ci=;δ为扩散层厚度。
随着电沉积的进行,因i离子放电消耗,Ci0不断下降。极端情况下,当传质速度太低时,i离子的还原消耗远高于向扩散层的传质速度(i又大时),则Ci0趋于零,阴极上无主盐金属离子还原,而只发生析氢等阴极副反应,此时的扩散电流密度称为“极限电流密度”,以jd表示,则:

扩散传质表现出的特征为:
(1) 当溶液完全处于静止状态时,扩散主导着传质速度。
(2) 主盐金属离子浓度Ci、盐的扩散系数Di是影响扩散传质速度的主要因素。要提高极限电流密度,需考虑如何减小扩散层的厚度。对于高速电沉积而言,提高允许电流密度是关键之一。
(3) 搅拌并不直接影响扩散传质速度,但可有效减薄扩散层厚度,从而增大极限电流密度。
1.1.3 对流
对流是在速度场力作用下,物质微粒随着流体的流动而被移运的传质方式。由于流体不同部位间存在温度差或浓度差,因此会产生自然对流。当自然对流不足时,需外力干预而形成强制对流。
设物质在x方向的对流传质速度为xv[mol/(cm2·s)],研究物质的浓度为Ci(mol/cm3),溶液在x方向的流速为Ux(cm/s),则

可见,对流传质速度仅取决于溶液流速与物质浓度。在既定浓度下,只有加大流速,才能提高对流传质速度。实际溶液总存在自然对流而非绝对静止不动,对流传质永远存在。强制搅拌时,提高了流速Ux,对流传质加快;搅拌强度越大,对流传质越快。
1.2 不同物质的传质方式
采用可溶性阳极进行电沉积时,主盐金属离子要经历从阳极表面传质到镀液深处,再从镀液深处传质到阴极表面的两大传质过程。镀铬等不溶性阳极电镀时的主盐金属离子以及加入镀液中的其他有机或无机物质,则只需经历后一个传质过程。
非离子型物质的传质手段只有扩散与对流两种。化学法形成转化膜的工艺液中物质及清洗时工件表面附着物向清洗水的传质也是一样。
配合物电镀时的配阴离子要在阴极放电,必须克服电迁移的反作用力,即扩散、对流速度远大于电迁移的相反方向传质,才能到达阴极表面。另外还要克服阴极极化后阴极表面过剩负电荷的排斥作用。因此配阴离子往往造成比配阳离子与电中性配合物更大的阴极浓差极化与电化学极化。
电镀中被广泛应用的具有表面活性的有机添加剂,既要吸附性好,又要易于脱附(以免在镀层中过多地夹附),则在阴极表面不间断、快速地发生相反方向的传质过程。
2 搅拌的作用
2.1 搅拌对传质作用的影响
搅拌的作用归根结底在于提高了溶液中的传质速度。从以上分析可知,搅拌并不影响电迁移传质,也不直接影响扩散传质速度,其主要作用在于加大对流传质速度。高速电镀技术中,要求在不降低阴极电流效率的前提下使镀层不致烧焦而允许阴极电流密度达到几十甚至上百A/dm2的办法之一,就是采用极其强烈的强制搅拌。例如,采用高速液流法时,流速应达到使阴极界面液层呈紊流(湍流)而不是层流;喷射法则是将镀液高速喷射向阴极工件;而超声波电镀是利用超声波强大的“空化效应”所形成的微观高压而起强烈搅拌效果。这些方法的目的都在于极大提高极限电流密度。
2.2 搅拌对镀层的影响
2.2.1 减少镀层烧焦,扩大允许阴极电流密度
众所周知,与静镀相比,对镀液采用搅拌能在更大的平均阴极电流密度下工作而镀层又不致烧焦。烧焦故障的实质是:工件高电流密度处因主盐金属离子放电过快,在阴极界面液层中因传质不足,产生与溶液深处具有过大的浓差,阴极极化值过大,此时在低阴极电流密度下放电困难的H+乘机大量放电还原,一方面产生氢气,另一方面界面也因H+传质不足而pH升高,形成金属氢氧化物等夹杂于金属层中,镀层或粗糙无光,或疏松多孔而呈海绵状,于是出现烧焦。
由于搅拌提高了金属离子及H+的传质速度,它们向阴极界面液层补充及时,则在一定阴极电流密度范围内不致产生出现烧焦的条件,较大阴极电流密度处的镀层相对纯度较高、结晶细密而处于正常状态。扩大允许阴极电流密度,可提高镀速和生产效率。
在焦磷酸盐及HEDP 等无氰碱性预镀铜时,为了减小临界活化电流密度、防止制件上产生置换铜,要采用低主盐浓度、高配合比的单配位或多配位工艺。其所带来的问题之一是允许阴极电流密度小。此时,采用搅拌以提高允许阴极电流密度,是应该具备的工艺条件。在高焦磷酸盐闪镀铜时,甚至要求强烈空气搅拌。实际上,在高浓度、高效率的氰化镀铜时,也要求采用空气搅拌[2]。
2.2.2 提高镀层光亮整平性
对于光亮性电镀,静镀时镀层的光亮整平性欠佳,几乎无例外地都要采用搅拌措施。搅拌对镀层光亮整平性提高的原理尚未见详细的论述,在此作些不很成熟的讨论。
(1) 实验现象。对光亮酸性镀铜液及亮镍液作赫尔槽试验,比较试片的光亮平整性及范围,可以发现:静镀时,烧焦区较宽,整个试片的镀层光亮整平效果不太好,但低区光亮整平性及其光亮整平范围比搅拌时要好;搅拌镀时,烧焦区变窄,高中区镀层光亮整平性比静镀时大有提高,但低区光亮整平及光亮范围反而比静镀时差;阴极电流密度越大且不烧焦处,光亮整平性越好;搅拌越强烈,上述现象越明显。
(2) 搅拌提高镀层整平的原因。
第一、不管用何种理论来解释整平作用,共同的现象是:整平剂不可避免地会在阴极还原消耗而使镀液积累有机杂质,同时存在于镀层中的夹附消耗而降低镀层纯度。
第二、按照选择性吸附理论,整平剂是易于在阴极表面产生吸附层而阻化电沉积的表面活性物质,由于其在微观峰处的吸附量大于微观谷处,谷处吸附层薄,阻化作用小,相应谷处的阴极电流密度比峰处大,镀速快,沉积量大,从而起到正整平作用。当整平剂消耗后传质速度不足时,微观峰处吸附层也薄,阻化作用也小,加之尖端放电现象,峰处阴极电流密度大,则起不到正整平作用。搅拌提高了传质补充消耗的速度,因此可提高整平能力。
第三、按“扩散消耗型”理论,整平剂是易于电解消耗,对电沉积具阻化作用,电极过程受扩散控制的物质。由于微观谷处与峰处存在距离差,整平剂扩散到峰处比谷处更容易,在峰处产生的阻化作用比谷处更大,峰处的阴极电流密度比谷处小,因而谷处镀层沉积量大于峰处,因而起到正整平作用。搅拌使扩散层厚度减小,峰谷处均有较多整平剂到达且峰处传质到达更易,故搅拌提高了整平剂的阻化作用,从而提高整平能力。
(3) 搅拌提高镀层光亮性的原因。
第一,光亮剂在电解时同样存在消耗。
第二,宏观平整的表面不一定光亮。例如,经机械研磨的阀门密封平面,很平整但并不光亮;镀前经过目数很大的金刚砂磨削得很平整的表面,在未经软布轮或麻轮加抛光油抛光时仍不光亮。相反,宏观粗糙的工件即使未经磨抛,也可镀亮。
第三,表面平滑、结晶细密是光亮的前提条件,但不是充分条件。例如,酸性暗铜与暗镍层结晶也可能很细密,但并不光亮。
第四,人眼感知的光亮性是接收到了光线的反射。平板玻璃非常平整,但只是透光,而只有再于其上形成银镜之类的反光层来反射光线,才能起到镜子的作用。光线透射到结晶粗糙的表面会产生漫反射,不会光亮。但单纯微观正整平性良好时,也不一定光亮。某些半光亮镀镍工艺的整平性很好,但却带乳色而不光亮,这可能与结晶的取向性有关,未形成光线的定向反射。
第五,光亮是多种作用下的综合效果,包括晶粒细化、微观正整平、结晶取向等,使光线产生定向反射,防止漫反射。
有关镀层整平与光亮的机理,较为详细的讨论可参看文献[3]。搅拌提高了镀层光亮性,一方面是因为提高了正整平作用,另一方面是增大了传质速度后能及时补充作为晶粒细化剂、改变结晶取向的光亮剂的消耗。
(4) 搅拌对低电流密度区的不良影响。无论整平剂还是光亮剂都要求在阴极界面液层中的浓度恰当,过多或过少时效果都不好。为防止镀液中本底浓度过高,从镀液维护的角度来讲,必须少加勤加。若其在镀液中的平均浓度控制在较佳水平,但搅拌提高了传质速度,在小电流密度处,电解消耗速度慢,过快的补充,反而造成低电流密度处浓度过大,会降低光亮整平效果。镀液中平均浓度越高,这种影响越明显。当搅拌强度连续可调时,若对复杂件电镀,搅拌强度应略微调小,以利于低电流密度区光亮整平性的提高。搅拌时,应采用尽可能大的阴极电流密度,并选择低电流密度区光亮整平性优异的组合光亮剂。
综合而论,搅拌使阴极界面整平剂与光亮剂同时达到最佳浓度,共同提高了光亮整平效果。
2.2.3 减小镀层对杂质的敏感性
搅拌在提高允许阴极电流密度、减少镀层烧焦的同时,也抑制了析氢副反应,减少了析氢量,从而使镀层产生气体针孔、麻点的故障率下降,镀层渗氢量减少,氢脆危险性下降。搅拌使阴极表面析出的氢气不易滞留在表面而尽快均匀逸出,不至于降低镀层的光亮均匀性。举一实例:大生产中发现平面件氯化物镀锌黑钝化时,若静镀则可能出现彩钝与白钝均不易发现的由下至上的亮色条纹,而进行阴极移动时却无类似现象。其原因是静镀时,从平面某一些点上不断产生沿工件表面向上的氢气流,其局部冲刷搅拌而出现比其他地方亮度更高的条带范围。阴极移动可以防止析氢条带的产生。
镀液中的杂质离子是否在阴极表面放电还原,取决于多种因素,如杂质离子的还原电位、杂质的绝对浓度、杂质离子与主盐金属离子的相对浓度等。正常情况下,阴极界面液层中主盐金属离子与杂质离子的浓度比很高,杂质离子不易乘机还原。若传质速度不足,主盐金属离子放电消耗后补充不及时,则杂质离子相对浓度提高,放电还原机会增加。搅拌提高了主盐金属离子传质补充速度,能减小杂质离子还原的机会,减小镀液对杂质的敏感性。
顺便指出,利用相对浓度的概念可以解释电镀中的一些现象。
【例1】笔者[4]试验发现,HEDP 镀无氰碱铜时,采用通电10 s、断电1~2 s 的直流间隙镀,能大大减轻镀液对杂质的敏感性。间歇镀的这种作用可作如下解释:由于镀液不能采用过于强烈的空气搅拌,因此不足以使阴极界面液层中Cu2+浓度长期处于绝对优势;在间隙镀的停镀时间,主盐Cu2+无电沉积消耗,搅拌及时地使阴极界面液层中的Cu2+在一个周期内维持在相对较高的浓度,从而抑制了杂质离子的还原。所采用的平均阴极电流密度越大,间隙镀的周期应越短。
【例2】在镀锌低铬钝化过程中,钝化液中的Cr3+、Zn2+、Fe2+等杂质增加至一定量时,钝化性能恶化。此时,提高钝化液中六价铬含量,钝化液又可恢复性能而继续使用。这也是不少处置不当的单位在使用过程中导致低铬钝化逐步演变为中铬钝化的原因。
2.3 搅拌与浓差极化
浓差极化是因为电极表面液层中带电离子浓度与溶液深处浓度出现较大差异而使电极实际电位偏离平衡电位的一种电化学现象:在阴极上,阳离子因浓度下降,放电迟缓而不能及时中和掉电源不断提供的负电子而使阴极电位变得更负;在阳极介面附近液层中,可溶性阳极溶解下来的金属阳离子浓度上升,电源从阳极不断“抽走”负电子而金属阳离子又不能及时传质到溶液深处,使阳极上积累了更多的正电荷,而使阳极电位更正。
搅拌由于增大了传质速度,总会使浓差极化减小。阳极浓差极化害多利少,而搅拌能够减小阳极浓差极化,其好处如下:有利于阳极溶解,减少或防止阳极电位过正时的析氧副反应;可防止在液温低时阳极袋上生成盐类结晶而堵塞袋孔;可使镀液中的阳极去极剂尽快传质到阳极界面。
搅拌减小阴极浓差极化则有利有害。有利之处在于可提高允许阴极电流密度,害处是会缩小一些工艺的低区光亮整平电流密度范围,甚至降低镀液深镀能力。
对于不含强配位剂的简单盐电镀,要求保持适度的浓差极化。以硫酸盐光亮酸性镀铜为例,若采用静镀,虽镀层光亮整平性不很良好,但低电流密度区具有宽的光亮整平范围和更好的镀液分散能力与深镀能力。从保持适度的阴极浓差极化出发,笔者主张采用“中酸中铜”工艺,但所用光亮剂应具有良好的光亮整平能力[5]。某些工艺为了弥补不太理想的光亮整平性,要求采用强烈空气搅拌(甚至还加阴极移动),因而主盐硫酸铜的质量浓度要求达到240~260 g/L,以减小浓差极化,才允许采用更大的阴极电流密度。同时,所用光亮剂的低区光亮整平性应十分良好。高染料型光亮剂在这方面表现突出,虽其固有缺陷明显,仍大受欢迎。
氯化物镀锌液中,Cl-对Zn2+仅有微弱的配位能力,属简单盐电镀。除需要钝化的平面工件电镀外,阴极移动可能会大大加剧因浓差极化减小而造成的深镀能力不足。举一实例:某厂原电镀超市推车大件,槽本较宽且深,又采用了阴极移动,后来镀有孔眼的平面工件时,因镀液本身深镀能力未调好,孔眼周围镀层发白无光而不知所措;笔者命关掉阴极移动,故障消失。
3 低浓度镀镍的困难性
镀液的低浓度化能降低配液成本,减少带出损耗,是人们多年来追求的目标之一。但实施难度很大,应用范围受到限制。其根本原因在于主盐Ni2+的传质速度 太慢。从前述可知,电迁移、扩散、对流速度及极限电流密度均与主盐金属离子的浓度成正比。低主盐浓度电镀时,金属离子的浓度过小,最终使极限电流密度减小,生产上允许的阴极电流密度就变小,生产效率下降。
为了弥补低浓度镀镍时传质速度小的问题,可采取以下措施:
(1) 采用扩散系数大的盐类。主盐的扩散系数越大,电迁移速度越快,扩散速度制约的极限电流也具有片面性。
(2) 在允许的范围内采用尽量大的搅拌强度,以提高传质速度。
(3) 要配套采用适配的光亮整平剂。
笔者并不反对浓度镀镍,也曾专门讨论过溶液低浓度化的问题[6]。但认为,低浓度镀亮镍仅适于厚铜薄镍工艺镀取薄层亮镍,对于要求镀速快、光亮整平性优良的单层镍-铬工艺,则不适合。
(未完待续)
[1]李铭华,袁诗璞,黄渭澄,等.高速电镀[M].成都:四川人民出版社,1980.
[2]青谷薰,今井雄一,川合慧.金属メッキ技術(1)[M].东京:槙书店,1974(昭和49年).
[3]张立茗,方景礼,袁国伟,等.实用电镀添加剂[M].北京:化学工业出版社,2007.
[4]袁诗璞,毛茂财,汪小英.采用两级跳间歇镀电源的无氰碱铜研究[J].电镀与涂饰,2008,27 (1):7-10.
[5]袁诗璞.实践逼出来的点滴创新:第二部分──浓差极化与“中酸中铜”[J].电镀与涂饰,2006,25 (12):58-60.
[6]袁诗璞.对溶液低浓度化的讨论[C]// 2008 中国电镀技术研讨会论文集.广州:中国表面工程协会,2008:19-22.

