柱前衍生-高效液相色谱荧光法测定人血浆中乙酰半胱氨酸及其生物等效性研究
张 乐,胡岚岚,周世文,汤建林
(第三军医大学新桥医院国家药物临床试验机构,重庆 400037)
0 引 言
N-乙酰半胱氨酸(N-acetylcysteine,NAC)是一种巯基化合物,作为关键的生理物质广泛存在于动物细胞和组织中。NAC不仅在细胞生物学,生物化学方面发挥重要功能,而且具有多种药理作用,比如:溶解黏液,抗氧化,消炎,保护肝脏、心脏和神经细胞等[1-2]。NAC的临床应用领域还在不断拓宽,在药物及重金属中毒、肿瘤、艾滋病、帕金森病等过程中NAC都能起到一定预防、治疗作用[3]。目前国内外关于巯基化合物测定方法的报道较多,包括荧光光度法[4],气相色谱质谱法[5],离子色谱法[6]和高效液相色谱-紫外[7]、质谱[8]或电化学检测法等。但上述方法在分析性能,成本,操作复杂性,样品处理,灵敏度等方面多存在着种种不足。这些不足大大增加了实验难度或成本,导致上述检测方法难以应用于常规检测和推广。同时,有研究表明,荧光试剂衍生高效液相色谱荧光分析法在测定巯基化合物含量时,具有灵敏度高,操作相对简单,易于自动化,特异性高等特点。据此,本研究采用 N-(1-芘) 马来酰亚胺 (N-(1-Pyrenyl)maleimide,NPM)为荧光衍生试剂,设计、建立了柱前衍生-高效液相色谱荧光分析方法,用于人血浆中NAC浓度的测定。
1 实验部分
1.1 仪器与试剂
Waters-600E型高效液相色谱系统(配2475型荧光检测器,717plus型自动进样器及Millennium32色谱管理软件,Waters公司);色谱柱:Diamonsil C18柱(5μm×150mm×4.6mm,系列号 8013909,迪马公司);保护柱:C18柱芯(4mm×3.0mm,迪马公司);MC-210S型电子天平(精度0.01mg,Sartorius公司);高速离心机(Abbott公司);XH-86多用途旋涡混合器(江苏阜宁县罗桥校办工厂);Millipore超纯水系统。
受试制剂:乙酰半胱氨酸咀嚼片(海南海神同洲制药有限公司,规格:0.6g/片,批号:20071101);参比制剂:乙酰半胱氨酸泡腾片(浙江康恩贝生物制药有限公司,规格:0.6g/粒,批号:070828);乙酰半胱氨酸对照品(纯度99.5%,批号:20031001,海南海神同洲制药有限公司);N-(1-Pyrenyl)maleimide(NPM,含量 98%,Sigma公司);Tetramethylammonium hydroxide pentahydrate(TMA,含量 98%,Alfa Aesar试剂,Johnson Matthey公司);乙腈、甲醇均为色谱纯(Burdick& Jackson公司);磷酸(分析纯,重庆川东化学试剂厂);磷酸二氢钠(分析纯,重庆北碚化学试剂厂);三乙胺(含量≥99.5%,Fluka公司),试验用水均为Millipore超纯水。
1.2 实验方法
1.2.1 流动相的配制
精密称取0.78 g磷酸二氢钠于500mL容量瓶中,用超纯水定容,即得10mmol/L溶液,经0.45μm的水性滤膜过滤后于室温保存即可。
1.2.2 标准溶液的配制
精密称取NAC 6.4mg,用乙腈溶解定容至50mL,即得128μg/mL的NAC标准储备溶液。精密称取NPM 44.7mg,用乙腈溶解定容至100mL,即得1.5mmol/L NPM储备溶液,4℃冰箱保存备用。取NAC储备液用乙腈对半稀释至浓度分别为 64.0,32.0,16.0,8.0,4.0,2.0μg/mL的标准工作液;取上述1.5mmol/L NPM溶液1mL于50mL容量瓶中,乙腈定容至即得30μmol/L NPM衍生溶液,4℃冰箱保存备用。
1.2.3 血浆样品的处理及衍生化反应
取血浆样品100μL于1.5mL离心试管中,加入800μL NPM衍生液,涡旋1min,室温反应5min后,加50%乙酸中止反应,10500 r/min离心3min,取上清20μL进样。
1.2.4 色谱条件
色谱柱:Diamonsil C18柱;流动相:乙腈-10mmol/L NaH2PO4(含TMA 10mmol/L,H3PO4调pH至3.4)为50∶50。流速:1mL/min;激发波长:330nm,发射波长:380nm;柱温:30℃。进样量为20μL。
1.2.5 方法验证
本文对高效液相色谱荧光法进行了线性、定量下限、精密度、回收率、稳定性的验证。
2 结 果
2.1 分离特性
在上述色谱条件下,分别考察了7个不同来源的空白血浆,空白血浆+标准品、标准品及实测样品的色谱分离情况,测得NAC色谱图如图1所示。由图可见,被测物峰形良好,无杂质峰干扰,血样中NAC的保留时间为3.8min。
2.2 标准曲线和线性范围
取上述配置好的NAC工作液50μL于0.95mL血浆中,按血浆处理方法配制成血浆浓度为:6.58,3.29,1.64,0.82,0.41,0.20,0.10 μg/mL 的溶液进样分析,每个浓度平行2份。每一浓度进样20μL。记录色谱图,以浓度为横坐标,峰面积为纵坐标进行线性回归,得回归方程:y=9.91×105x+4.47×104(r=0.9945,n=3,各点 RSD<12%,见表 2),线性范围为 0.1~6.58μg/mL,血浆中 NAC 定量下线为 0.1μg/mL(S/N=5,0.101±0.002,RSD=2.3%,n=5)。
2.3 回收率试验
配制 0.20,1.64,6.58μg/mL NAC 血样各 5份,按照1.2.3“血浆样品处理”项下步骤操作,进样分析,计算得低、中、高3种浓度的NAC的相对回收率(n=6)分别为94.8%、93.1%、90.7%;变异系数分别为3.8%、8.7%、6.0%。结果表明,低、中、高3种浓度的相对回收率均符合要求,方法准确可靠。结果见表1。
2.4 精密度试验
配制 0.20,1.64,6.58μg/mL NAC 血样各 5份,按照1.2.3操作,在1 d内不同时间处理测定,考察日内精密度;连续3 d于同一时间配制0.20,1.64,6.58μg/mL NAC血样各5份,处理测定,考察日间精密度。结果见表2。
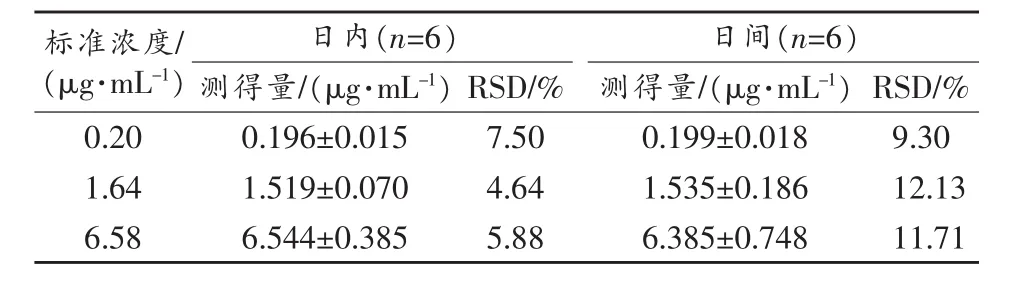
表2 乙酰半胱氨酸精密度试验
2.5 稳定性试验
2.5.1 血浆样品处理后室温放置的稳定性
配制 0.20,1.64,6.58μg/mL NAC 血样各两份,-80℃冰箱放置冻存,按照1.2.3“血浆样品处理”项下操作,于 0,1,2,3,4,6,12h 测定,每个浓度平行 2份。考察血浆样品处理后室温放置的稳定性,其结果见表3。由表可见,血浆样品可于室温下至少保存12h(RSD<11.3%)。
2.5.2 冻融稳定性
配制 0.20,1.64,6.58μg/mL NAC 血样各两份,-80℃冰箱放置冻存,然后在室温融化,融化后的样品在同样条件下重新冷冻。按照1.2.3操作,于每个冻融循环测定,每个浓度平行两份。考察3次冻融循环血样的稳定性,其结果见表3。由表可见,血浆样品冻融3次仍稳定(RSD<12.8%)。
2.5.3 血浆样品冰箱冻存的长期稳定性
配制 0.20,1.64,6.58μg/mL NAC 血样各 14份,-80℃冰箱放置冻存,按照1.2.3操作,于0,1,2,3,6,7,10 d 测定,每个浓度平行两份。考察血浆样品长期冻存的稳定性,其结果见表3。由表可见,血浆样品可于-80℃冰箱至少保存10d(RSD<12.6%)。

表3 乙酰半胱氨酸稳定性试验
2.6 实测样品结果
男性健康受试者20名,完全随机分成两组,每组10人,分两个阶段采用双交叉给药方案,分别口服被试制剂和参比制剂 1.2g,于给药前和后 15,30,45,60,75min,1.25,1.5,2,2.5,3,4,6,8 h 抽取上肢静脉血3mL,分离血浆,柱前衍生-HPLC荧光检测法测定人血浆中NAC浓度,所得数据经BECS软件处理,统计分析。20名受试者口服参比之际和受试制剂1.2g后,NAC不同制剂的平均血药浓度-时间曲线图见图2。
受试制剂与参比制剂NAC的Tmax分别为(1.35±0.59),(1.47±0.72)h,Cmax分别为(3.76±1.35),(3.80±1.48)μg·mL-1,用梯形法计算所得的 AUC0-t分别为(8.13±2.35),(8.40±2.23)μg·h·mL-1,AUC0-∞分别为(9.62±2.60),(10.03±2.64)μg·h·mL-1。对经对数转换后的Cmax、AUC0-t、AUC0-∞进行方差分析和双单侧T检验及90%可信限判断,受试制剂的Cmax落在参比制剂的80.39%~123.99%范围内,受试制剂的AUC0-t落在参比制剂的82.70%~112.20%范围内,AUC0-∞落在参比制剂的83.14%~111.16%范围内,对Tmax经Wilcoxon检验,无显著差异,受试制剂NAC咀嚼片AUC0-t的相对生物利用度为(101±34)%,AUC0-∞ 为(103±40)%,符合生物等效性规定要求。

图2 20名健康受试者分别口服1.2g受试制剂和参比制剂后乙酰半胱氨酸血药浓度均值-时间曲线
3 结束语
曾经使用高效液相荧光法测定人血浆中NAC含量,试用了固相萃取法处理血浆样品或调整流动相比例的办法用以克服空白血浆对样品测定的干扰,但效果不佳。故在随后的实验中选择柱前衍生高效液相荧光法来进行测定,在此条件下,杂质峰对样品峰干扰小,保留时间适宜。
NAC本身是一种强大的抗氧化剂,其分子式中的活性巯基(-SH)很容易被氧化为二聚物或与生物基质中的内源性巯基以混合二聚物形式存在。因此,NAC在生物样品中不稳定。在实验过程中发现NAC的血浆样品在-80℃冰箱中保存6h后,NAC含量发生明显改变;在室温条件下放置1 h后,含量也开始降低。鉴于此,需要引入一种衍生试剂,通过衍生反应增强NAC在生物样品中的稳定性。NPM作为一种衍生试剂,与巯基的衍生步骤非常简单(不需要任何特殊试剂,反应在室温下孵育5min即可完成),且衍生后的样品相对稳定。衍生化反应式见路线图3。因此,在实验中选择了NPM对获得的血浆样品立即进行衍生化处理,并将衍生后的样品在-80℃条件下保存。随后,在10日内完成检测。
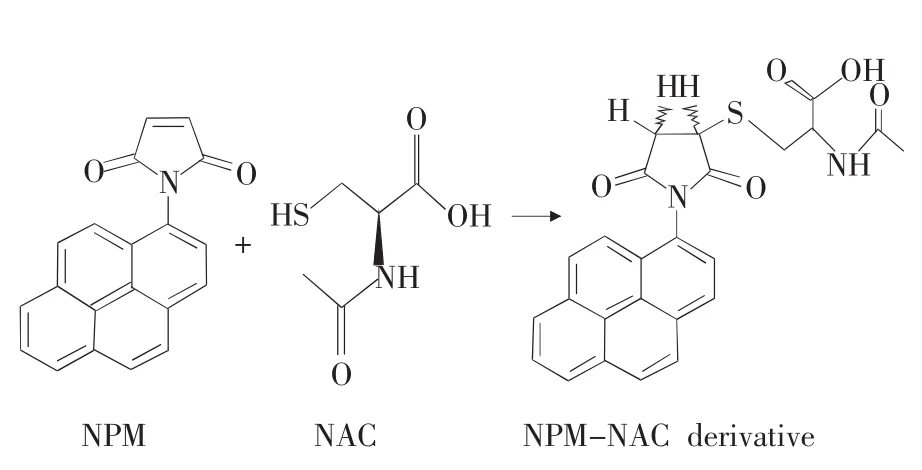
图3 NAC衍生化反应式
试验结果表明,本法符合化学药物制剂人体生物利用度和生物等效性研究技术指导原则。且本法简便易行,灵敏度较高,重现性好,生物样本中内源性杂质对测定不产生干扰,可用于该药的生物样本中含量的测定。
通过对20名健康志愿者采用随机、双交叉试验,比较NAC咀嚼片及泡腾片的相对生物利用度。结果显示,NAC咀嚼片和泡腾片各主要药动学参数均无显著性差异,认为受试制剂与参比制剂间具有生物等效性。
[1]张智健.N-乙酰半胱氨酸在呼吸系统疾病中的应用[J].中国药物应用与监测,2007(2):20-22.
[2]魏琳琳,段钟平.N-乙酰半胱氨酸药物作用机制实验研究进展[J].中国药学杂志,2008,43(12):887-889.
[3]樊金伟,刘亚男.乙酰半胱氨酸药理作用及其临床应用综述[J].中国新技术新产品,2011(2):18.
[4]Liang S C,Wang H,Zhang Z M,et al.Spectrofluorimetric determination of thiols by use of N[P-(2-benzoxazolyl)phenyl]maleimide[J].Fresenius J Anal Chem,2001,370(8):1117-1119.
[5]Capitan P,Malmezat T,BreuilléD,et al.Gas chromatographic-mass spectrometric analysis of stable isotopes of cysteine and glutathione in biological samples[J].J Chromatogr B Biomed Sci Appl,1999,732(1):127-135.
[6]Chitre SA,Lobo G A,Rathod SM,et al.Bromide-sulfur interchange:ion chromatographic determination of total reduced thiol levels in plasma[J].J Chromatogr B Analyt Technol Biomed Life Sci,2008,864(1-2):173-177.
[7]Karakosta T D,Tzanavaras P D,Themelis D G.Automated pre-column derivatization of thiolic fruitantibrowning agents by sequential injection coupled to highperformance liquid chromatography using a monolithic stationary phase and an in-loop stopped-flow approach[J].J Sep Sci,2011,34(16-17):2240-2246.
[8]Iwasaki Y,Saito Y,Nakano Y,et al.Chromatographic and mass spectrometric analysis of glutathione in biological samples[J].J Chromatogr B Analyt Technol Biomed Life Sci,2009,877(28):3309-3317.

