异烟酸-硫代巴比妥酸显色反应测定酒中氰化物的研究
张 娅,李春江,王 茜
(红河州质量技术监督综合检测中心,云南 蒙自 661100)
氰化物是食品安全重点关注的物质之一,其是一类剧毒化合物,可经过呼吸道、消化道以及皮肤进入体内,迅速作用于呼吸酶,引起组织内窒息,从而引起组织衰竭以至机体死亡[1]。白酒中的氰化物主要来自于原料,如木薯以及其他含有氰甙类配糖体的野生植物发酵过程中水解产生氢氰酸。大部分氢氰酸在原料蒸煮是可挥发掉,但仍会有少量的氢氰酸残留在白酒中[2]。
氰化物的检测方法有很多种,如气相色谱法[3-5]、离子色谱法[6-7]、液相色谱法[8]、离子选择电极法[9-11]、分光光度法[12-14]等。国标中酒的氰化物测定方法是异烟酸-吡唑啉酮分光光度法[15],异烟酸-巴比妥酸光度法是国标测定生活饮用水中氰化物的方法之一[16],而硫代巴比妥酸与巴比妥酸具有相似的结构。本实验对异烟酸-硫代巴比妥酸光度法测定酒中氰化物进行的研究,结果表明,在弱酸性环境和氯胺T存在的条件下,氰化物可与异烟酸-硫代巴比妥酸形成一种蓝色染料,该染料在波长642nm处有一个最大吸收峰,其吸光度值与氰化物含量在一定范围内呈良好的线性关系,可用于微量氰化物的定量分析。将该方法用于酒中氰化物的测定,结果与国家标准方法相吻合,加标回收率为96.6%~105.6%,方法的稳定性和灵敏度均令人满意。
1 材料与方法
1.1 材料与试剂
酒样:采购于当地市场;氰化物:上海徐行化工厂;KH2PO4-NaOH、;NaOH、乙酸、乙酸乙酯:天津市风船化学试剂科技有限公司;异烟酸-硫代巴比妥酸、氯胺T:国药集团化学试剂有限公司;以上试剂均为分析纯,实验用水为超纯水。
氰化物标准溶液配制:100μg/mL(准确浓度用银盐法[1]标定);KH2PO4-NaOH缓冲溶液:0.05mol/L;异烟酸-硫代巴比妥酸溶液配制:称取2.5g异烟酸和2.0g硫代巴比妥酸,加入1mol/L NaOH溶液30mL,溶解后钾纯水至100mL;氯胺T溶液:10.0g/L,现用现配;NaOH溶液:0.05mol/L和0.50mol/L;3%乙酸溶液的配制;乙酸溶液:10g/L;酚酞指示剂:1.0g/L;乙酸乙酯溶液:10g/L。
1.2 仪器与设备
T6新世纪型紫外可见分光光度计:北京普析通用有限公司;UV-2550型紫外可见分光光度计:日本岛津公司。
1.3 方法
1.3.1 标准曲线的绘制
取10μg/mL 氰化物标准溶液0.1mL~1.0mL于25mL比色管中,加入0.05mol/L NaOH 溶液至12.5mL,放置10min,加入一滴酚酞指示剂,用乙酸调节至红色刚好消失,再加入KH2PO4-NaOH缓冲溶液5.0mL,氯胺T溶液0.5mL,混匀,放置4 min后,加入异烟酸-硫代巴比妥酸溶液5.0mL,并用水稀释至刻度,混匀,放置30min后,以试剂空白为参比,用比色皿,于波长642nm处测定吸光度值A,以氰化物含量(2cm)对A绘制标准曲线。
1.3.2 酒样分析
取1.0mL试样与25mL具塞比色管中(若酒样浑浊和有色,按照文献[1]方法进行蒸馏,取样量为2mL),按1.3.1操作测定吸光度值。以标准曲线法定量同时进行对照分析以及加标回收率实验。氰化物含量计算公式:
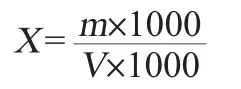
式中:X为试样中氰化物含量,mg/L;m为从标准曲线查到的试样中氰化物质量,μg;V为试样的体积,mL。
2 结果与讨论
2.1 吸收光谱
氰化物标准溶液的吸收光谱见图1。在该实验条件下,氰化物与异烟酸-硫代巴比妥酸形成的蓝色染料,在波长642nm处有一个最大吸收峰,所以本方法选择642nm作为测量波长。
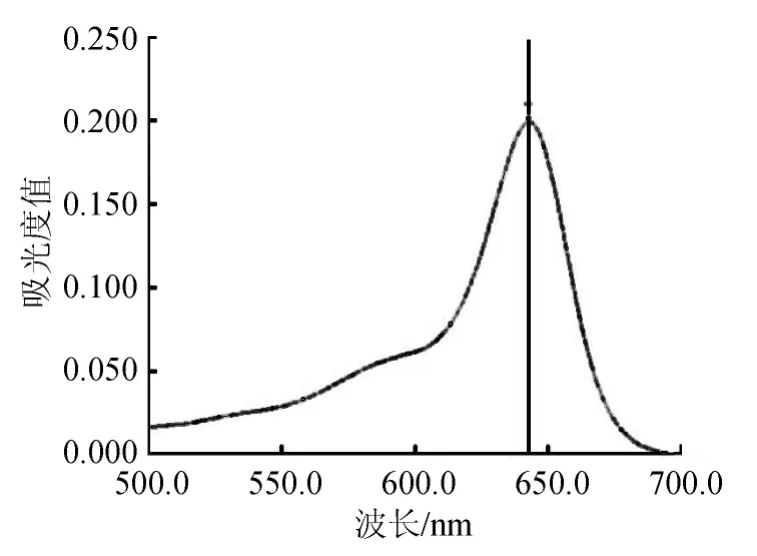
图1 氰化物标准溶液的吸收光谱图Fig.1 Absorption spectra of standard cyanide solution
2.2 酸度的影响
取不同pH值的KH2PO4-NaOH缓冲溶液进行实验,结果见表1。实验结果表明,溶液的pH值为5.7时的吸光度值达到最大,因此选用pH 5.7的KH2PO4-NaOH缓冲溶液进行后续实验。

表1 酸度对氰化物含量的影响Table 1 Effect of acidity on cyanide content
2.3 氰化物转化时间及氯胺T用量的影响
选用不同的氯胺T用量和氰化物转化时间进行实验,结果见表2和表3。从表2、表3可知,实验选择氰化物转化时间4min和0.4mL的氯胺T用量具有较大的吸光度值(A)。
2.4 异烟酸-硫代巴比妥酸用量的影响
显色剂的用量对显色反应有较大影响,显色剂用量不够会导致显色反应不完全。不同用量的异烟酸-硫代巴比妥酸显色反应吸光度值(A)见表4。由表4可知,实验选用5mL异烟酸-硫代巴比妥酸反应具有最大且稳定的吸光度值。
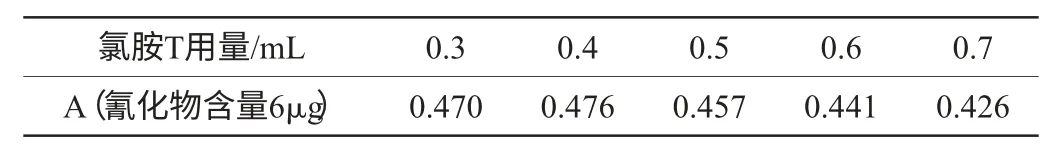
表2 氯胺T用量对氰化物含量的影响Table 2 Effect of the amount of chloramine-T on cyanide content

表3 氰化物转化时间对氰化物含量的影响Table 3 Effect of cyanide conversion time on cyanide content
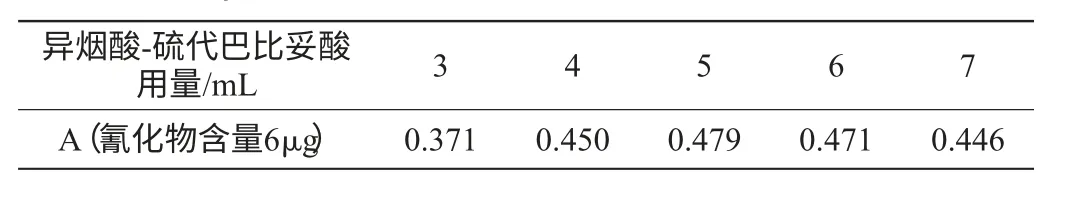
表4 异烟酸-硫代巴比妥酸用量对氰化物含量的影响Table 4 Effect of the amount of isonicotinic acid-thiobarbituric acid on cyanide content
2.5 共存物质的影响
酒中含有一定量的乙酸乙酯、乙酸和大量的乙醇,为确定其对测定结果的影响,本实验加入无水乙醇0.6mL,1g/L~5g/L的乙酸乙酯和乙酸。当测定含量为6.0μg氰化物时,相对误差在±5%范围内。可见酒中常见物质对测定基本没有影响,方法的选择性较好。
2.6 标准曲线
本检测方法氰化物含量在0~10.0μg/25mL范围内符合朗伯比尔定律,标准曲线的回归方程为A=0.0663c+0.0038,r=0.9997。
2.7 精密度实验
对1.00μg和8.00μg 氰化物标准溶液和2份白酒样平行测定5次,测定结果的平均值分别为为1.03μg 和8.05μg,0.24mg/L和0.12mg/L,相对标准偏差(relative standard deviation,RSD)分别为2.1%和1.5%,2.9%和3.2%,反映该方法精密度良好。
2.8 酒样分析
取3份酒样按按1.3.2操作测定氰化物含量,同时与国标法(异烟酸-吡唑啉酮法)对照,并作加标回收率实验,结果见表5。
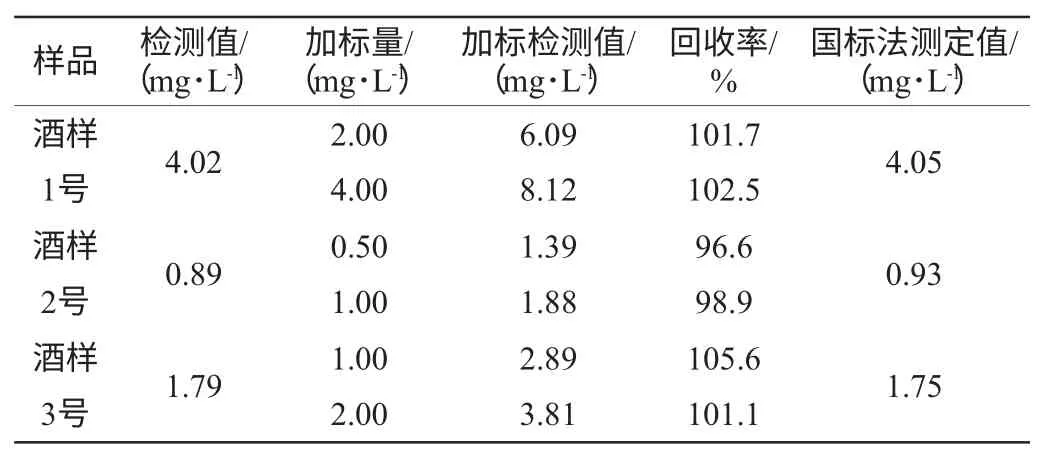
表5 酒样中氰化物含量的分析结果Table 5 Analytical results of cyanide content in alcoholic drink
由表5可知,该方法对氰化物含量的检测结果与国标法吻合,加标回收率为96.6%~105.6%,说明该检测方法准确度高。
3 结论
结果表明,在pH 5.7,氯胺T用量0.4mL,氰化物转化时间4min,异烟酸-硫代巴比妥酸用量5mL的条件下,吸光度值达到最大。据此建立了酒中氰化物的异烟酸-硫代巴比妥酸分光光度法,用本法检测的结果与国标法吻合,方法精密度良好,加标回收率为96.6%~105.6%,准确度高,可以用于酒中微量氰化物的检测。
[1]张新威.毒品和毒物检验[M].北京:中国人民公安大学出版社,2003.
[2]董文宾.白酒中氰化物的化学发光测定法[J].中国酿造,1997,16(5):23-25.
[3]武和平,张爱霞,武景福.空气中氰化物气相色谱测定法[J].职业与健康,2008,24(12):1163-1164.
[4]刘凤海,陈亚娜,陈伟东,等.顶空气相色谱法快速测定水中氰化物[J].中国卫生检验杂志,1999,9(5):369-370.
[5]黄绳炳.气相色谱法测定电镀废水中氰化物[J].海峡科学,2008(3):27-29.
[6]戴安(DIONEX)(中国)有限公司.紫外—离子色谱法直接检测金属氰化物[J].环境化学,2008,27(3):405-407.
[7]龙素群,钟志京,刘秀华,等.离子色谱法测定氰化物方法研究[J].四川大学学报:自然科学版,2006,43(6):1352-1356.
[8]孟 梁,申贵隽,张 强.金属配位剂衍生—高效液相色谱法测定粮食及白酒中的游离氰化物[J].分析科学学报,2009,25(5):587-589.
[9]温孚波,王 娟.离子选择电极法测定水中氰化物方法探讨[J].中华预防医学杂志,2001,35(2):125-126.
[10]余月仙.氰离子选择电极测定酒中氰化物[J].浙江预防医学,1999,11(2):61-63.
[11]潘腊青.银离子电极法现场快速测定水中氰化物[J].中国环境监测,2000,16(3):51-53.
[12]金安宝,郑黎明.狗肉中氰化物的测定[J].中国卫生检验杂志,2006,16(4):481-483.
[13]梁永清,郭慧理.金精矿中氰化物的测定[J].黄金,2006,27(12):63-64.
[14]齐占虎.吡啶-吡唑啉酮分光光度法测定土壤中的氰化物[J].河北化工,2009,32(3):66-67.
[15]北京市卫生防疫站.GB 5009.48-2003 蒸馏酒与配制酒卫生标准的分析方法[S].北京:中国标准出版社,2004.
[16]金银龙.GB 5750.5-2006 生活饮用水标准检验方法无机非金属指标[S].北京:中国标准出版社,2007.

