化学镀Ni-P非晶Ti2Ni0.95Zn0.05的储氢性能
王寅杰,赵相玉,马立群,沈晓冬
(南京工业大学材料科学与工程学院,江苏南京 210009)
Ti2Ni系储氢电极合金结构中具有较多的储氢位置,晶态Ti2Ni的电化学储氢比容量达到500 mAh/g,但只能放出40%,且循环稳定性差[1]。B.Luan 等[2-3]认为,容量的急剧衰减是充放电过程中不可逆相Ti2NiH0.5的形成、积累及合金的氧化所致[3]。X.Y.Zhao等[4]采用球磨晶态 Ti2Ni合金及Ti、Ni混合粉末的方法制备非晶Ti2Ni,并通过热处理制备具有纳米晶结构的Ti2Ni合金,产物的循环稳定性较晶态合金有较大的提高,以60 mA/g的电流充电6 h、放电至-0.6 V(vs.Hg/HgO),循环50次的容量保持率达93.6%。
马永栋等[5]研究发现:化学镀铜可以提高储氢合金La0.6Nd0.2Mg0.2Ni3.3Co0.3Al0.25的循环稳定性,以60 mA/g的电流充电8 h、放电至-0.6 V(vs.Hg/HgO),循环50次的容量保持率由未处理的80.43%增加到89.3%。B.Luan等[2]研究发现:低温化学镀Ni-P的工艺简单,可改善晶态Ti2Ni合金电极的耐腐蚀性。S.N.Jenq等[6]研究了化学镀Ni、Ni-P及双层镀层对Ti0.35Zr0.65Ni1.2V0.6Mn0.2合金电化学储氢性能的影响,发现化学镀可阻止合金早期氧化,延长合金的循环寿命,以60 mA/g的电流充电6 h、放电至-0.6 V(vs.Hg/HgO),循环30次的容量保持率由未处理的28.1%增加到93.7%。这些研究均未分析化学镀时间。
本文作者用机械合金化(球磨100 h)制备非晶Ti2Ni0.95Zn0.05储氢合金,再进行表面活化及化学镀Ni-P,研究化学镀时间对非晶Ti2Ni0.95Zn0.05合金电化学储氢性能的影响。
1 实验
1.1 非晶Ti2Ni0.95Zn0.05合金的制备
以Ti粉(Alfa公司,99.5%,200目)、Ni粉(国药集团,99.5%,200目)和Zn粉(上海产,99.99%,100目)为原料,将按名义组成Ti2Ni0.95Zn0.05,混合均匀后,置于250 ml的不锈钢真空球磨罐中(内含若干直径为10 mm和6 mm的不锈钢球),用QM-WX4卧式球磨机(南京产)在氩气气氛中、密封条件下,以300 r/min的转速球磨(球料比20∶1)100 h。球磨一定时间后,取适量粉末进行研究。
1.2 化学镀Ni-P及热处理
将70%HNO3(国药集团,AR)与40%HF(国药集团,AR)按体积比1∶1混合后,稀释10倍,制成侵蚀液;浸锌液的成分为:3 g/L ZnSO4(国药集团,AR)和20 ml/L 40%HF;镀液的成分为:12.5 g/L柠檬酸钠(国药集团,AR)、30 g/L Ni-SO4·6H2O(国药集团,AR)、10 g/L NaH2PO2·H2O(国药集团,AR)、5 g/L CH3COONa(国药集团,AR)和 2 mg/L NH2CSNH2(国药集团,AR),pH 值为4.6。
将合金粉末放入侵蚀液中浸泡2 min,取出后用去离子水洗涤3次;然后在浸锌液中浸锌3 min,取出后用去离子水洗涤3次;再在侵蚀液中退锌1 min,取出后用去离子水洗涤3次;在浸锌液中二次浸锌3 min,取出后用去离子水洗涤3次,之后进行化学镀。
将材料在镀液中、92℃下化学镀1 h或2 h,取出后用去离子水洗涤3次,再在60℃下鼓风干燥2 h。干燥后的样品在150℃下真空(真空度为133 Pa)干燥1 h,进行热处理。
每2 g合金粉末使用400 ml溶液(侵蚀液、浸锌液、退锌液及镀液)。将二次浸锌水洗后的样品记为活化后的样品。
1.3 电极的制备
将0.1 g合金粉末与0.3g Ni粉混匀后,以15 MPa的压力压制成直径为10 mm的圆片。用两片面积为4 cm2的正方形泡沫镍片(江苏产)将圆片夹在中间,以5 MPa的压力压紧,点焊泡沫镍、镍片与铜导线,制成测试用电极。
1.4 合金的分析及电化学性能测试
用JSM-5610V型扫描电镜(日本产)分析合金试样的形貌和粒径;用ARL X’TRA型Cu靶X射线衍射仪(美国产)分析粉末试样的相组成和相结构,CuKα,连续扫描,扫描速度为 5(°)/min,管压40 kV、管流 30 mA。
电化学性能测试采用三电极体系,所用辅助电极为烧结式Ni(OH)2电极(江苏产),参比电极为Hg/HgO电极,电解液为6 mol/L KOH(国药集团,AR)。
在BT-2000多通道电池综合性能测试仪(美国产)上进行充放电测试。循环性能测试:分别在25℃及40℃时,以60 mA/g的电流充电6 h,静置10 min,以60 mA/g电流放电至-0.6 V。高倍率放电性能测试:在25℃时,以120 mA/g、300 mA/g、600 mA/g及900 mA/g的电流放电至-0.6 V。
在合金电极第2次循环时,以60 mA/g的电流充电6 h,静置10 min,以60 mA/g的电流放电至50%放电深度(DOD),静置1 h,待电极电位稳定后,在CHI606D电化学工作站(上海产)上进行电化学阻抗谱(EIS)和线性极化测试,测试温度为25℃。EIS测试的频率为10-3~105Hz,交流振幅为0.005 V;线性极化测试是以1 mV/s的速度在平衡电位±10 mV的范围内进行线性扫描。
2 结果与讨论
2.1 合金的结构
图1为不同球磨时间的Ti2Ni0.95Zn0.05粉末的XRD图。

图1 不同球磨时间的Ti2Ni0.95Zn0.05粉末的XRD图Fig.1 XRD patterns of Ti2Ni0.95Zn0.05powders milled for different time
从图1可知,未球磨的粉末包含Ti、Ni和Zn单质,球磨10 h后,Zn的衍射峰消失,Ti和Ni的衍射峰宽化,原因是粉末在球磨过程中受到碰撞挤压,产生了位错、晶界和亚晶界等缺陷,导致相结构改变。球磨30 h后,出现明显的“宽化峰”,表明生成了非晶态合金;球磨80 h后,Ti峰消失,说明各组分已经完全非晶化。
图2是球磨100 h的Ti2Ni0.95Zn0.05合金经过不同时间化学镀后的XRD图。
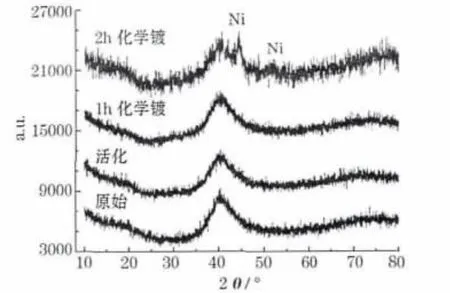
图2 表面处理前后Ti2Ni0.95Zn0.05合金的XRD图Fig.2 XRD patterns of Ti2Ni0.95Zn0.05alloy before and after surface treatment
从图2可知,活化处理及化学镀1 h的样品与原始合金样品类似,只有非晶合金的鼓包峰,而化学镀2 h的样品出现了Ni的衍射峰,说明该衍射峰为镀层的衍射峰。Ni-P镀层的结构会随P的含量变化而变化:当P含量较低时,镀层为晶态;当P含量较高时,Ni的晶体结构被破坏,镀层为非晶态。镀层中P的含量较低,Ni的晶体结构较为完整,但少量P仍在Ni晶格中存在,因此Ni的衍射峰有一定程度的宽化。
2.2 合金的形貌及表面成分
原始样品、活化样品及化学镀2 h样品的SEM图见图3。

图3 表面处理前后合金表面的SEM图Fig.3 SEM photographs of alloy surface before and after surface treatment
从图3可知,经过活化处理,去除了原始合金表面的氧化层后,合金表面变得比较光滑;经过2 h的化学镀,有一些合金颗粒表面形成了一层完整的镀层,如图3d所示;而另一些颗粒上的镀层不完整,如图3c所示。
2.3 合金的电化学储氢性能
合金电极在25℃及40℃时的循环性能见图4,最大放电比容量及容量保持率见表1。
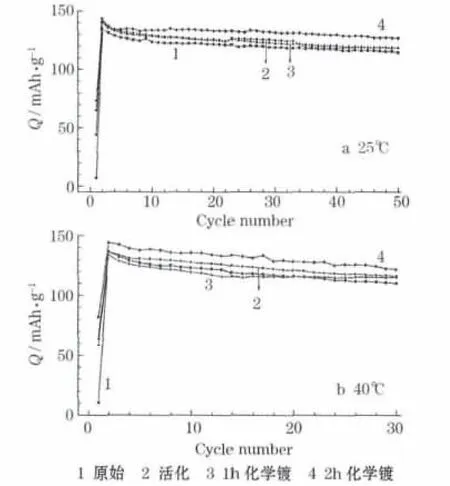
图4 表面处理前后的合金电极在25℃及40℃的循环性能Fig.4 Cycle performance of alloy electrodes before and after surface treatment at 25℃and 40℃
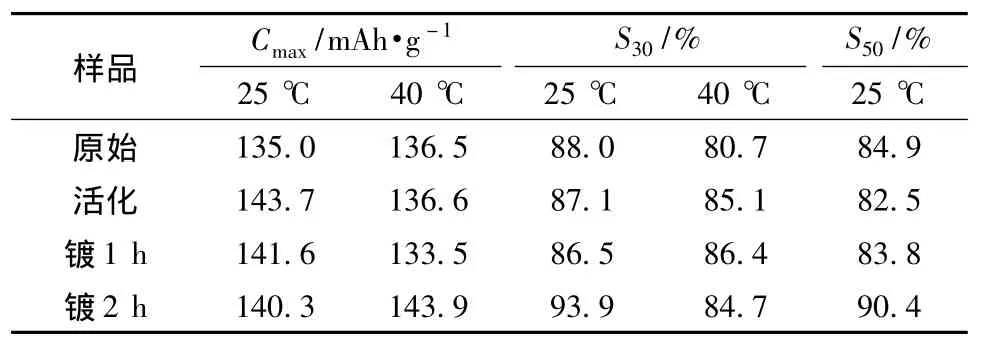
表1 表面处理前后合金电极的最大放电比容量(Cmax)及容量保持率Table 1 Maximum specific discharge capacity(Cmax)and capacity retention rate of alloy electrodes before and after surface treatment
从表1可知,在25℃时,活化后的样品Cmax最大,随着化学镀时间的延长,Cmax逐渐减小。活化工艺去除了原始合金颗粒表面的氧化层,并提高了合金表面活化性能,因此提高了Cmax;Ni-P镀层不吸氢,随着化学镀时间的延长,镀层质量逐渐增大,导致储氢容量逐渐减小。容量保持率先减小、后增大,化学镀2 h的样品S30为93.9%,S50由84.9%提高到90.4%。合金表面的氧化层对合金在充放电时的腐蚀有抑制作用,活化工艺除去了氧化层,使合金耐腐蚀性降低、容量保持率减小。化学镀1 h的样品,施镀时间较短、Ni-P镀层不完整,合金表面的镀层及基体间会形成腐蚀原电池,加速合金腐蚀,导致容量保持率进一步减小。化学镀2 h的样品,施镀时间较长,耐腐蚀的Ni-P镀层完整包覆了基体表面,容量保持率得到提高。在40℃时,碱液的腐蚀性增大,只有具有完整Ni-P镀层的镀2 h样品的Cmax超过140 mAh/g,同时,各样品的S30均偏低。原始合金表面的氧化层耐腐蚀性降低,在充放电过程中的溶解速度加快,会与基体形成腐蚀原电池,加速腐蚀,使S30减少到80.7%。活化后的样品及化学镀样品容量保持率相似,但镀2 h的样品比容量更高,说明完整的镀层在40℃时的耐腐蚀性能仍然较好。
合金电极在不同放电电流下的最大放电比容量见图5。

图5 表面处理前后的合金电极在不同放电电流下的最大放电比容量Fig.5 Maximum specific discharge capacity of alloy electrodes before and after surface treatment under different discharge current
从图5可知,经过表面处理的样品,大电流放电比容量均高于原始合金,且随着化学镀时间的延长而增加。电极/电解液界面的电荷转移反应及氢在电极内部的扩散,是影响高倍率放电性能的主要因素[7]。活化处理使电极表面活性增强,促进了电荷转移反应,增强了合金的高倍率放电性能。
合金电极的EIS见图6,图中高频区的半圆代表合金电极与集流体的接触阻抗和容抗,中频区的半圆代表合金颗粒间的阻抗和容抗,低频区的半圆代表电极的电化学反应阻抗,低频区的斜线代表双电层容抗和Warburg扩散阻抗。
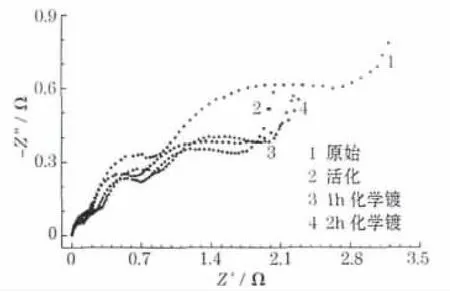
图6 表面处理前后合金电极的EISFig.6 Electrochemical impedance spectra(EIS)of alloy electrodes before and after surface treatment
从图6可知,经过表面处理的样品与原始合金相比,低频区的半圆减小,原因是活化处理去除了合金表面的氧化层,使电极表面反应的阻抗减小,合金的表面活性增强。
合金电极第2次及第30次循环的线性极化曲线见图7,计算出的合金极化电阻列于表2。

图7 表面处理前后合金电极的线性极化曲线Fig.7 Linear polarization curves of alloy electrodes before and after surface treatment

表2 表面处理前后合金电极的阻抗Table 2 Impedance of alloy electrodes before and after surface treatment
从表2可知,经过活化的样品极化电阻最小,随着化学镀时间的增加,阻抗逐渐增大,镀2 h的样品,阻抗与原始合金相似。阻抗的变化规律即是合金在碱液中电荷转移速度的变化规律,而溶液中电荷转移的速度与合金粉末的比表面积及合金表面的活性原子的数量有关。活化处理去除了合金表面的氧化层,增加了合金表面活性原子数量,使合金电极阻抗减小,而后的化学镀使得合金表面包覆了Ni-P合金,活性比新鲜的原始合金表面低,使阻抗增大,并随化学镀时间的延长而变大。循环30次,各样品的极化阻抗均大幅增加,原因是合金表面在充放电过程中被不断腐蚀,使表面活性原子数量减少。活化样品和镀1 h样品的极化电阻接近,说明不完整的镀层在循环过程中不断溶解,最终接近活化样品的表面活性。
3 结论
2 h的化学镀,可在样品表面包覆一层Ni-P镀层。活化工艺去除了原始合金颗粒表面的氧化层,合金的最大放电比容量由135.0 mAh/g提高到143.7 mAh/g;合金表面的活性原子数量增加,合金电极的极化电阻由288.4 mΩ减小到212.7 mΩ。
化学镀2 h的样品,施镀时间较长,耐腐蚀的Ni-P镀层完整包覆基体表面,容量保持率提高较多,在25℃时,S30由88.0%提高到93.9%,S50由84.9%提高到90.4%。合金的高倍率放电性能提高,电流为900 mA/g时,最大放电比容量由原始合金的29.7 mAh/g增加到49.0 mAh/g。
[1]HU Zi-long(胡子龙).储氢材料[M].Beijing(北京):Chemical Industry Press(化学工业出版社),2002.
[2]Luan B,Cui N,Liu H K,et al.Low temperature surface microencapsulation of Ti2Ni hydrogen storage alloy powders[J].J Power Sources,1994,52(2):295 -299.
[3]Luan B,Cui N,Zhao H,et al.Mechanism of early capacity loss of Ti2Ni hydrogen storage alloy electrode[J].J Power Sources,1995,55(1):101-106.
[4]Zhao X Y,Zhou J F,Shen X D,et al.Structure and electrochemical hydrogen storage properties of A2B-type Ti-Zr-Ni alloys[J].Int J Hydrogen Energy,2012,37(6):5 050 -5 055.
[5]MA Yong-dong(马永栋),ZHOU Nan(周楠),ZHAO Xin-e(赵新娥),et al.化学镀铜和热处理对La0.6Nd0.2Mg0.2Ni3.3Co0.3Al0.25的影响[J].Battery Bimonthly(电池),2012,42(6):324-326.
[6]Jenq S N,Yang H W,Wang Y Y,et al.Discharge performance of Ti0.35Zr0.65Ni1.2V0.6Mn0.2alloy electrode modified by electroless nickel plating[J].Mater Chem Phys,1997,48(5):l0 - 16.
[7]Zhao X Y,Ma L Q,Ding Y,et al.Structural evolution and electrochemical hydrogenation behavior of Ti2Ni[J].Intermetallic,2010,18(5):1 086-1 090.

