Ni-Cu合金镀液中镍铜的分光光度法分析
陈海春
(沈阳理工大学环境与化工学院,辽宁沈阳 110168)
Ni-Cu合金镀液中镍铜的分光光度法分析
陈海春
(沈阳理工大学环境与化工学院,辽宁沈阳 110168)
在pH=8.0的NH3-NH4Cl缓冲溶液中,4-(2-吡啶偶氮)-间苯二酚作为显色剂,利用吸收比K1、K2恒定的特点,同时测定镍-铜合金镀液中的镍和铜。实验表明,在本测定条件下,镀液中镍、铜的吸光度加和性良好,镍的吸收比 K1=0.941,线性方程为A=0.982c+0.034,线性范围为0.12 ~0.80mg/L;铜的吸收比 K2=0.953,线性方程为 A=0.739c-0.023,线性范围为 0.12 ~1.20 mg/L;相对标准偏差为:镍1.1%,铜2.5%,加标回收率分别为:镍96.01% ~103.5%,铜93.8% ~103.2%。
分光光度法;Ni-Cu合金镀液;铜;镍;测定
引 言
影响镍-铜合金镀层性能的主要因素是镀液成分,为了保证镍-铜合金镀层质量稳定,要保持镀液中镍、铜含量的相对稳定,因此在生产过程中必须对镀液成分进行跟踪检测。近几年,利用分光光度法同时测定混合物中金属离子浓度的研究较为活跃,如双波长标准加入法[1-2]等,而利用吸收比同时测定镀液中的镍、铜还未见报道。本实验以4-(2-吡啶偶氮)-间苯二酚(PAR)为显色剂,在pH=8.0的NH3-NH4Cl缓冲溶液中与镍、铜离子显色,在吸收比K1、K2确定之后,仅需将试液在两个测量波长处测得代入计算公式,即可将多组分分析成功地转化为单组分分析[3]。
1 原理
根据吸光度具有加和性的原理可知
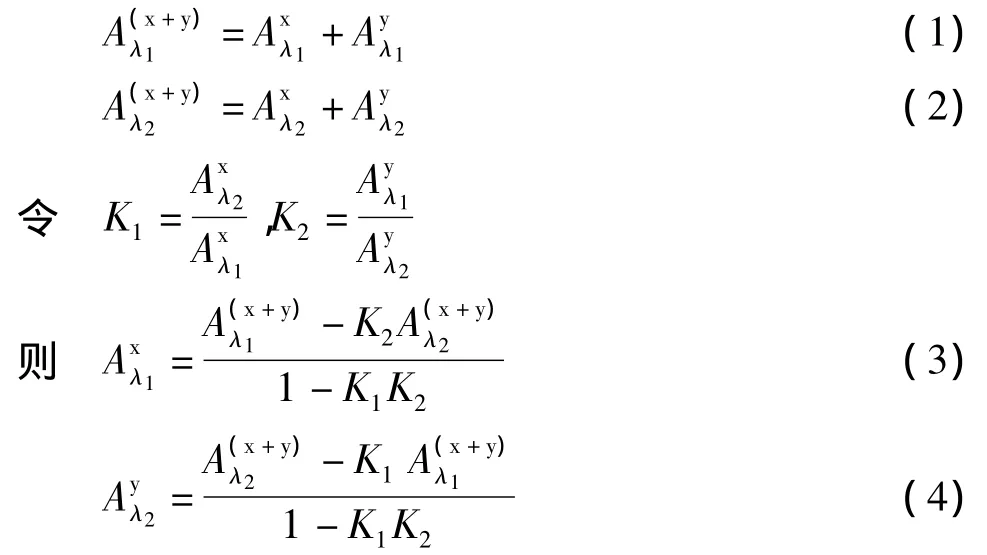
式中:K1、K2分别为镍、铜离子吸收比;λ1、λ2分别为镍、铜离子的测量波长,nm。
2 实验部分
2.1 主要仪器和试剂
756PC型分光光度计,0.01g/L镍标准溶液,0.01 g/L 铜标准溶液,pH=8.0 的 NH3-NH4Cl缓冲溶液,0.5g/L PAR 溶液。
2.2 实验方法
取一定量的待测镀液于25mL的比色管中,加入1.5mL显色剂PAR溶液,3mL NH3-NH4Cl缓冲溶液,加蒸馏水定容并摇匀。15min后,用1.0cm的比色皿,试剂空白为参比,分别在镍、铜测量波长处测定其吸光度值,然后按回归方程计算镍和铜的质量浓度。
3 结果与讨论
3.1 测量波长的确定
在NH3-NH4Cl缓冲溶液中,镍、铜与PAR形成配合物的吸收谱图重叠,用常规方法无法同时测定。选择最大吸收波长为测量波长,即镍的测量波长为496nm,铜的测量波长为506nm。
3.2 实验条件的影响
3.2.1 pH 的影响
氨缓冲和硼砂缓冲溶液,镍、铜络合物在硼砂缓冲溶液中吸光度较小,而在pH为8.0~10.0的NH3-NH4Cl缓冲溶液中,镍、铜络合物的吸光度大,且稳定,故选定 pH为8.0的氨缓冲溶液。1.0~5.0 mL氨缓冲溶液,镍、铜络合物的吸光度大且稳定,本实验选用3.0mL。
3.2.2 表面活性剂的选择
实验表明,加入表面活性剂,可以使铜吸光度变小;而对镍吸光度影响相对较小,综合考虑,本实验不加入表面活性剂。
3.2.3 显色剂
实验表明,1.5~2.5mL显色剂 PAR溶液,镍、铜络合物的吸光度大且稳定,本实验选择1.5mL。
3.2.4 显色时间及络合物的稳定性
实验表明,两种有色络合物显色时间较快,10min吸光度达到最大,且稳定24h以上。本实验选择显色15min。
3.3 加和性实验
由于本实验是基于镍、铜离子吸光度加和性的原理,所以有必要对实验体系的加和性进行考察。配制单一浓度的镍、铜标准溶液及二组分的标准混合液,分别在镍、铜测量波长处测定吸光度,并将由标准混合液测得的吸光度与单一组分测得的吸光度之和相比较。实验表明,吸光度加和性良好。
3.4 镍、铜吸收比K1、K2的确定
取一系列不同体积的镍标准溶液,按实验方法在镍、铜测量波长处测定吸光度,求出镍的吸收比K1,结果见表1。

表1 吸收比K1的确定 (n=7)
同理求得铜的吸收比K2平均值为0.953,RSD为 1.1%。
3.5 线性方程及线性范围
镍的线性回归方程为A=0.982c+0.034(R=0.996),线性范围为 0.12 ~0.80mg/L;铜的线性回归方程为 A=0.739c-0.023(R=0.998),线性范围为 0.12 ~1.20mg/L。
3.6 干扰离子实验
实验表明,Mg2+、Ca2+、Mn2+、Zn2+、Cd2+、Cr6+、Fe3+、Al3+及Ag+等离子的允许量小,易产生干扰,利用酒石酸钠和三乙醇胺联合掩蔽有很好的效果。
4 试样分析
准确移取一定量的镍、铜合金镀液,加水稀释1 000倍,取20.0mL,加入1g/L 的酒石酸钠溶液1.0 mL,2g/L的三乙醇胺溶液1.0mL,滴加2%氢氧化钠溶液调pH至8.0,定容于100mL容量瓶中,摇匀,备用。将上述处理后的试样准确移取2.0mL,按实验方法在镍、铜测量波长处分别测定吸光度,求得镍和铜的质量浓度,并做回收试验,平行测定5次,结果见表2。
由表2中数据可得,试样中镍的平均质量浓度为0.496 9 mg/L,铜的平均质量浓度为0.174 9 mg/L,计算求得原合金镀液中镍的质量浓度为31.06 g/L,铜的质量浓度为10.93g/L。

表2 精密度考察数据表(n=5)
5 结论
镍和铜在测量波长处吸光度加和性良好,吸收比K1、K2基本恒定,利用吸收比同时测定合金镀液中镍、铜可行,具有一定的应用价值。
[1]陈海春,王宏.用光度法同时测定合金镀液中的锌和镍[J].材料保护,2008,41(6):78-79.
[2]毕韶丹,高俊杰,余萍.铜-镍合金镀液中铜(Ⅱ)和镍(Ⅱ)的测定[J].电镀与精饰,2009,31(5):37-38.
[3]张凌,李德亮,崔节虎,等.紫外光谱法同时测定强力霉素废水中磺基水杨酸与对甲基苯磺酸[J].分析测试学报,2006,25(4):108-110.
Spectrophotometric Analysis of Nickel and Copper in Ni-Cu Alloy Plating Bath
CHEN Hai-chun
(School of Environmental and Chemical Engineering,Shenyang Ligong University,Shenyang 110168,China)
By considering the stable absorption characteristic of copper and nickel,the concentration of copper and nickel in the nickel and copper alloy plating bath were determined in NH3-NH4Cl buffer system with pH value of 8.0 and 4-(2-pyridylazo)-resorcinol as reagent.The results showed that under these testing systems nickel and copper have a good additive property.The absorption ratio of nickel was K1=0.941,and the concentration of nickel was followed the equation of A=0.982c+0.034 in the range of 0.12 ~0.80mg/L.The absorption ratio of copper was K2=0.953,and the concentration of copper was followed the equation of A=0.739c-0.023 in the range of 0.12 ~1.20mg/L.The standard deviation of nickel and copper was 1.1%and 2.5%,and the nickel and copper standard addition recoveries were 96.01% ~103.5%and 93.8% ~103.2%respectively.
spectrophotometric analysis;Ni-Cu alloy plating bath;copper;nickel;determination
TG115.335
B
1001-3849(2012)04-0039-03
2011-10-20

