RCHOP与ECHOP方案治疗初治的中高危组B细胞非霍奇金淋巴瘤的临床观察
徐吉兵 王季石 惠 阳
1 枣阳市第一人民医院血液科,湖北枣阳 441200
2 贵阳医学院附属医院血液科,贵阳 550004
非霍奇金淋巴瘤(non-Hodgkin's lymphoma,NHL)是临床常见的淋巴造血系统恶性肿瘤,大多数起源于B淋巴细胞,95%以上的B细胞NHL表达CD20抗原。根据NHL的国际预后指数(international prognostic index,IPI)危险分层,分为低危、中低危、中高危、高危组。RCHOP方案是初治B细胞淋巴瘤包括中、高危组B细胞NHL的新一代标准方案。ECHOP方案常用于复发难治性淋巴瘤的补救治疗或初治的中、高危组淋巴瘤的治疗。本院对于初治的中高危组B细胞NHL,常给予ECHOP或RCHOP化疗,本文回顾性分析两种方案的疗效和安全性,初步探讨两种方法对初治中、高危组B细胞NHL患者的疗效及预后的影响。
1 资料与方法
1.1 一般资料
60例患者,其中男35例,女25例,年龄20~84岁,中位年龄62岁;男35例中,RCHOP组18例,ECHOP组17例;女25例中,RCHOP组14例,ECHOP组11例;有B症状者40例中,RCHOP组23例,ECHOP组17例;有结外侵犯者34例中,RCHOP组17例,ECHOP组17例;血清乳酸脱氢酶(LDH)水平升高者51例,其中RCHOP组30例,ECHOP组21例。按Ann Arbor分期,RCHOP组Ⅰ~Ⅱ期者7例,Ⅲ~Ⅳ期者25例;ECHOP组Ⅰ~Ⅱ期者6例,Ⅲ~Ⅳ期者22例;体能评分(ECOG):RCHOP组0~1分者7例,2~4分者25例,ECHOP组0~1分者7例,2~4分者21例;肿块大小≤5cm者24例,5~10cm者l5例,≥10cm者7例。经统计学分析,两组治疗前相关因素(性别、年龄、有B症状者、LDH水平、分期、IPI评分)差异无统计学意义(P>0.05),具有可比性。
1.2 诊断及排除标准
选取2006年9月—2010年9月本院收治的256例NHL患者进行病例收集和整理,选取符合中高危组B细胞淋巴瘤的初治患者。诊断标准包括:①符合2001年WHO关于淋巴瘤的诊断和分类标准[1]。临床分期按照Ann Arbor分期所建议的标准;②细胞免疫组化均显示CD20阳性;③IPI评分在3分以上,其中RCHOP组至少完成2个疗程化疗。经筛选共有60例满足上述条件,其中RCHOP组的有32例,ECHOP组的有28例,所有患者常规进行全面临床检查,包括体检、血常规、生化常规、胸(腹)部和盆腔CT、骨髓检查。
1.3 治疗方法
RCHOP治疗组化疗方案:利妥昔单抗375mg/m2,第1天,静脉滴注,利妥昔单抗输注前30min常规给予肌肉注射非那根25mg,或静脉注射地塞米松5 mg,以预防利妥昔单抗输注的相关不良反应;环磷酰胺(CTX)750mg/m2,阿霉素(ADM)50mg/m2,长春新碱(VCR)1.4mg/m2,均于第2天静脉滴注;泼尼松60mg/m2,于第2~6天静脉滴注,每3周重复1次,最少进行2个疗程。
ECHOP治疗组化疗方案:依托泊苷每天50mg/m2,于第1~4天静脉滴注;其余同RCHOP方案,21 d为1个周期,共进行4~6个周期。对于ECOG分期为3、4期的患者先给予相应的针对性支持、对症治疗,待患者整体状况改善,重新评估体能达到ECOG2级后再给予相应的化疗。
1.4 疗效评价及不良反应
60例患者按IPI评分均>3分,属于中、高危组,治疗前所有患者经组织学检查并经免疫组化证实CD20阳性。患者均化疗4个疗程的1个月后进行疗效评估。按照 WHO关于NHL的疗效判断标准[1],将反应分为完全缓解(CR)、不确定的完全缓解(CRu)、部分缓解(PR)、稳定(SD)、进展(PD)、复发(RD),总有效率=[(CR+CRu+PR)例数/总例数]×100%。不良反应按照 WHO不良反应评价标准,分为0级、Ⅰ级、Ⅱ级、Ⅲ级、Ⅳ级。本文将分别从持续缓解时间、总生存时间和无病生存时间及不良反应四个方面评价二者的作用。持续缓解时间定义为自开始判定为CR起,至肿瘤开始再现的时间;总生存时间定义为自开始化疗至死亡或末次随诊时间;无病生存时间定义为CR患者从开始化疗至开始复发或死亡的时间。
1.5 统计学处理
采用SPSS 13.0统计软件进行处理。以χ2检验评价影响临床疗效的因素,Kaplan-Meier法计算生存率、绘制生存曲线,组间生存率比较采用Log-rank检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
RCHOP组中,21例获得CR,2例归入CRu,7例获得PR,1例为SD,1例为PD,5例为RD,总有效率为93.7%。ECHOP组中,CR为13例,CRu为1例,PR为9例,SD为3例,PD为2例,RD为10例,总有效率为82.1%。两组总有效率经统计学分析差异无统计学意义(P>0.05),两组的CR差异有统计学意 义(P<0.05)。见表1。
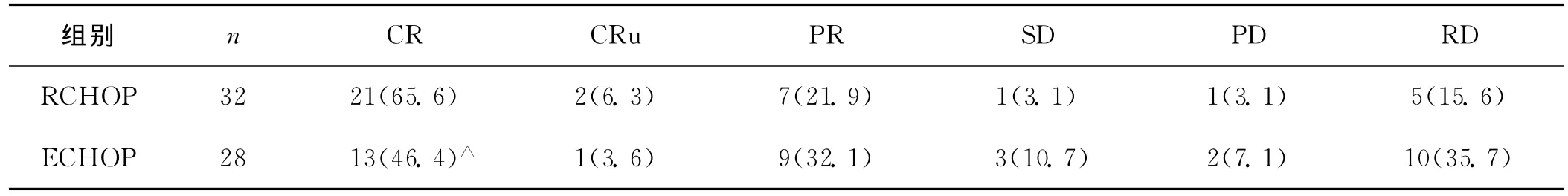
表1 两组的疗效比较(例,%)
2.2 两组患者生存率比较
RCHOP组中,8例死亡,中位生存时间为34.0个月(95%可信区间28.9~39.1个月),3年总生存率为75.0%。ECHOP组中,13例死亡,中位生存时间为27.6个月(95%可信区间22.7~32.5个月),3年总生存率为53.6%。经Log-rank分析,两组的差异无统计学意义(P>0.05)。见表2。
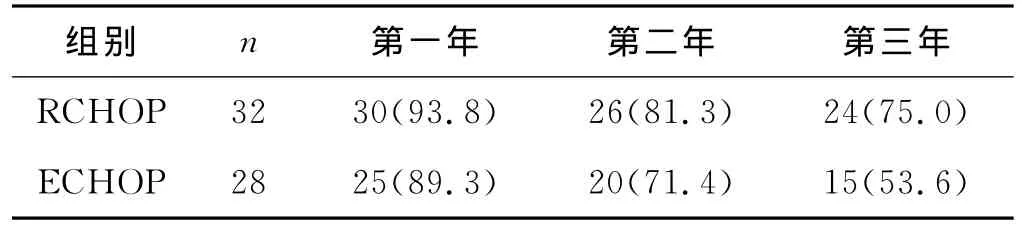
表2 两组的生存率比较(例,%)
2.3 两组患者持续缓解时间比较
RCHOP组中位缓解时间为32.2个月(95%可信区间为27.1~37.2个月)。ECHOP组中位缓解时间为22.5个月(95%可信区间为17.4~27.5个月),两组差异有统计学意义(P<0.05)。见图1。
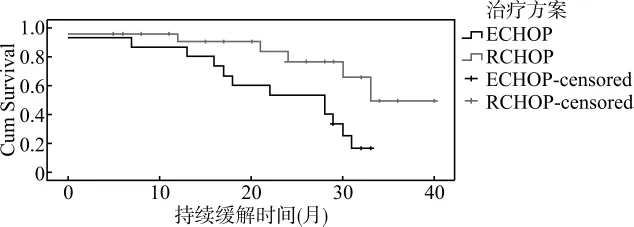
图1 两组持续缓解时间曲线
2.4 两组患者无病生存时间
RCHOP组中位无病生存时间为36.4个月(95%可信区间为31.2~41.5个月);ECHOP组中位无病生存时间为25.8月(95%可信区间为20.4~31.2个月),经Log-rank检验,两组间差异有统计学意义(P<0.05)。
2.5 安全性分析
两组患者均可评价不良反应。两组共同的主要临床不良反应包括骨髓抑制、消化系统反应、肝肾损害、脱发等。RCHOP组有个别患者出现无症状性血压下降和传导阻滞及QT间期延长,减慢输注速度或停止输注可缓解。ECHOP组有明显口腔黏膜炎,这与ECHOP方案化疗的强度较高有关,其他各种不良反应总体上ECHOP组要多于RCHOP组,但差异无统计学意义。
3 讨论
NHL是一种全身性疾病,不同类型及分期的NHL其生存预后存在极大的不同,1993年Shipp等[2]建立了IPI,结果表明患者发病时IPI积分与患者的预后明显相关,中高危组预期5年OS为43%,高危组为26%。
本研究回顾分析了利妥昔单抗或依托泊苷联合CHOP方案治疗初治中高危组B细胞淋巴瘤的临床效果及安全性,在本文的观察中,RCHOP方案可以取得较高的完全缓解率,持续缓解时间和无病生存时间均明显长于ECHOP组,表明RCHOP组患者的生存质量优于ECHOP组。两组的生存率无显著性差异,表明IPI积分是NHL生存率的独立预后因素,不受化疗方案影响,但不能排除非肿瘤因素、或病例数较少的影响,需要临床大样本进一步验证。
有研究[3-4]报道用RCHOP方案治疗60~80岁的初治DLBCL患者的CR为76%,2年生存率为70%,均低于本文的研究结果,经分析差异无统计学意义(P=0.21),笔者分析与处理方法无关,可能与本文的样本数较少有关。Pfreundschuh等[5]报道用ECHOP治疗老年侵袭性NHL的CR约为70.0%,5年无进展生存率和总体生存率分别为32.5%和46.0%。CR高于本文,可能与本文的IPI评分较高有关,而总体生存率、无进展生存率低于本文的结果,可能与其观察时间较长有关。本研究中两组的临床疗效与国外进行的临床研究结果基本一致。
总之,本研究提示,RCHOP方案治疗中、高危组B细胞NHL的完全缓解率、持续缓解时间、无病生存时间均明显优于ECHOP方案,两组的不良反应发生率均不高,安全性好,故两种方案均可作为中、高危组NHL的治疗方案。RCHOP组生存质量更好,是治疗初治的中、高危组B细胞NHL的更好选择。
[1]张之南,沈悌.血液病诊断及疗效标准[M].3版.北京:人民卫生出版社,2007:220-227.
[2]SHIPP MA.Prognostic factors in aggressive non-Hodgkin's lymphoma:who has“high-risk”disease?[J].Blood,1994,83(5):1165-1173.
[3]FEUGIER P,van HOOF A,SEBBAN C,et al.Longterm results of the R-CHOP study in the treatment of elderly patients with diffuse large B-cell lymphoma:a study by the Groupe d’Etude des Lymphomes de l’Adulte[J].J Clin Oncol,2005,23(18):4117-4126.
[4]HORNBERGER JC,BEST JH.Cost utility in the United States of rituximab plus cyclophosphamide,doxorubicin,vincristine and prednisone for thetreatment of elderly patients with diffuse large B-cell lymphoma [J].Cancer,2005,103(8):1644-1651.
[5]PFRUNDSCHUH M,TRÜMPER L,KLOESS M,et al.Two-weekly or 3-weekly CHOP chemotherapy with or without etoposide for the treatment of elderly patients with aggressive lymphomas:results of the NHL-B2trial of the DSHNHL[J].Blood,2004,104(3):634-641.

