化学除磷工艺研究进展
刘 宁,陈小光,崔彦召,柳建设,徐晓雪
(东华大学环境工程与科学学院,上海 201620)
进展与述评
化学除磷工艺研究进展
刘 宁,陈小光,崔彦召,柳建设,徐晓雪
(东华大学环境工程与科学学院,上海 201620)
化学除磷是抑制水体富营养化以及从废水中回收磷资源的有效手段。本文阐述了铁盐、铝盐和石灰 3种常见化学除磷药剂的除磷机理及其影响因素,如pH值、投加量、投药点以及经济性分析;概述了前置化学辅助除磷、协同化学辅助除磷、后置化学辅助除磷以及旁路化学辅助除磷 4种化学辅助生物除磷工艺的特点,最后介绍了吸附法和结晶法除磷新兴工艺,阐明了磷资源回收是未来化学除磷工艺的方向发展。
化学除磷;除磷药剂;化学辅助生物除磷;影响因素
磷在生物圈中的循环过程不同于碳和氮的循环,属于典型的沉积型循环,起始于岩石的风化,终止于水中的沉积。在生物圈内,大部分磷只是单向流动,构不成循环,磷酸盐也因此成为一种不能再生的资源[1]。以目前开采速度计算,地壳中优质磷矿石(P2O5>15%)将在一百年内耗至殆尽[2],我国的磷矿产资源也将在七十年内耗竭[3]。
磷既是一种不可再生资源,又是导致水体富营养化的主要元素。农田施加的过量磷肥,城市生活污水含有较多的磷,某些工业废水也含有丰富的磷,它们均是是水体富营养化的重要诱因。为预防水体富营养化,《城镇污水处理厂污染物排放标准》(GB 18918—2002)中将一级A出水磷标准由磷酸盐计提标升至由总磷(0.50 mg/L)计。因此,研发污水除磷工艺的形势十分迫切。
目前常用的除磷工艺主要有生物法、化学法。生物法是利用聚磷菌在缺氧、厌氧和好氧交替的情况下完成对污水中磷的去除。但运行实践表明,单纯的生物除磷很难使出水达标排放[4]。近年来,化学除磷连同化学辅助生物除磷工艺因其处理效率高,处理速度快而备受青睐。本文作者介绍了化学除磷机理、影响因素以及化学辅助生物联合除磷工艺特点,最后介绍了化学除磷工艺的新兴方法——吸附法、结晶法除磷工艺。
1 化学除磷机理
化学除磷是通过化学沉析过程形成磷酸盐沉淀而完成的,是自然界磷酸盐沉析的人为强化。自然界的磷来源于磷酸盐岩石、沉积物、鸟粪石和动物化石,经过天然侵蚀或人工开采,以磷酸盐的形式进入水体或土壤,由此构成了磷酸盐沉析。而化学除磷是向污水中人为投加除磷试剂(金属盐药剂)与污水中溶解性的磷(磷酸盐)混合后,形成颗粒状、非溶解性的难溶沉淀物而从水中析出的过程(图1)[5]。常用的除磷试剂有铁盐、铝盐和石灰。

图1 除磷机理
1.1 铁盐除磷机理
化学除磷过程中铁离子既可以生成磷酸盐沉淀也可以生成金属氢氧化物沉淀,反应方程式如式(1)、式(2)(以三氯化铁为例)[6]。
主反应

副反应

溶于水中后,Fe3+一方面与磷酸盐生成难溶盐,一方面通过溶解和吸水发生强烈水解,并在水解的同时发生各种聚合反应,生成具有较长线性结构的多核羟基络合物,这些含铁的羟基络合物能有效降低或消除水体中胶体的ζ电位,通过中和,吸附架桥及絮体的卷扫作用使胶体凝聚,再通过沉淀分离将磷去除[7]。Roger等[8]用红外研究了铁盐除磷后的产物,表明氢氧化铁凝胶及各种铁氧化物都能吸附大量磷酸根,而且产物中存在双核络合物,从而推断出在两个 Fe3+之间形成桥结构。
1.2 铝盐除磷机理
化学除磷过程中铝离子既可以生成磷酸盐沉淀也可以生成金属氢氧化物沉淀,反应方程式如式(3)、式(4)(以硫酸铝为例)[6]。

1.3 石灰除磷机理
石灰除磷反应式如式(5)、式(6)[6]。
主反应

副反应

其中,主反应在石灰除磷中占主导地位[7],它决定了废水软化和脱碱所消耗的石灰量,同时,主反应生成的碳酸钙可作为增重剂,有助于副反应生成的磷酸盐沉淀。而Ca(OH)2作为混凝剂还有良好的凝聚吸附作用[11]。在磷酸盐沉淀形成的过程中,起主要作用的不是Ca2+,而是OH-,因为随着pH值的提高,Ca5(OH)(PO4)3的溶解度降低[12]。周元祥等[13]的实验表明可以通过提高溶液中离子浓度、升高pH值或温度等方式提高溶液的过饱和度以实现磷酸钙盐的沉淀。
2 化学除磷的影响因素
2.1 pH值的影响
pH值对化学除磷的影响主要表现在它显著影响磷酸盐沉淀的溶解度。张亚勤等[14]绘制了 Fe、A l、Ca磷酸盐的平衡溶解度图(图2)。根据图2,磷酸铁、磷酸铝和磷酸钙最小溶解度对应的pH值范围分别为5.0~5.5,6.0~7.0和8.0~9.0。若低于这一pH值,磷酸铁、磷酸铝和磷酸钙将重新溶解,导致水中的磷浓度升高,不利于磷的去除。利用pH值和磷酸钙之间的关系可优化除磷效率。铁盐和铝盐沉淀正磷酸的最佳pH值为5.0、6.0[6]。但石灰法除磷实践表明,pH值必须调节至较高值(10.5左右),李京雄[15]实验表明,用钙盐做除磷试剂的最佳pH值为10.0~12.0。
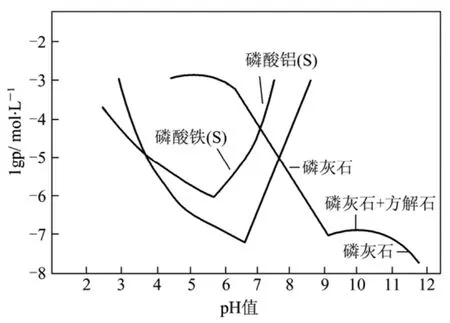
图2 Fe、Al、Ca磷酸盐的平衡溶解度图
2.2 投加量的影响
投加量对化学除磷也有直接影响。当采用铁盐和铝盐进行化学除磷时,三价金属离子与磷酸根离子以等摩尔进行反应,因此药剂的投加量应取决于磷的含量。但是实际运行时,化学药剂的投加量总是大于按化学计量关系预测的药剂投加量。这是因为污水中还存在氢氧根离子与药剂反应生成氢氧化物而消耗一部分金属离子。要求出水总磷(TP)浓度为0.50~1.00 mg/L时,典型的金属投加量范围为1.0~2.0 mol金属盐/mol去除磷[6],要求出水 TP浓度低于0.50 mg/L时,所需投加量明显增大。俞蕴芳等[16]的实验结果表明,在TP 浓度分别为4.19 mg/L和4.22 mg/L、pH值为7.3和7.8的条件下随着铝盐投加量的增加,水体中残留TP逐渐减少,去除率增加。在进水总磷为4.38 mg/L、pH值为7.8的条件下,随着三氯化铁投加量的增加,总磷去除率也呈不断增加的趋势。对于投加石灰的化学除磷,在pH值大于10.0条件下,污水中的碳酸氢根和石灰发生反应生成碳酸钙沉淀。石灰除磷所需的石灰投加量很大程度上取决于污水的碱度(满足除磷要求的石灰投加量大致为总碳酸盐碱度的1.5倍)而不是污水的含磷量[17-18]。
2.3 加药点的影响
对于化学辅助生物除磷工艺,除磷试剂加药点的选择显得至关重要,不同的加药点要选用不同的试剂。如硫酸亚铁来源稳定、价格低廉,在浓度满足要求的情况下,作为除磷试剂使用可大幅降低除磷费用[17]。但Fe2+在pH值为7.5~8.5的条件下,不易生成沉淀,这在一定程度上限制了其在废水化学除磷中的应用[19]。王文超等[19]的实验结果表明,因Fe2+不易被完全氧化,致使结晶颗粒沉淀效果不佳,故Fe2+试剂不宜在生物反应前投加。由于上述原因,在生产实践中,常将Fe2+投加在曝气沉砂池或曝气池中将Fe2+氧化为Fe3+,如Clack等[20]研究的Fe2+在曝气生物滤池除磷中的应用。当废水中存在丹宁酸等有机物时会影响铝盐的除磷效率[21],所以铝盐除磷一般在生物处理后进行。夏宏生等[22]实验结果表明,控制适宜的pH值,在生化反应后的化学除磷中采用铝盐可达到 90%~95%的除磷效率。加药点的影响将在后文进一步叙述。
2.4 经济性分析

表1 除磷试剂经济性分析
除磷试剂的经济性也是选择化学除磷药剂的重要影响因素之一。罗富金[23]分别计算了铁盐、铝盐和石灰3种试剂处理含磷废水的费用,理论计算表明除磷费用铝盐最高为0.027元/t,石灰次之为0.016元/t,铁盐最低为0.013元/t。念东等[24]的小试和生产性实验的结果表明,硫酸亚铁的加药费用最低,约为0.08元/m3,硫酸铝和聚合氯化铝铁都能在较低的成本下使出水达到较高的水质,其药剂成本约为0.11~0.20元/m3(表1)。
总的来说,水体pH值、碱度、化学药剂的投加量、加药点以及处理成本都对化学除磷有较大影响。为使污水磷达标排放,即出水总磷 TP<0.50 mg/L时,石灰除磷系统的pH值应大于10.0,铁盐和铝盐除磷系统的pH值应维持在7.0左右。其它条件相同时,污水含磷量越高,除磷药剂的利用率也越高。投加费用为铁盐最便宜,铝盐最贵。
3 化学辅助生物除磷工艺特点
根据化学除磷试剂投加点与生物除磷反应的先后顺序,可将化学辅助生物除磷工艺分为前置化学辅助除磷工艺、协同化学辅助除磷工艺、后置化学辅助除磷工艺和旁路化学辅助除磷工艺。
目前饲料加工常用的是锤片式粉碎机。锤片式粉碎机的适应性很强,通过调整粉碎机的参数可生产各种粒度的颗粒,可适用于各种各样的原料,设备投入成本低,维护费用低,相对容易操作。但它是通过筛片孔径控制粒度,物料粒度都小于筛片孔径,加工过程中高速旋转时容易造成很大一部分物料粒度远远小于筛片孔径,造成物料粒径不均匀[3]。在生产实践中通过降低转子转速调整物料粒度又导致制粒后粒度不整齐,均匀性差,并存在能量利用率低、电耗高、产热、粉尘多、噪音大等缺陷。
3.1 前置化学辅助除磷工艺
前置化学辅助除磷工艺是指投药点设在生物反应前,如将除磷药剂投放在沉砂池(也可投加在初沉池进水渠、文丘里渠)中,产生的沉淀物在沉砂池中即被分离去除[25]。污水厂前置除磷过程中,因副反应生成的金属氢氧化物絮体可吸附和絮凝污水中含碳、含氮有机物,对二者的去除起到一定的促进作用。孟永进等[26]的实验结果表明,在控制稳定运行的情况下,前置除磷对磷的去除率可达到90%以上,对磷的去除而言是一种有效的工艺。念东等[24]的前置实验表明,硫酸铝和三氯化铁对磷均有很好的去除效果,当药剂投加量与总磷质量比(Me/P)大于2.5时,磷含量可以降到1.00对mg/L左右。张键[27]通过用-P与A l3+物质的量比为1∶4的铝盐进行实验得到前置除磷率为68.2%。
前置化学辅助除磷工艺适合于有机物浓度较高的废水除磷处理。而对于有机物浓度不高,且工艺要求反硝化脱氮(需要碳源)的工艺不宜采用(因为前置加药会引起碳源不足),如以生活污水为主的城镇污水厂。再者,对有机物浓度不高的污水,除磷药剂对微生物生长的影响不可忽略[14]。
3.2 协同化学辅助除磷工艺
协同化学辅助除磷工艺是指投药点设在生物反应中,将除磷药剂投放在曝气池中,产生的沉淀物通过二沉池去除。凌霄等[28]的协同实验结果表明,当反应器水力负荷为1.30 m3/(m2·h),进水总磷(TP)为0.12~0.13 kg/(m3·d)时,投加铝盐后TP去除率可提高至 70.0%~86.0%。王刚[29]通过实验表明,利用硫酸铝溶液进行协同沉淀是降低出水TP含量的有效方法,在进水TP浓度为2.29 mg/L的情况下,TP的去除率为 88.4%。张键[27]通过用与A l3+物质的量之比为1∶4的铝盐进行实验得到协同除磷率为56.0%。此外,在生化反应系统中,通过回流可以充分利用沉析药剂,减少药剂使用量,而且金属盐药剂会增加活性污泥重量,从而一定程度上避免了污泥膨胀[30]。
协同化学辅助除磷工艺适宜pH值较为稳定的生化系统。随着生物反应的进行,所导致的pH值变化必然引起系统除磷效果的变化。因为,生物反应适宜pH值往往与化学除磷反应适宜pH值有一定差距,两者很难同时兼顾。如钙盐要求 pH值为10.0~12.0,这会影响微生物的增值和活性以及污泥泥龄,继而对生化作用产生影响[6]。此外,邹联沛等[31]研究表明,当进水TP浓度较高时,对于膜生物反应器中亦不建议采用协同化学辅助除磷工艺,这是因为化学辅助除磷使反应器内的总污泥浓度升高,会导致膜通量和污泥活性降低。
3.3 后置化学辅助除磷工艺
后置化学辅助除磷是目前最普遍采用的化学辅助生物除磷工艺,但其自身也存在缺陷。如因生成极细小的磷酸盐晶体,需要增设专用的混合、反应和沉淀设施,才能进入沉滤池,从而增加基建费用。3.4 旁路化学辅助除磷工艺
旁路化学辅助除磷工艺主要是针对A2/O工艺而言,将该工艺中厌氧池的富磷上清液引入专一化学除磷池,在此设置投药点进行化学除磷,再将除磷沉淀后的上清液排入缺氧池进行后续反应。侯红勋等[4]为解决A2/O型氧化沟工艺除磷不稳定、出水磷难以达标的问题,在 A2/O型氧化沟工艺除磷的基础上,增加了旁路除磷段,以提高其除磷效率,结果表明:增加化学除磷能够提高系统的除磷效果,使出水TP<1.00 mg/L,达到了国家排放标准(GB 18918—2002)一级 B标准,并且化学除磷剂的投配率为1∶1(与TP质量之比),低于传统化学除磷的1.5∶1(与TP质量之比)。李伟民等[33]也进行了类似的研究,结果表明出水TP≤0.70 mg/L达到国家排放标准(GB 18918—2002)一级B标准。吴剑等[34]采用旁路除磷工艺,得到在 FeSO4·7H2O、A l2(SO4)3·12H2O和Ca(OH)2与P最佳投加质量比分别为10.7、12.0和5.6时,均可使出水TP稳定在0.30mg/L以下。
4 化学除磷工艺的新发展
传统的化学除磷工艺是在生物除磷的基础上辅以化学沉淀除磷,依旧无法克服化学污泥产量大、磷资源难以回收利用的弊端。为了解决这些问题,许多研究者对吸附法除磷工艺和结晶法除磷工艺进行了大量的研究。
4.1 吸附法除磷工艺
吸附法是利用某些多孔或大比表面积的固体物质对水中的磷酸根离子的亲和力来实现污水除磷的目的,机理如图3所示。通过在吸附剂表面的物理吸附、离子交换或表面沉淀作用,将磷从污水中分离出来,再通过一定的手段可以回收磷资源。除磷吸附剂一般分为天然吸附剂和合成吸附剂,其中天然吸附剂有粉煤灰、钢渣、沸石、凹凸棒、海泡石、活性氧化硅等;合成吸附剂有Al、Mg、Fe、Ca和La等多种金属的氧化物及其盐类[35]。
杨杰等[36]研究了固定化氧化镧化学-吸附除磷技术,其原理都是基于活性氧化镧是一种多孔、高分散度的材料,有很大的比表面积,具有强吸附能力。通过控制煅烧温度将镧系物质固定于La-SBR-15的孔内,获到了能快速高效吸附磷的合成吸附剂。
Jacobs等[37]研究了将纳米级的铁离子稳定于来自极耐热古菌(PfFrt)的耐热铁蛋白中,然后通过纳米级的铁离子对磷酸盐进行吸附。Jacobs等认为这个过程存在两种完全不同的吸附机理,即相继吸附(sequential phosphate incorporation method )和同时吸附(simultaneous phosphate incorporation method )(图4)。但实验结果均表明这种耐热性的蛋白纳米笼状物质可以通过对铁的催化氧化作用,实现对磷的快速吸附。Delaney等[38]研究了含各种金属离子(Zr,Ti,Fe,A l)且排列有序的氧化硅,通过吸附作用完成对废水中磷酸盐离子的去除。此材料的比表面积在600~700 m2/g,在适当的条件下可以达到对水体中磷的完全去除。

图3 吸附除磷机理
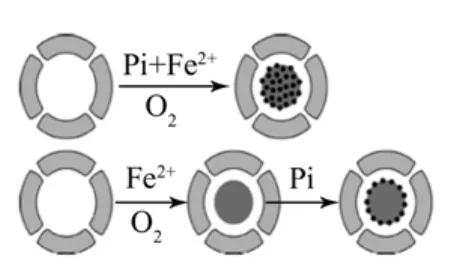
图4 纳米级铁离子对磷吸附机理
4.2 结晶法除磷工艺
结晶法除磷是目前国内外在废水除磷及磷回收领域研究的热点[39]。它是指通过控制一定的反应条件,使废水中的磷以磷酸铵镁(MgNH4PO4·6H2O、鸟粪石、MAP)或羟基磷酸钙[Ca5(PO4)3OH、HAP]的结晶形式从废水中去除,并能作为磷资源加以利用[40]。在结晶法除磷的过程中,废水中的磷在晶种上以晶体的形式析出,理论上不产生污泥,不会造成二次污染[41]。
结晶除磷的影响因素包括pH值、反应物物质的量比、晶种和反应时间(HRT)。
王广伟等[40]的研究表明,pH值会影响溶解性磷酸盐(、、、H3PO4)的比例进而影响晶体的过饱和度;再者在一定范围内,MAP和HAP随着体系pH值的升高,溶解度均有不同程度的降低,有利于晶体形成。Song等[42]的研究发现,当pH值升至10.3时,MAP的溶解度降至最低,继续提高pH值,MAP的溶解度会转而升高。其原因可能是当pH>10左右时,发生了副反应[如生成Mg(OH)2等],使Mg2+的浓度降低,从而降低了MAP的过饱和度。姜世坤等[43]的研究发现,在MAP形成过程中,当Mg/P>1(物质的量之比)时晶体形成迅速,磷的去除率随物质的量比增大而增高,但当Mg2+达到一定浓度后,磷的去除率不再变化。晶种的选择对结晶法除磷及磷回收也有重要的影响,其重要性表现在成核过程的最初阶段是形成亚稳态且无定形的前体物质,然后转化为最终晶体物质[44](HAP或MAP)。而利用晶种诱导可以降低结晶所需要的活化能,减少结晶反应时间[45]。Corre等[46]用不锈钢材料制成网眼形式的晶种,使结晶除磷效率达到80.0%。Quintana等[47]利用氧化镁副产物作晶种,可以有效缩短反应时间以及提高 MAP结晶质量,便于回收利用;郝凌云等[48]的实验得出,因为反应时间过长,会破坏MAP沉淀体系,使晶体沉降性能降低,所以并不是反应时间越长,磷回收效率越好。
因为有利于磷资源的回收,吸附法和结晶除磷工艺已经在欧美日等发达国家和地区取得了较大发展,如日本利用碱液浸泡技术进行解吸附释放出磷,磷酸根以磷酸钠晶体形式回收,回收率高于80%,回收晶体可以用做高效肥料[49]。日本的Shinji污水净化中心建有的MAP系统,每天可回收MAP 500~550 kg,并将其用于缓释肥料和工业原材料,实现磷资源的可持续发展[50]。
5 结 语
本文阐述了铁盐除磷、铝盐除磷和石灰除磷三种常见化学除磷机理,从pH值、投加量、加药点和处理成本的角度分析了化学除磷的影响因素,概括了前置化学辅助除磷工艺、协同化学辅助除磷工艺、后置化学辅助除磷工艺和旁路化学辅助除磷工艺这4种化学辅助生物除磷工艺的特点,并以吸附法和结晶法为例,阐明了磷资源回收是化学除磷的新发展方向。
[1] 人与生态网. 磷循环[EB/OL]. http://amuseum.cdstm.cn/AMuseum/ renyushengtaihuanjing/docc/stxtbrow.asp-id=2032&classid=2.htm l.
[2] Isherwood K F. M ineral fertilizer use and the environment [C]// International Fertilizer Industry Association United Nations Environment Prigramme,Paris:IFA/UNEP,106.
[3] 郝晓地,甘一萍. 排水研究新热点——从污水处理过程中回收磷[J]. 给水排水,2003,29(1):20-24.
[4] 候红勋,王淑莹,王亚宜,等. A2/O型氧化沟的旁侧化学除磷试验研究[J]. 中国给水排水,2006,22(7):30-33.
[5] 高廷耀,顾国维,周琪. 水污染控制工程[M]. 北京:高等教育出版社,2006:301.
[6] 邱维,张智. 城市污水化学除磷的探讨[J]. 重庆环境科学,2002,24(2):81-84.
[7] 徐丰果,罗建中,凌定勋. 废水化学除磷现状与进展[J]. 工业水处理,2003,23(5):18-20.
[8] Roger L P,Roger J A. The mechanism of phosphate fixation by iron oxides[J].Soil.Sci.Amer.Proc.,1975,39:837-841.
[9] Galarneau E,Gehr R. Phosphorus removal from wastewaters:Experimental and theoretical support for alternative mechanisms[J].Wat. Res.,1997,31(2):328-338.
[10] Boisseret Jean-Philippe,et al. Phosphate adsorption in flocculation process of alum inum ulphate and poly-alum inum-silicate-sulphate[J].Wat. Res.,1997,31(8):1936-1946.
[11] 尔丽珠. 石灰法处理高浓度含磷废水技术[J]. 电镀与精饰,2008,30(5):39-40.
[12] 王亮,彭志雄. 化学辅助除磷药剂比选及试验研究[J]. 广东化工,2011,38(219):39-40.
[13] 周元祥,黄健,张华,等. 化学磷回收促进生物除磷效果的实验研究[J]. 合肥工业大学学报,2005,28(10):1244-1248.
[14] 张亚勤. 污水处理厂达到一级A排放标准中的化学除磷[J]. 中国市政工程,2009(5):40-41.
[15] 李京雄. 化学除磷絮凝剂的选择[D]. 广东:广东工业大学,2005.
[16] 俞蕴芳,顾俊. 城市污水化学除磷药剂的选择实验研究[J]. 污染防治技术,2010,23(4):74-76.
[17] 郑兴灿,李亚新. 污水脱氮除磷技术[M]. 北京:中国建筑工业出版社,1988.
[18] 唐受印,戴邮芝. 水处理工程师手册[M]. 北京:化学工业出版社,2000.
[19] 王文超,张华,张欣. 化学除磷在城市污水处理中的应用[J]. 水科学与工程技术,2008 (1):14-16.
[20] Clack T,Stephenson T,Pearce P A. Phosphorus removal by chem ical precipitation in a biological aerated filter[J].Water Research,1997,31(10):2257-2563.
[21] Bashan L E,Bashan Y. Recent advances in removing phosphorus from wastewater and its future use as fertilizer(1997—2003)[J].Water Research,2004,38(19):4222-4246.
[22] 夏宏生,向欣. 废水除磷技术及进展分析[J]. 环境科学与管理,2006,31(1):125-128.
[23] 罗富金. 城市污水处理升级改造中化学除磷原理及费用[J]. 山西建筑,2010,36(29):174-175.
[24] 念东,王佳伟,刘立超. 城市污水处理厂化学除磷效果及运行成本研究[J]. 给水排水,2008,34(5):7-10.
[25] 高学艳. 污水中磷元素的净化措施[J]. 煤炭技术,2011,30(6):217-218.
[26] 孟永进,李旭峰. 浅谈化学除磷在城市污水处理中的应用[J]. 河北建筑工程学院学报,2005,23(3):19-21.
[27] 张健. 杭州七格污水处理厂化学除磷工艺[J]. 中国给水排水,2010,26(21):145-147.
[28] 凌霄,胡勇有,马骥. 曝气生物滤池铝盐化学强化与生物协同除磷[J]. 环境科学学报,2006,26(3):409-415.
[29] 王刚. 化学除磷在污水处理工艺中的运用[J]. 城市道桥与防洪,2009,4(4):70-72.
[30] 朱敏. 啤酒废水化学除磷的实施[J]. 啤酒科技,2010(6):27,30.
[31] 邹联沛,薛罡,王宝贞. 膜生物反应器中化学除磷的研究[J]. 中国给水排水,2002,18(11):19-21.
[32] 顾俊,董仁杰,丁根宝,等. 污水厂二沉池出水化学除磷实验[J].环境科学与管理,2009,34(8):79-81.
[33] 李伟民,刘杰,王涛,等. A2/O工艺的旁路化学除磷及污泥减量研究[J]. 中国给水排水,2010,26(17):16-22.
[34] 吴剑,王世和. MB(A2/O)处理城市污水富磷上清液的化学除磷研究[J]. 环境工程学报,2008,2(2):190-194.
[35] 龚云峰,孙素敏,钱玉山,等. 污水化学除磷处理技术[J]. 能源环境保护,2009,23(3):2-4.
[36] Yang Jie, Zhou Liang, Zhao Lingzhi,et al. A designed nanoporous material for phosphate removal w ith high effciency[J].Journal of Materials Chemistry,2011,21(8):2489-2494.
[37] Jacobs Johannes F,Hasan M Nahid,Kamal H P,et al. Development of bionanotechnological phosphate removal system with thermostable ferritin[J].Biotechnology and Bioengineering,2010,105(5):918-923.
[38] Delaney Paul,M cManamon Colm,Hanrahan John,et al. Development of chem ically engineered porous mental oxides for phosphate removal[J].Journal of Hazardous Materials,2011,185:382-391.
[39] Doyle J D,Parsons S A T. Struvite formation,control and recovery [J].Water Research,2002,36(16):3925-3940.
[40] 王广伟,邱立平,张守彬. 废水除磷及磷回收研究进展[J]. 水处理技术,2010,36(3):17-22.
[41] 亓延敏,吕锡武,徐微. 污水除磷及回收技术[J]. 山西建筑,2008,34(4):191-192.
[42] Song Y H,Yuan P,Zheng B H,et al. Nutrients removal and recovery by crystallization of magnesium ammonium phosphate from synthetic sw ine waste water[J].Chemosphere,2007,69(2):319-324.
[43] 姜世坤,尹军,赵玉鑫,等. 废水中回收磷技术研究进展[J]. 中国资源综合利用,2009,27(8):35-37
[44] Bellier N,Chazarenc F,Comeau Y. Phosphorus removal from wastewater by m ineral apatite [J].Water Research,2006,40(15):2965-2971.
[45] Kim E H,Yim S B,Jung H C,et al. Hydroxyapatite crystallization from a highly concentrated phosphate solution using powdered converter slag as a seed material [J].Journal of Hazardous Materials,2006,136(3):690-697.
[46] Corre K S,Jones E,Hobbs P,et al. Struvite crystallization and recovery using a stainless steel structure as a seed material [J].Water Research,2007,41(11):2449-2456.
[47] Quintana M,Colmenarejo M F,Barrera J,et al. Removal of phosphorus through struvite precipitation using a by-product of magnesium oxide production(BMP):Effect of the mode of BMP preparation [J].Chemical Engineering Journal,2008,136(2-3):204-209.
[48] 郝凌云,周荣敏,周芳,等. 磷酸铵镁沉淀法回收污水中磷的反应条件优化[J]. 工业用水与废水,2008,39(1):58-61.
[49] Yuhei Inamori,Toshihiro Sankai,Toshikatu Ozawa. Popularization and Development of High-performance Johkasou [M]. Tokyo:Gyosei Co.,2002
[50] Ueno Y,Fujii M. 3 years operating experience selling recovered struvite from full-scale palnt[DB/OL]. http ://www.nhm.ac.uk/m ineralogy/phos/finalprog3.doc.
Research progress of chem ical dephosphorization process
LIU Ning,CHEN Xiaoguang,CUI Yanzhao,LIU Jianshe,XU Xiaoxue
(Department of Environmental Engineering and Scientific,Donghua University,Shanghai 201620,China)
Chem ical phosphorus removal is an effective approach to controlling eutrophication and recycling phosphorous resource from waste water. The mechanisms of three major phosphorus removal reagents,such as ferric salt,alum inum salt and lime,were presented,and the influence factors of these three reagents,including pH,dosage,optimal dosing points and econom ic analysis,were also discussed. The processes of pre-chem ical-aid,synergic-chem ical-aid,post-chem ical-aid and bypass-chemical-aid phosphorus removal technologies were summarized. The adsorption and crystallization phosphorus removal new process was introduced,and the prospect of recycling phosphorous resource as the development orientation of phosphate removal process in the future was presented.
chem ical phosphorus removal; phosphorus removal reagents;chem ical-aid biological phosphorus removal;influence factor
X 522
A
1000–6613(2012)07–1597–07
2012-01-15;修改稿日期:2012-03-14。
中央高校专项资金自由探索项目(12D11307)及东华大学校基金(113-07-0053012)东华大学教改项目。
刘宁(1988—)女,硕士,主要从事废水生物处理及资源化的研究。E-mail liuningdorothia@yahoo.com.cn。联系人:陈小光,工学博士,讲师,主要从事废水生物处理工艺及装备的研究。E-mail cxg@dhu.edu.cn。

