利奈唑胺致慢性肾脏病患者转氨酶升高、血小板减少、乳酸酸中毒一例并文献复习
赵新菊,王 梅
利奈唑胺是新型口恶唑烷酮类抗菌药物,与其他抗菌药物无交叉耐药,在耐药革兰阳性菌感染的治疗中具有显著优势[1-2]。但慢性肾脏病(CKD),尤其是终末期肾脏病(ESRD)患者应用该药治疗的经验尚少。我科收治1例进展至ESRD合并心力衰竭、严重肺部感染,且多种抗生素治疗无效的患者,最后使用利奈唑胺及莫西沙星,患者发热得到控制,但出现血小板减少、转氨酶升高和乳酸酸中毒,停用利奈唑胺、并积极对症治疗后,患者上述指标迅速改善,随访1年余,病情无反复。特将此例患者的诊治与随访情况报道如下,并进行相关文献复习。
1 病例资料
患者,男,24岁,主因“反复双下肢水肿2.5年,腹泻4个月,喘憋伴发热2d”于2010年12月21日入院。2008年8月,患者曾因“反复双下肢水肿”在我院就诊,化验血白蛋白15~20 g/L,24 h尿蛋白8~15 g/d,肌酐110 μmol/L 左右,诊断为肾病综合征,行肾活检病理示局灶增生性IgA肾病,给予激素及免疫抑制剂,效果不佳。2010年10月前患者门诊复诊,血肌酐波动在100~140 μmol/L,尿蛋白7~10 g/d。2010年10月后未再复诊。患者入院前2d无诱因出现喘憋,夜间不能平卧,咳粉红色泡沫痰,急诊收入病房。患者否认发热,无腰痛,睡眠尚可,食欲差,稀水样便,每天10余次,尿量减少至100~200 mL/d,未测体重。入院查体:体温37.8℃,脉搏112次/min,呼吸24次/min,血压125/80 mmHg。端坐位,神志清楚,精神差,颜面部水肿,口唇及结膜苍白,双肺呼吸音粗,双肺底可闻及散在湿啰音,心率112次/min,律齐,心尖部可闻及收缩期2~3/6级杂音,腹软,肝脾肋下未及,全腹无压痛、反跳痛,肠鸣音正常(4次/min),双下肢重度对称性凹陷性水肿。入院后检查:血常规:白细胞14.65×109/L,中性粒细胞86.09%,血红蛋白62.4 g/L,血小板599×109/L。感染相关性检查:细小病毒、巨细胞病毒、嗜肺军团菌、肺炎支原体、肺炎衣原体检查均 阴 性。ESR 146mm/h,C 反 应 蛋 白120 mg/L,PCT(降钙素原)>10 ng/mL,真菌d-葡聚糖检测:<5 pg/mL,肥达氏反应、布氏杆菌凝集试验:阴性,多次查血、尿、便培养、深静脉置管管端培养、痰培养均为阴性。免疫相关性检查未见阳性发现。铁蛋白:399.8~955.6 ng/mL(13~400 ng/mL)。多次行胸片、肺CT检查示:双肺渗出性改变,考虑肺水肿,伴感染不除外,双侧大量胸腔积液,心影增大。腹部CT:未见感染灶。3次经胸超声心动图、1次经食道超声心动图(阜外医院):未见赘生物。患者入院血肌酐1 110 μmol/L,合并心衰,遂给予规律床旁血滤治疗,心衰症状明显好转。患者入院时即有发热,先后应用多种抗生素效果不佳,患者免疫抑制状态,发热使用多种抗生素无效,不能除外耐药菌株,遂联用拜复乐400 mg(1次/d)及利奈唑胺注射液(斯沃)计11d(2011年2月12-23日),患者用药6d体温降至正常范围,用药第7天(2月18日)复查肝功能正常,谷丙转氨酶(ALT)5 U/L,谷草转氨酶(AST)18 U/L,但25日复查ALT 1 580 U/L,AST 1 969 U/L(肝功能情况见图1)。凝血分析:PTA 31%,患者同时出现血小板减少(血小板变化情况见图2),乳酸酸中毒,乳酸最高7.4 mmol/L。考虑为利奈唑胺不良反应。给予保肝、支持治疗后,患者转氨酶降至正常范围,血小板恢复正常,乳酸酸中毒纠正。患者一般情况稳定,准予出院。院外规律血液透析,随访1年余,患者目前一般情况好,血小板、肝功能在正常范围。
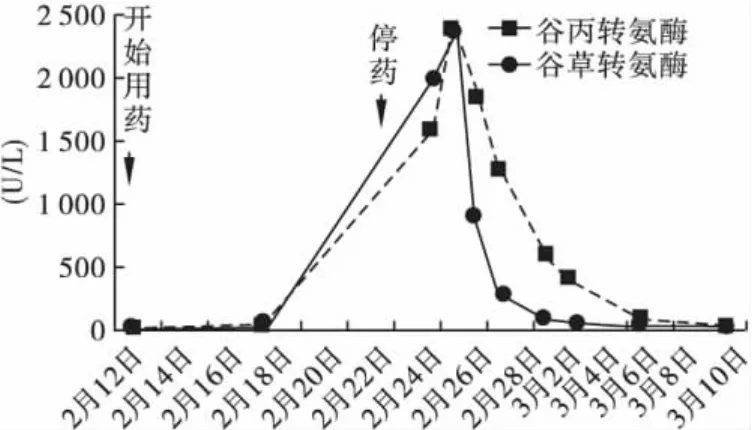
图1 患者肝功能变化情况
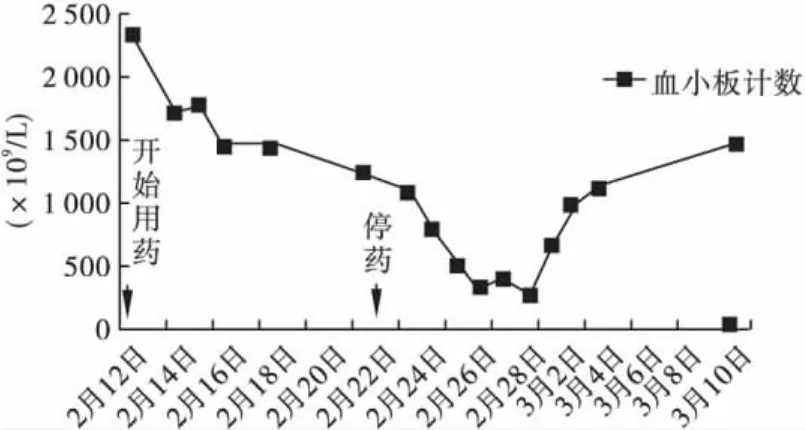
图2 患者血小板变化趋势
2 讨论
CKD是世界范围内的公共健康问题。研究表明,30岁以上人群CKD患病率为7.2%,而64岁以上人群CKD患病率则高达23.4%~35.8%[3]。且CKD患病率仍在不断升高,ESRD患者亦逐年增多[4-9]。心血管疾病和感染是导致ESRD患者死亡的两大主因,感染不仅通过直接途径增加患者死亡率,同时还因为激活炎症,间接增加患者死亡风险[10-11]。由于CKD患者本身即存在不同程度的免疫缺陷:尿毒症毒素影响、缺乏某些细胞因子、继发性甲状旁腺功能亢进症、血液透析使用生物相容性差的膜材料,这些都可能导致免疫抑制[12]。治疗过程中使用激素、免疫抑制剂等药物,使CKD患者尤其是ESRD患者感染发生率较一般人群明显增高,感染情况可能更为复杂。
利奈唑胺主要与细菌50S亚基上核糖体RNA的23S位点结合,阻止形成70S始动复合物,从而抑制细菌蛋白质的合成,发挥抑菌作用,与其他抑制蛋白合成的抗菌药物无交叉耐药性,体外也不易诱导产生耐药性,对MRSA、耐万古霉素肠球菌(VRE)、多重耐药肺炎链球菌(MDRSP)等有强大的抗菌活性。有报道,利奈唑胺可以有效治疗感染性心内膜炎、结核和厌氧菌感染[1-2,13]。其血浆蛋白结合率约为30%。主要由肝脏代谢(50%~70%),但不通过人体细胞色素P450酶代谢,也不抑制人体细胞色素同工酶(1A2、2C9、2C19、2D6、2El、3A4)的活性。利奈唑胺因其药理作用独特、适用人群多样(老年、肾功能不全、轻至中度肝功能不全患者用药时无需调整剂量),在临床的应用日益广泛。
随着利奈唑胺用药日益广泛,其不良反应也越来越受到关注。早期,利奈唑胺Ⅲ期临床试验结果表明,应用利奈唑胺的患者药物相关的不良反应发生率显著高于对照药物组,但严重的药物不良反应发生率相似,因不良反应导致停药几率以及死亡风险亦相似,只是应用利奈唑胺患者的胃肠道不良反应发生率高于对照药物组[14]。利奈唑胺不良反应包括:①血液系统:血栓性血小板减少症、贫血或全血细胞减少。Kuter等[15]研究表明,这3种不良反应的发生率分别为:血栓性血小板减少症1/1 700,贫血1/2 900,全血细胞减少1/6 000。尽管利奈唑胺血液系统不良反应发生率与对照药物相似,但在长疗程治疗(如用药超过14d)的患者中,血液系统不良反应发生率显著提高[16]。Birmingham 等[17]研究表明,治疗≤14d的患者血液系统不良反应发生率为1.9%,治疗15~28d的患者发生率约为5.1%,而治疗>28d者发生率则高达7.4%。用药超过2周后,贫血、血小板减少和白细胞减少的发生率分别为9%、4.1%、4.7%[18]。②神经病变:包括周围神经病变和视神经病变,多与用药时间长(超过最长推荐疗程28d)有关。③肝酶异常:谷丙转氨酶(ALT)、谷草转氨酶(AST)、γ-谷胺酰转移酶、胆红素升高等[15,24-25]。研究表明,ALT、AST 升高发生率不高于对照药物(分别为ALT:7.4%vs.7.2%;AST:4.1%vs.5.3%)[15]。④乳酸酸中毒[26-31]:患者可以出现恶心、呕吐等症状,也可以完全无症状。
本例患者肾功能受损,应用利奈唑胺共计11d,出现了严重的肝损伤、单纯血小板下降(临床上没有血栓证据)、乳酸酸中毒3种不良反应。利奈唑胺治疗时间未超过推荐的14d。查阅文献发现,肾功能已经受损的患者应用利奈唑胺的不良反应发生率较一般人群高,尤其是血液系统相关的不良反应[32-35]。Vincent等对患有G+细菌感染的ESRD人群和非ESRD人群应用利奈唑胺的有效性和安全性进行了前瞻性随机对照研究,发现非ESRD组患者血栓性血小板减少症的发生率为42.9%,而ESRD组患者的发生率高达78.6%。回归分析显示,ESRD为发生利奈唑胺相关的血栓性血小板减少症的独立危险因素。另外,国内亦有研究显示,肾功能不全是利奈唑胺致血小板减少风险增加的重要因素[36]。研究表明,利奈唑胺进入人体后,通过肾脏途径和非肾途径排泄,约30%的药物以原型从肾脏直接排出[37]。单次给药后,利奈唑胺及其代谢产物通过非肾途径可以完全排出;重复给药时,利奈唑胺蓄积,其非肾途径排泄能力饱和,此时肾脏排泄能力对于药物排泄至关重要。在肾功能受损患者中,利奈唑胺血药浓度升高[38]。最近,日本有学者在人群中对利奈唑胺进行大样本的药代动力学和药效动力学研究[39],通过模型模拟发现,对于肾功能不全的患者(肌酐清除率Ccr 10~30 mL/min),使用利奈唑胺1 200 mg/d,疗程为14d时,患者发生血栓性血小板减少症的风险达32.6%~51%。根据AUC/MIC,研究者认为,对于这部分患者,减量使用利奈唑胺(600 mg/d)安全有效。而对于严重肾功能不全者(Ccr<10 mL/min),即使给予600 mg/d剂量,发生血栓性血小板减少症的风险仍然很高。对于利奈唑胺相关的血栓性血小板减少症的发生机制,有研究表明,血栓性血小板减少症的患者骨髓中有足够数量的巨核细胞,因而推断血小板减少与骨髓抑制无关[40-41]。有研究发现,静点丙种球蛋白可以改善患者病情,进而推断其或许与免疫介导有关[41]。日本的研究则表明,利奈唑胺相关的血栓性血小板减少症除与利奈唑胺暴露有关外,与患者易感性也密切相关[39]。
另外,如果同一个患者发生多种不良反应,在病程上,多种不良反应发生发展较为一致,如本例患者的肝损伤和血小板减少进展较为平行。同时,还提示临床上即使患者血小板计数仍在正常范围,一旦出现持续下降趋势,医务人员即应给予足够重视,患者可能已经出现药物不良反应,需要密切监测。
综上所述,CKD(尤其是合并肾功能受损)患者应用利奈唑胺并不安全,即使利奈唑胺在推荐疗程内,也有发生各种不良反应的风险。利奈唑胺在CKD患者中使用的安全性和耐受性低于一般人群,其安全性和耐受性需要临床进一步验证,肾功能受损患者减量使用利奈唑胺同样安全有效的观点也需要临床进一步验证。建议在CKD(尤其是肾功能受损)患者中使用利奈唑胺时,应密切观察患者临床症状,增加肝脏功能、血细胞计数和血乳酸的监测频率,以便早期发现药物不良反应。
[1]Gary French.Safety and tolerability of linezolid[J].Journal of Antimicrobial Chemotherapy,2003,51(Suppl):45-53.
[2]曲俊兵.利奈唑胺的研究进展[J].中国药业,2010,19(1):60-61.
[3]Zhang QL,Rothenbacherd.Prevalence of chronic kidney disease in population-based studies:Systematic review[J].BMC Public Health,2008,8:117.
[4]National Kidney Foundation.K/DOQI clinical practice guidelines for chronic kidney disease:evaluation,classification,and stratification[J].Am J Kidney Dis,2002,39:S1.
[5]Coresh J,Selvin E,Stevens LA,et al.Prevalence of chronic kidney disease in the United States[J].JAMA,2007,298:2038-2047.
[6]Obrador GT,Pereira BJ,Kausz AT.Chronic kidney disease in the United States:an underrecognized problem[J].Semin Nephrol,2002,22:441.
[7]Chadban SJ,Briganti E,Kerr PG,et al.Prevalence of kidney damage in australian adults:the aus diab kidney study[J].J Am Soc Nephrol,2003,14:S131-S138.
[8]Imai E,Horio M,Iseki K,et al.Prevalence of chronic kidney disease(CKD)in the Japanese general population predicted by the MDRD equation modified by a Japanese coefficient[J].Clin Exp Nephrol,2007,11:156-163.
[9]Zhang L,Zhang P,Wang F,et al.Prevalence and factors associated with CKD:A population study from Beijing[J].Am J Kidney Dis,2008,51:373-384.
[10]Ishani A,Collins AJ,Herzog CA,et al.Septicemia,access and cardiovascular disease in dialysis patients:The USRDS Wave 2 study[J].Kidney Int,2005,68:311-318.
[11]Rocco MV,Yan G,Gassman J,et al.Comparison of causes of death using HEMO Study and HCFA end-stage renal disease death notification classification systems.The National Institutes of Health-funded Hemodialysis.Health Care Financing Administration[J].Am J Kidney Dis,2002,39(1):146-153.
[12]Verkade MA,Van Druningen CJ,Vaessen LM,et al.Functional impairment of monocyte-derived dendritic cells in patients with severe chronic kidney disease[J].Nephrol Dial Transplant,2007,22(1):128-138.
[13]唐神结,肖和平.利奈唑胺抗结核作用的研究及其最新进展[J].中华临床医师杂志(电子版),2010,4(1):54-57.
[14]Rubinstein E,Isturiz R,Standiford HC,et al.Worldwide assessment of linezolid's clinical safety and tolerability:comparator-controlled phase III studies[J].Antimicrob Agents Chemother,2003,47:1824-1831.
[15]Kuter DJ,Tillotson GS.Hematologic effects of antimicrobials:focus on the oxazolidinone linezolid[J].Pharmacotherapy,2001,21(8):1010-1013.
[16]Gerson SL,Kaplan SL,Bruss JB,et al.Hematologiceffectsoflinezolid:summary of clinical experience[J].Antimicrob A-gents Chemother,2002,46(8):2723-2726.
[17]Birmingham MC,Rayner CR,Meagher AK,et al.Linezolid for the treatment of multidrug-resistant,Gram-positive infections:experience from a compassionate-use program[J].Clin Infect Dis,2003,36:159-168.
[18]Bemstein WB,Trotta RF,Rector JT,et a1.Mechanisms for linezolid-induced anemia and thromboeytopenia[J].Ann Pharm,2003,37(4):517-520.
[19]Bressler AM,Zimmer SM,Gilmore JL,et al.Peripheral neuropathy associated with prolonged use of linezolid[J].Lancet Infect Dis,2004,4:528-531.
[20]Legout L,Senneville E,Gomel JJ,et al.Linezolid-induced neuropathy[J].Clin Infect Dis,2004,38:767-768.
[21]Rho JP,Sia IG,Crum BA,et al.Linezolid-associated peripheral neuropathy[J].Mayo Clin Proc,2004,79:927-930.
[22]Zivkovic SA,Lacomisd.Severe sensory neuropathy associated with long-term linezolid use[J].Neurology,2005,64:926-927.
[23]Ferry T,Ponceau B,Simon M,et al.Possibly linezolid-induced peripheral and central neurotoxicity:report of four cases[J].Infection,2005,33:151-154.
[24]Gould FK.Linezolid:safety and efficacy in special populations[J].J Antimicrob Chemother,2011,66(Suppl 4):3-6.
[25]Jauregui LE,Babazadeh S,Seltzer E,et al.Randomized,double-blind comparison of once-weekly dalbavancin versus twicedaily linezolid therapy for the treatment of complicated skin and skin structure infections[J].Clin Infect Dis,2005,41:1407-1415.
[26]Pea F,Scudeller L,Lugano M,et al.Hyperlactacidemia potentially due to linezolid overexposure in a liver transplant recipient[J].Clin Infect Dis,2006,42:434-35.
[27]Kopterides P,Papadomichelakis E,Armaganidis A.Linezolid use associated with lactic acidosis[J].Scand J Infect Dis,2005,37:153-154.
[28]Palenzuela L,Hahn NM,Nelson RP Jr,et al.Does linezolid cause lactic acidosis by inhibiting mitochondrial protein synthesis[J].Clin Infect Dis,2005,40(12):113-116.
[29]Soriano A,Miro O,Mensa J.Mitochondrial toxicity associated with linezolid[J].N Engl J Med,2005,353:2305-2306.
[30]Wiener M,Guo Y,Patel G,et al.Lactic acidosis after treatment with linezolid[J].Infection,2007,35:278-281.
[31]Scotton P,Fuser R,Torresan S,et al.Early linezolid-associated lactic acidosis in a patient treated for tuberculous spondylodiscitis[J].Infection,2008,36:387-388.
[32]Wu VC,Wang YT,Wang CY.High frequency of linezolid-associated thrombocytopenia and anemia among patients with end-stage renal disease[J].Clinical Infectious Diseases,2006,42:66-72.
[33]Lin YH,Wu VC,Tsai IJ.High frequency of linezolid-associated thrombocytopenia among patients with renal insufficiency[J].Int J Antimicrob Agents,2006,28(4):345-351.
[34]Matsumoto K,Takeda Y,Takeshita A,et al.Renal function as a predictor of linezolid-induced thrombocytopenia[J].Int J Antimicrob Agents,2009,33(1):98-99.
[35]Soriano A,Ortega M,García S,et al.Comparative study of the effect of pyridoxine,rifampin,and renal function on hematological adverse events induced by linezolid[J].Antimicrob A-gents Chemother,2007,51(7):2559-2563.
[36]王海燕,崔杰,候莉,等.静脉注射利奈唑胺致血小板减少的相关因素分析[J].中国药物应用与监测,2010,7(5):266-268.
[37]陈东红,张旭华,吴立华,等.利奈唑胺治疗重症肺炎的临床疗效及安全性研究[J].实用药物与临床,2011,14(5):376-379.
[38]Tsuji Y,Hiraki Y,Matsumoto K,et al.Thrombocytopenia and anemia caused by a persistent high linezolid concentration in patients with renal dysfunction[J].J Infect Chemother,2011,17(1):70-75.
[39]Sasaki T,Takane H,Ogawa K,et al.Population pharmacokinetic and pharmacodynamic analysis of linezolid and a hematologic side effect,thrombocytopenia,in Japanese patients[J].Antimicrob Agents Chemother,2011,55(5):1867-1873.
[40]Ebeling F,Helminen P,Anttila VJ.Appearance of ring sideroblasts in bone marrow during linezolid therapy[J].Scand J Infect Dis,2009,41(6-7):480-482.
[41]Bernstein WB,Trotta RF,Rector JT,et al.Mechanisms for linezolid-induced anemia and thrombocytopenia[J].Ann Pharmacother,2003,37(4):517-520.

