新型β-环糊精交联聚合物的合成及其对儿茶素的吸附
王恩举,尚彦菁,张 利
(海南师范大学 化学与化工学院,海南 海口 571158)
具有包合功能的β-环糊精(β-CD)是目前应用最广泛的超分子主体化合物.β-CD分子中含有多达21个羟基,其中葡萄糖单元2位和6位的共14个羟基,具有较高的反应活性,可以与双官能团或多官能团羟基交联剂反应,使β-CD形成交合聚合物(β-CDP).在聚合物中β-CD具有与游离态相似的包络性能,而且β-CDP中相邻的环糊精单元之间具有协同效应,从而使其对一些大体积分子的包络能力远远大于游离的β-CD[1].环氧氯丙烷[2],乙二醇二缩水甘油醚[3],二异氰酸酯[4],柠檬酸[5]等都可以作为β-CD的交联剂,其中研究最多、使用最广的是环氧氯丙烷.β-CD与环氧氯丙烷一般在在碱水介质中反应得到β-CDP[5],但在碱水中环氧基易与氢氧根离子发生开环反应,产物中可能存在大量的环糊精甘油醚,而且产品的性状对反应时间,碱的浓度、环氧氯丙烷的用量和滴加速度等因素非常敏感.本文首次在非水介质中合成了环氧氯丙烷交联的β-CDP,避免了环氧基与OH-的副反应.并将其应用于绿茶提取物脱咖啡因研究,结果显示所合成的β-CDP对儿茶素类物质、尤其是表没食子儿茶素没食子酸酯有较强的选择性,对咖啡因几乎不吸附.
1 实验部分
1.1 仪器与试剂
三用紫外线分析暗箱(武汉药科新技术开发有限公司);Nexus-470型傅里叶变换红外光谱仪(美国Nicolet公司).
硅胶GF254薄层层析预制板(青岛海洋化工厂);β-环糊精(98%,北京奥博星生物技术有限公司,使用前110℃干燥3小时);环氧氯丙烷(阿拉丁公司);碳酸钾(广州化学试剂厂);N,N-二甲基甲酰胺(DMF,国药集团化学试剂有限公司,使用前用分子筛干燥,然后减压蒸馏收集76℃/36 mmHg的馏分);绿茶(产地:五指山);所用试剂均为市售分析纯.
1.2 β-CD交联聚合物(β-CDP)的合成
将干燥的β-CD(11.4 g)溶解于无水DMF(30 mL)中,加入无水碳酸钾(18 g),常温搅拌30 min,升温到100℃,充分搅拌下慢慢滴入环氧氯丙烷(9 g,溶于10 mL DMF中),滴加过程约需40 min,加完后,升温至120℃继续剧烈搅拌反应30 min,冷却至室温,抽滤,用大量水和丙酮交替洗涤产品,50℃真空干燥得浅灰色固体10 g.研细过筛.
1.3 β-CDP对绿茶提取物的吸附
绿茶末(1 g)加55%的乙醇(20 mL),室温(28℃)搅拌2 h,抽滤,滤液减压浓缩至无醇味,加适量水使成澄清溶液,总体积为10 mL.
β-CDP(10 g)用水溶胀3 h,超声除去气泡,装入内径为2 cm的玻璃柱中,从柱顶均匀加入绿茶提取物水溶液(5 mL),依次用水,不同浓度的乙醇(20%,40%,50%,60%,70%,80%)梯度洗脱.硅胶薄层检验各洗脱液,展开剂:V(氯仿)∶V(丙酮)∶V(甲酸)=5∶4∶1.
2 结果与讨论
2.1 β-CDP的合成
环氧氯丙烷交联β-CDP的合成一般在碱水介质中进行,但在碱水中环氧基可以发生许多副反应.由于环氧基的水解,环氧氯丙烷需要过量许多倍,更重要的是环氧基β-CD可以水解生成大量的β-CD甘油醚(1),β-CD甘油醚还可以继续反应生成更长链的甘油醚(2)或通过一个长的甘油醚链连接两个β-CD分子(3),碱的浓度、β-CD的浓度,温度、环氧氯丙烷的用量和滴加速度等因素都会影响这些副反应[7].相关反应如图1所示.

图1 相关反应方程式Fig.1 Related reaction equation
文献曾在水相条件下合成了β-CDP[6],聚合产品大量吸水后呈凝胶状,作为色谱固定相流速太慢.聚合物中大量的甘油醚基、以及β-CD间较长的甘油醚连接臂可能是导致β-CDP吸水溶胀率特别大的原因[8].为了得到有较小的吸水溶胀率、结构均匀、适合作为色谱固定相的β-CDP,本文在非水介质合成了一种新的β-CDP,在本方法中能与环氧基发生开环反应的官能团只有环糊精的羟基,避免了在水介质中的的副反应.合成产物的吸水性适中,作为色谱固定相流速适中(比微晶纤维素稍慢),具有很好的应用前景.
2.2 红外光谱
采用KBr压片法测定了两种方法合成的β-CDP及β-CD的红外光谱(见图2),β-CD分子的2位O—H和3位O—H间存在较强的氢键作用,这些氢键在β-CD大口端形成一个闭合的大环,在两种β-CDP中氢键的闭合大环结构被破坏,氢键作用减弱,因此,两种β-CDP在3400 cm-1附近的O—H伸缩振动吸收比β-CD更加尖锐且吸收强度更大.水相中合成的β-CDP具有较多的亚甲基(CH2),因此在谱图b中相应于CH2在2850 cm-1附近的对称伸缩振动和1500~1600 cm-1的弯曲振动最强,β-CD中的亚甲基最少,相应在这两个位置的吸收最弱.三个谱图在1000~1050 cm-1都有强吸收,归属为C—O伸缩振动,在β-CD中主要为醇的C—O,醚的O—C—O较少,而在β-CDP中O—C—O数量相对增多,O—C—O有对称和不对称两种伸缩振动,二者与醇C—O振动吸收叠合使1000 cm-1附近的吸收峰变宽、变钝,精细结构消失,这种变化在谱图b中表现的更明显,这与我们关于反应机理的分析一致.但三者的主要结构单元都是吡喃型葡萄糖,引起红外吸收的官能团基本相同,这使它们的主要吸收峰也基本相同.
2.3 β-CDP对绿茶提取物的选择性吸附性能

图2 红外光谱:(a)本文合成的β-CDP;(b)水相中合成的β-CDP[6];(c)β-CDFig.2 FT-IR spectra:(a)β-CDP obtained in nonaqueous medium;(b)β-CDP obtained in aqueous medium[6];(c)β-CD
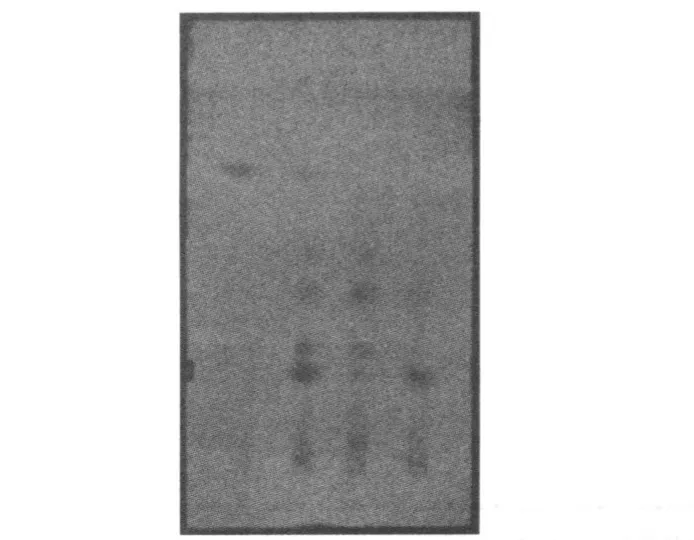
图3 β-CDP乙醇洗脱液的TLC照片Fig.3 TLC photograph of ethanol elutions of β-CDP
在实验条件下,β-CDP不吸附咖啡因,咖啡因可以被水快速洗脱下来.但能很好地吸附儿茶素类多酚,而且对不同的儿茶素多酚表现出一定的选择性.当洗脱剂乙醇的浓度小于40%时,几乎没有多酚类物质被洗下来.50%的乙醇对非酯型儿茶素的洗脱较好,随着乙醇浓度的增加,洗脱液中酯型儿茶素的比例逐渐增加.70%乙醇洗脱得到的是纯度很高的表没食子儿茶素茶没食子酸酯(EGCg),80%的乙醇中已经没有多酚类物质.图3为梯度乙醇洗脱液的薄层色谱照片,从左向右依次分别为:水洗脱物、绿茶提取物对照品、50%乙醇洗脱液、70%乙醇洗脱液.粗提物对照品斑点由上向下依次为:咖啡因、表儿茶素(EC)、表没食子儿茶素(EGC)、表儿茶素没食子酸酯(ECg)、表没食子儿茶素茶没食子酸酯(EGCg).绿茶提取物中酯型儿茶素和咖啡因的含量较高,尤其是EGCg的含量最高.水洗脱液中只有咖啡因,在50%的乙醇洗脱液中虽然4种儿茶素类物质的含量相差不大,但相对粗提物而言,非酯型儿茶素得到了富集,粗提物中含量最高的EGCg在50%的乙醇洗脱液中却非常少.70%乙醇洗脱液中基本上只有EGCg.
文献曾研究过在碱水体系中合成的β-CDP对绿茶提取物的静态吸附性能[6],本文所合成的β-CDP对两类儿茶素(酯型和非酯型儿茶素)的选择性明显高于前者.这可能与二者的微孔结构有关,也可能是由于色谱洗脱法优于静态吸附法.
3 结论
在非水介质中合成了一种新型的β-CD交联聚合物,与传统的碱水介质合成法相比,本合成法避免了由于环氧乙基易开环引起的副反应,得到的β-CDP吸水性适中,特别适合作为柱色谱固定相.对绿茶提取物的吸附研究表明,β-CDP能从绿茶提取物中选择性吸附儿茶素类多酚,不吸附咖啡因,而且表现出了对EGCg的特殊高选择性.因此,本文所合成的β-CDP不但可以用于绿茶提取物脱咖啡因,而且可以用于纯化EGCg单体.
[1]王永健,张政朴,何炳林.环糊精聚合物的高分子效应[J].化学进展,2000,12(3):318-324.
[2]黄怡,郭金婵,王晓芳,等.β-环糊精微球对染料分子吸附作用研究[J].化学研究与应用,2009,21(10):1392-1396.
[3]李英杰,张文治,韩家军.烷基二环氧甘油醚交联剂制备β-环糊精聚合物及其应用的研究[J].分子科学学报,2001,17(2):105-108.
[4]黄娟,周玉青,韩萍芳,等.二苯基甲烷二异氰酸酯改性β-环糊精吸附性能[J].化学工程,2011,39(9):6-10.
[5]Zhao D,Zhao L,Zhu C S,et al.Water-insoluble β-cyclodextrin polymer crosslinked by citric acid:synthesis and adsorption properties toward phenol and methylene blue[J].J Incl Phenom Macrocycl Chem,2009,63(3):195-201.
[6]尚彦菁,赵铭春,张利,等.β-环糊精聚合物的合成及其对儿茶素的吸附[J].海南师范大学学报,2012,25(2):191-193.
[7]王齐放,李三鸣,张予阳,等.通过交联度控制β-环糊精聚合物对药物的载入与释放[J].药学学报,2011,46(2):221-226.
[8]刘郁杨,范晓东,曹哲.β-环糊精/环氧氯丙烷水凝胶中水的存在状态及其溶胀特性[J].功能高分子学报,2001,14(2):169-173.

