(Z)-2-(2-叔丁氧羰氨基噻唑-4-基)-2-戊烯酸的合成
孙 会 汪祝胜 潘镇浩 全嘉铭 裴 文*
(1.浙江工业大学化学工程与材料学院,杭州 310014;2.浙江华方药业有限责任公司,浙江,台州 318000)
化合物(Z)-2-(2-叔丁氧羰氨基噻唑-4-基)-2-戊烯酸是合成头孢卡品酯的关键中间体。头孢卡品酯化学名为7-[2-(2-氨基-1,3-噻唑-4-基)戊-3-烯酰胺基]-3-氨基甲酰氧甲基-8-氧代-5-硫-1-氮杂双环[4.2.0]辛-2-烯-2-甲酸 2,2-二甲基丙酰氧甲基酯盐,由日本盐野义制药株式会社开发。头孢卡品酯是第4代可口服头孢类抗生素。药理研究结果表明,头孢卡品酯较现有口服的头孢品种相比抗菌活性强,剂量小的特点。因此,深入研究头孢卡品酯关键中间体(Z)-2-(2-叔丁氧羰氨基噻唑-4-基)-2-戊烯酸化合物的合成方法,有着重要的学术意义和广阔的应用前景[1-2]。
目前,关于(Z)-2-(2-叔丁氧羰氨基噻唑-4-基)-2-戊烯酸的合成路线主要是以4-氯乙酰乙酸乙酯为原料,先后与硫脲、丙醛反应成环,然后用碳酸二叔丁酯保护氨基,再进行水解制得[3-5]。但4-氯乙酰乙酸乙酯与硫脲关环时活性低,产物收率难以提高;如果直接使用4-溴乙酰乙酸乙酯进行反应,虽然反应物活性增加了,但是原料的成本较高,而且在2缩合反应中副产物也增加。另外,在2缩合反应中,文献报道都是使用无机碱和有机碱进行催化,产物收率较低,色泽不好,纯度不高。
因此,笔者等利用4-氯乙酰乙酸乙酯与丙醛进行第1步缩合反应,然后利用卤素交换反应,用溴化钠将氯原子取代制得溴代中间物,然后再与硫脲进行关环;在缩合反应中,利用氧化镁和三氧化二铝为催化剂,高收率和高纯度地制得了目标产物。
1 实验部分
1.1 仪器及试剂
WRS-1A数字熔点测定仪(温度计未经校正),Mercury Plus(400 MHz)型核磁共振仪(CDCl3为溶剂,四甲基硅烷TMS为内标),TSQ Quantum LC-MS型质谱仪;RE-52A型旋转蒸发器,85-1型磁力搅拌器,SHZ-3型循环水式真空泵,等。
试剂均为市购化学纯。
1.2 2-溴乙酰基丁烯酸乙酯的合成
在250 mL三口烧瓶中加入二氯甲烷100 mL、4-氯乙酰乙酸乙酯 16.5 g(0.1 mol)、丙醛 6.4 g(0.11 mol)、冰乙酸 0.5 g(0.08 mol),降温到-55 ℃,加入哌啶 0.5 g,控温-55~-50℃反应 5 h,加入到 100 mL稀盐酸搅拌0.5 h,分层;分出的有机层质量分数用1%的氢氧化钠洗涤,分层;分出的有机层,用无水硫酸钠干燥,抽滤,滤液加入溴化钠15.5 g(0.15 mol)、二甲基乙酰胺50 mL,在室温下搅拌反应,TLC薄层色谱跟踪检测至原料点消失,反应5 h。然后加入质量分数5%的稀盐酸洗涤,分出有机层,水层用少量二氯甲烷萃取,合并有机层,减压蒸除有机溶剂,得到黄色液体24.1 g,收率96.8%。
1.3 2-(2′-氨基噻唑-4-基)戊烯酸乙酯的合成
在250 mL三口烧瓶中加入2-溴乙酰基丁烯酸乙酯24.9 g(0.1 mol)、二氯甲烷 100 mL,降温至-10℃,加入溶有硫脲8 g(0.105 mol)的二甲基乙酰胺50 mL,TLC薄层色谱跟踪检测至原料点消失,反应1 h。分别用质量分数10%的稀碱溶液和饱和食盐水洗涤,用无水硫酸钠干燥,抽滤,减压蒸除溶剂,得到棕色油状物20.8 g,收率91.9%。
1.4 2-(2′-叔丁氧硫酰氨唑-4-基)戊烯酸的合成
在150 mL三口烧瓶中加入2-(2′-氨基噻唑-4-基)戊烯酸乙酯 22.6 g(0.1 mol)、二甲基乙酰胺 30 mL,在室温搅拌下,慢慢滴加碳酸二叔丁酯19 g(0.11 mol),TLC薄层色谱跟踪检测至原料点消失,反应6 h。然后加入质量分数5%的氢氧化钠溶液100 mL,TLC薄层色谱跟踪检测,在65℃水解6 h。冰盐浴冷却下,用盐酸调pH为3~4,放置析出固体,过滤,水洗,得产物22.3 g,收率75%。
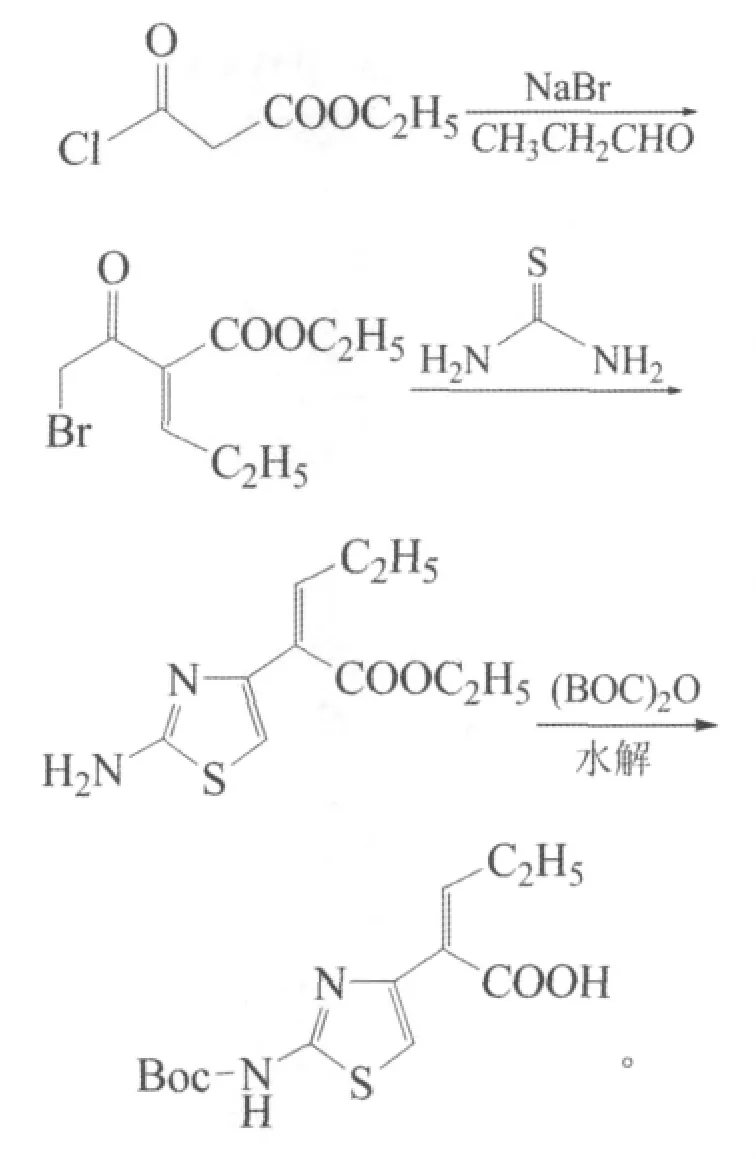
反应式如下:
产物熔点 159~161 ℃(分解)。1H-NMR(DMSO-d6,δ):0.97(t,3H),1.45(s,9H),2.18(m,2H),6.69(m,1H),6.84(s,1H);13C-NMR(DMSO-d6,δ):13.89,22.66,28.71,80.75,111.0,131.1,143.2,145.7,152.5,158.2,168.9;IR(KBr)ν:3 433、3 187、2 975、2 933、1 720、1 682、1 553、1 455、1 369、1 289、1 245、1 159、1 074、874、769、716 cm-1;MS m/z:298[M+]。
2 结果与讨论
2.1 2-溴乙酰基丁烯酸乙酯的合成
如果直接以4-氯乙酰乙酸乙酯为起始原料与丙醛进行缩合,再与硫脲进行闭环反应,氯原子活性较小,反应收率难以提高;如果利用溴代乙酰乙酸乙酯为起始原料,从工业化的角度,成本高,原料难以获得。在实验中发现,也产生许多杂质。
因此,通过反应机理分析认为,在4-氯乙酰乙酸乙酯与丙醛反应时,首先是4-氯乙酰乙酸乙酯的亚甲基生成碳负离子,然后与丙醛发生亲核加成消除反应,该反应中应有顺、反2种异构体的存在。而且实验结果表明,4-氯乙酰乙酸乙酯与丙醛的反应时,反应温度和时间对反式体的产生影响较大(见表1)。

表1 反应温度、时间对E体生成的影响Tab 1 Effect of reaction temperature and time on E type isomer production
当反应生成2-氯乙酰基丁烯酸乙酯后,利用非质子极性溶剂,易于发生卤素交换反应。当利用二甲基乙酰胺进行溴代反应时发现,4-氯乙酰乙酸乙酯与丙醛在二甲基乙酰胺中也很易发生反应。因此,在二甲基乙酰胺溶剂中首先由4-氯乙酰乙酸乙酯与丙醛反应制得2-氯乙酰基丁烯酸乙酯,然后直接与溴化钠进行溴化反应,成功地制得了2-溴乙酰基丁烯酸乙酯(C9H13O3Br)。
2.2 2-(2′-氨基噻唑-4-基)戊烯酸乙酯的合成
在上步反应中,利用控制反应温度和时间减少产物中E体的生成,取得了理想的效果。从操作简便的角度考虑,能否继续使用相同的溶剂进行反应。根据2-溴乙酰基丁烯酸乙酯与硫脲进行闭环反应机理来看,环合时反应温度、时间,对产物E异构体也有比较大的影响,反应温度越高,时间越长,越有利于E异构体的生成(见表2)。

表2 环合时反应温度对E体的影响Tab 2 Effect of cyclization reaction temperature on E type isomer
另外,该步反应中硫脲(CH4N2S)的配比对产物的收率影响显著(如表3)。

表3 硫脲用量对收率的影响Tab 3 Effect of thiourea dosage on yield
实验结果表明,通过反应温度和时间成功地控制了反应中E异构体的生成,通过控制硫脲的配比成功的提高了收率,制得了闭环产物,也证明了分析的正确性。
2.3 2-(2′-叔丁氧硫酰氨唑-4-基)戊烯酸的合成
在氨基的保护和酯基的水解反应中,氨基保护需要在碱的作用下进行反应,酯基的水解也是在传统的碱性条件进行。因此,仍然使用二甲基乙酰胺作为反应溶剂,在氢氧化钠溶液的作用下,氨基的保护和酯基的水解同时进行,即简化了操作,又成功地制得了产物,为今后工业化生产提供了思路。
3 结论
以4-氯乙酰乙酸乙酯为原料,经丙醛缩合、溴化钠进行氯原子交换制得2-溴乙酰基丁烯酸乙酯,然后与硫脲进行取代和加成消除得到2-(2′-氨基噻唑-4-基)戊烯酸乙酯闭环产物,最后在碱性条件下,一步进行碳酸二叔丁酯氨基保护和酯基水解制得目标产物(Z)-2-(2-叔丁氧羰氨基噻唑-4-基)-2-戊烯酸。3步反应总收率达到66.7%,纯度达到99.5%。该方法简单易行、收率高、纯度好,是一条适合工业化生产的合成方法。
[1]夏成才,程冬萍,于文博,等.第四代头孢研究进展及合成综述[J].应用化工,2005,34(3):137-140.
[2]李红梅.头孢类抗生素头孢卡品酯的合成[D].济南:山东大学药学院,2006.
[3]余晓玲.浅谈头孢卡品酯的合成路线选择[J].河北职业技术学院学报,2008,8(4):39-41.
[4]陈言德,赵桂林,金荣庆,等.盐酸头孢匹伏卡品酯的合成[J].化工中间体,2009(10):35-38.
[5]王书涛.头孢卡品酯的合成[J].化学通报,2012,75(4):341-347.

