Pb掺杂对尖晶石型锰酸锂结构和性能的影响
牛莎莎,陈海清,王志兴,蒋光辉
(1.湖南有色金属研究院,湖南长沙 410015;
2.中南大学冶金科学与工程学院,湖南长沙 410083)
Pb掺杂对尖晶石型锰酸锂结构和性能的影响
牛莎莎1,陈海清1,王志兴2,蒋光辉1
(1.湖南有色金属研究院,湖南长沙 410015;
2.中南大学冶金科学与工程学院,湖南长沙 410083)
以电解二氧化锰为锰源,碳酸锂为锂源,硝酸铅为铅源,采用高温固相法在800℃下焙烧24 h合成尖晶石型Li1.05Mn1.95-xPbxO4。系统地研究了掺杂不同量的元素铅对尖晶石锰酸锂结构、形貌以及电化学性能等的影响,结果表明:当Li1.05Mn1.95-xPbxO4中掺杂量x>0.02时,材料的XRD图中出现杂质峰,随着x的增大,锰酸锂的颗粒有团聚趋势;当x=0.02时锰酸锂的循环性能得到一定的改善,锂离子扩散阻抗有所减小,之后随着x增大,Li1.05Mn1.95-xPbxO4的循环性能下降,材料的电化学性能变差。
锂离子电池;锰酸锂;铅;掺杂
锂离子电池是飞速发展的新一代二次电池,随着新能源汽车行业的崛起,锂离子电池市场供不应求,正极材料是制约我国高性能锂离子电池发展的瓶颈[1]。目前,国内市场上的正极材料主要有钴酸锂和镍钴锰三元材料,因钴系材料的成本高,人们逐渐将研究方向转向成本相对低廉、性能优异的正极材料[2]。
我国是锰生产和消费大国,利用锰作为正极材料的来源,则成本大大降低[3]。锰能形成稳定的尖晶石型结构LiMn2O4,理论比容量为148 mAh/g,虽没有钴酸锂的比容量高,但有90%的可逆Li脱嵌率[4]。安全廉价的锰酸锂具有独特的优势成为一种重要的正极材料,已逐步应用在电动车等领域。
尖晶石型锰酸锂的合成方法主要可分为固相法[5]和液相法[6,7]。D.G.Wichham等[8]以Li2CO3和MnO2的混合物为前驱体,在850℃下首次采用高温固相法合成锰酸锂。陈艳芳等[9]利用溶胶凝胶法制得纳米锰酸锂,获得的产物形貌均匀,颗粒细小,首次放电比容量达135 mAh/g。锰酸锂在充放电存储过程中发生Jahn-Teller效应[10],以及活性物质的溶解,导致不可逆容量损失,这是制约尖晶石锰酸锂材料商业化的主要问题。研究者尝试用各种方法对材料进行性能改善,并研究各种元素对锰酸锂性能的影响。Masaru等[11]则采用导电聚苯胺对LiMn2O4材料进行表面包覆,合成的材料在50℃下循环20次后的比容量有110 mAh/g。高农等[12]对锰酸锂分别进行了Ni、Co掺杂,经掺杂后的材料颗粒均匀,50次循环后比容量仍有107.2 mAh/g和103.3 mAh/g。Strobel.P等人[13]对尖晶石LiMn2O4进行氟掺杂,掺杂前后的LiMn2O4的电压平台和充放电曲线特征区别不大,但抑制了材料的高温分解。陈健等[14]研究了Al掺杂对锰酸锂结构及性能的影响,掺杂一定的Al有利于提高材料的电化学性能。本文采用高温固相合成法合成尖晶石型LiMn2O4, Pb为掺杂元素,研究了Pb掺杂对尖晶石型锰酸锂结构、形貌以及电化学性能的影响。
1 实验原料及反应机理分析
1.1 实验原料及反应机理分析
锰源采用电解二氧化锰,二氧化锰的含量约95%,为γ晶型MnO2,含少量结晶水,二氧化锰的SEM图如图1所示。

图1 电解二氧化锰分别在不同倍率下的SEM图
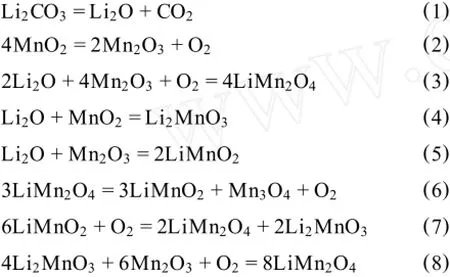
由图1可以看出,锰源电解二氧化锰为类球形,颗粒均匀,粒度在10~20μm之间,在大颗粒表面存在少许细小的小颗粒二氧化锰。MnO2+Li2CO3体系的热重曲线如图2所示。由图2可以看出,在100℃附近发生失重,主要是吸附水的脱除。随着温度升高,材料失重明显,主要是发生Li2CO3分解以及MnO2分解反应,如式(1)、式(2)。在400~450℃,固相反应生成不规则的尖晶石LiMn2O4,如式(3),同时会发生一些副反应,如式(4)、式(5),导致500℃时的中间产物中常含有Li2MnO3、LiMnO2和Mn2O3[15]。当温度为700~850℃,材料的质量基本不变,可见合成尖晶石型LiMn2O4的焙烧温度在此温度范围内较适宜。当温度高于850℃时,LiMn2O4会发生分解,呈现高温不稳定性,发生式(6)的分解反应。分解生成的LiM-nO2在低温下不稳定,在冷却过程中,会继而分解为LiMn2O4和Li2MnO3,生成的Li2MnO3和Mn2O3反应生成LiMn2O4,如式(7)、式(8)[16]。由此可见,实验中不仅需控制焙烧温度,而且在降温时需控制降温速率,才能制备得到标准尖晶石型LiMn2O4。
1.2 实验方法
采用高温固相法制备锂离子电池正极材料锰酸锂。首先称取一定量的前驱体电解二氧化锰和碳酸锂,以硝酸铅为掺杂铅源,按一定比例掺杂一定量的元素铅,混合均匀之后装入烧舟。将烧舟置于马弗炉中,以10℃/min的升温速率升至800℃下焙烧24 h,冷却取出即得到正极材料。将正极材料制备成扣式电池,检测其电化学性能。
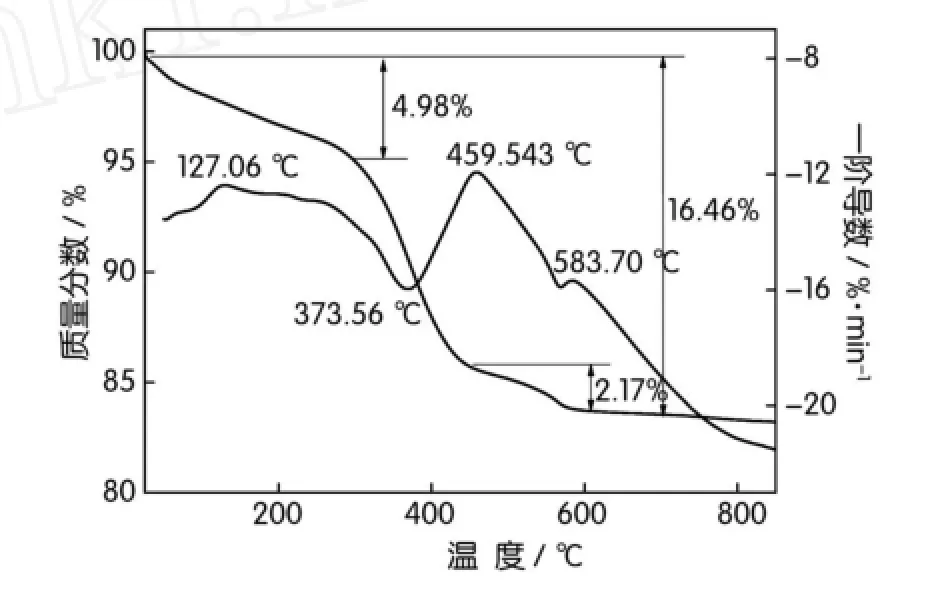
图2 MnO2+Li2CO3体系的热重曲线
1.3 材料的表征
采用J EOL公司的JSM-5600LV Scanning Electron Microscope观察材料表面形貌。利用Neware公司生产的充放电测试系统对电池进行充放电测试,采用CHI660A型电化学工作站对电池进行交流阻抗测试。
2 结果与讨论
2.1 Pb掺杂对锰酸锂的结构的影响
掺杂不同量的元素Pb合成的Li1.05Mn1.95-x-PbxO4的XRD图如图3所示。
由图3可以看出,Li1.05Mn1.95-xPbxO4中掺杂量x≤0.02时,合成的样品的XRD图谱中未发现杂质化合物的衍射峰,可见元素Pb已经掺入尖晶石锰酸锂的晶格之中,形成了有少量Pb替代部分金属阳离子的单相尖晶石型锰酸锂。随着Pb加入量的增加,所合成样品中的各主要衍射峰的强度逐渐减弱,且图谱中出现杂质峰,这说明材料的结晶性变差,材料中各原子的混乱程度增加。
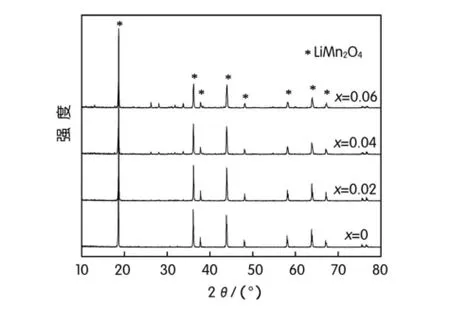
图3 Li1.05Mn1.95-xPbxO4的XRD图
2.2 Pb掺杂对尖晶石锰酸锂形貌的影响
掺杂不同量的元素Pb合成的Li1.05Mn1.95-x-PbxO4的SEM图如图4所示。
由图4中可以看出,随着铅掺杂量的增加,合成的样品的团聚现象逐渐增多,且颗粒变得很不均匀,有很小的颗粒出现,且颗粒的边缘变得圆滑,主要由于随着铅加入量的增加,有部分铅未掺入锰酸锂的晶格内部,成为材料中的杂质物质,材料的团聚现象明显增大,部分铅在高温下被氧化生成氧化铅,生成极细小颗粒,使得颗粒很不均匀。

图4 Li1.05Mn1.95-xPbxO4的SEM图
2.3 Pb掺杂对锰酸锂电化学性能的影响
掺杂不同量的元素Pb合成的锰酸锂的在0.1C倍率首次放电曲线如图5所示。由图5可以看出,曲线上都具有两个平台:位于4.15 V的平台和位于3.95 V左右的平台,这是尖晶石型LiMn2O4所特有的两个平台。随着加入量的增加,首次放电容量有所降低,且位于3.95 V左右的电压平台逐渐有所下降,且3.95 V左右的平台逐渐缩短,这可能是由于铅的掺杂量增加,有一部分的铅未掺入锰酸锂晶格内部形成氧化铅,在材料进行充放电过程中,这些杂质破坏锰酸锂的结构。
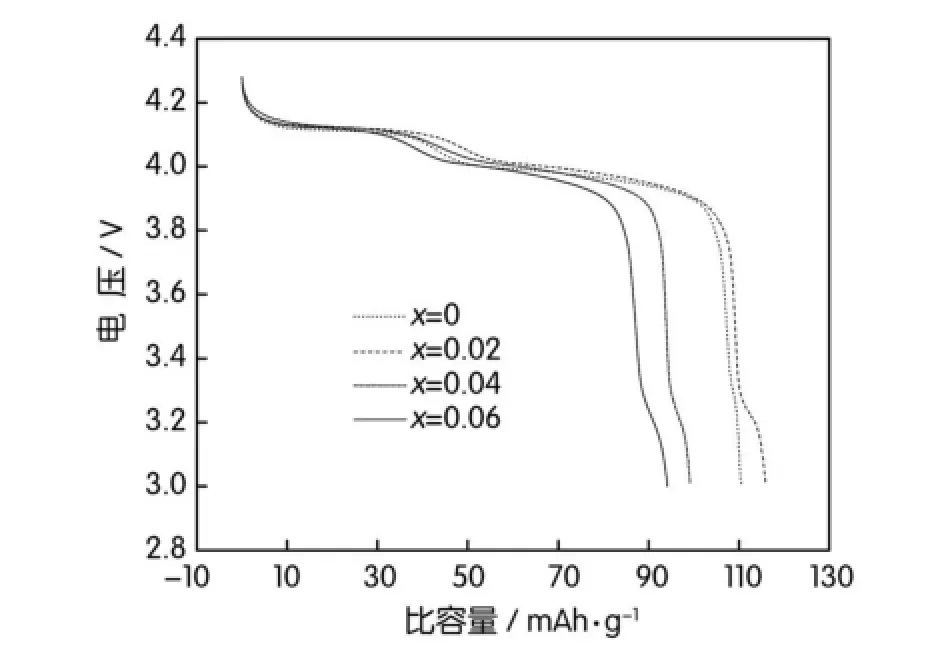
图5 Li1.05Mn1.95-xPbxO4的放电曲线图
掺杂不同量的元素Pb合成的锰酸锂在1.0C倍率下的循环性能图如图6所示。由图6可以看出,当铅掺杂量x=0.02时,锰酸锂的循环性能较未经掺杂的锰酸锂有一定程度的改善,但之后随着铅掺杂量的增大,锰酸锂的循环性能逐渐下降,这主要是因为当掺杂量x>0.02时,锰酸锂的结构被破坏,从而导致材料在充放电过程中可逆容量衰减。
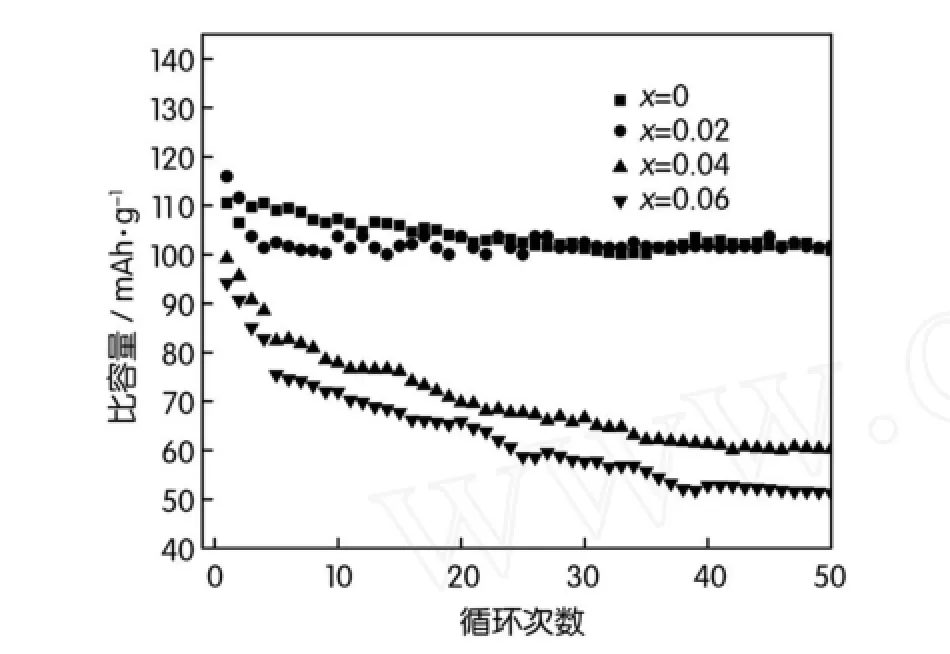
图6 Li1.05Mn1.95-xPbxO4的循环性能图
掺杂不同量的元素Pb合成的锰酸锂的交流阻抗图如图7所示。Z′表示阻抗的实部,反映了电极的包容性以及表面电荷转移阻抗,Z″表示阻抗的虚部。从图7可以看出,未掺杂铅的锰酸锂的表面电荷转移阻抗大约为120Ω,掺杂铅之后,材料的表面电荷转移阻抗均有所增大,但是掺入元素铅的锰酸锂的锂离子扩散阻抗均有所减少,其中当x=0.02时,锂离子扩散阻抗有明显减少。
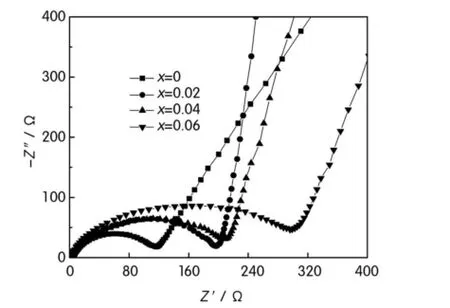
图7 Li1.05Mn1.95-xPbxO4的交流阻抗图
3 结 论
1.采用高温固相法合成Li1.05Mn1.95-xPbxO4,当x>0.02时,材料的XRD图出现杂质峰;随着x的增大,锰酸锂的颗粒有团聚趋势,在表面出现细小颗粒,材料的循环性能下降,阻抗增大,材料的电化学性能变差。
2.当Li1.05Mn1.95-xPbxO4中掺杂量x=0.02时,尖晶石型锰酸锂的循环性能得到一定程度的改善,锰酸锂的锂离子扩散阻抗有所降低。
[2] 雷永泉,万群,石永康.新能源材料[M].天津:天津大学出版社,2001.1-16.
[3] 谭柱中,梅光贵,李维健,等.锰冶金学[M].长沙:中南大学出版社,2004.
[4] Tu J,Zhao X B,Zhuang D G,et al.Studies of cycle ability of LiMn2O4and LiLa0.01Mn1.99O4as cathode materials for Lithiumion battery[J].Physica B,2006,382:12-13.
[5] 邱滟,胡文成.高温固相分段反应制备LiMn2O4的研究[J].中国锰业,2003,21(4):36-38.
[6] 李琪,乔庆东.LiMn2O4的溶胶凝胶法合成及其电化学性能[J].应用化学,2003,20(12):1 171-1 175.
[7] 李嵩,程杰锋,季世军,等.水热合成锂离子正极材料LiMn2O4[J].稀有金属材料与工程,2003,32(6):468-470.
[8] Wichham D G,Croft WJ.Crystallographic and magnetic properties of several spinels containing trivalent manganese[J].Phys Chem Solids,1958,7(4):351-360.
[9] 陈艳芳,赵胜利,陈海云,等.尖晶石LiMn2O4纳米粉体的制备及电化学性能[J].河南科技大学学报,2009,30(3):5-8.
[10]Chen Z Y,Liu X Q,Gao L Z,et al.Electrochemical capacity fading
in high temperature of spinel LiMn2O4and its improvement[J].
Chinese Journal of Inorganic Chemistry,2001,17(3):325-329. [11]Masaru S,Hideyuki N,Yoshio M.Electrochemical behavior of polyaniline coated spinel LiMn2O4[J].Denki Kagaku oyobi Kogyo Butsuri Kagaku,2000,68(7):587-590.
[12]高农,张旭,顾大明,等.钴镍掺杂锰酸锂的电化学性能研究[J].材料科学与工艺,2008,16(2):232-238.
[13]Strobel P,Anne M,ChabreY,et al.Characteristies of the 4V plateau in LiMnO4-xF studied by bin situ synehrotron x-rayd diffraction[J].Journal of Power Sources,1999,81~82:458-462.
[14]陈健,王志兴,李新海,等.Al掺杂对锰酸锂结构与性能的影响[J].电池,2005,(2):119-124.
[15]李群,卢世刚,邱向东,等.阴极材料正尖晶石型LiMn2O4制备方法研究现状[J].电源技术,1999,23(5):289-292.
[16]王要武.尖晶石锂锰氧材料作为锂离子二次电池正极材料的
研究[D].长沙:湖南大学,1999.28-39.
Abstract:Taking electrolytic manganese dioxide as manganese sources,Li2CO3as lithium sources,Pb(NO3)2as the leas sources,LiMn2O4cathode was prepared by roasting at the temperature of 800℃for 24 h.The influence of Pb dopingon the structure and performance of spinel LiMn2O4was studied.It was found that whenx>0.02 in Li1.05Mn1.95-xPbxO4,the XRD patterns showed there were some impurities in the material,asxincreased,the particles of lithium manganese oxide reunion trended;the electrochemical performance of the Li1.05Mn1.95-xPbxO4cathode increased to a certain extent whenx=0.02,the lithium ion diffusion resistance was reduced,then asxincreased,the cycle performance and the electrochemical properties of Li1.05Mn1.95-xPbxO4attenuated.
Key words:lithium-ion battery;LiMn2O4;Pb;doping
Study on the Influence of Pb Doping on Structure and Performance of the Spinel Manganese Lithium
NIU Sha-sha1,CHEN Hai-qing1,WANG Zhi-xing2,J IANG Guang-hui1
(1.Hunan Research Institute of Nonferrous Metals,Changsha410015,China;
2.School of Metallurgical Science and Engineering,Central South University,Changsha410083,China)
TG146.26
A
1003-5540(2012)05-0043-05
2012-06-30
牛莎莎(1986-),女,助理工程师,主要从事新能源材料、湿法冶金、电化学等方面的研究。

