SPECT/CT同机融合显像对分化型甲状腺癌转移灶诊治的增益价值
龙亚红 LONG Yahong
丁 勇 DING Yong
方 毅 FANG Yi
分化型甲状腺癌(differentiated thyroid cancer,DTC)经手术切除后辅助131I治疗预后较好,但复发、转移的部位和数量影响手术及其131I治疗方案,因此,对于DTC患者复发、转移的部位和数量,以及病灶是否有放射性摄取的正确判断很重要。与超声、CT、MRI等影像学方法相比,131I全身扫描(whole body scan, WBS)具有较高的灵敏度和特异性,已成为诊断DTC有无残留、复发或转移,判定131I疗效和制订治疗计划的常规临床手段。但由于131I-WBS缺乏解剖定位标志,其结果易受生理性摄取和污染等多种因素的影响,有时很难对放射性摄取增高灶的部位和性质作出准确的判断[1]。单光子发射型计算机断层显像与CT(SPECT/CT)同机融合技术将SPECT的功能信息和CT的解剖信息有机结合,能很好地进行病灶定位和定性[2]。本研究旨在分析和评价131I-SPECT/CT融合显像在DTC患者诊断和治疗随访中的增益价值。
1 资料与方法
1.1 研究对象 分析2009-06~2010-04在军事医学科学院附属医院核医学科行131I治疗的诊断有复发或转移的分化型甲状腺癌患者。纳入标准:①成功清除术后残留的甲状腺组织,主要依据为既往治疗剂量的131I-WBS显示颈部无功能性摄碘甲状腺组织;②临床诊断复发或转移,主要根据影像学检查(包括颈部B超、CT、MRI、131I-WBS或PET/CT),同时结合血清甲状腺球蛋白(Tg)、甲状腺球蛋白抗体(TGAb)、甲状腺过氧化物酶抗体(TPOAb)检测结果,最终经穿刺活检证实或临床诊断共筛选出57例患者,男27例,女30例;年龄13~77岁,平均(47.3±15.6)岁;乳头状癌52例,滤泡状癌5例。
1.2 治疗情况 患者采用甲状腺激素撤退(停用甲状腺素类药物3~4周)或rhTSH(肌肉注射rhTSH 0.9mg,1次/d,连续2d,次日行131I治疗)介导的131I治疗。57例患者中,52例使用甲状腺素撤退,5例使用rhTSH介导,完成131I治疗前准备,主要根据患者经济或意愿选择。131I治疗前患者血清TSH>30IU/ml。131I剂量参考甲状腺癌NCCN指南和核医学治疗规范,局部肿瘤复发或淋巴结转移患者服用131I剂量为4.44~5.55GBq;肺转移或骨转移5.55~9.25GBq。服用131I后,第5~7天行WBS和SPECT/CT。
1.3 显像方法 患者取仰卧位,行前后位WBS和131I-SPECT/CT同机断层融合显像。使用Siemens Symbia T2 型SPECT/CT仪,采用高能平行孔准直器,先行WBS,矩阵256×1024,床速10cm/min,在所发现的常规不能排除污染或生理性等非特异性放射性碘摄取增高部位,行局部SPECT/CT断层融合显像,先行发射扫描后透射扫描。SPECT/CT显像矩阵128×128,旋转360°,1帧/5°,15s/帧。CT管电流100mA,电压110keV,扫描层厚3.0mm,层距1.0mm。迭代法重建(子集4,迭代8),获得的SPECT和CT图像在DICOM工作站完成图像融合。
1.4 图像分析 平面图像由2名核医学医师结合患者病情和其他相关检查结果判读。非甲状腺床区的生理性摄取(包括鼻咽部、唾液腺对称性、胃肠道以及膀胱的摄取),肝脏的弥漫性摄取,体表污染不纳入本研究。其余经视觉判定后认为的放射性摄取增高灶考虑为异常浓聚的转移性病灶。双肺弥漫性转移,或多个病灶融合时病灶数计为1。SPECT/CT图像由1名核医学医师和1名放射科医师共同完成,意见不一致时由3名以上医师共同讨论后达成一致意见。明确浓聚灶的解剖部位,或鉴别转移灶和生理或其他病理性摄取,即认为SPECT/CT具有增益价值。
1.5 统计学方法 采用SPSS 11.0软件,SPECT/CT与WBS对摄碘转移灶的检出率比较采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 病灶检出情况 57例术后复发或转移的DTC患者共接受77次131I治疗,WBS和131I-SPECT/CT最终发现的放射性摄取增高灶为269处,经多种影像学检查或病理诊断,最终临床诊断转移灶281处,其中摄碘转移灶236处,不摄碘转移灶45处。WBS共发现215处放射性摄取增高灶,其中201处为转移性病灶(包括12处假阳性病灶)和14处为非转移性病灶(包括7处假阴性病灶);54处WBS未发现的摄碘病灶中,33处或因摄碘能力较弱或病灶较小或靠近颜面部腺体而未发现(其中19处为摄碘非转移灶,14处为摄碘转移灶),16处为病灶融合不能分辨数目,5处误认为生理性摄取。经SPECT/CT融合显像后,236处摄碘转移灶均明确定位。
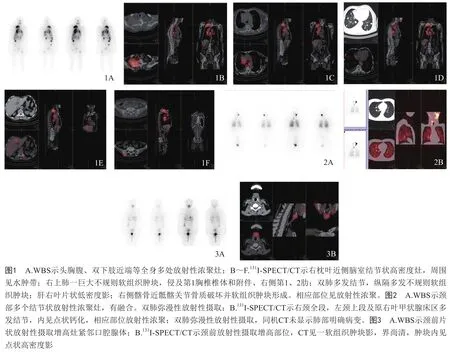
2.2 融合显像的诊断价值 ①SPECT/CT融合显像补充了平面显像在病灶定位方面的不足。本组1例77岁女性甲状腺滤泡状癌患者,第4次9250MBq131I治疗后第7天行WBS,结果显示全身多处点状、不规则浓聚灶。131I-SPECT/CT融合显像,所有病灶准确定位于脑、双肺、纵隔、肝、多处骨,诊断全身多发转移(图1)。②SPECT/CT融合显像在病灶定性方面也有较大的优势。131I-SPECT/CT融合显像排除了WBS显示的12处假阳性病灶,包括2处体表污染,5处残余甲状腺,4处生理性摄取,1处肺部炎性疾病的摄取(图2);诊断了WBS显示的7处假阴性摄碘病灶,其中1处为甲状腺癌复发(该病灶因靠近口腔唾液腺而漏诊,图3),6处为颈部淋巴结转移。57例DTC患者最终诊断236处有摄碘能力的复发或转移灶,WBS和131I-SPECT/CT显像诊断DTC摄碘复发或转移灶的敏感性分别为80.1%、100.0%;特异性分别为63.6%、81.8%;准确性分别为78.1%、97.8%,见表1。此外,SPECT/CT融合显像还发现了45处不摄碘的甲状腺癌转移灶,其中颈部淋巴结转移10处,纵隔淋巴结转移10处,肺转移13处,骨转移7处,软组织转移5处。
WBS和131I-SPECT/CT融合显像对摄碘转移灶的检出结果不同(χ2=8.50, P<0.05)。131I-SPECT/CT融合显像对总体及各部位DTC复发或转移灶的检出率均高于 WBS(P<0.05)(表 2)。

表1 SPECT/CT与WBS检出DTC摄碘病灶情况(个)

表2 57例DTC摄碘转移灶的分布情况(个)
2.3 融合显像的治疗价值131I-SPECT/CT融合显像明确了WBS显示的12处假阳性和7处假阴性病灶,并新发现了40处摄碘转移灶,对摄碘转移灶的诊断价值增加了24.5%(66/269)。另外,131I-SPECT/CT融合显像使临床医师对26.3%(15/57)患者的治疗策略作出调整。根据SPECT/CT融合显像结果,2例患者排除转移减少了131I治疗剂量;5例患者转移灶摄碘差而暂缓了131I治疗(如1例肺转移DTC患者,WBS显示双肺放射性摄取高于本底,131I-SPECT/CT融合显像未证实双肺结节有摄碘功能,故改用维甲酸诱导再分化下的131I治疗);8例患者确诊为转移增加了131I治疗剂量(4例将颈部淋巴结摄取误认为甲状腺组织残留,2例为淋巴结摄取稍高于周围本底而忽略,2例将淋巴结阳性摄取认为生理性摄取)。
3 讨论
血清Tg和131I-WBS是诊断DTC术后复发或转移最常用的检测方法。但131I-WBS作为一种平面显像,不能对病灶进行准确定位和形态描述,降低了131I全身扫描寻找DTC术后复发或转移灶的诊断价值。CT诊断难以区分正常淋巴结与<1cm的转移淋巴结,也很难准确区分肿瘤复发与手术等治疗后的瘢痕、纤维组织增生等解剖结构改变[3,4],更不易于发现无实体瘤的转移灶。SPECT/CT融合显像将解剖结构和功能信息融合,为甲状腺癌及其转移灶的精确定位定性提供可靠的依据。本研究采用SPECT结合同机CT断层融合显像,弥补了平面显像定位和定性的不足,提高了病灶的诊断准确性,并改进了治疗方案。
本研究中131I-SPECT/CT融合显像对59处放射性摄取增高灶进行了重新评估和判断,排除WBS的7处假阴性以及12处假阳性摄取增高灶,并新诊断WBS未发现的40处摄碘转移灶。Leitha等[1]认为131I-WBS的主要临床问题是由于污染和生理性摄取等因素造成的。本研究也得出类似的结论,WBS发现的可疑摄碘转移灶中,1例的假阴性放射性摄取增高灶和7例的假阳性放射性摄取增高灶与炎性[5]或生理性摄取以及体外污染有关。另一方面,由于颈部结构较复杂,WBS作为平面检查方法,缺乏解剖标志,很难对颈部残留的甲状腺组织和转移淋巴结等进行区别。本研究中WBS发现的12.8%(6/47)的假阴性放射性摄取增高灶和41.7%(5/12)的假阳性放射性摄取增高灶均为残留甲状腺组织。Schmidt等[6]对57例DTC术后患者行治疗剂量131I-WBS和SPECT/CT融合显像分析,结果显示,131I-SPECT/CT重新诊断了WBS的6处颈部转移淋巴结,WBS显示的15处转移性病灶中有11处为残留正常甲状腺组织。由此可见残留甲状腺组织、生理性摄取和体外污染是造成WBS假阳性或假阴性的主要原因。131I-SPECT/CT融合显像能结合CT的优势,对病灶进行准确定位和定性,减少假阳性和假阴性的发生。此外,本研究中131I-SPECT/CT新发现40处WBS未发现的摄碘转移灶,笔者认为与扫描速度慢和容易被忽略的低摄碘能力病灶有关。本研究得出的另一结论是,131I-SPECT/CT融合显像对DTC总体摄碘转移灶的诊断率高于WBS。
综上所述,131I-SPECT/CT断层融合显像较WBS的优势在于:①定位准确:鉴别全身各部位摄碘灶,特别能准确定位全身多发碘浓聚灶;②排除污染,确定生理性、病理性、病理性非特异性摄取;③发现了其他影像学检查(包括B超、CT、PET/CT)诊断为无摄碘功能的转移灶,并改变了部分患者的治疗策略。总之,131I-SPECT/CT融合显像能更好地检出并鉴别DTC转移灶的部位和性质,提高诊断的敏感性、特异性和准确性,协助临床医师调整治疗方案,进而改善患者预后[7],有较高的临床应用价值。
[1]Leitha T, Staudenherz A. Frequency of diagnostic dilemmas in 131I whole body scanning. Nuklearmedizin, 2003, 42(2):55-62.
[2]Yamamoto Y, Nishiyama Y, Monden T, etal. Clinical usefulness of fusion of 131I SPECT and CT images in patients with differentiated thyroid carcinoma. J Nucl Med,2003, 44(12): 1905-1910.
[3]Akoylu E, Dutipek M, Bekis R, etal. Assessment of cervical lymph node metastasis with different imaging methods in patients with head and neck squamous cell carcinoma. J Otolaryngol, 2005, 34(6): 384-394.
[4]Even-Sapir E, Keidar Z, Bar-Shalom R. Hybrid imaging(SPECT/CT and PET/CT)—improving the diagnostic accuracy of functional/metabolic and anatomic imaging.Semin in Nucl Med, 2009, 39(4): 264-275.
[5]Jong I, Taubman K, Schlicht S. Bronchiectasis simulating pulmonary metastases on iodine-131 scintigraphy in welldifferentiated thyroid carcinoma. Clin Nucl Med, 2005,30(10): 688-689.
[6]Schmidt D, Szikszai A, Linke R, etal. Impact of 131I SPECT/spiral CT on nodal staging of differentiated thyroid carcinoma at the first radioablation. J Nucl Med, 2009,50(1): 18-23.
[7]Kohlfuerst S, Igerc I, Lobnig M, etal. Posttherapeutic (131)I SPECT-CT offers high diagnostic accuracy when the findings on conventional planar imaging are inconclusive and allows a tailored patient treatment regimen. Eur J Nucl Med Mol Imaging, 2009, 36(6): 886-893.

